Elektronov obal Elektronov obal obal atomu je tvoen

Elektronový obal

Elektronový obal • obal atomu je tvořen elektrony – lehké částice nesoucí záporný náboj – počet elektronů je v elektroneutrálním atomu stejný, jako počet protonů • od složení elektronového obalu se odvíjí chemické vlastnosti prvků

Elektronový obal – elektron má duální charakter • chová se jako pevná částice i jako vlnění – nepohybuje se po pevně daných drahách • nemůžeme předpovídat jeho dráhu • lze určit pravděpodobnost jeho výskytu ve vybrané části prostoru • orbital – část prostoru v okolí jádra, ve kterém se elektron s 95% pravděpodobnstí vyskytuje

Elektronový obal – elektronový obal lze rozdělit do vrstev (slupek) • podle energie <= záleží na vzdálenosti od jádra – nejnižší má vrstva nejblíže k jádru • jsou postupně obsazovány elektrony od nejnižších • valenční vrstva – poslední (nejvzdálnější) vrstva, která ještě obsahuje elektrony – valenční elektrony = elektrony ve valenční vrstvě » nejvíce se projevují na vlastnostech prvku
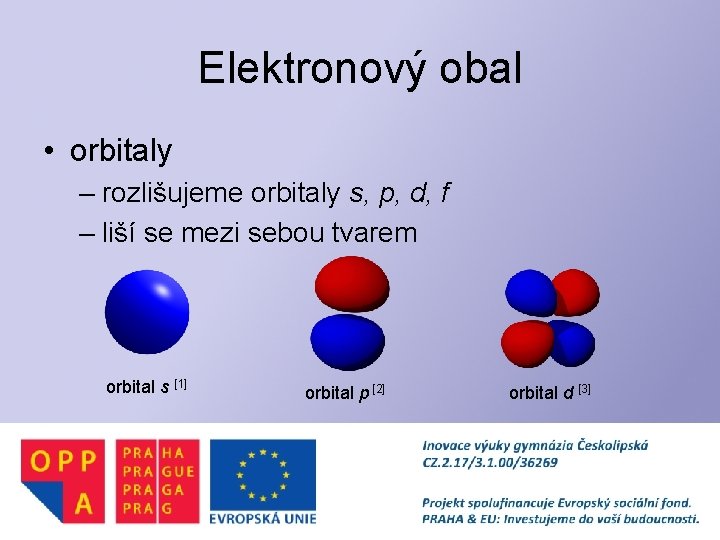
Elektronový obal • orbitaly – rozlišujeme orbitaly s, p, d, f – liší se mezi sebou tvarem orbital s [1] orbital p [2] orbital d [3]

Elektronový obal • Kvantová čísla – popisují oblast nejpravděpodobnějšího výskytu elektronu – elektrony se v atomovém obalu uspořádávají do vrstev podle vzrůstající energie • energetické hladiny popisujeme pomocí hlavního kvantového čísla n

Elektronový obal – hlavní kvantové číslo n • nabývá hodnot přirozených čísel (1, 2, 3, . . ) – těmto číslům se někdy připisují písmena K, L, M, . . . • rozhoduje o energii elektronu a jeho vzdálenosti od jádra Bohrův model atomu [4]

Elektronový obal – vedlejší kvantové číslo l • nabývá hodnot přirozených čísel od 0 do (n – 1) – pro n = 3 může l nabývat hodnot 0, 1 a 2 • společně s hlavním kvantovým číslem určuje energii elektronu • popisuje typ orbitalu (s, p, d, f), ve kterém se elektron vyskytuje

Elektronový obal – orientace orbitalu je popsána magnetickým kvantovým číslem m • nabývá hodnot celých čísel od –l po +l – pro l = 2 nabývá m hodnot -2, -1, 0, 1, 2 • určuje orientaci orbitalu v prostoru (konkrétní tvar daného typu orbitalu)

Elektronový obal – vnitřní moment hybnosti (spin) elektronu popisuje spinové kvantové číslo s • nabývá hodnot -½ a + ½ – tato 4 kvantová čísla jednoznačně charakterizují každý elektron v atomu • n, l a m přesně určují orbital, s přesněji určuje elektron v tomto orbitalu

Elektronový obal – orbital • část prostoru kolem jádra, kde se mohou vysktovat maximálně 2 elektrony – mají stejná čísla n, l i m, liší se číslem s – podslupka • orbitaly se stejnými čísly n a l – slupka • orbitaly se stejným číslem n

Elektronový obal • Tvar a prostorová orientace orbitalů – popsány kvantovými čísly l (tvar) a m (orientace) – každé hodnotě vedlejšího kvantového čísla l je přiřazen jeden typ orbitalu • • l=0 l=1 l=2 l=3 orbital s orbital p orbital d orbital f

Elektronový obal – s orbital • má tvar koule • pro l = 0 nabývá m pouze hodnot 0 orbital s [1] => jediná možná orientace => každá vrstva obsahuje pouze jeden orbital s • vyskytuje se již od první slupky elektronového obalu
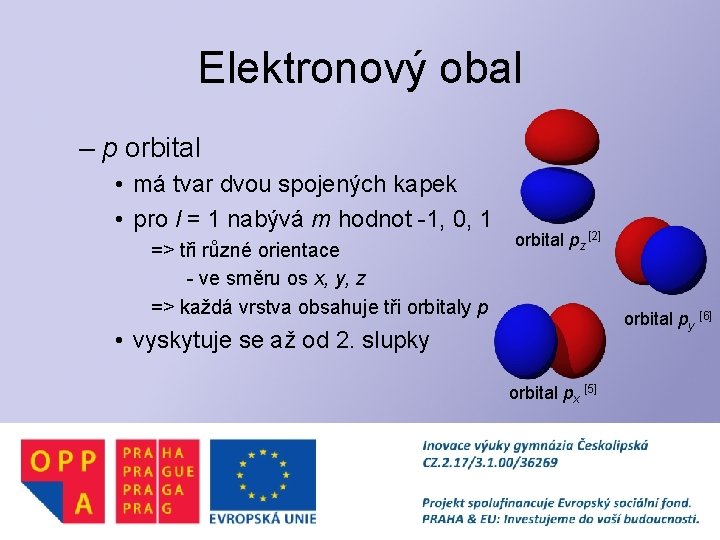
Elektronový obal – p orbital • má tvar dvou spojených kapek • pro l = 1 nabývá m hodnot -1, 0, 1 => tři různé orientace - ve směru os x, y, z => každá vrstva obsahuje tři orbitaly p orbital pz [2] orbital py [6] • vyskytuje se až od 2. slupky orbital px [5]
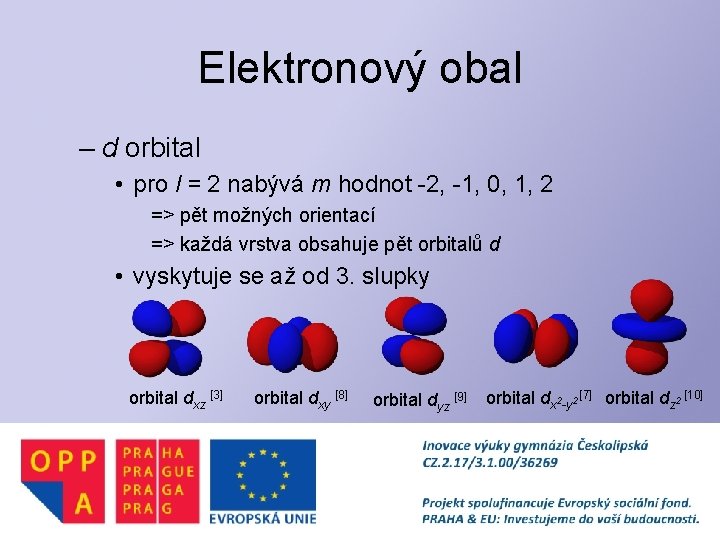
Elektronový obal – d orbital • pro l = 2 nabývá m hodnot -2, -1, 0, 1, 2 => pět možných orientací => každá vrstva obsahuje pět orbitalů d • vyskytuje se až od 3. slupky orbital dxz [3] orbital dxy [8] orbital dyz [9] orbital dx 2 -y 2 [7] orbital dz 2 [10]

Elektronový obal – f orbital • pro l = 3 nabývá m hodnot -3, -2, -1, 0, 1, 2, 3 => sedm možných orientací => každá vrstva obsahuje sedm orbitalů f • vyskytuje se až od 4. vrstvy přehled typů orbitalů v jednotlivých vrstvách

Odkazy 1. 2. 3. 4. 5. 6. 7. 8. www. wikipedia. org, Hydrogen eigenstate n 2 l 0 m 0 [online]. 2005 -08 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/9/9 b/Hydrogen_eigenstate_n 2_l 0_m 0. png www. wikipedia. org, P 2 M 0 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/d/d 4/P 2 M 0. png www. wikipedia. org, D 3 M 1 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/5/5 b/D 3 M 1. png www. wikipedia. org, Bohr-atom-PAR [online]. 2007 -11 -16 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/5/55/Bohr-atom-PAR. svg www. wikipedia. org, P 2 M 1 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/5/5 a/P 2 M 1. png www. wikipedia. org, P 2 M-1 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/8/89/P 2 M-1. png www. wikipedia. org, D 3 M-2 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/9/9 b/D 3 M-2. png www. wikipedia. org, D 3 M 2 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/4/45/D 3 M 2. png
![Odkazy 9. 10. www. wikipedia. org, D 3 M-1 [online]. 2008 -09 -25 [cit. Odkazy 9. 10. www. wikipedia. org, D 3 M-1 [online]. 2008 -09 -25 [cit.](http://slidetodoc.com/presentation_image_h2/54e122c013f46e962577632e0f38f8c8/image-18.jpg)
Odkazy 9. 10. www. wikipedia. org, D 3 M-1 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/e/e 3/D 3 M-1. png www. wikipedia. org, D 3 M 0 [online]. 2008 -09 -25 [cit. 2013 -12 -03]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/5/57/D 3 M 0. png
- Slides: 18