ELEKTRONOV OBAL Dopl vhodn slova pokud to nejde

ELEKTRONOVÝ OBAL

Doplň vhodná slova, pokud to nejde použij nápovědu Atom je nejjednodušší částice hmoty. Skládá se z jádra a obalu Jádro tvoří protony a neutrony. V obalu se pohybují elektrony ve slupkách. Atom je elektro- neutrální částice. Jádro má kladný náboj, obal záporný. . . . . . . . . . . . . . . . . . částice, kladný, neutrony, jádra, záporný, obalu, protony, slupkách, neutrální, elektrony . . . . . . .

Způsob uspořádání elektronů v elektronovém obalu se nazývá elektronová konfigurace. Elektrony ve vnější slupce – nejdále od jádra, se nazývají valenční elektrony. Jsou rozhodující pro chemické vlastnosti prvku, protože se účastní chem. vazeb mezi atomy.

• Počet valenčních elektronů většinou určuje maximální oxidační číslo atomu (výjimkou jsou přechodné prvky v B. skupinách – I. a VIII. )

Elektronová konfigurace Elektrony jsou v obalu umístěny ve vrstvách (slupkách) V kolikáté periodě (řádce) PSP prvek je, tolik bude mít elektronový obal vrstev Vrstva má tolik elektronů, kolik je prvků v periodě (na řádce)

Příklad: Hliník Al Má protonové číslo 13 má 13 protonů a 13 elektronů Je ve 3. periodě obal bude mít 3 vrstvy V 1. vrstvě jsou 2 prvky 2 elektrony Ve 2. vrstvě je 8 prvků 8 elektronů Ve 3. vrstvě jsou ke hliníku včetně 3 prvky 3 elektrony Celkem: 2 + 8 + 3 = 13
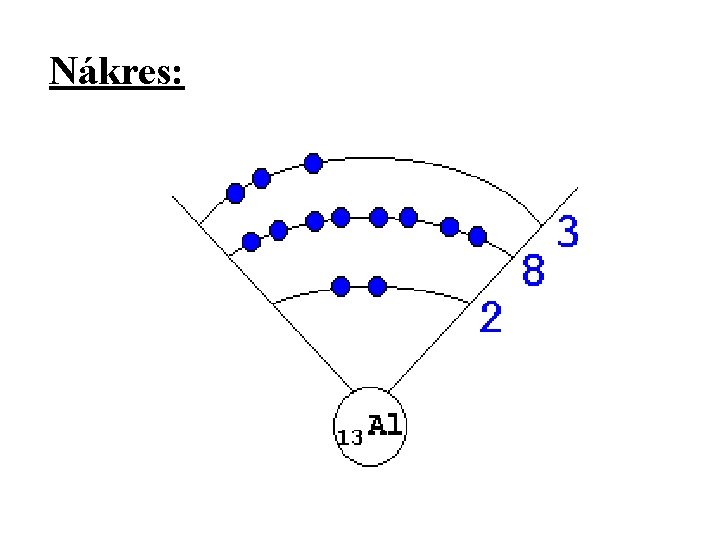
Nákres:

Orbital = prostor kolem jádra atomu, kde se vyskytuje elektron (část elektronové slupky) Každý orbital je charakterizován 3 kvantovými čísly: 1) hlavní kvantové číslo n, je to číslo řádku (periody) v PSP, udává energii elektronu 2) vedlejší kvantové číslo l, vyjadřuje prostorový tvar orbitalu, číslice v zápise nahrazuje písmeno (s, p d, f) s – 1 orbital, kulový tvar, obsahuje maximálně 2 elektrony p – 3 orbitaly, 6 elektronů d – 5 orbitalů, 10 elektronů 3) magnetické kvant. č. m, vyjadřuje prostorovou orientaci orbitalu

K popisu chování elektronu v orbitalu se zavádí ještě čtvrté číslo, tzv. spinové kvantové číslo s, charakterizuje rotaci elektronu, nabývá hodnot +1/2 a -1/2 Kombinací všech 4 kvant. čísel lze jednoznačně charakterizovat kterýkoliv elektron v obalu atomu. (Pauliho princip výlučnosti: v atomu neexistují dva elektrony, které by měly všechny 4 kvant. č. stejná) Ke znázornění elektronové konfigurace se používají rámečkové diagramy (orbitaly zapisujeme pomocí hlavního a vedlejšího kvantového čísla, orbitaly lišící se magn. č. se nerozlišují, zapisujeme je souhrnně (1 s, 2 s, 3 p…). Počet elektronů zapisujeme do exponentu (2 s 2, 3 p 6)

ZAPLŇOVÁNÍ ORBITALŮ 1) výstavbový princip – pořadí, ve kterém se orbitaly zaplňují (orbitaly s nižší energií se zaplňují dříve) 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p…. . 2) Pauliho princip – každý orbital může mít max. 2 elektrony, tzv. elektronový pár 3) Hundovo pravidlo – orbitaly se zaplňují postupně, nejprve jedním elektronem a podle počtu se doplňují

př. C – 6 elektronů 1 s 2, 2 p 2 1 s 2 s 2 p → čtyři valenční elektrony př. Al – 13 elektronů 1 s 2, 2 p 6 , 3 s 2, 3 p 1 → tři valenční elektrony

Použité zdroje obrázků - galerie Microsoft office
- Slides: 12