ELEKTROLIZ A KLARA KAKUKA prof hemije MAVANSKA SREDNJA












- Slides: 15

ELEKTROLIZ A KLARA KAKUČKA, prof. hemije MAČVANSKA SREDNJA ŠKOLA

Definicija ■ Elektroliza je razlaganje hemijskog jedinjenja pod dejstvom električne struje. ■ Kada se jonsko jedinjenje rastvori u vodi ili rastopi (prevede u tečno stanje) oslobode se pozitivni i negativnio joni ■ Električna struja se primenjuje preko elektroda. ■ Pozitivna elektroda ANODA ■ Negativna elektroda KATODA ■ Svaka elektroda privlači jone obrnutog naelektrisanja.

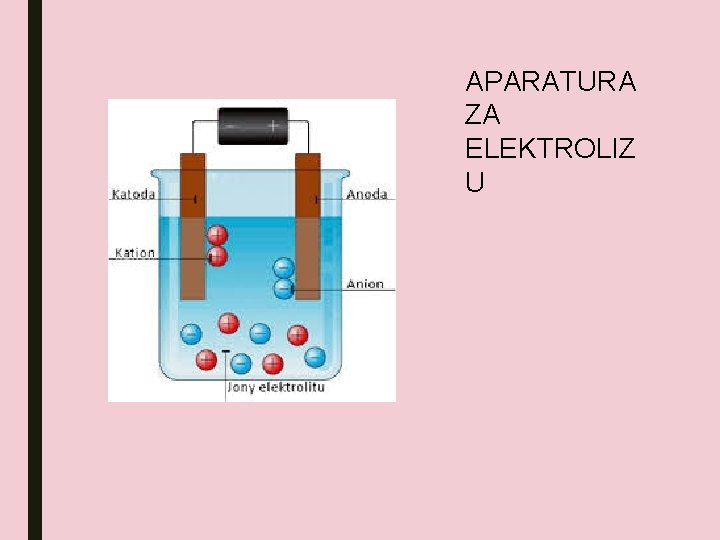
APARATURA ZA ELEKTROLIZ U

Procesi prolasku struje ■ Pozitivni katjoni kreću se ka negativnoj katodi, uzimaju elektrone i razelektrišu se. ■ Negativni anjoni kreću se ka pozitivnoj anodi, ostavljaju elektrone i razelektrišu se. https: //youtu. be/32 Lj. Dax. Moic

Faradejevi zakoni elektrolize ■ I zakon: Količina elemenata izdvojena pomoću jednosmerne struje proporcionalna je količini elektriciteta koja je prošla kroz ćeliju. ■ II zakon: Mase razdvojenih elemenata direktno su proporcionalne atomskim masama elemenata kada se podele sa brojem izmenjenih elektrona

Industrijska primena ■ Proizvodnja Al, Li, Na, K, aspirina. ■ Proizvodnja H 2 za automobile. ■ Proizvodnja Cl 2 i Na. OH, KCl ■ Elektrometalurgija je proces redukcije metala polazeci od jedinjenja da bi se dobio čist metal. Na primer: Na. OH pomoću elektrolize daje Na i H 2 (imaju važnu primenu). ■ Električna rafinacija se koristi da se metala očisti od nepoželjnih primesa elektrolizom. Npr. u jedinjenju bakra ima nekih primesa. Pri elektrolizi bakar se formira oko katode, a nečistoće oko anode (uglavnom Ag, Au I sl. . )

Elektrometalurgija i Električna rafinacija ■ Elektrometalurgija je proces redukcije metala polazeci od jedinjenja da bi se dobio čist metal. Na primer: Na. OH pomoću elektrolize daje Na i H 2 (imaju važnu primenu). ■ Električna rafinacija se koristi da se metala očisti od nepoželjnih primesa elektrolizom. Npr. u jedinjenju bakra ima nekih primesa. Pri elektrolizi bakar se formira oko katode, a nečistoće oko anode (uglavnom Ag, Au I sl. . ) ■ Galvanizacija-prevlačenje metala otpornijim M (zaštita)


Elektrohemijski izvor struje Elektrohemijska ćelija je uređaj koji pretvara hemijsku energiju spontanog redoks procesa u električnu struju. Vrste ćelija su galvanska i voltina ćelija. Elektrohemijska ćelija ima 2 elektrode (anodu i katodu). Anoda je elektroda na kojoj se vrši oksidacija, a na katodi redukcija. Elektrode se prave od nekog provodljivog materijala: metala, poluprovodnika, grafita, čak i provodnih polimera. Između njih je elektrolit, koji sadrži jone koji se mogu slobodno kretati.

Katoda u alkalnim baterijama je od mangan diosida Mn. O 2, a anoda od cinka u prahu

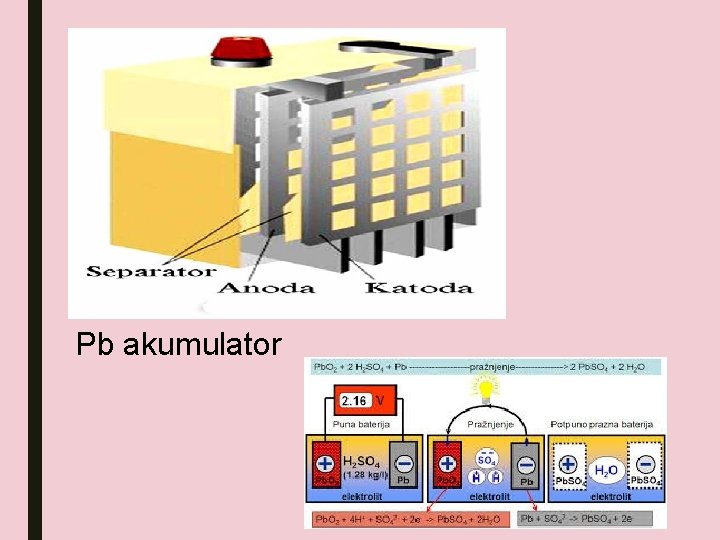
Pb akumulator

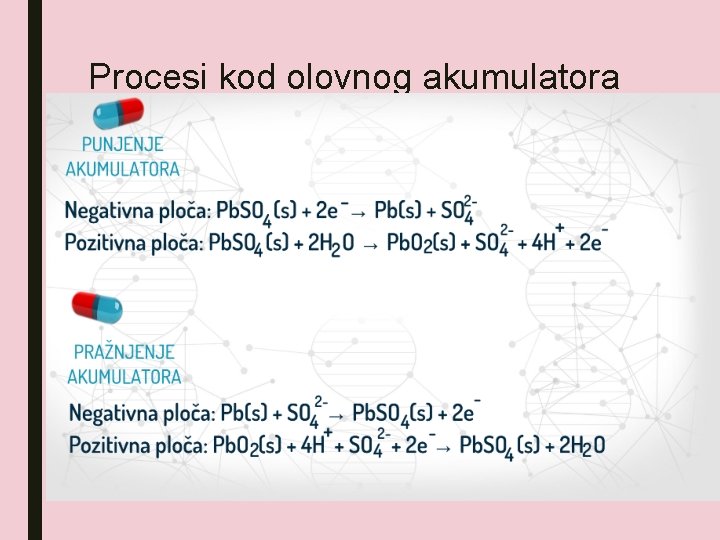
Procesi kod olovnog akumulatora

Procesi kod olovnog akumulatora

Korozija – neželjena oksidacija metala Posrebravanje
