Elektroanalytick metody Modernizace vuky technickch a prodovdnch obor

Elektroanalytické metody Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Elektroanalytické metody • Potenciometrie • Konduktometrie • Elektrogravimetrie • Coulometrie • Polarografie Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Základní pojmy • Elektroda – heterogenní elektrochemický systém tvořený alespoň dvěma fázemi (kov – roztok) • Elektrodový děj – oxidačně-redoxní reakce umožňující přenos náboje mezi fázemi elektrody • Galvanické napětí (potenciál) – mezi kovem a roztokem vzniká elektrická dvojvrstva, projeví se rozdíl potenciálů Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Elektrodové rovnováhy • Ponoříme-li stříbrný plíšek do roztoku Ag. NO 3, vznikne stříbrná elektroda: • Před ustavením rovnováhy Ag+ odebírají z plíšku e- a Ag se vylučuje jako kov. Plíšek se nabíjí kladně. Rozdíl potenciálů je rovnovážné napětí elektrody. Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Základní pojmy • Chemický galvanický článek – tvořen dvěma různými elektrodami, jeho napětí určují rozdílné chemické reakce na obou elektrodách • Elektroda 1. druhu – tvořeny prvkem a jeho iontem v roztoku (zinková, stříbrná) • Elektroda 2. druhu – kov pokrytý vrstvou své málo rozpustné soli a ponořený do roztoku aniontů této soli (kalomelová- Hg/Hg 2 Cl 2/KCl) Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Potenciometrie • měření EMN galvanického článku • galvanický článek složený z měrné elektrody (změna E s koncentrací stanovovaného iontu) a z elektrody referentní (E = konst. ) • v galvanickém článku probíhají na elektrodách samovolně elektrochemické reakce – bezproudový stav • chemická energie se mění na elektrickou Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Měrné (indikační) elektrody • elektrodový potenciál se mění se změnou koncentrace těch iontů, na které je měrná elektroda citlivá • • vodíková elektroda kovové elektrody redoxní elektrody membránové elektrody Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Měrné (indikační) elektrody • kovové elektrody - citlivé na svoje vlastní ionty (stříbrná elektroda) • redoxní elektrody - z ušlechtilých kovů (Pt, Pd, Au), změna poměru látkových koncentrací oxidované a redukované formy redoxního páru • membránové elektrody - selektivní jen na určité ionty, membránový potenciál vzniká na rozhraní dvou roztoků přes membránu - ISE Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Vodíková elektroda • EH, 0 = 0 vztahovány všechny E • vodíková elektroda se skládá z Pt plíšku potaženého platinovou černí v roztoku H+ iontů • článková poloreakce vodíkové elektrody: • vhodná k měření p. H ve vodných i částečně vodných rozpouštědlech a ke zjišťování p. H standardních tlumivých roztoků Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Skleněná elektroda • vhodná pro měření vodíkových iontů • tvořena membránou ze speciálního skla, naplněná roztokem o konst. hodnotě p. H • uvnitř eldy vnitřní referentní elektroda (chloridostříbrná) • na povrchu elektrody dochází k výměnným reakcím (Na+ z eldy za H+ v roztoku) Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Referentní kalomelová elda • kapka rtuti a vrstva kalomelu (Hg 2 Cl 2) utěsněny v trubičce zatavené s Pt kontaktem • v nosné trubici elektrody zataveno azbestové vlákno nebo hustá frita • na porézních přepážkách se vytváří kapalinový spoj s nasyc. roztokem KCl Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Referentní kalomelová elda z článkové poloreakce vyplývá vztah (Nernstova rovnice) pro elektrodový potenciál (při 25 o. C): Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
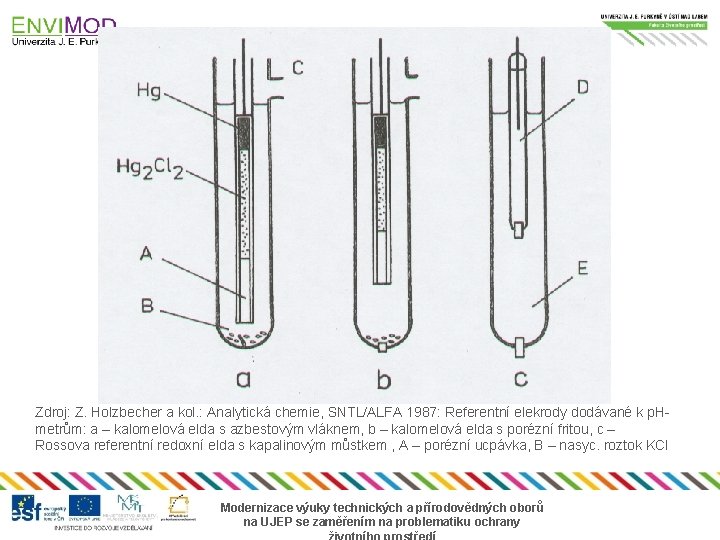
Zdroj: Z. Holzbecher a kol. : Analytická chemie, SNTL/ALFA 1987: Referentní elekrody dodávané k p. Hmetrům: a – kalomelová elda s azbestovým vláknem, b – kalomelová elda s porézní fritou, c – Rossova referentní redoxní elda s kapalinovým můstkem , A – porézní ucpávka, B – nasyc. roztok KCl Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Referentní chloridostříbrná elda • stříbrný drátek potažený vyloučeným Ag. Cl ponořený do roztoku chloridových iontů • používá se ke standardizaci tlumivých roztoků často v kombinaci s vodíkovou elektrodou • často tvoří vnitřní svodnou elektrodu u ISE Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
Chloridostříbrná elektroda Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany 15

Přímá potenciometrie • metoda, při které přímo zjišťujeme aktivitu nebo koncentraci iontu či molekuly • pomocí měrné a referentní elektrody • k měření neznámých vzorků používáme metodu kalibrační křivky • regresními metodami zjišťujeme vztah mezi elektromotorickým napětím článku a koncentrací příslušného iontu Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Zdroj: CD technoprocur cz Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Potenciometrická titrace • závislost potenciálu na přidávaném titračním činidle • neutralizační, oxidačně-redukční titrace, stanovení organických a anorganických látek v nevodných prostředích • v praxi velmi rozšířená, pracovně a přístrojově jednoduchá • metody se snadno automatizují • používá se tam, kde selhává vizuální indikace Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Konduktometrie • vodivost je způsobená migrací všech iontů mezi elektrodami v roztoku • vodivost je aditivní veličinou, která je ovlivněna koncentrací, elektrickým nábojem a pohyblivostí jednotlivých iontů • přímá konduktometrie je vhodná ke stanovení koncentrace elektrolytu na základě měření vodivosti roztoku • k indikaci bodu ekvivalence sledováním změn vodivosti při konduktometrických titracích Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Konduktometrie • vodivost elektrického vodiče představuje konstantu úměrnosti v Ohmově zákonu I = (1/R)U a je převrácenou hodnotou odporu; jednotkou je siemens, S = -1 • elektrickou vodivost G určitého materiálu charakterizuje měrná vodivost, má rozměr S m-1, resp. S cm-1) Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

• u čistého roztoku elektrolytu závisí měrná vodivost na jeho koncentraci, stejně tak i molární vodivost: • molární vodivost má jednotku S m 2 mol-1. • v roztoku silného elektrolytu migrují kationty a anionty působením elektrického pole vzájemně opačnými směry Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

• kolem každého iontu se vytváří iontová atmosféra obsahující ionty opačného náboje, anionty a kationty se brzdí, a to tím více, čím je koncentrace elektrolytu vyšší • ve zředěných roztocích silného elektrolytu se molární vodivost zvyšuje, a to v závislosti na klesající koncentraci • H+ a OH- ionty mají velmi vysoké molární vodivosti • vysokou pohyblivost těchto iontů v roztoku vysvětlujeme přenosem protonu na sousední molekulu vody (resp. ion OH-) Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Přímá konduktometrie • na základě přímého měření vodivosti roztoku je možné stanovit koncentraci elektrolytu jen tehdy, jestliže je složení elektrolytu známé a konstantní • kalibrační přímku sestrojujeme na základě měření roztoků se známou koncentrací • v praxi je přímá konduktometrie nejčastější při rychlém ověřování celkového obsahu solí rozpuštěných ve vodě (pramenité, říční i destilované), lze určit celkový obsah minerálních látek v cukrovarnických surovinách apod. Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
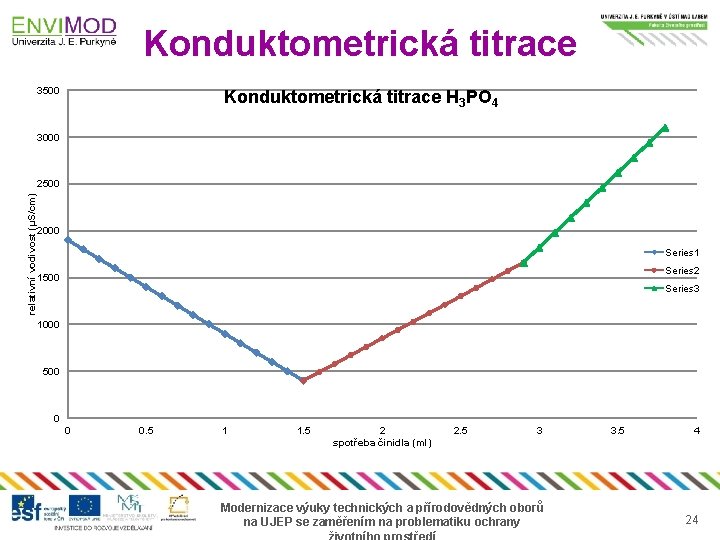
Konduktometrická titrace 3500 Konduktometrická titrace H 3 PO 4 3000 relativní vodivost (µS/cm) 2500 2000 Series 1 Series 2 1500 Series 3 1000 500 0 0 0. 5 1 1. 5 2 spotřeba činidla (ml) 2. 5 3 Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany 3. 5 4 24

Elektrogravimetrie • založena na vážení produktu elektrochemické reakce • elektrochemická reakce probíhá v roztoku a na elektrodách a je systému vnucena působením vnějšího napětí • při stanovení dochází k úplnému vyloučení stanovovaného kovu na pracovní elektrodě a určí se přírůstek její hmotnosti • elektrogravimetrické metody jsou oceňovány pro svou vynikající přesnost a správnost Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

• elektrolytické dělení stanovovaného kovu od jiného, který se vylučuje při negativnějším potenciálu, lze uskutečnit elektrolýzou za konstantního potenciálu pracovní elektrody • pro elektrogravimetrii se zhotovují elektrody z platiny • používá se Winklerova síťková katoda a spirálová anoda • elektrody se zavěšují do roztoku v kádince a nechává se proběhnout elektrochemická reakce Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
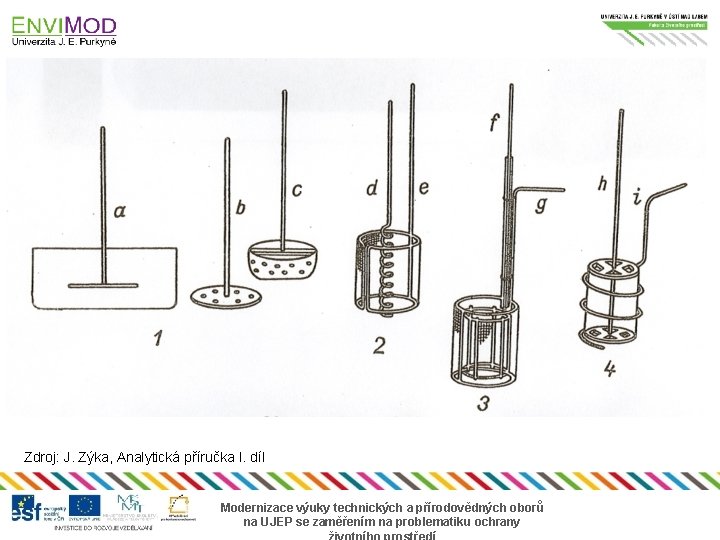
Zdroj: J. Zýka, Analytická příručka I. díl Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Coulometrie • Podle Faradayových zákonů je hmostnost m. B látky B vyloučené na elektrodě úměrná elektrickému náboji Q, který prošel článkem. K redukci nebo oxidaci jednoho molu chemických ekvivalentů se spotřebuje náboj odpovídající Faradayově konstantě (96 484, 56 C mol-1), a tak platí kde MB je molární hmotnost a z je počet elektronů vyměněných při elektrodové reakci. Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

• stanovení je založeno na měření náboje, který je nutný k úplné chemické přeměně stanovované látky • coulometrická analýza se může uskutečňovat za konstantního potenciálu pracovní elektrody nebo za konstantního proudu (coulometrická titrace) • elektrodová reakce musí na pracovní elektrodě probíhat se 100%ním proudovým výtěžkem • nesmí probíhat vedlejší elektrodové reakce, čehož dosáhneme vhodnou volbou podmínek pro coulometrické stanovení Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany

Coulometrická titrace Sekundární coulometrická titrace • při stanovení SO 2 se z roztoku jodidu vygeneruje jod • jod pak reaguje s SO 2 za vzniku síranů • přebytečný I 2 vyvolá náhlou změnu proudu mezi polarizovatelnými elektrodami • sekundární titrace jsou rozšířené - umožňují stanovit velký počet látek • generováním lze vytvářet i činidla, která se obtížně připravují nebo vyžadují inertní atmosféru • k indikaci konce titrací se nejčastěji používá biamperometrická titrace Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
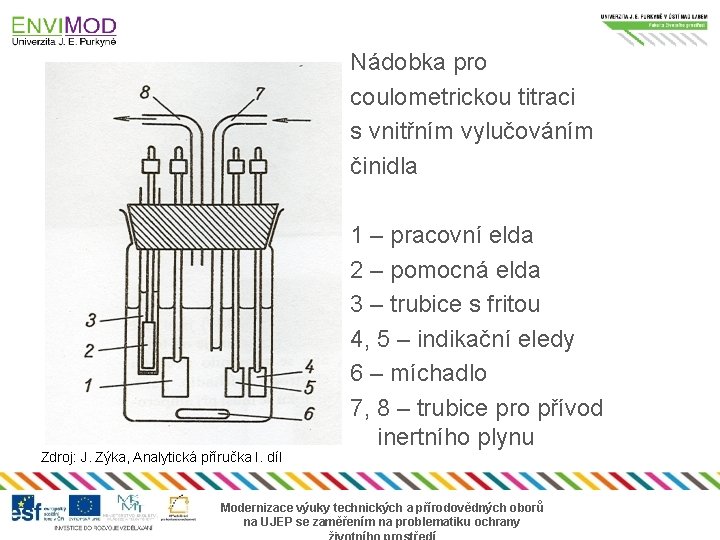
Nádobka pro coulometrickou titraci s vnitřním vylučováním činidla Zdroj: J. Zýka, Analytická příručka I. díl 1 – pracovní elda 2 – pomocná elda 3 – trubice s fritou 4, 5 – indikační eledy 6 – míchadlo 7, 8 – trubice pro přívod inertního plynu Modernizace výuky technických a přírodovědných oborů na UJEP se zaměřením na problematiku ochrany
- Slides: 31