Electroqumica Captulo 19 Copyright The Mc GrawHill Companies






![Ocurrirá la siguiente reacción en forma espontánea a 250 C si [Fe 2+] = Ocurrirá la siguiente reacción en forma espontánea a 250 C si [Fe 2+] =](https://slidetodoc.com/presentation_image_h/b7a24878c02a85420377885857fe465e/image-20.jpg)

- Slides: 31

Electroquímica Capítulo 19 Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display.

Los procesos electroquímicos son las reacciones de oxidación-reducción en que: • la energía liberada por una reacción espontánea se convierte en electricidad o • la energía eléctrica se usa para causar una reacción no espontánea 0 0 2+ 2 - 2 Mg (s) + O 2 (g) 2 Mg. O (s) 2 Mg 2+ + 4 e- Oxidación media reacción (pierde e-) Reducción media reacción O 2 + 4 e- 2 O 2(gana e-) 19. 1

Número de oxidación La carga del átomo que tendría en una molécula (o un compuesto iónico) si los electrones fueran completamente transferidos. 1. Los elementos libres (estado no combinado) tienen un número de oxidación de cero. Na, Be, K, Pb, H 2, O 2, P 4 = 0 2. En los iones monoatómicos, el número de oxidación es igual a la carga en el ion. Li+, Li = +1; Fe 3+, Fe = +3; O 2 -, O = -2 3. El número de oxidación del oxígeno es normalmente – 2. En H 2 O 2 y O 22 - este es – 1. 4. 4

4. El número de oxidación del hidrógeno es +1 excepto cuando está enlazado a metales en los compuestos binarios. En estos casos, su número de la oxidación es – 1. 5. Los metales del grupo IA son +1, metales de IIA son +2 y el flúor siempre es – 1. 6. La suma de los números de oxidación de todos los átomos en una molécula o ion es igual a la carga en la molécula o ion. HCO 3¿Los números de oxidación de todos los elementos en HCO 3 - ? O = -2 H = +1 3 x(-2) + 1 + ? = -1 C = +4 4. 4

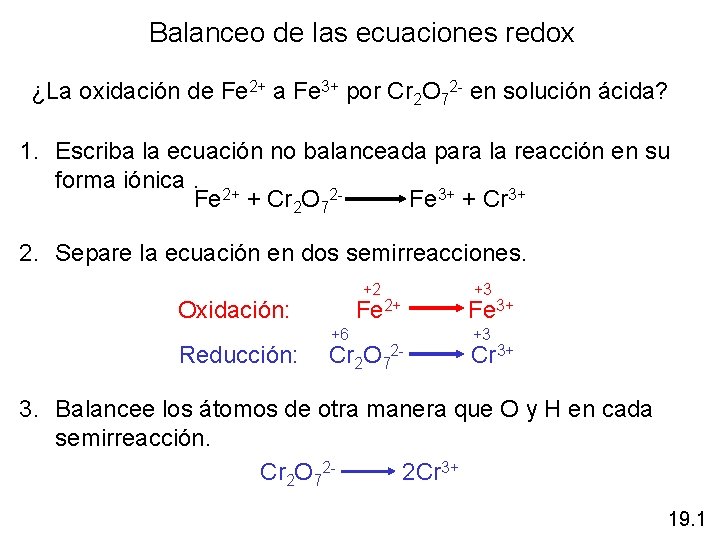
Balanceo de las ecuaciones redox ¿La oxidación de Fe 2+ a Fe 3+ por Cr 2 O 72 - en solución ácida? 1. Escriba la ecuación no balanceada para la reacción en su forma iónica. Fe 2+ + Cr 2 O 72 - Fe 3+ + Cr 3+ 2. Separe la ecuación en dos semirreacciones. +2 Oxidación: Reducción: +3 Fe 2+ Fe 3+ +6 Cr 2 O 7 +3 2 - Cr 3+ 3. Balancee los átomos de otra manera que O y H en cada semirreacción. Cr 2 O 72 - 2 Cr 3+ 19. 1

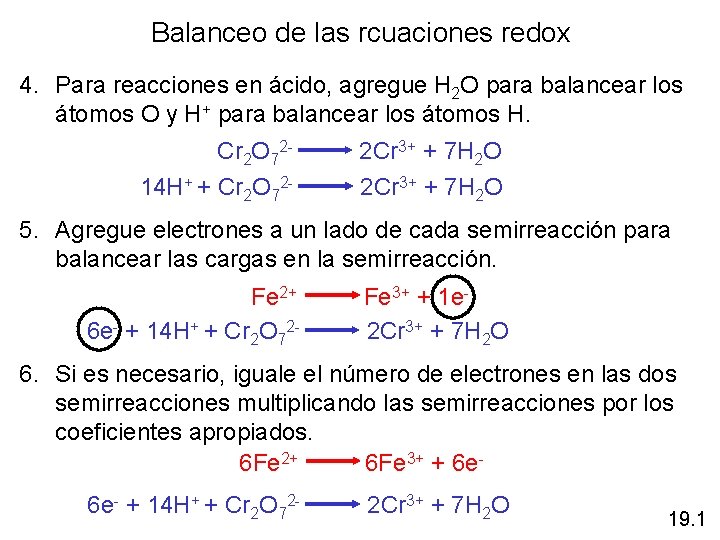
Balanceo de las rcuaciones redox 4. Para reacciones en ácido, agregue H 2 O para balancear los átomos O y H+ para balancear los átomos H. Cr 2 O 72 - 2 Cr 3+ + 7 H 2 O 14 H+ + Cr 2 O 72 - 2 Cr 3+ + 7 H 2 O 5. Agregue electrones a un lado de cada semirreacción para balancear las cargas en la semirreacción. Fe 2+ Fe 3+ + 1 e 6 e- + 14 H+ + Cr 2 O 72 - 2 Cr 3+ + 7 H 2 O 6. Si es necesario, iguale el número de electrones en las dos semirreacciones multiplicando las semirreacciones por los coeficientes apropiados. 6 Fe 2+ 6 Fe 3+ + 6 e 6 e- + 14 H+ + Cr 2 O 72 - 2 Cr 3+ + 7 H 2 O 19. 1

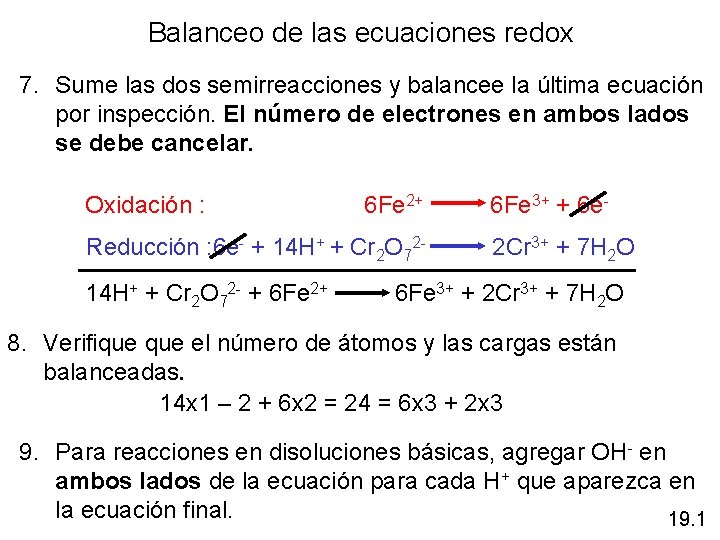
Balanceo de las ecuaciones redox 7. Sume las dos semirreacciones y balancee la última ecuación por inspección. El número de electrones en ambos lados se debe cancelar. Oxidación : 6 Fe 2+ 6 Fe 3+ + 6 e- Reducción : 6 e- + 14 H+ + Cr 2 O 72 - 2 Cr 3+ + 7 H 2 O 14 H+ + Cr 2 O 72 - + 6 Fe 2+ 6 Fe 3+ + 2 Cr 3+ + 7 H 2 O 8. Verifique el número de átomos y las cargas están balanceadas. 14 x 1 – 2 + 6 x 2 = 24 = 6 x 3 + 2 x 3 9. Para reacciones en disoluciones básicas, agregar OH- en ambos lados de la ecuación para cada H+ que aparezca en la ecuación final. 19. 1

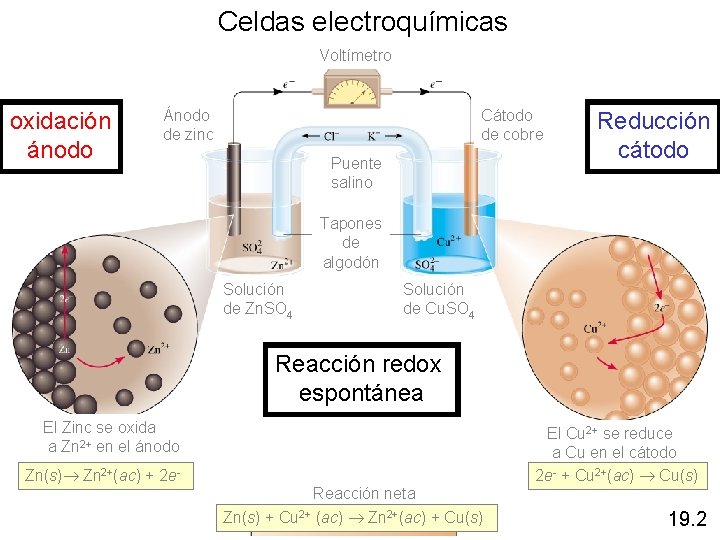
Celdas electroquímicas Voltímetro oxidación ánodo Ánodo de zinc Cátodo de cobre Puente salino Reducción cátodo Tapones de algodón Solución de Zn. SO 4 Solución de Cu. SO 4 Reacción redox espontánea El Zinc se oxida a Zn 2+ en el ánodo El Cu 2+ se reduce a Cu en el cátodo 2 e- + Cu 2+(ac) Cu(s) Zn 2+(ac) + 2 e- Reacción neta Zn(s) + Cu 2+ (ac) Zn 2+(ac) + Cu(s) 19. 2

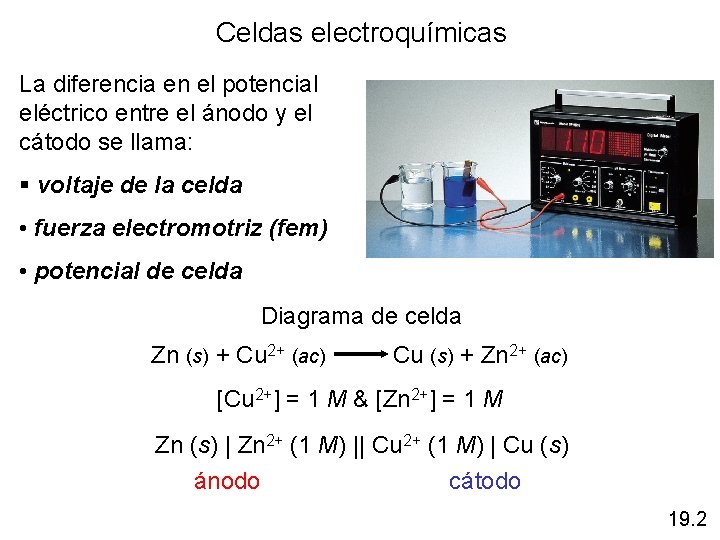
Celdas electroquímicas La diferencia en el potencial eléctrico entre el ánodo y el cátodo se llama: § voltaje de la celda • fuerza electromotriz (fem) • potencial de celda Diagrama de celda Zn (s) + Cu 2+ (ac) Cu (s) + Zn 2+ (ac) [Cu 2+] = 1 M & [Zn 2+] = 1 M Zn (s) | Zn 2+ (1 M) || Cu 2+ (1 M) | Cu (s) ánodo cátodo 19. 2

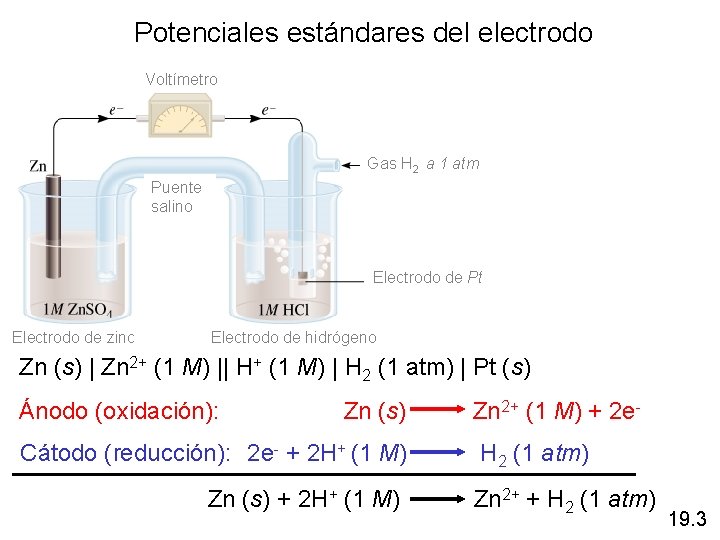
Potenciales estándares del electrodo Voltímetro Gas H 2 a 1 atm Puente salino Electrodo de Pt Electrodo de zinc Electrodo de hidrógeno Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) Ánodo (oxidación): Zn (s) Zn 2+ (1 M) + 2 e- Cátodo (reducción): 2 e- + 2 H+ (1 M) H 2 (1 atm) Zn (s) + 2 H+ (1 M) Zn 2+ + H 2 (1 atm) 19. 3

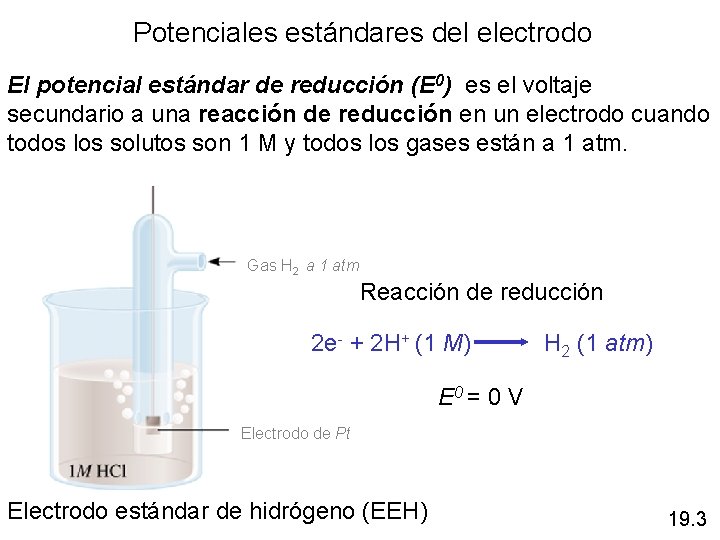
Potenciales estándares del electrodo El potencial estándar de reducción (E 0) es el voltaje secundario a una reacción de reducción en un electrodo cuando todos los solutos son 1 M y todos los gases están a 1 atm. Gas H 2 a 1 atm Reacción de reducción 2 e- + 2 H+ (1 M) H 2 (1 atm) E 0 = 0 V Electrodo de Pt Electrodo estándar de hidrógeno (EEH) 19. 3

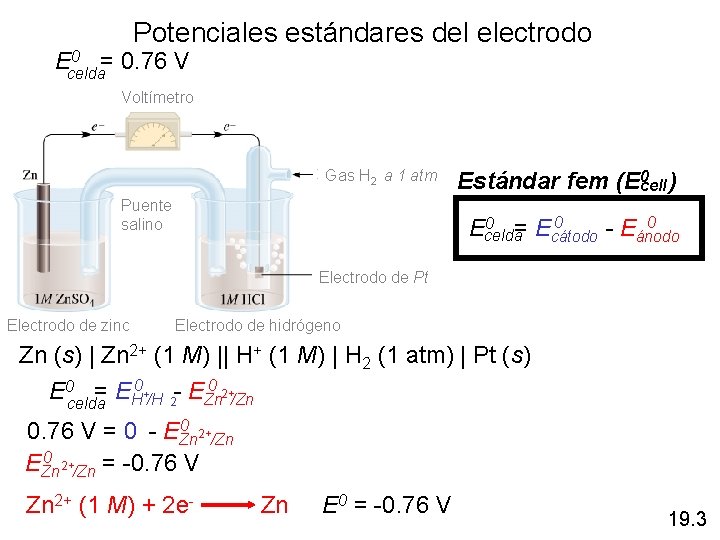
Potenciales estándares del electrodo 0 = 0. 76 V Ecelda Voltímetro Gas H 2 a 1 atm Puente salino Estándar fem (E 0 cell ) 0 0 = E 0 Ecelda cátodo - Eánodo Electrodo de Pt Electrodo de zinc Electrodo de hidrógeno Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) 0 2+ E 0 celda = EH 0+/H 2 - EZn /Zn 0 2+ 0. 76 V = 0 - EZn /Zn 0 2+ = -0. 76 V EZn /Zn Zn 2+ (1 M) + 2 e- Zn E 0 = -0. 76 V 19. 3

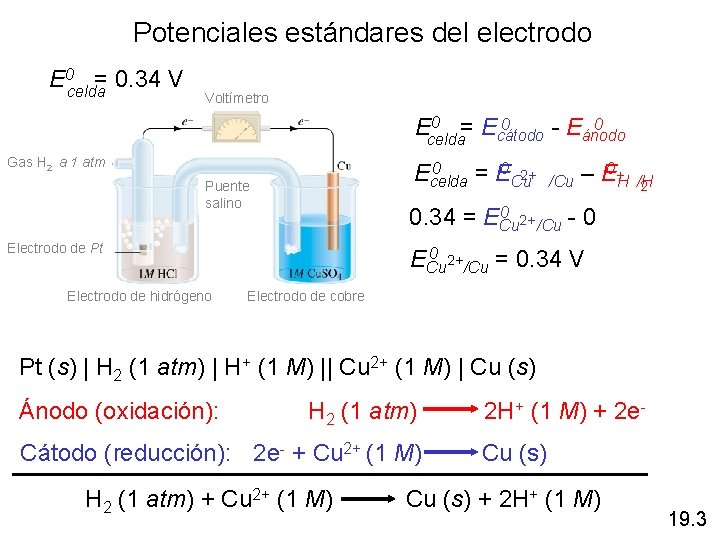
Potenciales estándares del electrodo E 0 celda = 0. 34 V Voltímetro 0 = E 0 0 Ecelda cátodo - Eánodo Gas H 2 a 1 atm 0 Ecelda = E 0 Cu 2+ Puente salino 0 2+ 0. 34 = ECu /Cu - 0 Electrodo de Pt Electrodo de hidrógeno 0 /Cu – E+H /H 2 0 2+ ECu /Cu = 0. 34 V Electrodo de cobre Pt (s) | H 2 (1 atm) | H+ (1 M) || Cu 2+ (1 M) | Cu (s) Ánodo (oxidación): H 2 (1 atm) 2 H+ (1 M) + 2 e- Cátodo (reducción): 2 e- + Cu 2+ (1 M) Cu (s) H 2 (1 atm) + Cu 2+ (1 M) Cu (s) + 2 H+ (1 M) 19. 3

• E 0 es para la reacción como lo escrito • Cuanto más positivo E 0 mayor será la tendencia de la sustancia a reducirse • Las reacciones de semicelda son reversibles • El signo de E 0 cambia cuando la reacción se invierte • Si se cambia los coeficientes estequiométricos de una reacción de semicelda no cambia el valor de E 0 19. 3

¿Cuál es el fem estándar de una celda electroquímica formada de un electrodo de Cd en una disolución 1. 0 M de Cd (NO 3)2 y un electrodo de Cr en una disolución 1. 0 M de Cr(NO 3)3? Cd 2+ (ac) + 2 e- Cd (s) E 0 = -0. 40 V Cd es el oxidante más fuerte Cr 3+ (ac) + 3 e- Cr (s) E 0 = -0. 74 V Cd oxidará Cr Ánodo (oxidación): Cr (s) Cr 3+ (1 M) + 3 e- x 2 Cátodo (reducción): 2 e- + Cd 2+ (1 M) Cd (s) x 3 2 Cr (s) + 3 Cd 2+ (1 M) 3 Cd (s) + 2 Cr 3+ (1 M) 0 0 = E 0 Ecelda cátodo - Eánodo 0 = -0. 40 – (-0. 74) Ecelda 0 = 0. 34 V Ecelda 19. 3

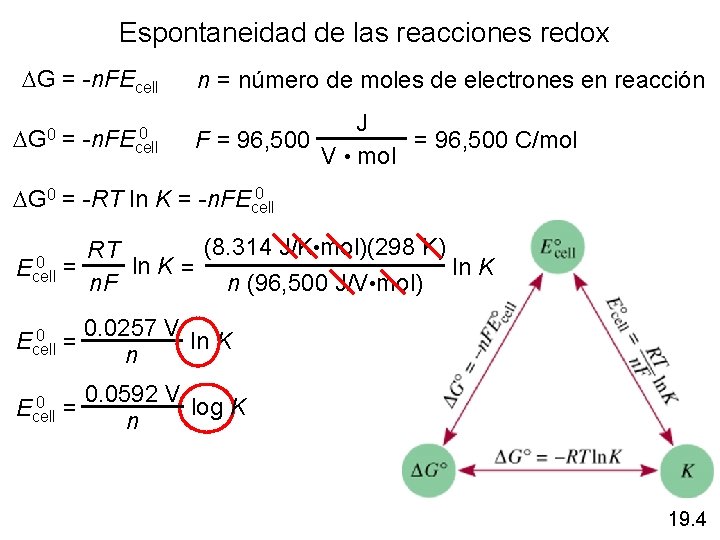
Espontaneidad de las reacciones redox DG = -n. FEcell 0 DG 0 = -n. FEcell n = número de moles de electrones en reacción J F = 96, 500 C/mol V • mol 0 DG 0 = -RT ln K = -n. FEcell (8. 314 J/K • mol)(298 K) RT 0 = ln K Ecell n. F n (96, 500 J/V • mol) 0 Ecell = 0 Ecell 0. 0257 V ln K n 0. 0592 V log K = n 19. 4

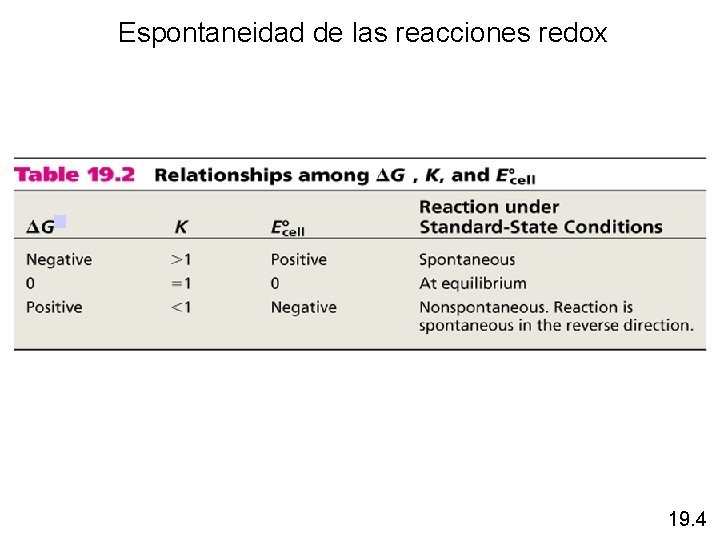
Espontaneidad de las reacciones redox 19. 4

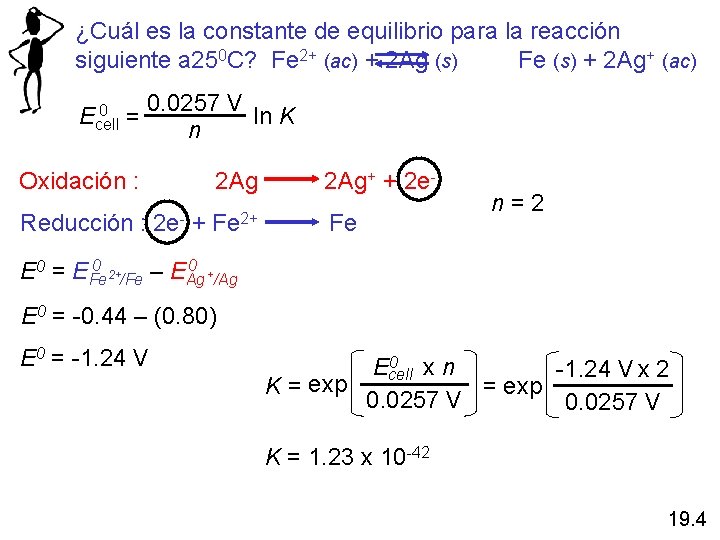
¿Cuál es la constante de equilibrio para la reacción siguiente a 250 C? Fe 2+ (ac) + 2 Ag (s) Fe (s) + 2 Ag+ (ac) 0 Ecell = 0. 0257 V ln K n Oxidación : Reducción : 2 Ag+ + 2 e 2 e- + Fe 2+ Fe n = 2 0 0 E 0 = EFe 2+/Fe – EAg +/Ag E 0 = -0. 44 – (0. 80) E 0 = -1. 24 V 0 x n Ecell -1. 24 V x 2 exp = exp K = 0. 0257 V K = 1. 23 x 10 -42 19. 4

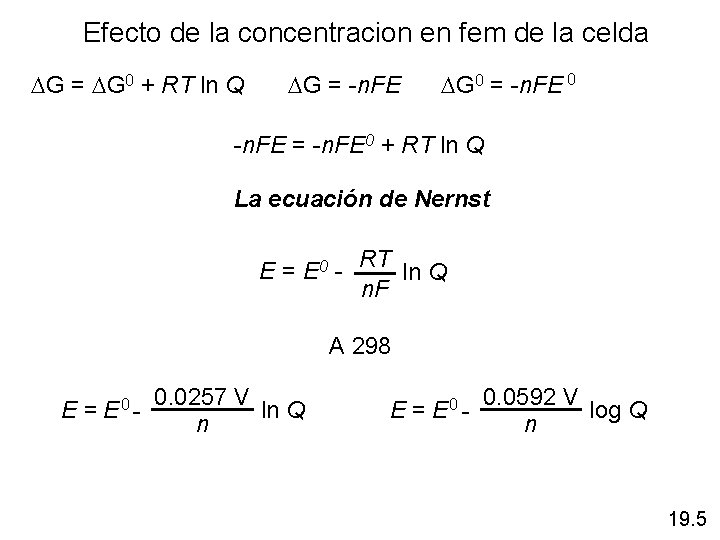
Efecto de la concentracion en fem de la celda DG = DG 0 + RT ln Q DG = -n. FE DG 0 = -n. FE 0 -n. FE = -n. FE 0 + RT ln Q La ecuación de Nernst E = E 0 - RT ln Q n. F A 298 E = E 0 - 0. 0257 V ln Q n E = E 0 - 0. 0592 V log Q n 19. 5
![Ocurrirá la siguiente reacción en forma espontánea a 250 C si Fe 2 Ocurrirá la siguiente reacción en forma espontánea a 250 C si [Fe 2+] =](https://slidetodoc.com/presentation_image_h/b7a24878c02a85420377885857fe465e/image-20.jpg)
Ocurrirá la siguiente reacción en forma espontánea a 250 C si [Fe 2+] = 0. 60 M y [Cd 2+] = 0. 010 M? Fe 2+ (aq) + Cd (s) Fe (s) + Cd 2+ (aq) Oxidación : Reducción : Cd 2+ + 2 e 2 e- + Fe 2+ 2 Fe n = 2 0 0 E 0 = EFe 2+/Fe – ECd 2+/Cd E 0 = -0. 44 – (-0. 40) E 0 = -0. 04 V 0. 0257 V ln Q n 0. 010 0. 0257 V ln E = -0. 04 V 2 0. 60 E = 0. 013 E = E 0 - E > 0 Espontánea 19. 5

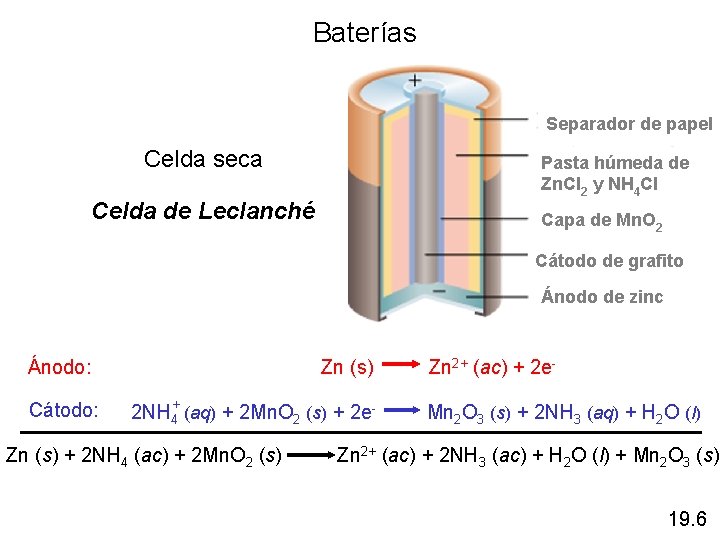
Baterías Separador de papel Celda seca Celda de Leclanché Pasta húmeda de Zn. Cl 2 y NH 4 Cl Capa de Mn. O 2 Cátodo de grafito Ánodo de zinc Ánodo: Cátodo: Zn (s) Zn 2+ (ac) + 2 e 2 NH 4+ (aq) + 2 Mn. O 2 (s) + 2 e- Mn 2 O 3 (s) + 2 NH 3 (aq) + H 2 O (l) Zn (s) + 2 NH 4 (ac) + 2 Mn. O 2 (s) Zn 2+ (ac) + 2 NH 3 (ac) + H 2 O (l) + Mn 2 O 3 (s) 19. 6

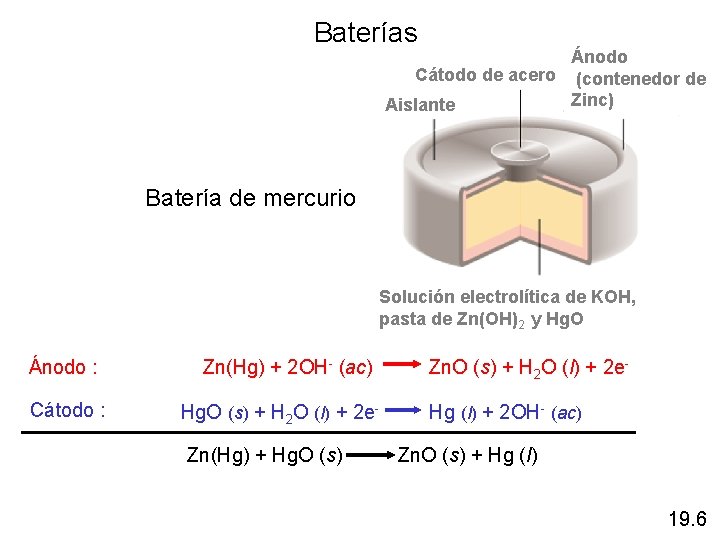
Baterías Ánodo Cátodo de acero (contenedor de Zinc) Aislante Batería de mercurio Solución electrolítica de KOH, pasta de Zn(OH)2 y Hg. O Ánodo : Cátodo : Zn(Hg) + 2 OH- (ac) Zn. O (s) + H 2 O (l) + 2 e. Hg. O (s) + H 2 O (l) + 2 e- Hg (l) + 2 OH- (ac) Zn(Hg) + Hg. O (s) Zn. O (s) + Hg (l) 19. 6

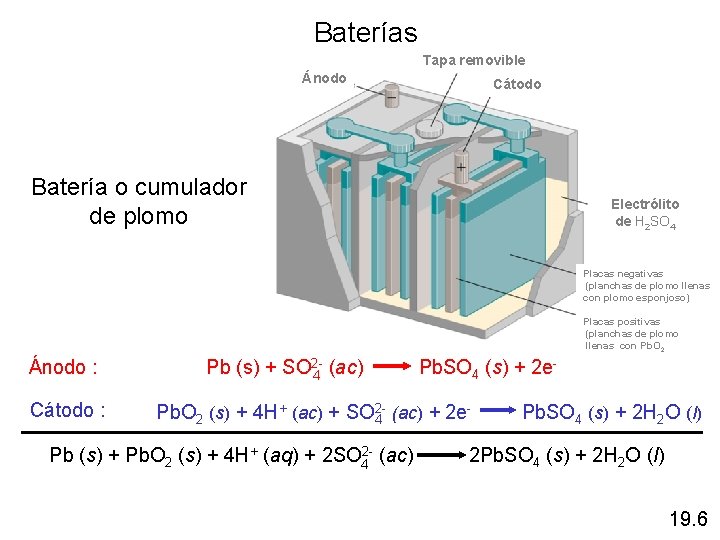
Baterías Tapa removible Ánodo Cátodo Batería o cumulador de plomo Electrólito de H 2 SO 4 Placas negativas (planchas de plomo llenas con plomo esponjoso) Placas positivas (planchas de plomo llenas con Pb. O 2 Ánodo : Cátodo : Pb (s) + SO 2 -4 (ac) Pb. SO 4 (s) + 2 e. Pb. O 2 (s) + 4 H+ (ac) + SO 24 (ac) + 2 e Pb. SO 4 (s) + 2 H 2 O (l) Pb (s) + Pb. O 2 (s) + 4 H+ (aq) + 2 SO 42 - (ac) 2 Pb. SO 4 (s) + 2 H 2 O (l) 19. 6

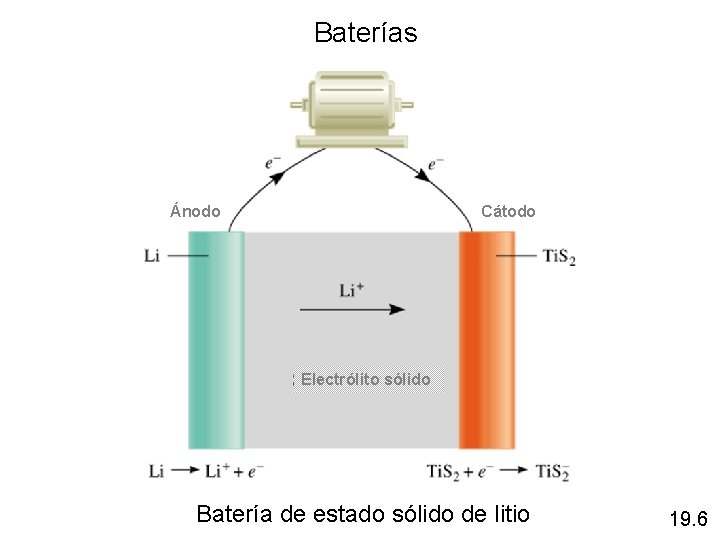
Baterías Ánodo Cátodo Electrólito sólido Batería de estado sólido de litio 19. 6

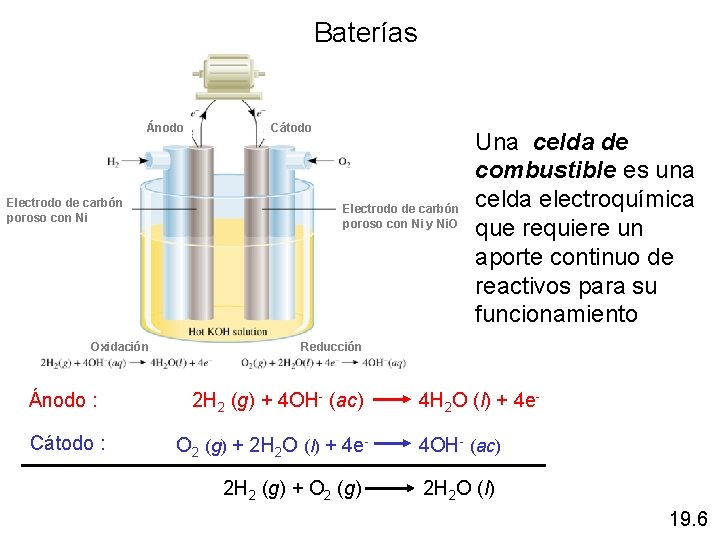
Baterías Ánodo Electrodo de carbón poroso con Ni Oxidación Ánodo : Cátodo Electrodo de carbón poroso con Ni y Ni. O Una celda de combustible es una celda electroquímica que requiere un aporte continuo de reactivos para su funcionamiento Reducción 2 H 2 (g) + 4 OH- (ac) 4 H 2 O (l) + 4 e. O 2 (g) + 2 H 2 O (l) + 4 e- 4 OH- (ac) 2 H 2 (g) + O 2 (g) 2 H 2 O (l) 19. 6

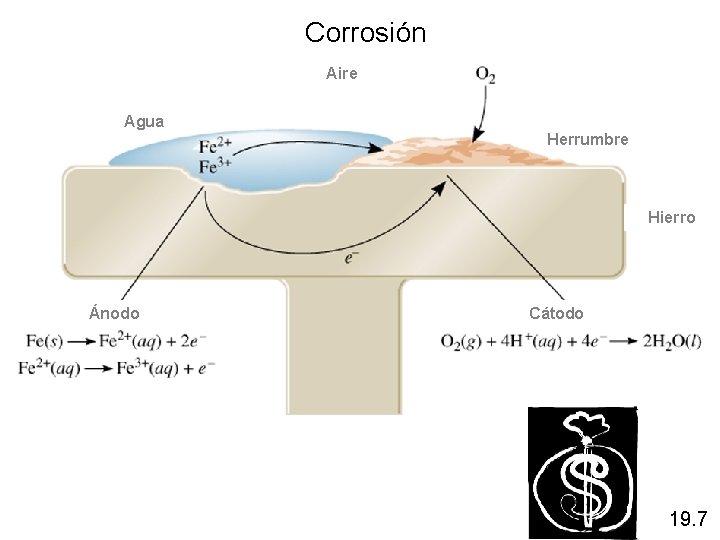
Corrosión Aire Agua Herrumbre Hierro Ánodo Cátodo 19. 7

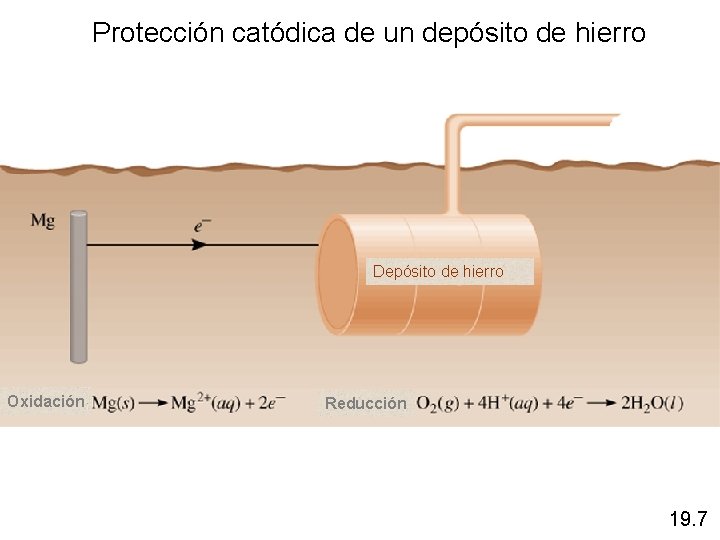
Protección catódica de un depósito de hierro Depósito de hierro Oxidación Reducción 19. 7

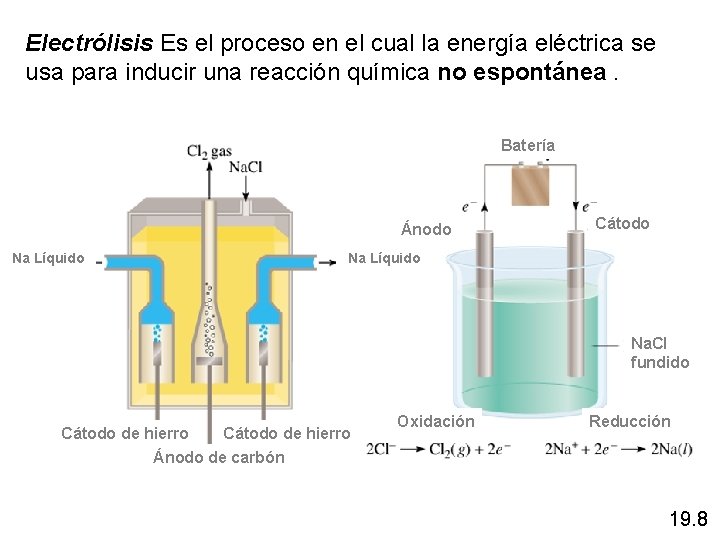
Electrólisis Es el proceso en el cual la energía eléctrica se usa para inducir una reacción química no espontánea. Batería Ánodo Na Líquido Cátodo Na Líquido Na. Cl fundido Cátodo de hierro Ánodo de carbón Oxidación Reducción 19. 8

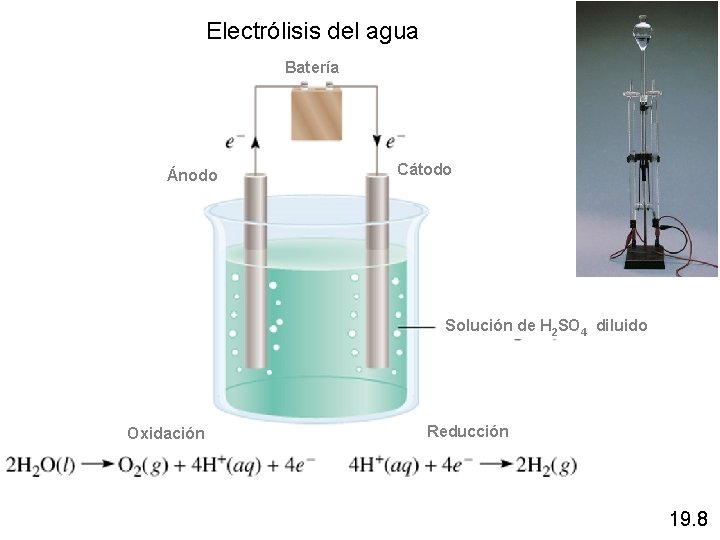
Electrólisis del agua Batería Ánodo Cátodo Solución de H 2 SO 4 diluido Oxidación Reducción 19. 8

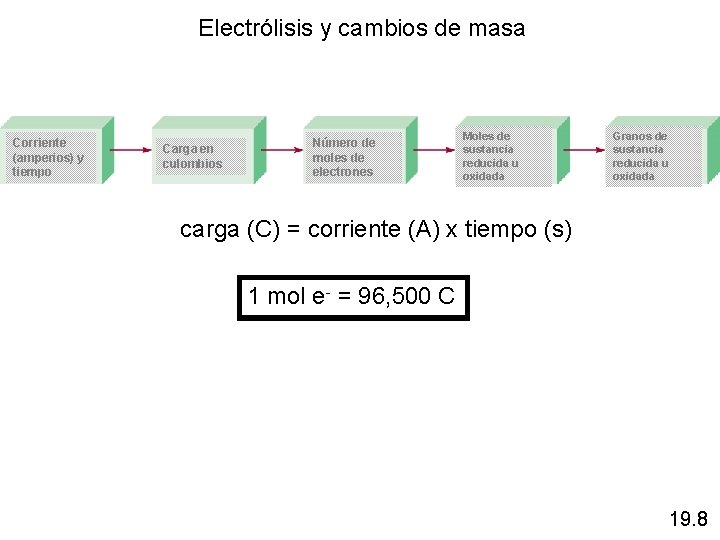
Electrólisis y cambios de masa Corriente (amperios) y tiempo Carga en culombios Número de moles de electrones Moles de sustancia reducida u oxidada Granos de sustancia reducida u oxidada carga (C) = corriente (A) x tiempo (s) 1 mol e- = 96, 500 C 19. 8

¿Cuánto Ca se producirá en una celda electrolítica de Ca. Cl 2 fundido si una corriente de 0. 452 UN se pasa a través de la celda durante 1. 5 horas? Ánodo : Cátodo : 2 Cl- (l) Cl 2 (g) + 2 e. Ca 2+ (l) + 2 e- Ca (s) Ca 2+ (l) + 2 Cl- (l) Ca (s) + Cl 2 (g) 2 mol e- = 1 mol Ca C s 1 mol e- 1 mol Ca = 0. 452 x 1. 5 hr x 3600 x x s hr 96, 500 C 2 mol e= 0. 0126 mol Ca = 0. 50 g Ca 19. 8