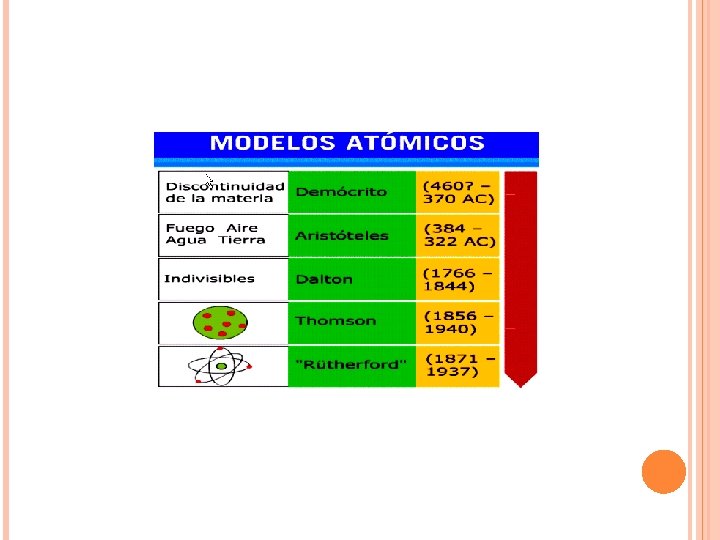
EL TOMO DIVISIBLE Modelos atmicos Profesora Yamileth Hernndez

EL ÁTOMO DIVISIBLE Modelos atómicos Profesora Yamileth Hernández

OBJETIVOS: VALORAR LA IMPORTANCIA HISTÓRICA DE LOS MODELOS ATÓMICOS. Profesora Yamileth Hernández COMPRENDER LA DESCRIPCIÓN ELEMENTAL DE ALGUNOS MODELOS ATÓMICOS PRECURSORES DE LA TEORÍA ATÓMICA MODERNA DEL ÁTOMO.

Profesora Yamileth Hernández ¿CÓMO ES LA ESTRUCTURA DEL ÁTOMO? , ¿QUÉ PARTÍCULAS TIENE? , ¿CUÁLES SON SUS CARACTERÍSTICAS? , ¿CÓMO ESTÁN ORGANIZADAS?
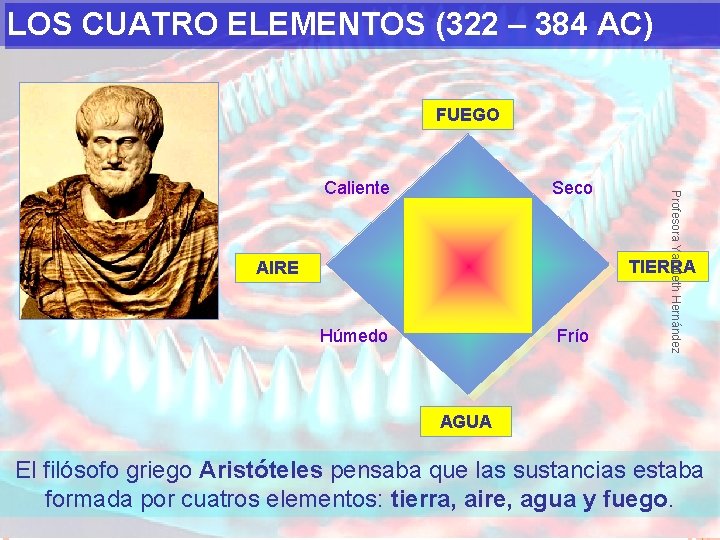
LOS CUATRO ELEMENTOS (322 – 384 AC) FUEGO Seco Profesora Yamileth Hernández Caliente TIERRA AIRE Húmedo Frío AGUA El filósofo griego Aristóteles pensaba que las sustancias estaba formada por cuatros elementos: tierra, aire, agua y fuego.

Profesora Yamileth Hernández

Profesora Yamileth Hernández

Profesora Yamileth Hernández

MODELO DE THOMSON (1904) Profesora Yamileth Hernández Modelo de sandía o budín de pasas: Imaginó al átomo (10 -8 cm) como un globo formado por una masa fluida con carga positiva; los electrones, de masa despreciable y carga negativa, estarían incrustados en esa masa fluida.

MODELO DE RUTHERFORD (1911) Si imaginamos un átomo con las dimensiones de un estadio de fútbol, su núcleo sería del tamaño de una canica colocada en el centro. Profesora Yamileth Hernández Imaginó a los átomos (10 -8 cm) casi vacíos, con la carga positiva concentrada en una zona llamada núcleo (1013 cm) y los electrones dando vueltas en torno a él.

DESCUBRIMIENTO DEL PROTÓN: RUTHERFORD, 1919 Observó que al bombardear distintos átomos (N, B, Ne, F, Na…) con partículas alfa, se emitían partículas positivas. • Esas partículas eran idénticas a las que se producían cuando se arrancaban electrones de los átomos de hidrógeno. • Emitió la siguiente hipótesis: todos los núcleos contienen núcleos de hidrógeno, a los que llamó protones. Profesora Yamileth Hernández •

RESUMEN DEL MODELO ATÓMICO DE RUTHERFORD En el centro de cada átomo hay un núcleo donde está concentrada toda la masa, y que tiene carga positiva (protones y neutrones). § Alrededor del núcleo se encuentran los electrones, de carga negativa y masa despreciable. Los electrones en su órbita tienen una energía, que es menor cuanto más cerca del núcleo se encuentren. § Cada elemento está caracterizado por su número atómico (Z) que indica el nº de protones. Si el átomo es neutro, ese será también su número de electrones § El nº de partículas en el núcleo es el número másico (A) Profesora Yamileth Hernández §

PERO EL MODELO DE RUTHERFORD NO EXPLICA… Los átomos de un mismo grupo no se parecen ni en su masa ni en su número atómico. ¿En qué se parecen entonces? , ¿por qué se combina de forma tan parecida con otros elementos? § Átomos de parecida masa atómica y número atómico (F y Na), (Cl y K), ¿por qué se comportan de forma tan distinta? Profesora Yamileth Hernández §

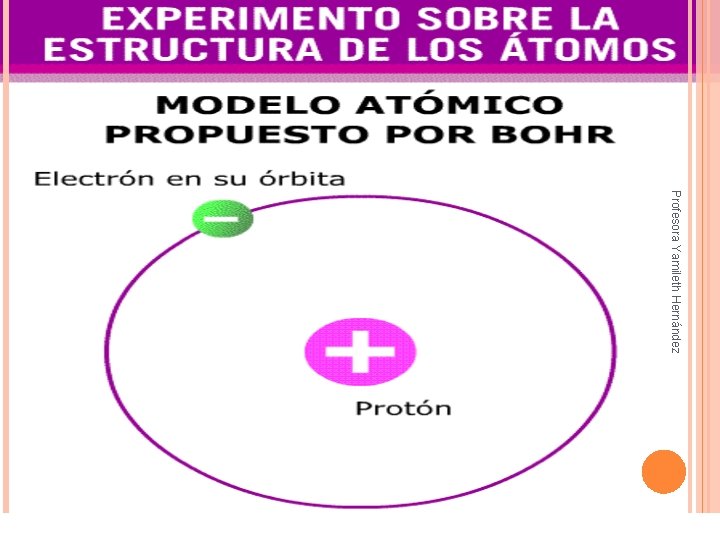
MODELO DE BOHR: COMPLETA EL MODELO DE RUTHERFORD ü Para ü Mientras un electrón se encuentra en una órbita, no absorbe ni emite energía alguna. ü Sólo cuando un electrón pasa de una órbita a otra es cuando absorbe o emite energía Profesora Yamileth Hernández cada tipo de átomos, sólo existen ciertas órbitas de radio permitido. Sólo están permitidos ciertos valores de la energía del electrón en el átomo.
Profesora Yamileth Hernández

ÓRBITAS PERMITIDAS EN EL ÁTOMO DE HIDRÓGENO Representación de las órbitas distancia 1 0, 53 Å 2 2, 12 Å 3 4, 76 Å 4 8, 46 Å 5 13, 22 Å 6 19, 05 Å n=1 Primer nivel de energía permitido n=2 Segundo nivel de energía permitido …. Profesora Yamileth Hernández n

MODELO CUÁNTICO ACTUAL Los electrones no son simples corpúsculos que siguen trayectorias determinadas § No se habla de órbitas sino de orbitales: zona en la que hay mayor probabilidad de encontrar un electrón Profesora Yamileth Hernández §
Profesora Yamileth Hernández

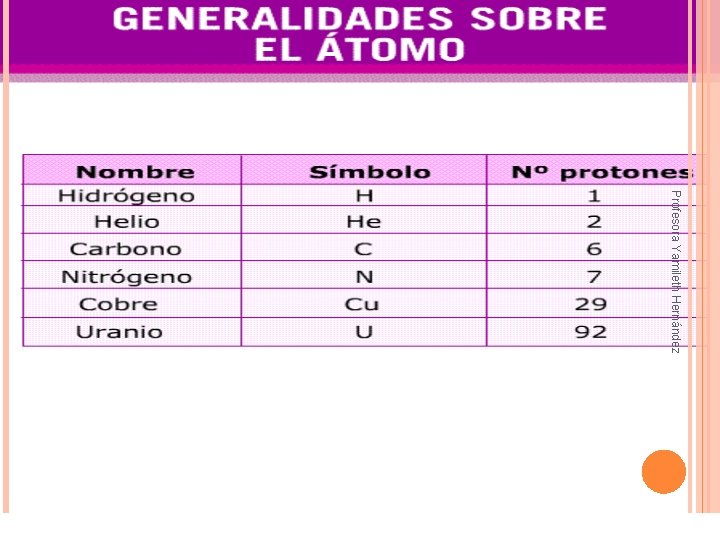
NÚMERO ATÓMICO (Z) • Corresponde al número total de protones presente en el núcleo. z X Ej Na 11 Profesora Yamileth Hernández Z = número de protones (p+)
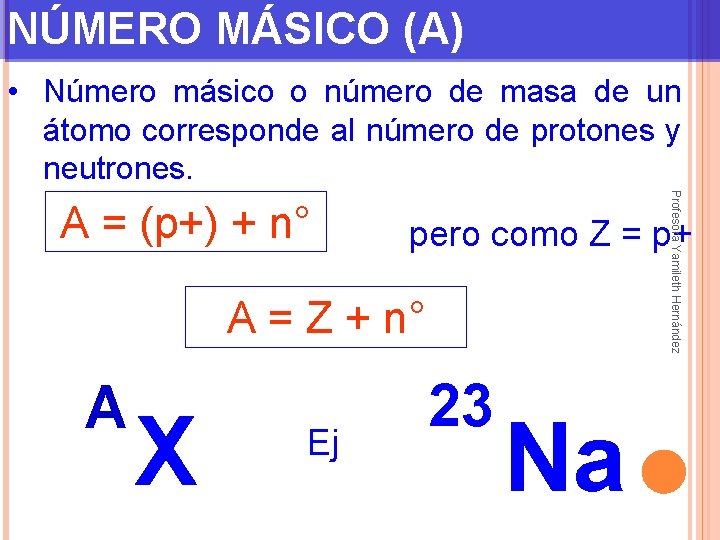
NÚMERO MÁSICO (A) • Número másico o número de masa de un átomo corresponde al número de protones y neutrones. Profesora Yamileth Hernández A = (p+) + n° pero como Z = p+ A = Z + n° A X Ej 23 Na

EN RESUMEN Profesora Yamileth Hernández

EJERCICIOS: 1. Completa los siguientes datos: 7 3 4 3 Profesora Yamileth Hernández 3

ISÓTOPO Ejemplo: Isótopos del elemento Hidrógeno. Nombre Protio Deuterio Tritio Protones 1 1 1 Neutrones 0 1 2 (Animación) Z 1 1 1 A 1 2 3 Profesora Yamileth Hernández • Átomos perteneciente a un mismo elemento que conservan el número atómico (n° de protones), pero de distinto número másico (debido a la diferencia en el número de neutrones).

Profesora Yamileth Hernández
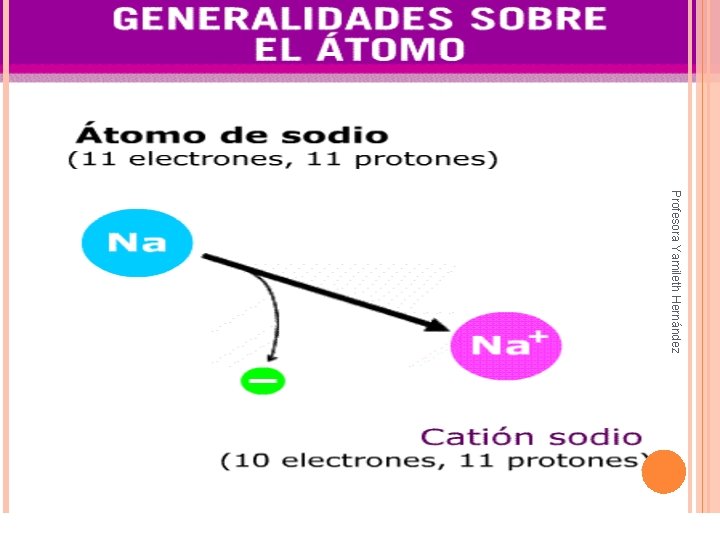
Profesora Yamileth Hernández
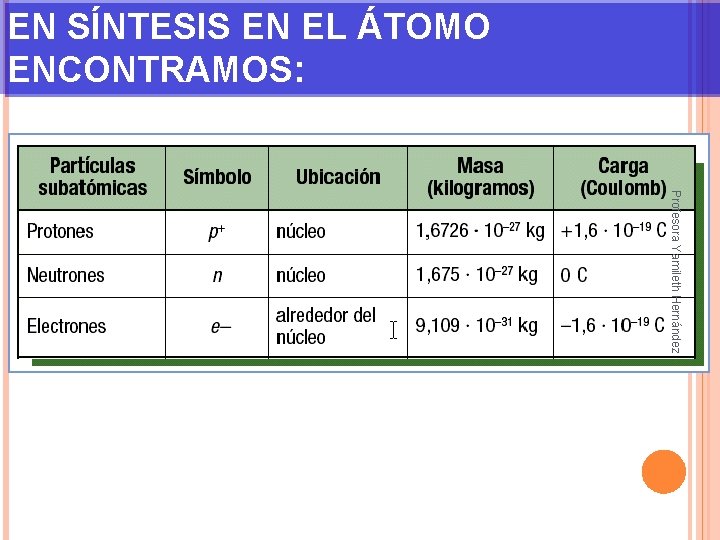
EN SÍNTESIS EN EL ÁTOMO ENCONTRAMOS: Profesora Yamileth Hernández
- Slides: 26