El manejo de los nmeros Profesor Joel Martnez














































- Slides: 47

El manejo de los números Profesor Joel Martínez Reyes Rev. 2011

El manejo de los números a. Con frecuencia los químicos trabajan con números que son muy grandes o muy pequeños. Para evitar errores matemáticos se expresan estos números en notación científica.

El manejo de los números n a. M x 10 en donde, b. M es un número entre 1 y 10 c. n es un exponente que debe ser un número entero positivo o negativo.

Cómo cambiar un número de notación estándar a científica Ejemplo: 1. 0. 00056798 Corres el punto hacia la derecha hasta tener un número ≥ 1 ó <10.

Cómo cambiar un número de notación estándar a científica Luego escribe una multiplicación con base 10 y el exponente es la cantidad de veces que corriste el punto de lugar y el signo de (-) si se mueve el punto hacia la derecha. 00005. 6798 x 10^(-4)

Cómo cambiar un número de notación estándar a científica Ejemplo: b) 0. 0000043 = 4. 3 x 10^(-6)

Cómo cambiar un número de notación estándar a científica Ejemplo: c) 1 987 567 432 Corres el punto hacia la izquierda hasta tener un número ≥ 1 ó <10.

Cómo cambiar un número de notación estándar a científica a. Luego escribe una multiplicación con base 10 y el exponente es la cantidad de veces que corriste el punto de lugar y el signo de (+) si se mueve el punto hacia la izquierda. 1 987 567 432 = 1. 9875 x 10^(9)

Cómo cambiar un número de notación estándar a científica Ejemplo: d) 6 759 = 6. 759 x 10^(3)

Aplicación: Convierte de notación estándar a científica o viceversa 1. 2 325 = 2. 4. 8567 = 3. 625 435 867 = 4. 5 256 734= 5. 367. 342 x 10^3 = 6. 0. 23567 =

Aplicación: Convierte de notación estándar a científica o viceversa 1. 0. 000356 = 2. 0. 000 000 785 = 3. 0. 00657 = 4. 3. 25 x 10^2 = 5. 2. 38 x 10^(-3)


Suma y resta a. Para sumar o restar en notación científica primero se escribe cada cantidad – M- con el mismo exponente n.

Suma y resta Ejemplos: a. (7. 4 x 103) + (2. 1 x 103) = 9. 5 x 103

Suma y resta 1. (4. 31 x 104) + (3. 9 x 103) = (4. 31 x 104) + (0. 39 x 104)= 4. 70 x 104

Multiplicación en notación científica a. Se multiplican los números M, pero los exponentes se suman.

Multiplicación en notación científica Ejemplo: a. (8. 0 x 104) x (5. 0 x 102) = (8. 0 x 5. 0) (104+2) = (40 x 106)= (4. 0 x 107)

División en notación científica a. Se dividen los números M, pero los exponentes se restan.

División en notación científica Ejemplo: (8. 5 x 104) / (5. 0 x 109) = 8. 5 / 5. 0 x 10(4 -9) = 1. 7 x 10 -5

Expresa las siguientes cantidades en notación científica 1. 700 m 2. 38 000 m 3. 4 500 000 m 4. 685 000 000 m

Expresa las siguientes cantidades en notación científica 1. 360 000 s 2. 0. 000 054 3. 5060 s 4. 89 000 000 s

Resuelve y expresa en notación científica a) (5 x 10^(-5) m) + (2 x 10^(-5) m) = b) (7 x 10^(8) m) – (4 x 10^(8) m) = c) (9 x 10^(2) m) – (7 x 10^(2) m) = d) (4 x 10^(-12) m) + (1 x 10^(-12) m) = e) (1. 26 x 10^(4) kg) + (2. 5 x 10^(3) kg =

Resuelve y expresa en notación científica f) (7. 06 x 10^(-3) kg) + (1. 2 x 10^(-4) kg = g) (4. 39 x 10^(5) kg – (2. 8 x 10^(4) kg = h) (5. 36 x 10^(-1) kg) x (7. 40 x 10^(-2) kg = i) (4 x 10^(2) cm) x (1 x 10^(8) cm) = j) (2 x 10^(-4) cm) x (3 x 10^(2) cm) =

Resuelve y expresa en notación científica k) (3 x 10^(1) cm) x (3 x 10^(-2) cm) = l) (1 x 10^(3) cm) x (5 x 10^(-1) cm) = m) (6 x 10^(2) g) ÷ (2 x 10^(1) cm^3) = n) (8 x 10^(4) g) ÷ (4 x 10^(1) cm^3) = g) (9 x 10^(5) g) ÷ (3 x 10^(-1) cm^3) =

Resuelve y expresa en notación científica o) (4 x 10^(-3) g) ÷ (2 x 10^(-2) cm^3) =


Análisis Dimensional a. Supón que tienes una receta para un aderezo de ensalada que requiere dos cucharaditas de vinagre. Planeas hacer 6 veces más aderezo para una fiesta.

Análisis Dimensional 3 cucharaditas = 1 cucharada/3 cucharaditas

Factor de conversión a. Es una razón (relación) de valores equivalentes utilizada para expresar la misma cantidad en unidades diferentes. Un factor de conversión siempres es igual a 1.

Análisis dimensional Es un método de solución de problemas que se centra en las unidades utilizadas para describir la materia.

Ejemplo a. Convertir km a m 48 km x 1000 m = 1 km 48 000 m

Convierte las unidades 1. 360 s =____ms 2. 4800 g = ____kg 3. 5600 dm = ____m 4. 72 g =____ mg

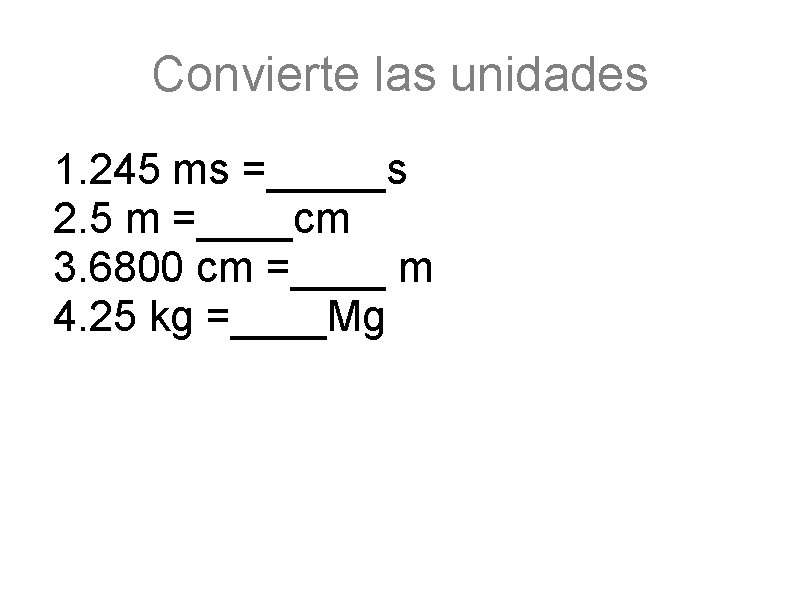
Convierte las unidades 1. 245 ms =_____s 2. 5 m =____cm 3. 6800 cm =____ m 4. 25 kg =____Mg

Problemas Adicionales a. ¿Cuántos segundos hay en 24 horas?

Problemas Adicionales a. La densidad del oro es 19. 3 g/m. L. ¿Cuál es la densidad del oro expresada en decigramos por litro?

Problemas Adicionales a. Un auto viaja a 90 kilómetros por hora. ¿Cuál es la velocidad expresada en millas por minuto? Un kilómetro = 0. 62 millas.


Cifras significativas a. Son los dígitos significativos en una cantidad medida o calculada. b. El mantener el número de cifras significativas me permite tener mayor precisión en los resultados.

Reglas cifras significativas 1. Cualquier dígito diferente de cero es significativo. a. 845 cm - tres cifras significativas • 1. 234 kg – cuatro cifras significativas

Reglas cifras significativas 1. Los ceros ubicados entre dígitos distintos de cero son significativos. a. 606 m - tres cifras significativas • 40, 501 kg – cinco cifras significativas

Reglas cifras significativas 1. Los ceros a la izquierda del primer dígito distinto de cero no son significativos. Estos ceros se utilizan para indicar el lugar del punto decimal. a. 0. 08 L – una cifra significativa • 0. 0000349 – tres cifras significativas

Reglas cifras significativas 4. Si un número es mayor de uno, todos los ceros escritos a la derecha del punto decimal cuentan como cifras significativas. a. 2. 0 mg – dos cifras significativas • 40. 062 m. L – cinco cifras significativas • 3. 040 dm – cuatro cifras significativas

Reglas cifras significativas 5. Si un número es menor que uno, sólo son significativos los ceros que están al final del número o entre dígitos distintos de cero. a. Ejemplo; • 0. 090 kg – dos cifras significativas • 0. 3005 L – 4 cifras significativas

Reglas cifras significativas 6. Para números sin punto decimal, los ceros ubicados después del último dígito distinto de cero pueden ser o no cifras significativas. a. Ejemplo: • 400 cm- una, dos o tres cifras significativas.


Reglas cifras significativas a. Suma y resta a. El número de cifras a la derecha del punto está determinado por el número menor de cifras a la derecha del punto decimal.

Reglas cifras significativas a. Multiplicación y división a. El número de cifras se determina por el número que menos cifras significativas tenga.