EL ENLACE QUMICO Las propiedades caractersticas de las



















- Slides: 28

EL ENLACE QUÍMICO

Las propiedades características de las sustancias están relacionadas con la forma en que están unidas sus partículas y las fuerzas entre ellas, es decir, con el tipo de ENLACE que existe entre sus partículas.


Una primera aproximación para interpretar el enlace Ø A principios del siglo XX, el científico Lewis, observando la poca reactividad de los gases nobles (estructura de 8 electrones en su último nivel), sugirió que los átomos al enlazarse “tienden” a adquirir una distribución de electrones de valencia igual a la del gas noble más próximo REGLA DEL OCTETO

Clasificación de los elementos de acuerdo con la regla del octeto Ø Metales: baja electronegatividad, baja energía de ionización. Tienden a soltar electrones. Ø No metales: alta electronegatividad. Tienden a coger electrones

Según el tipo de átomos que se unen: Ø Metal – No metal: uno cede y otro coge electrones (cationes y aniones) Ø No metal – No metal: ambos cogen electrones, comparten electrones Ø Metal – Metal: ambos ceden electrones

Algunos ejemplos…

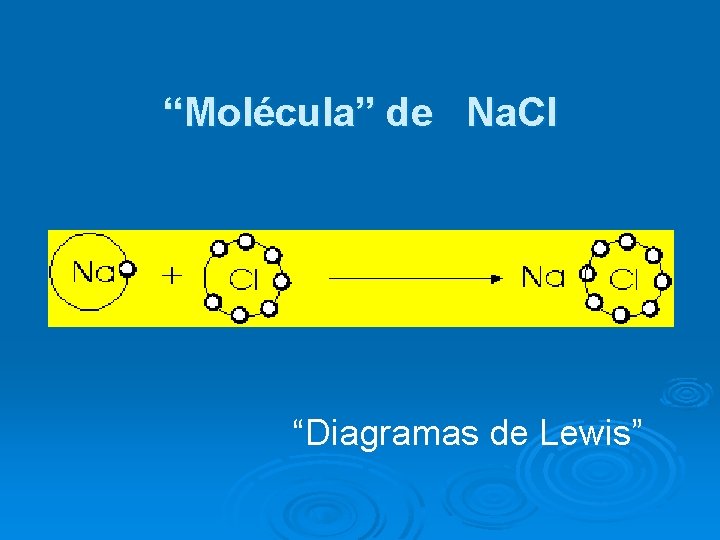
“Molécula” de Na. Cl “Diagramas de Lewis”

“Molécula” de Mg. F 2

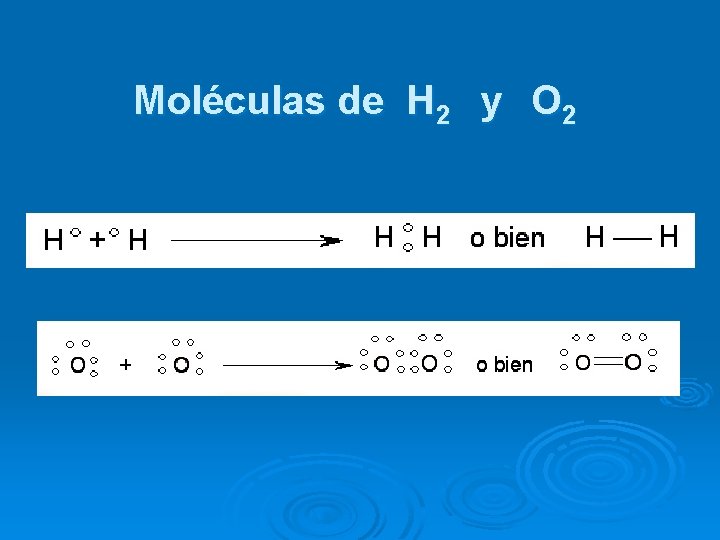
Moléculas de H 2 y O 2

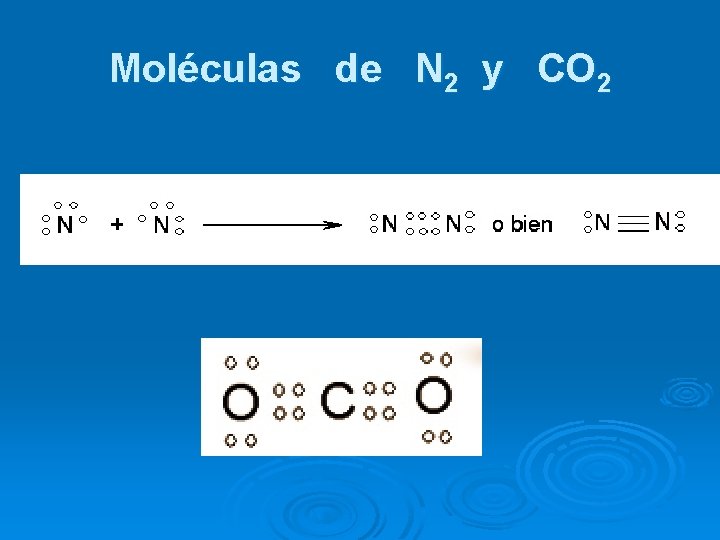
Moléculas de N 2 y CO 2

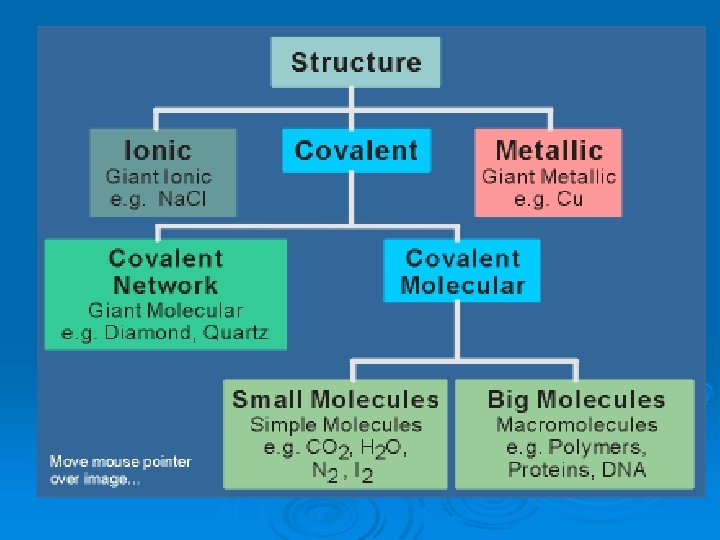
Tipos de enlace ØIónico ØMetálico ØCovalente

Enlace iónico Ø El compuesto iónico se forma al reaccionar un metal con un no metal. Ø Los átomos del metal pierden electrones (se forma un catión) y los acepta el no metal (se forma un anión). Ø Los iones de distinta carga se atraen eléctricamente, se ordenan y forman una red iónica. Los compuestos iónicos no están formados por moléculas.

Enlace iónico entre Cl y Na: formación del ión Cl- y Na+

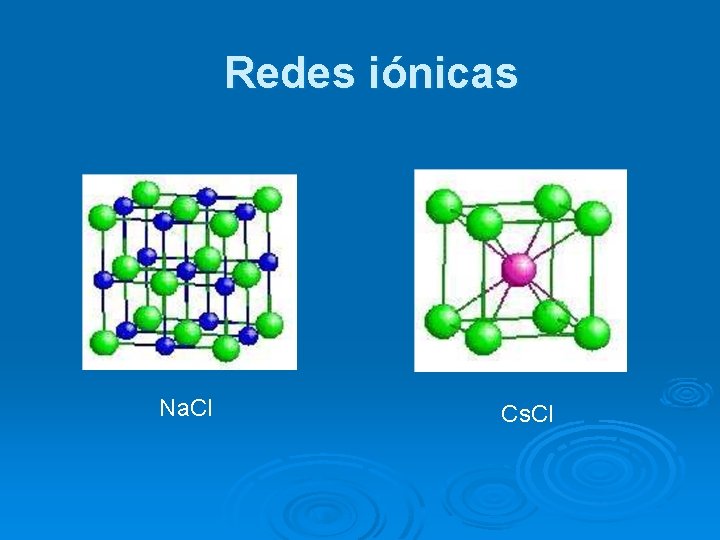
Redes iónicas Na. Cl Cs. Cl

Propiedades compuestos iónicos Ø Elevados puntos de fusión y ebullición Ø Solubles en agua Ø No conducen la electricidad en estado sólido, pero sí en estado disuelto o fundido (Reacción química: electrolisis) Ø Al intentar deformarlos se rompe el cristal (fragilidad)

Enlace metálico Ø Las sustancias metálicas están formadas por átomos de un mismo elemento metálico (baja electronegatividad). Ø Los átomos del elemento metálico pierden algunos electrones, formándose un catión o “resto metálico”. Ø Se forma al mismo tiempo una nube o mar de electrones: conjunto de electrones libres, deslocalizados, que no pertenecen a ningún átomo en particular. Ø Los cationes se repelen entre sí, pero son atraídos por el mar de electrones que hay entre ellos. Se forma así una red metálica: las sustancias metálicas tampoco están formadas por moléculas.

Propiedades sustancias metálicas Ø Elevados puntos de fusión y ebullición Ø Insolubles en agua Ø Conducen la electricidad incluso en estado sólido (sólo se calientan: cambio físico). La conductividad es mayor a bajas temperaturas. Ø Pueden deformarse sin romperse

Enlace covalente Los compuestos covalentes se originan por la compartición de electrones entre átomos no metálicos. Electrones muy localizados.

Diferentes tipos de enlace covalente Ø Enlace covalente normal: l l Simple Múltiple: doble o triple Ø Polaridad del enlace: l l Apolar Polar Ø Enlace covalente dativo o coordinado

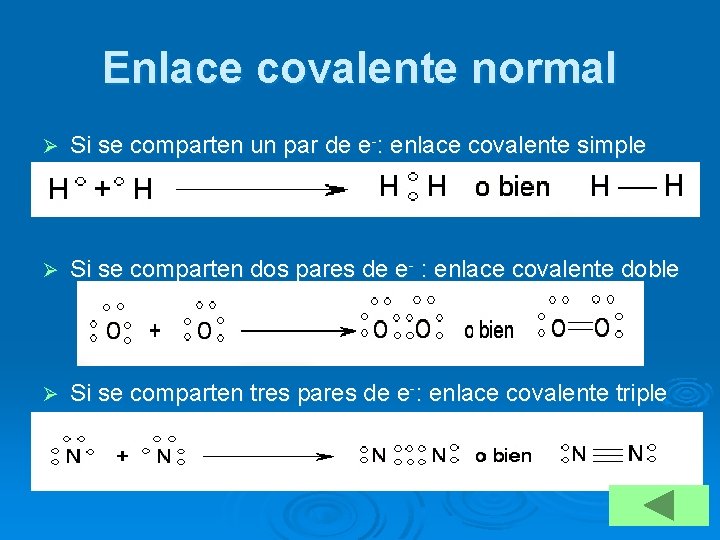
Enlace covalente normal Ø Si se comparten un par de e-: enlace covalente simple Ø Si se comparten dos pares de e- : enlace covalente doble Ø Si se comparten tres pares de e-: enlace covalente triple

Polaridad del enlace covalente Ø Enlace covalente apolar: entre átomos de idéntica electronegatividad (H 2, Cl 2, N 2…). Los electrones compartidos pertenencen por igual a los dos átomos. Ø Enlace covalente polar: entre átomos de distinta electronegatividad (HCl, CO…). Los electrones compartidos están más desplazados hacia el átomo más electronegativo. Aparecen zonas de mayor densidad de carga positiva (δ+) y zonas de mayor densidad de carga negativa (δ-)

Enlace covalente dativo o coordinado Ø Cuando el par de electrones compartidos pertenece sólo a uno de los átomos se presenta un enlace covalente coordinado o dativo. El átomo que aporta el par de electrones se llama donador (siempre el menos electronegativo) y el que los recibe receptor o aceptor (siempre el más electronegativo)

Enlace de átomos de azufre (S) y oxígeno (O) : S ═ O: ˙˙ ˙˙ Molécula de SO: enlace covalente doble Molécula de SO 2: enlace covalente doble y un enlace covalente coordinado o dativo ˙ ˙ ← S ═ O: : O ˙˙ ˙˙ ˙˙ Molécula de SO 3: enlace covalente doble y dos enlaces covalentes coordinado o dativo ˙ ˙ ← S ═ O: : O ↓ ˙˙ ˙˙ : O: ˙˙

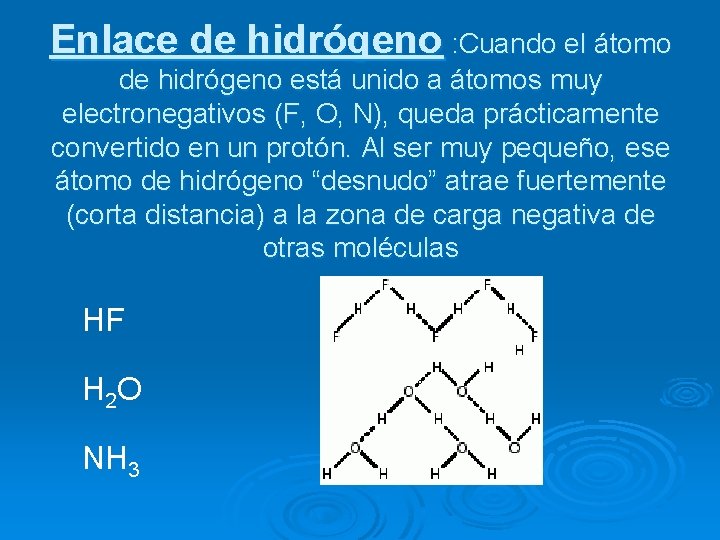
Enlace de hidrógeno : Cuando el átomo de hidrógeno está unido a átomos muy electronegativos (F, O, N), queda prácticamente convertido en un protón. Al ser muy pequeño, ese átomo de hidrógeno “desnudo” atrae fuertemente (corta distancia) a la zona de carga negativa de otras moléculas HF H 2 O NH 3

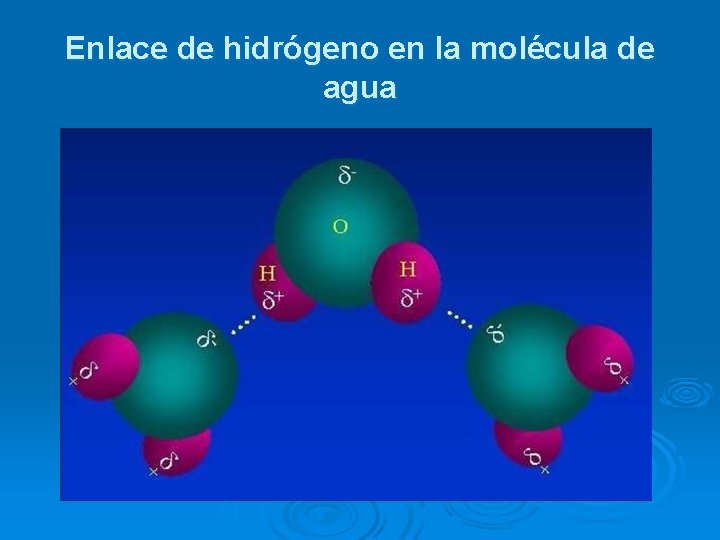
Enlace de hidrógeno en la molécula de agua

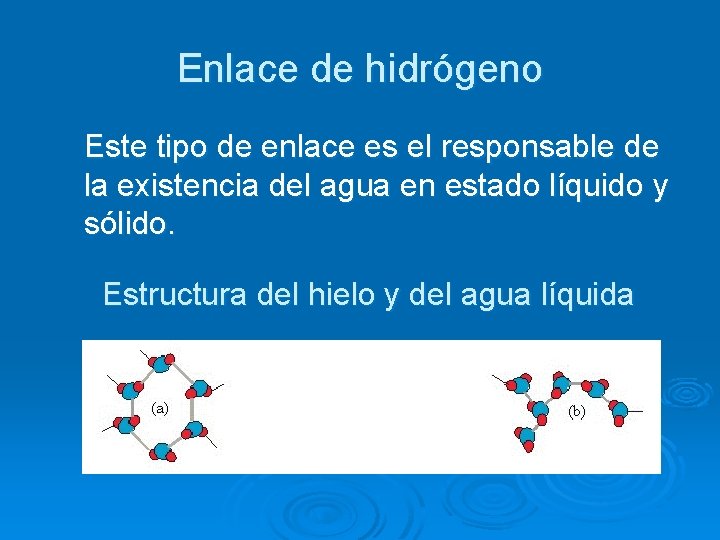
Enlace de hidrógeno Este tipo de enlace es el responsable de la existencia del agua en estado líquido y sólido. Estructura del hielo y del agua líquida

Enlaces de hidrógeno en el ADN Apilamiento de las bases. Esqueleto desoxiribosa fosfato Enlaces de Repul electrostá hidrógeno Bases nitrogenada s A: adenina G: guanina C: citosina T: timina Enlaces de hidrógeno Interior hidrófobo Exteri hidróf