EL ENLACE QUMICO Atomico Macro Atomico Macro Atomico





































- Slides: 57

EL ENLACE QUÍMICO

Atomico Macro

Atomico Macro

Atomico Macro

Atomico Macro

Atomico Macro

Atomico Macro

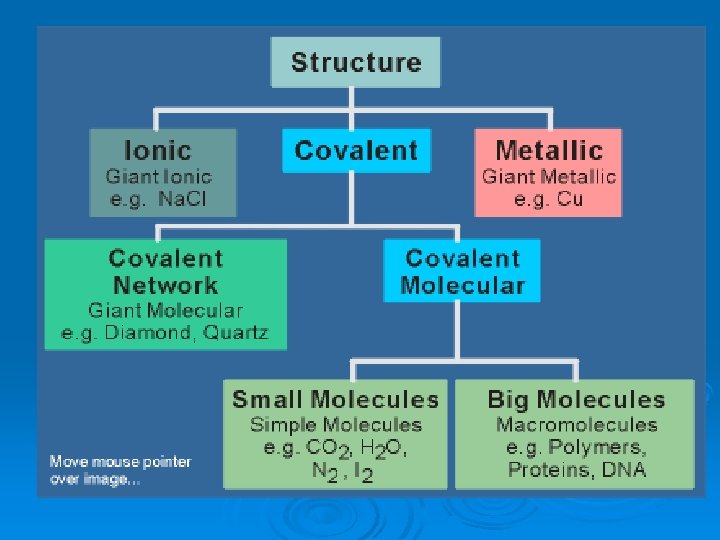
Planteamiento del problema 1. La mina de un lápiz se compone de grafito y arcilla. El grafito es una sustancia simple formada por átomos de carbono. Existe otra sustancia simple formada también por átomos de carbono llamada diamante. ¿Cuál es la causa de que ambas sustancias tengan propiedades tan distintas y sin embargo estén formadas por el mismo tipo de átomo? …

Planteamiento del problema 2. ¿Por qué los átomos se unen en unas proporciones determinadas y no en otras? ¿Por qué Na. Cl y no Na 2 Cl? 3. ¿Qué es lo que determina las propiedades de una sustancia: solubilidad, conductividad eléctrica, estado de agregación a temperatura ambiente…?

¿Por qué se unen los átomos? n Los átomos, moléculas e iones, se unen entre sí porque al hacerlo se llega a una situación de mínima energía, lo que equivale a decir, de máxima estabilidad. n Son los electrones más externos, los también llamados electrones de valencia, los responsables de esta unión.

Las propiedades características de las sustancias están relacionadas con la forma en que están unidas sus partículas y las fuerzas entre ellas, es decir, con el tipo de ENLACE que existe entre sus partículas.


Una primera aproximación para interpretar el enlace Ø A principios del siglo XX, el científico Lewis, observando la poca reactividad de los gases nobles (estructura de 8 electrones en su último nivel), sugirió que los átomos al enlazarse “tienden” a adquirir una distribución de electrones de valencia igual a la del gas noble más próximo REGLA DEL OCTETO

Teoría de Lewis: Los electrones de la capa de valencia juegan un papel fundamental en el enlace químico. Ø En algunos casos se transfieren electrones de un átomo a otro : → enlace iónico. Ø En otros casos se comparten pares de electrones entre los átomos → enlace covalente. Ø Los electrones se transfieren o comparten de manera que los átomos adquieren una configuración electrónica de gas noble Ø Ø → Regla del octeto.

Clasificación de los elementos de acuerdo con la regla del octeto Ø Metales: baja electronegatividad, baja energía de ionización. Tienden a ceder electrones. Ø No metales: alta electronegatividad. Tienden a tomar electrones

Según el tipo de átomos que se unen: Ø Metal – No metal: uno cede y otro toma electrones (cationes y aniones) Ø No metal – No metal: ambos toman electrones, comparten electrones Ø Metal – Metal: ambos ceden electrones

Los símbolos de Lewis son una representación de los átomos de acuerdo con la teoría de Lewis. Consisten en símbolos químicos que representan el núcleo y los electrones internos, junto con puntos alrededor del símbolo que representan los electrones e valencia. Colocamos puntos en los lados del símbolo hasta un máximo de 4 y después emparejamos puntos hasta alcanzar un Octeto.

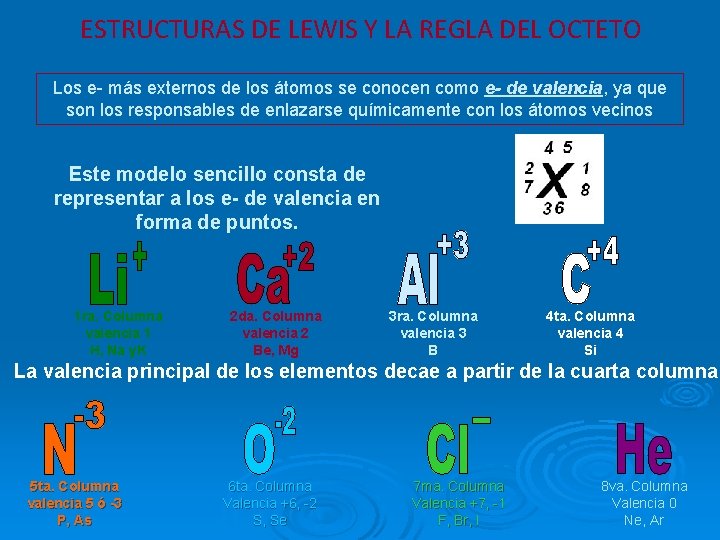
ESTRUCTURAS DE LEWIS Y LA REGLA DEL OCTETO Los e- más externos de los átomos se conocen como e- de valencia, ya que son los responsables de enlazarse químicamente con los átomos vecinos Este modelo sencillo consta de representar a los e- de valencia en forma de puntos. 1 ra. Columna valencia 1 H, Na y. K 2 da. Columna valencia 2 Be, Mg 3 ra. Columna valencia 3 B 4 ta. Columna valencia 4 Si La valencia principal de los elementos decae a partir de la cuarta columna 5 ta. Columna valencia 5 ó -3 P, As 6 ta. Columna Valencia +6, -2 S, Se 7 ma. Columna Valencia +7, -1 F, Br, I 8 va. Columna Valencia 0 Ne, Ar

Algunos ejemplos…

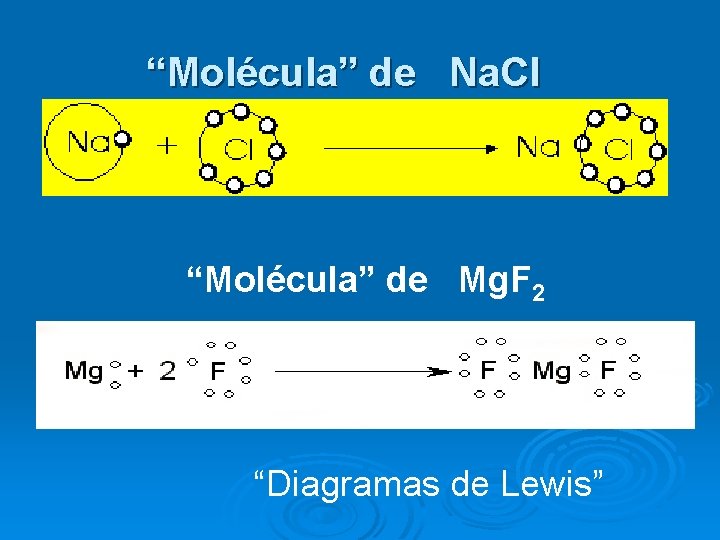
“Molécula” de Na. Cl “Molécula” de Mg. F 2 “Diagramas de Lewis”

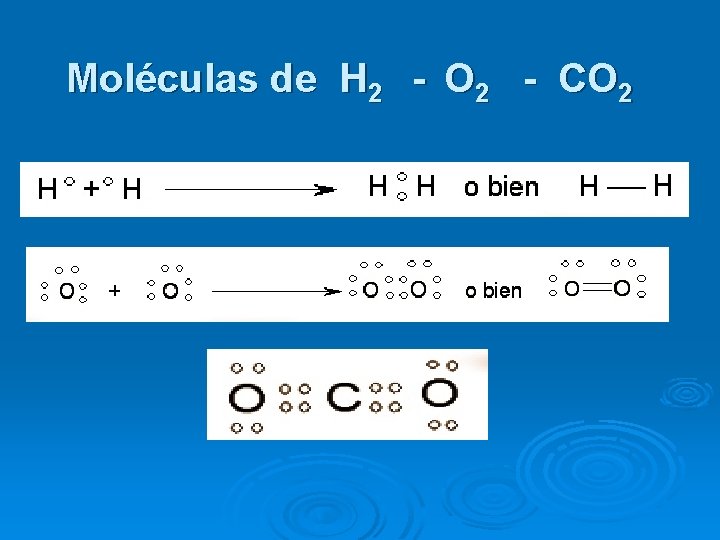
Moléculas de H 2 - O 2 - CO 2

Tipos de enlace ØIónico ØMetálico ØCovalente

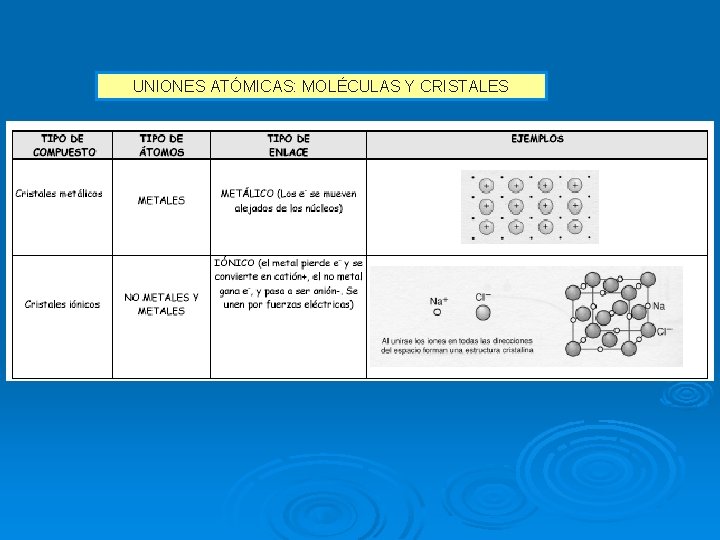
Enlace iónico Ø El compuesto iónico : metal con un no metal. Ø Los átomos del metal pierden electrones (se forma un catión) y los acepta el no metal (se forma un anión). Ø Los iones de distinta carga se atraen eléctricamente, se ordenan y forman una red iónica. Los compuestos iónicos no están formados por moléculas.

Enlace iónico entre Cl y Na: formación del ión Cl- y Na+

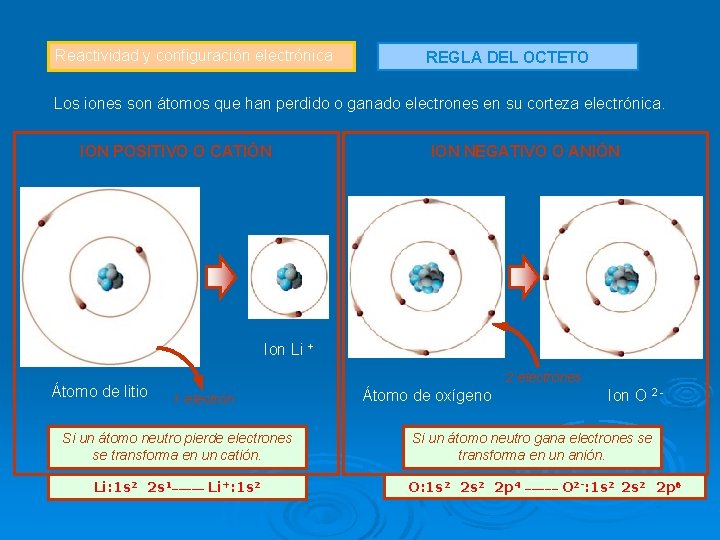
Reactividad y configuración electrónica REGLA DEL OCTETO Los iones son átomos que han perdido o ganado electrones en su corteza electrónica. ION POSITIVO O CATIÓN ION NEGATIVO O ANIÓN Ion Li + Átomo de litio 2 electrónes 1 electrón Si un átomo neutro pierde electrones se transforma en un catión. Li: 1 s 2 2 s 1_____ Li+: 1 s 2 Átomo de oxígeno Ion O 2 - Si un átomo neutro gana electrones se transforma en un anión. O: 1 s 2 2 p 4 _____ O 2 -: 1 s 2 2 p 6

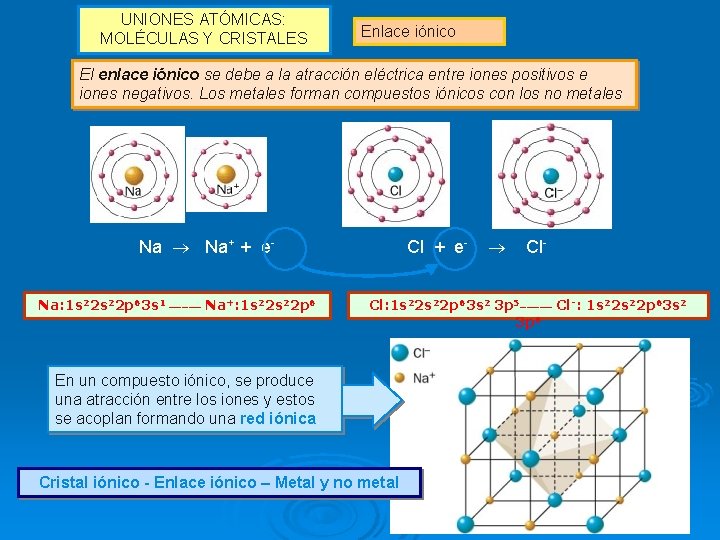
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES Enlace iónico El enlace iónico se debe a la atracción eléctrica entre iones positivos e iones negativos. Los metales forman compuestos iónicos con los no metales. Na+ + e. Na: 1 s 22 p 63 s 1 _____ Na+: 1 s 22 p 6 Cl + e- Cl: 1 s 22 p 63 s 2 3 p 5_____ Cl-: 1 s 22 p 63 s 2 3 p 6 En un compuesto iónico, se produce una atracción entre los iones y estos se acoplan formando una red iónica. Cristal iónico - Enlace iónico – Metal y no metal

Enlace iónico Ejemplo: Mediante el empleo de símbolos de Lewis, represente la reacción entre un átomo de litio y un átomo de fluor para formar Li. F Fórmula empírica: Li. F

Enlace iónico Si el catión y el anión no tienen la misma carga, las cargas se balancean para que el compuesto sea eléctricamente neutro. Li 2 O

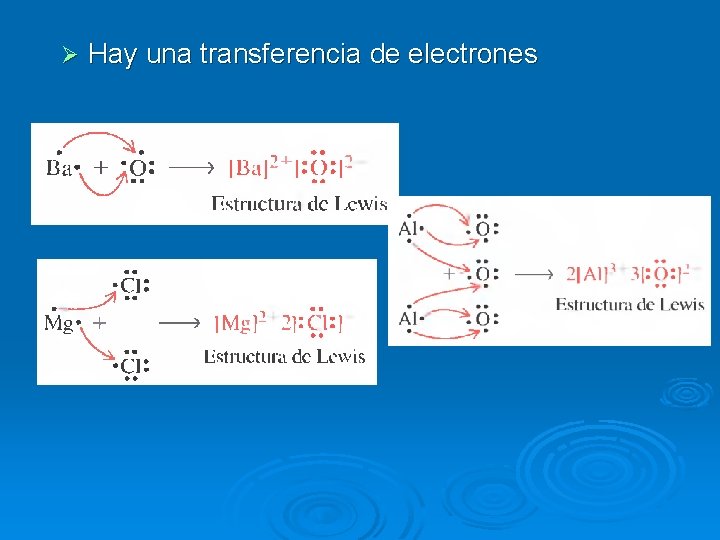
Ø Hay una transferencia de electrones

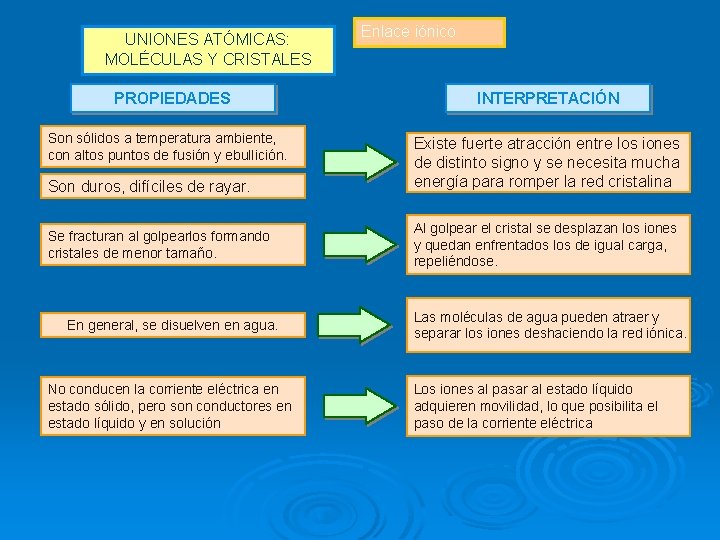
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES PROPIEDADES Son sólidos a temperatura ambiente, con altos puntos de fusión y ebullición. Son duros, difíciles de rayar. Se fracturan al golpearlos formando cristales de menor tamaño. En general, se disuelven en agua. No conducen la corriente eléctrica en estado sólido, pero son conductores en estado líquido y en solución. Enlace iónico INTERPRETACIÓN Existe fuerte atracción entre los iones de distinto signo y se necesita mucha energía para romper la red cristalina. Al golpear el cristal se desplazan los iones y quedan enfrentados los de igual carga, repeliéndose. Las moléculas de agua pueden atraer y separar los iones deshaciendo la red iónica. Los iones al pasar al estado líquido adquieren movilidad, lo que posibilita el paso de la corriente eléctrica.

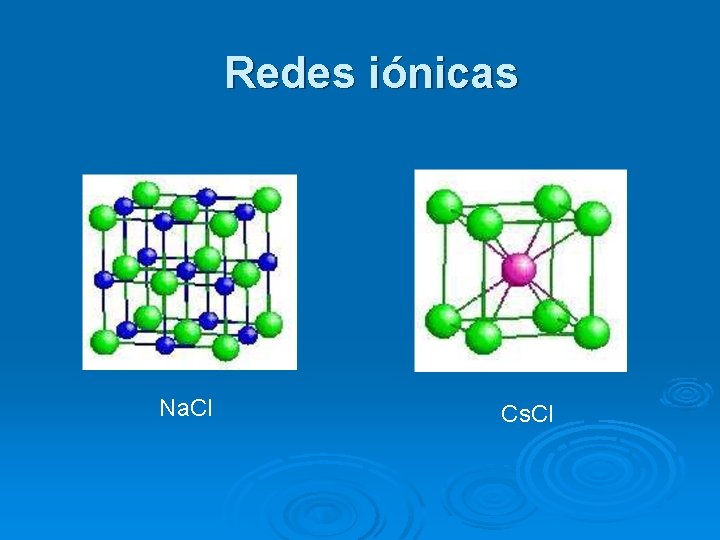
Redes iónicas Na. Cl Cs. Cl

Propiedades compuestos iónicos Ø Elevados puntos de fusión y ebullición Ø Solubles en agua Ø No conducen la electricidad en estado sólido, pero sí en estado disuelto o fundido (Reacción química: electrolisis) Ø Al intentar deformarlos se rompe el cristal (fragilidad)

Enlace metálico Ø Las sustancias metálicas están formadas por átomos de un mismo elemento metálico (baja electronegatividad). Ø Los átomos del elemento metálico pierden algunos electrones, formándose un catión o “resto metálico”. Ø Se forma al mismo tiempo una nube o mar de electrones: conjunto de electrones libres, deslocalizados, que no pertenecen a ningún átomo en particular. Ø Los cationes se repelen entre sí, pero son atraídos por el mar de electrones que hay entre ellos. Se forma así una red metálica: las sustancias metálicas tampoco están formadas por moléculas.

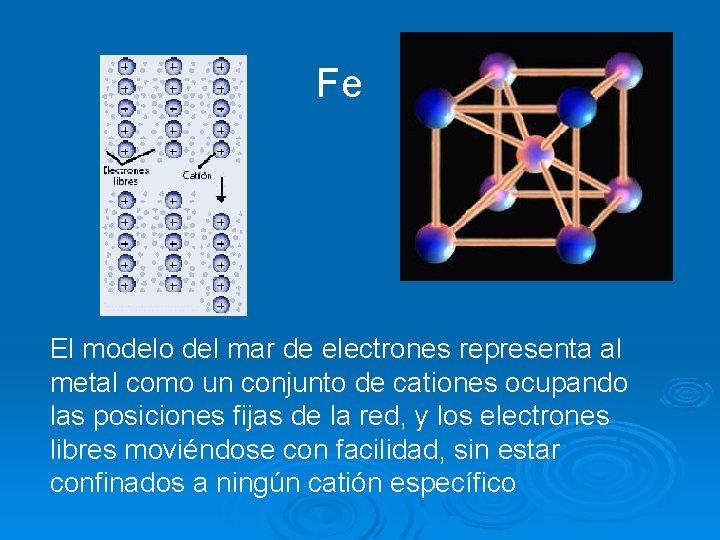
Fe El modelo del mar de electrones representa al metal como un conjunto de cationes ocupando las posiciones fijas de la red, y los electrones libres moviéndose con facilidad, sin estar confinados a ningún catión específico

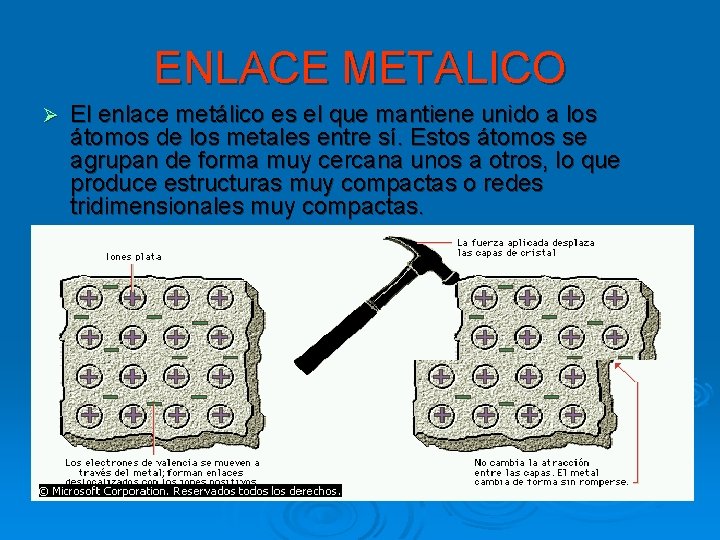
ENLACE METALICO Ø El enlace metálico es el que mantiene unido a los átomos de los metales entre sí. Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas o redes tridimensionales muy compactas.

Propiedades sustancias metálicas Ø Elevados puntos de fusión y ebullición Ø Insolubles en agua Ø Conducen la electricidad incluso en estado sólido (sólo se calientan: cambio físico). La conductividad es mayor a bajas temperaturas. Ø Pueden deformarse sin romperse

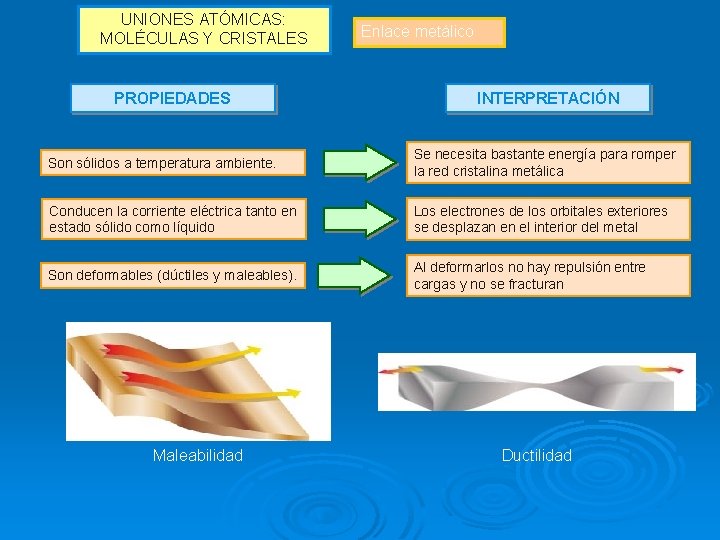
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES PROPIEDADES Enlace metálico INTERPRETACIÓN Son sólidos a temperatura ambiente. Se necesita bastante energía para romper la red cristalina metálica Conducen la corriente eléctrica tanto en estado sólido como líquido Los electrones de los orbitales exteriores se desplazan en el interior del metal Son deformables (dúctiles y maleables). Al deformarlos no hay repulsión entre cargas y no se fracturan Maleabilidad Ductilidad

Enlace covalente Los compuestos covalentes se originan al compartir electrones entre átomos no metálicos. Electrones muy localizados.

Diferentes tipos de enlace covalente Ø Enlace covalente normal: l l Simple Múltiple: doble o triple Ø Polaridad del enlace: l l Apolar Polar Ø Enlace covalente dativo o coordinado

Enlace covalente normal Ø Si se comparten un par de e-: enlace covalente simple Ø Si se comparten dos pares de e- : enlace covalente doble Ø Si se comparten tres pares de e-: enlace covalente triple

Enlace covalente El modelo utilizado para describir estas uniones es la notación de Lewis. Molécula de hidrógeno Molécula de flúor Molécula de cloro Molécula de agua Dos átomos unidos por enlace covalente pueden compartir varios pares de electrones.

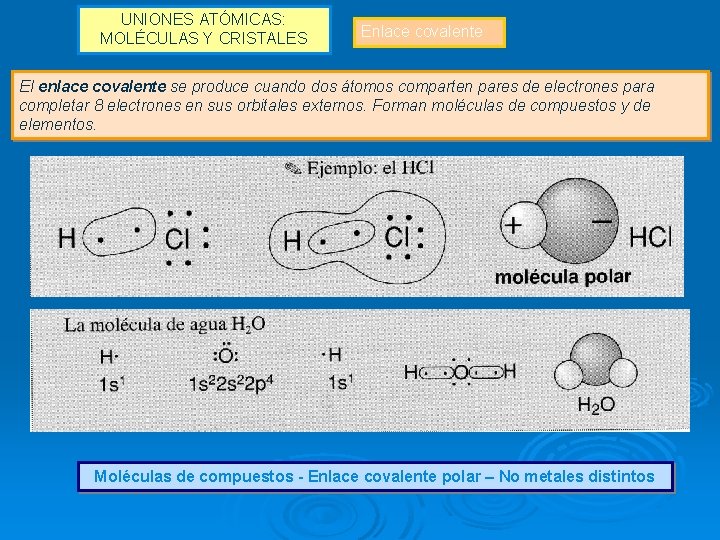
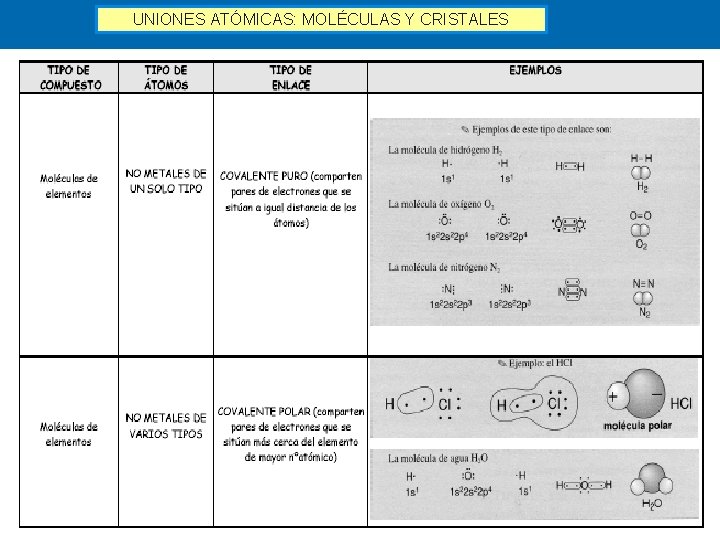
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES Enlace covalente El enlace covalente se produce cuando dos átomos comparten pares de electrones para completar 8 electrones en sus orbitales externos. Forman moléculas de compuestos y de elementos. Moléculas de elementos - Enlace covalente puro – No metales iguales

UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES Enlace covalente El enlace covalente se produce cuando dos átomos comparten pares de electrones para completar 8 electrones en sus orbitales externos. Forman moléculas de compuestos y de elementos. Moléculas de compuestos - Enlace covalente polar – No metales distintos

Polaridad del enlace covalente Ø Enlace covalente apolar: entre átomos de idéntica electronegatividad (H 2, Cl 2, N 2…). Los electrones compartidos pertenencen por igual a los dos átomos. Ø Enlace covalente polar: entre átomos de distinta electronegatividad (HCl, CO…). Los electrones compartidos están más desplazados hacia el átomo más electronegativo. Aparecen zonas de mayor densidad de carga positiva (δ+) y zonas de mayor densidad de carga negativa (δ-)

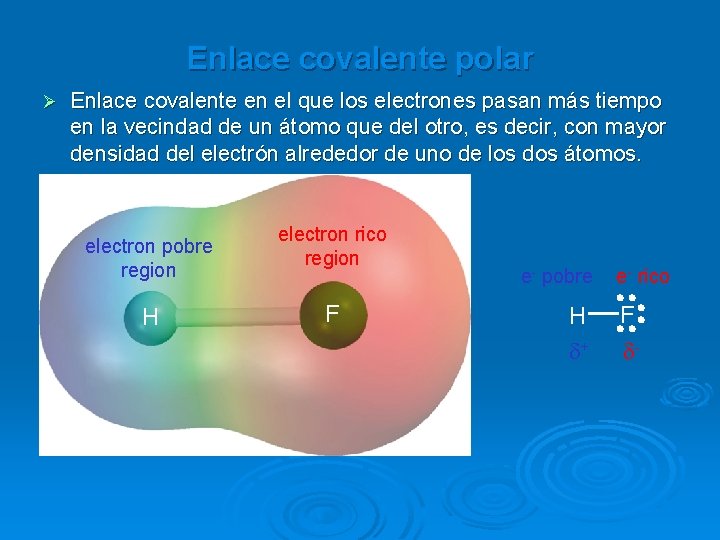
Enlace covalente polar Ø Enlace covalente en el que los electrones pasan más tiempo en la vecindad de un átomo que del otro, es decir, con mayor densidad del electrón alrededor de uno de los dos átomos. electron pobre region H electron rico region F e- pobre H d+ e- rico F d-

UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES

UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES

Enlace covalente dativo o coordinado Ø Cuando el par de electrones compartidos pertenece sólo a uno de los átomos se presenta un enlace covalente coordinado o dativo. El átomo que aporta el par de electrones se llama donador (siempre el menos electronegativo) y el que los recibe receptor o aceptor (siempre el más electronegativo)

Enlace de átomos de azufre (S) y oxígeno (O) : S ═ O: ˙˙ ˙˙ Molécula de SO: enlace covalente doble Molécula de SO 2: enlace covalente doble y un enlace covalente coordinado o dativo ˙ ˙ ← S ═ O: : O ˙˙ ˙˙ ˙˙ Molécula de SO 3: enlace covalente doble y dos enlaces covalentes coordinado o dativo ˙ ˙ ← S ═ O: : O ↓ ˙˙ ˙˙ : O: ˙˙

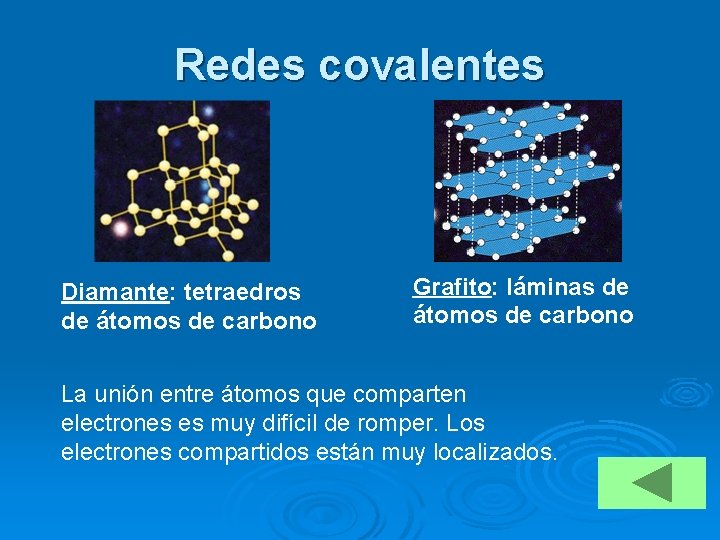
Redes covalentes Diamante: tetraedros de átomos de carbono Grafito: láminas de átomos de carbono La unión entre átomos que comparten electrones es muy difícil de romper. Los electrones compartidos están muy localizados.

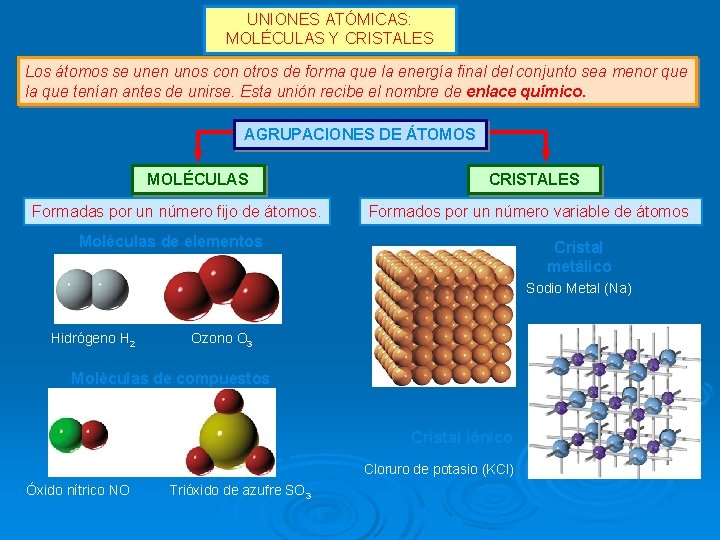
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES Los átomos se unen unos con otros de forma que la energía final del conjunto sea menor que la que tenían antes de unirse. Esta unión recibe el nombre de enlace químico. AGRUPACIONES DE ÁTOMOS MOLÉCULAS Formadas por un número fijo de átomos. CRISTALES Formados por un número variable de átomos. Moléculas de elementos Cristal metálico Sodio Metal (Na) Hidrógeno H 2 Ozono O 3 Moléculas de compuestos Cristal iónico Cloruro de potasio (KCl) Óxido nítrico NO Trióxido de azufre SO 3

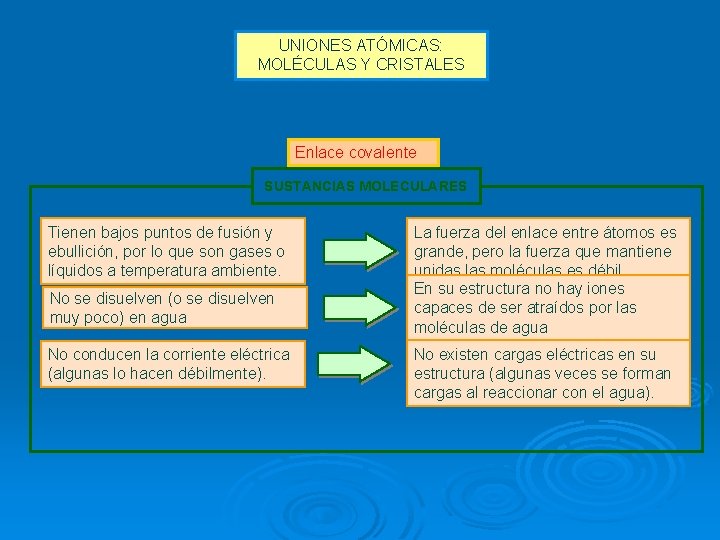
UNIONES ATÓMICAS: MOLÉCULAS Y CRISTALES Enlace covalente SUSTANCIAS MOLECULARES Tienen bajos puntos de fusión y ebullición, por lo que son gases o líquidos a temperatura ambiente. No se disuelven (o se disuelven muy poco) en agua No conducen la corriente eléctrica (algunas lo hacen débilmente). La fuerza del enlace entre átomos es grande, pero la fuerza que mantiene unidas las moléculas es débil. En su estructura no hay iones capaces de ser atraídos por las moléculas de agua No existen cargas eléctricas en su estructura (algunas veces se forman cargas al reaccionar con el agua).

Moléculas covalentes Ø Si el enlace es apolar: moléculas apolares (H 2, O 2, F 2…) Ø Si el enlace es polar: l l Moléculas polares (HCl, H 2 O. . . ) (dipolos permanentes) Moléculas apolares (CO 2) (simetría espacial)

Propiedades compuestos covalentes (moleculares) Ø No conducen la electricidad Ø Solubles: moléculas apolares – apolares Ø Insolubles: moléculas polares - polares Ø Bajos puntos de fusión y ebullición… Ø ¿Fuerzas intermoleculares?

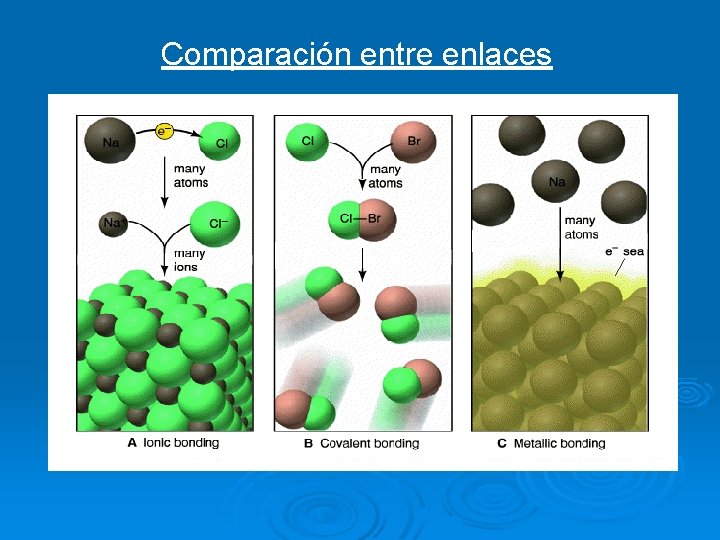
Comparación entre enlaces

Análisis del tipo de enlace más probable. Según el tipo de átomos que forman las sustancia • Enlace iónico: si se produce entre elementos que tienen muy diferente electronegatividad, entre metales (baja electronegatividad) y no metales (alta electronegatividad): • Enlace covalente Si se produce entre elementos que tienen alta electronegatividad pero muy parecida (no metal con no metal). • Enlace metálico: Si se produce entre elementos que tienen baja electronegatividad y muy parecida (metal con metal).

Predicción de tipo de enlace químico Diferencia de electronegatividad Tipo de unión química 0 a 0, 4 Covalente no polar 0, 4 a 1, 7 Covalente polar Más de 1, 7 Iónica Considerar como una guía, no es estricto