El cncer prstata es el cncer ms comnmente



















- Slides: 24


El cáncer próstata es el cáncer más comúnmente diagnosticado y la sexta causa de muerte relacionada con cáncer en hombres en todo el mundo. Las estrategias para bloquear los receptores de andrógenos se han desarrollado desde la descripción de la dependencia hormonal En la mayoría de los pacientes tratados para enfermedad avanzada con terapia de deprivación de andrógenos, la progresión ocurre a pesar de la efectiva supresión de testosterona El cancer de próstata resistente a la castración, siempre se asocia con aumentos en los niveles de PSA, sugiriendo que la enfermedad continúa siendo impulsada por la señalización del receptor de andrógenos

Pruebas preclínicas sugieren que la sobreexpresión de receptor de andrógenos en las celulas tumorales es suficiente para conferir resistencia a la terapia de deprivación de andrógenos en el cancer de próstata y que los niveles de andrógenos intratumorales son a menudo mayores en pacientes con cáncer de próstata avanzado Estas observaciones han proporcionado una base clara para el desarrollo de tratamientos más eficaces Enzalutamide es un inhibidor de receptor de andrógenos que se une competitivamente inhibiendo su translocación al nucleo, el reclutamiento de cofactores y su unión con el ADN En un ensayo de fase 1 -2, enzalutamide comparado con placebo, demostro actividad antitumoral en hombres con cáncer de próstata resistente a la castración, con mayor beneficio en hombres que aún no habian recibido quimioterapia

En un estudio fase 3 previo, enzalutamide comparado con placebo, prolongo la sobrevida global y la sobrevida libre de progresión, mejorando la calidad de vida, con retraso en el desarrollo de complicaciones esqueléticas en pacientes con cancer de próstata metastásico, resistente a la castración que habian recibido previamente docetaxel Este estudio fue realizado en pacientes en tratamiento con agentes hormonales que no habian recibido quimioterapia

Metodos Estudio fase 3, multinacional, doble ciego, aleatorio, controlados por placebo El estudio fue aprobado por el comité examinador independiente en cada sitio participante Todos los pacientes proporcionaron consentimiento informado antes de la participación en la prueba Un comité de supervisión independiente analizó los datos de seguridad a intervalos regulares y repaso el análisis preespecificado intermedio El estudio fue diseñado por expertos en cáncer de próstata y empleados de los patrocinadores, Medivation y Astellas Pharma Los datos eran ingresados en un sistema electrónico que fue verificado por monitores de una organización de investigación separada

Participantes De septiembre de 2010 a septiembre de 2012, los pacientes fueron enrolados en 207 sitios a escala mundial. Fueron asignados recibir enzalutamide oral (una dosis de 160 mg) o placebo Se necesitaba confirmación patológica de adenocarcinoma de próstata con metástasis documentada y elevación de PSA, progresión radiográfica en huesos o tejido blando, o ambas a pesar de recibir LHRH terapia análoga o orquiectomia Nivel de testosterona de 50 ng/dl o menos Continuación de la terapia de deprivación de androgeno. Se Permitio terapia de antiandrógenos previa y el empleo simultáneo de corticoides Los Pacientes eligibles no habían recibido quimioterapia citotóxica, ketoconazole, o el acetato abiraterone

ECOG de 0 o 1, y asintomático o levemente sintomático según el cuestionario breve del Inventario de Dolor Pacientes con enfermedad visceral, incluyendo pulmón o hígado, eran eligibles Pacientes con historia de convulsiones o una condición que podría conferir una predisposición a sufrirlas fueron excluidos El tratamiento continuo hasta la presencia de efectos secundarios inaceptables o progresión radiográfica La interrupción de tratamiento debido a un aumento del nivel de PSA solo fue desalentado.

Objetivos del estudio Los objetivos del estudio fueron sobrevida global y sobrevida libre de progresión radiográfica. Objetivos secundarios incluyeron el tiempo hasta el inicio de quimioterapia citotóxica, tiempo hasta el primer evento esquelético, la mejor respuesta total de tejido blando, tiempo hasta la progresion del PSA, y disminución en el nivel de PSA del 50 %. Obejtivos exploratorios preespecificados incluyeron calidad de vida y una disminución en el nivel de PSA del 90 % o más de la línea de base La enfermedad radiográfica fue evaluada con empleo de tomografía computada o de resonancia magnética. La imagenes fueron realizadas en el momento de la selección, y en las semanas 9, 17, y 25, y cada 12 semanas a partir de entonces Los radiólogos que determinaron si había progresion según RECIST 1, 1 eran inconscientes de las asignaciones del grupo de estudio

Análisis Estadístico La inscripción planificada fue de 1680 pacientes. Los objetivos primarios fueron analizados en la población a tratar con error total tipo I de 0. 05, para la progresión radiográfica y sobrevida global El análisis intermedio de sobrevida global se haria después de la presencia de aproximadamente 516 muertes, o el 67 % de las 765 muertes especificadas para el análisis final. El análisis final de sobrevida radiográfica sin progresión fue realizado después de la presencia de 439 acontecimientos El análisis intermedio de supervivencia total fue realizado después de la presencia de 540 muertes con el empleo de un tipo dos-sided yo la tarifa de error de 0. 0147 Los resultados presentados aquí están basados en la fecha límite del 16 de septiembre de 2013

Resultados Un total de 1. 717 pacientes fueron incluidos en el estudio: -872 en el grupo enzalutamide -845 en el grupo de placebo Las características de la enfermedad y y las características demográficas basales fueron bien equilibradas La mediana de tiempo que los pacientes recibieron un fármaco de estudio fue mayor en el grupo enzalutamide que en el placebo (16, 6 meses vs. 4. 6 meses).

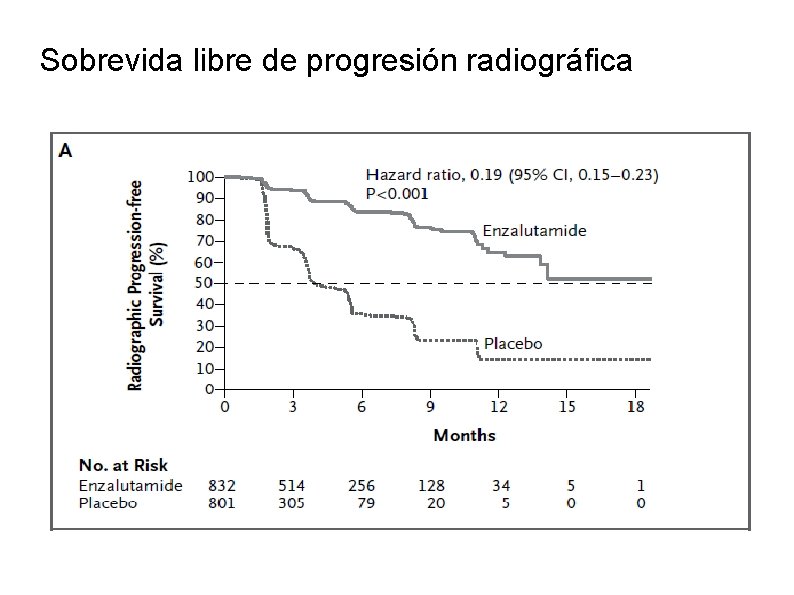
Sobrevida libre de progresión Radiográfica En 12 meses de seguimiento, la de sobrevida radiográfica sin progresión fue de 65 % en el grupo enzalutamide y el 14 % en el grupo de placebo El tratamiento con enzalutamide, comparado con el placebo, causó una reducción del 81 % del riesgo de progresión radiográfica o muerte Menos pacientes en el grupo enzalutamide tuvieron progresión radiográfica o murieron ( 14 % contra 40 %)

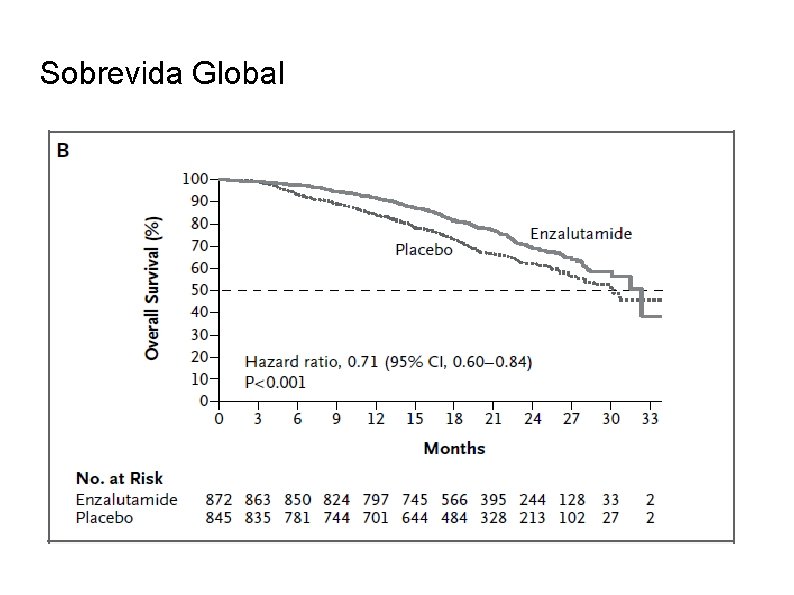
Sobrevida global La media de seguimiento al momento del analisis intermedio fue aproximadamente de 22 meses Menos muertes ocurrieron en el grupo enzalutamide que en el grupo de placebo ( 28 % Vs. 35 %) El tratamiento con enzalutamide, comparado con placebo, causó una disminución del 29 % el riesgo de muerte ( P <0. 001) La media de sobrevida global fue de 32. 4 meses en el grupo enzalutamide y 30. 2 meses en el grupo de placebo El efecto de enzalutamida fue consistente en todos los grupos prespecificados Los resultados no fueron alterados por la exposición previa a antiandrógenos. Después de la revisión de eficacia intermedia, el comité de supervisión de seguridad recomendo parar el estudio y ofrecer enzalutamide a pacientes que recibían placebo

Sobrevida Global

Sobrevida libre de progresión radiográfica

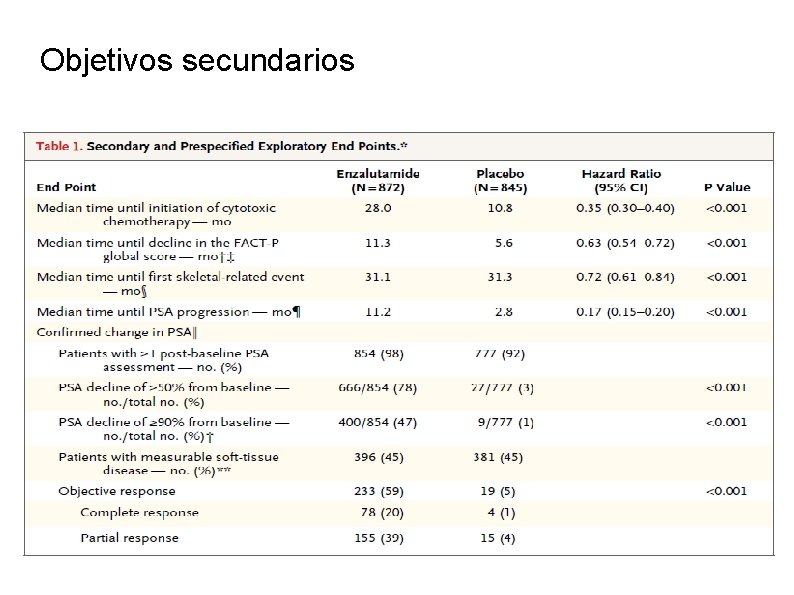
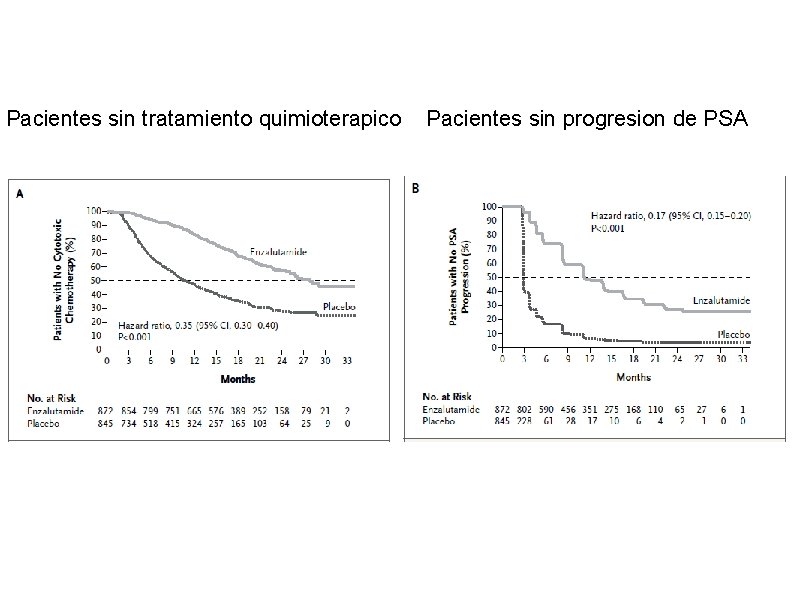
Objetivos secundarios Enzalutamide fue superior al placebo en lo que concierne a todos los objetivos secundarios La media hasta el inicio de quimioterapia fue de 28. 0 meses en el grupo enzalutamide, comparado con 10. 8 meses en el grupo de placebo ( HR 0. 35; P <0. 001) El tratamiento con enzalutamide redujo el riesgo de un primer evento esquelético, que ocurrió en 278 pacientes (el 32 %) en el grupo enzalutamide y 309 pacientes (el 37 %) en el grupo de placebo ( P <0. 001) En una mediana de aproximadamente 31 meses en cada uno de los dos grupos.

En pacientes con enfermedad de tejido blando, el 59 % del grupo de enzalutamide, comparado con el 5 % en el grupo de placebo, tuvieron una respuesta objetiva (P <0. 001) Respuesta completa y parcial fue observada en 20 % y 39 % de los pacientes, respectivamente, en el grupo enzalutamide, comparado con el 1 % y el 4 % en el grupo de placebo Enzalutamide fue superior al placebo en reducir al menos el 50 % en el nivel de PSA y el 90 % en el tiempo hasta PSA la progresión, y el tiempo hasta una disminución en la calidad de vida La media hasta un deterioro en la calidad de vida, fue de 11. 3 meses en el grupo enzalutamide y 5. 6 meses en el grupo de placebo (P <0. 001)

Objetivos secundarios

Pacientes sin tratamiento quimioterapico Pacientes sin progresion de PSA

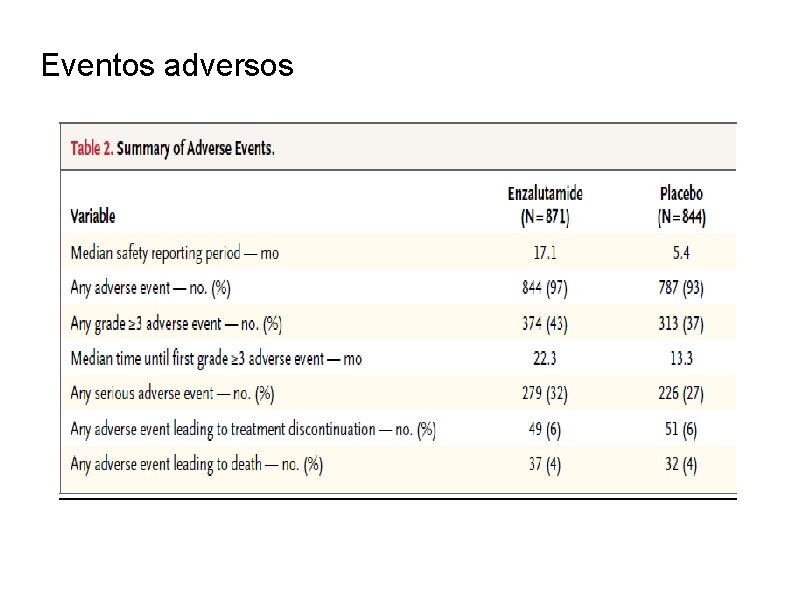
Seguridad Evento adverso grado 3 o mayor ocurrio en el 43 % de los pacientes en el grupo enzalutamide, comparado con el 37 % en el grupo de placebo La media hasta el primer acontecimiento de grado 3 o más fue de 22. 3 meses en el grupo enzalutamide y 13. 3 meses en el grupo de placebo Los eventos adversos más comunes que llevaron a la muerte fueron progresión de enfermedad y deterioro general en la salud, con incidencias similares en ambos grupos. Después del ajuste por el tiempo de exposición, los eventos más frecuentes en el grupo enzalutamide fueron hot flush (14 contra 12 acontecimientos por 100 años pacientes), hipertensión arterial (11 contra 7 acontecimientos por 100 años pacientes), y caídas (11 contra 9 acontecimientos por 100 años pacientes) El evento adverso grado 3 o mayor más común en el grupo enzalutamide fue hipertensión arterial, relatada en el 7 % de los pacientes.

Eventos adversos

Discusión Enzalutamide aumento el tiempo hasta la progresión radiográfica o muerte, mejoró la sobrevida global, y retrasó el inicio de quimioterapia por una media de 17 meses La ventaja de enzalutamide en la sobrevida sin progresión radiográfica fue observada a partir de los 2 meses de la evaluación y confirió una reducción relativa del 81 % en el riesgo de progresión o muerte El beneficio fue observado en todos los subgrupos preespecificados, incluyendo aquellos pacientes de peor pronostico Enzalutamide redujo considerablemente el riesgo de muerte en 29 % sobre el placebo, aun cuando los pacientes que progresaron en el grupo de placebo hubieran recibido terapia eficaz más antes que aquellos en el grupo enzalutamide.

La ventaja de enzalutamide fue observada tan pronto como 4 meses después de la ordenación aleatoria y fue mantenida en todo el estudio En esta población de hombres con cáncer de próstata metastatico, el deterioro en calidad de la vida fue retrasada por enzalutamide, un resultado que se traduce en ventajas percibidas por el paciente La ventaja de enzalutamide fue alcanzada con un perfil favorable de seguridad. Eventos adversos grado 3 o más fueron más comunes en el grupo de enzalutamide(43 % Vs. 37 %) probablemente debido al hecho que el período de seguimiento de eventos para el grupo enzalutamide fue aproximadamente 1 año más que para el grupo de placebo Una proporción similar de pacientes en cada grupo (el 6 %) interrumpió el tratamiento debido a un acontecimiento adverso

Convulsiones fueron reportadas solamente en un paciente en cada grupo, ambos pacientes tenian historias previas de convulsion desconocidas por los investigadores Hipertensión arterial fue más observada en el grupo enzalutamide que en el grupo de placebo (el 13 % contra el 4 %) más a menudo en pacientes con una historia médica previa. Estos acontecimientos no fueron asociados con síntomas de exceso mineralocorticoides o un riesgo aumentado de secuelas cardiovasculares o renales y generalmente fueron manejados con el empleo de terapias estándar Enzalutamide no fue asociado con hepatotoxicidad. Otros eventos adversos que fueron relatados más con frecuencia en el grupo enzalutamide fueron fatiga, dolor, rubor y caídas. .

Múltiples agentes reportados mejoran la sobrevida de pacientes con cáncer de próstata metastasico que ha progresado después de la terapia de deprivación andrógena. El empleo más eficaz de estas terapias ( orden de administración, duración de tratamiento, y la eficacia de combinaciones) aún no ha sido definido En hombres con cáncer de próstata mínimamente sintomático o asintomático metastasico que no recibieron quimioterapia, enzalutamide, retraso considerablemente la progresión de enfermedad radiográfica o muerte, la necesidad de la quimioterapia citotóxica, y el deterioro en la calidad de vida, mejorando la sobrevida global.