EL ATOMO 1 LA HISTORIA DEL ATOMO MODELOS













- Slides: 15

EL ATOMO 1. - LA HISTORIA DEL ATOMO (MODELOS ATOMICOS)

HISTORIA DEL ATOMO • LOS MODELOS ATOMICOS EN EL TIEMPO: ¿QUÉ ES UN MODELOS ATÓMICOS? Es la representación gráfica del átomo que permite describir la clase y el número de partículas fundamentales que lo componen y explica la forma como se comportan y organizan.

GRECIA: del año 600 al 500 A. C. • DEMOCRITO: ´fue un filosofó griego que considero al átomo como la partícula más pequeña de materia que ya no tiene división. • Sus ideas surgen de la observación del mundo real en base a la meditación e intuición. • Llego a la siguiente conclusión: EL ATOMO ES LA PARTICULA MÁS PEQUEÑA DE LA MATERIA, INDIVISIBLE E INDESTRUCTIBLE. • Para comprobar lo que dijo el Filosofo Demócrito: Toma un pedacito de papel y trata de romperlo • Escribe en tu cuaderno las conlcusiones

INGLATERRA (1803) : MODELO ATOMICO DE JOHN DALTON • Después de experimentar el llego a la siguiente conclusión que los atomos eran como esferas compactas de tamaño y masas diferentes • Propuso tres postulados: 1 er Postulado: La materia esta formada por partículas muy pequeñas llamados átomos y estos son indestructibles e indivisibles 2 do Postulado: Todos los átomos del mismo elemento son iguales en masa y tamaño; pero los átomos de diferentes elementos son diferentes en masa y tamaño 3 er Postulado: Los átomos se unen en una relación sencilla para formar los compuestos

¿CÓMO VIO DALTON AL ATOMO?

INGLATERRA (1909) MODELO ATÓMICO DE JOSEPH THOMPSON • Este científico realizo experimentos con tubos de rayos catódicos y con el, logro determinar la existencia de partículas negativas dentro del átomo a las que llamo ELECTRONES • El pensó que como el átomo es neutro entonces debía existir una parte positiva que contrarrestaran las cargas negativas (electrones) por eso su modelo es una esfera y dentro de ella se encuentran incrustados los electrones al igual que las pasas en un pudin por eso su modelo se conoce como: Budín o pastel de pasas

¿ COMO VIO THOMPSON AL ATOMO?

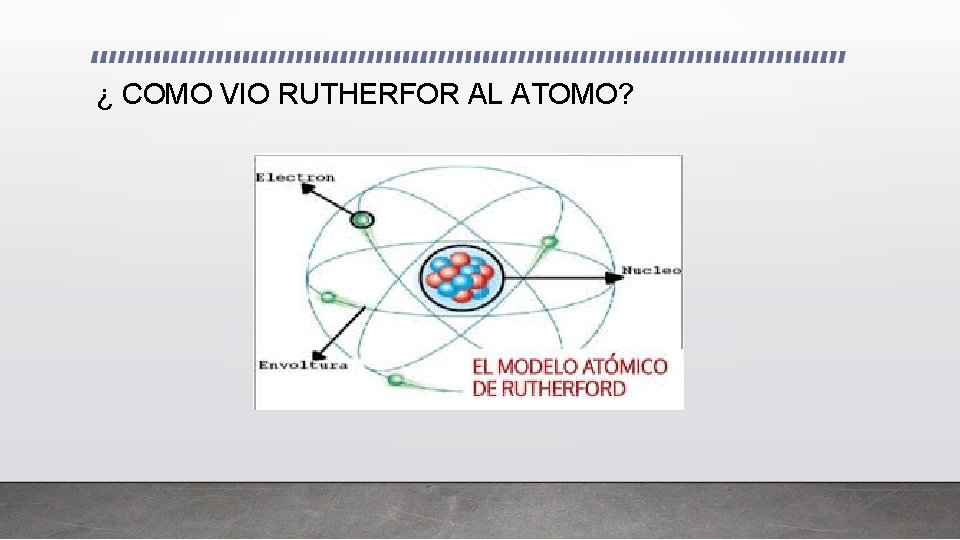
INGLATERRA (1911) MODELO ATOMICO DE ERNEST RUTERFORD • Este científico bombardeo una lamina de oro con radiaciones alfa (núcleos de helio) El observo que la mayoría de las radiaciones alfa atravesaban la lamina sin ser desviadas y que una mínima porción de radiaciones si era desviadas hacia atrás en ángulos agudos; con esta experiencia el llego a la siguiente conclusión: - El átomo tiene un núcleo en el que esta concentrada la masa y la carga positiva - Los electrones están en igual numero a las cargas positivas del núcleo pero distribuidos en un espacio muy grande fuera del núcleo - El volumen ocupado por un átomo en su mayor parte es etéreo y casi toda su masa se concentra en el núcleo

¿ COMO VIO RUTHERFOR AL ATOMO?

ALEMANIA (1912) TEORÍA DE MAX PLANCK • Con este científico el átomo empieza su recorrido hacia la teoría cuántica y explica que las radicaciones no pueden emitirse ni absorberse de manera continua sino que la energía es discontinua y que esta formada por paquetes de energía formados por fotones a los que se les llama CUANTO • Un Cuanto= Un paquete de fotones

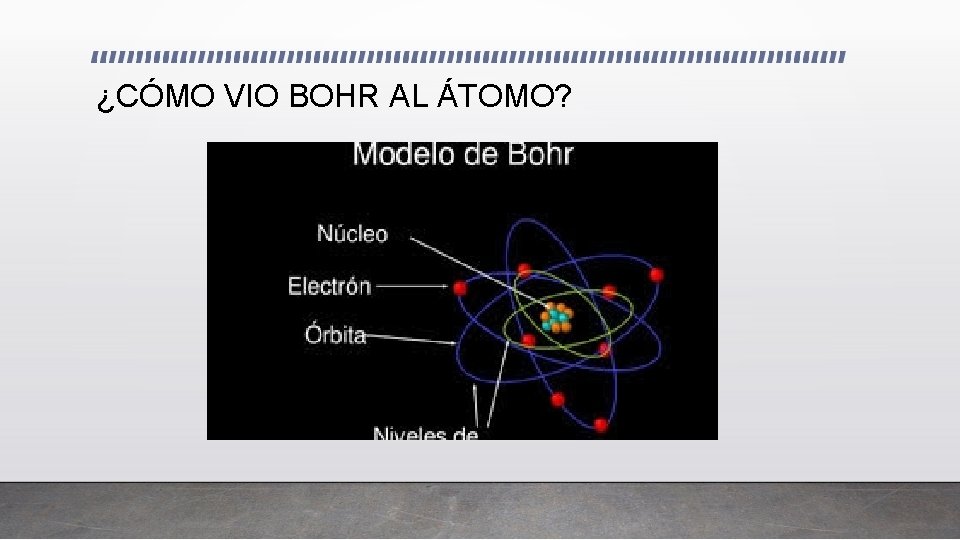
EEUU (1913) NIELS BOHR MEJORO EL MODELO DE RUTHERFORD • Rutherford no pudo responder a la pregunta ¿De donde sacan energía los electrones para viajar a grandes velocidades alrededor del núcleo? • Bohr, propuso que los electrones giran alrededor del núcleo en orbitas concéntricas como un sistema planetario, esto nos lleva a resumir su Teoría en tres postulados • 1 er Postulado: Los electrones se mueven alrededor del núcleo en trayectorias definidas llamadas orbitas • 2 do Postulado: Los electrones están ubicados en niveles definidos de energía ; los niveles mas inferiores son los de menos energía • 3 er Postulado: Los electrones se mueven de un nivel a otro (salto cuántico) ganando o perdiendo energía. Si los hacen de un nivel inferior a uno superior absorben energía y si es de un nivel superior a uno inferior emiten energía a otro atomo

¿CÓMO VIO BOHR AL ÁTOMO?

APORTES DE OTROS CIENTIFICOS PARA LLEGAR AL MODELO ACTUAL • NIELS BOHR: Aporto al nuevo concepto del átomo con su trabajo en el átomo de hidrógeno; el movimiento del electrón esta restringido a un numero discretos de orbitas circulares con el núcleo en el centro. El propuso la cuantización de la energía de los electrones • LUIS DE BROGLIE: en Francia en 1930 demostró que el electrón contiene una pequeña cantidad de masa y que se mueve en ondas (Teoría de la dualidad de la materia). El relaciono la longitud de onda y la masa del electrón con la siguiente ecuación: λ= V/f donde λ es longitud de onda, V es velocidad de la luz y f= frecuencia • Werner Karl Heisemberg en el año 1927 en Alemania propuso su teoría: “El principio de Incertidumbre” el cual dice: “No es posible conocer al mismo tiempo la velocidad y la posición del electrón por eso no se puede determinar su recorrido

EL ATOMO HOY • Todos los aportes dados fueron recogidos por el Científico Austriaco Erwin Shodringer en cual conceptualiza al átomo: - Es un sistema energético en movimiento en cuyo centro se encuentra el núcleo de carga positiva y alrededor de él se encuentran los electrones girando a grandes velocidades en sus respectivos niveles y sub niveles de energía A este modelo se le conoce como el Modelo Mecánico Ondulatorio

TAREA : • HACER UN ORGANIZADOR DE INFORMACIÓN EN EL QUE SE VEA LOS MODELOS ATOMICOS QUE NOS MUESTEAN COMO VIERON LOS CIENTÍFICOS AL ATOMO DESDE ANTES DE CRISTO (Filósofos griegos) HASTA LA ACTUALIDAD • INVESTIGAR: • 1. - Quien descubrió el electrón, el núcleo, el protón y el neutrón • 2. - ¿Qué son los saltos cuánticos?