EL AGUA BIOQUMICA INTRODUCCIN INTRODUCCIN EL AGUA ES

EL AGUA BIOQUÍMICA
INTRODUCCIÓN

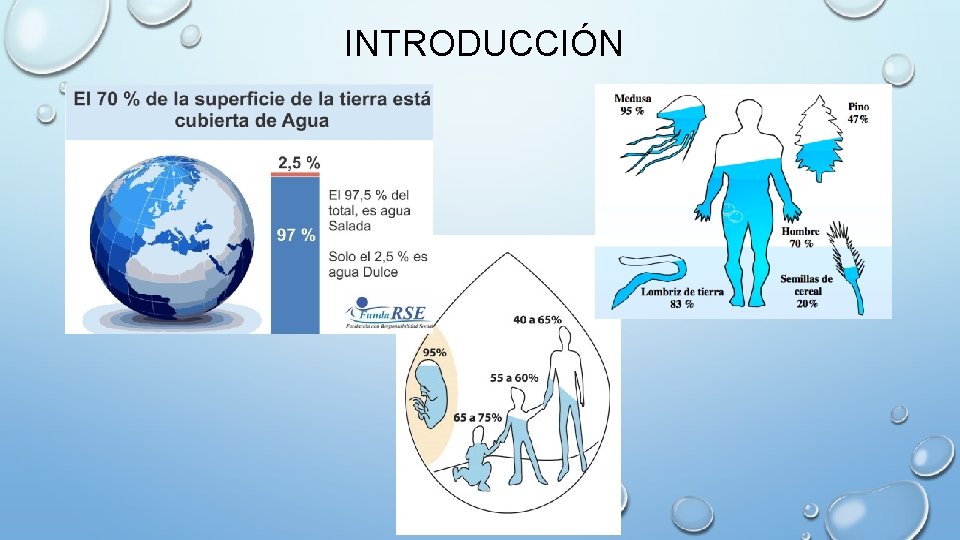
INTRODUCCIÓN • EL AGUA ES IMPORTANTE PARA REGULAR LA TEMPERATURA CORPORAL DEBIDO A SU ALTO CALOR ESPECÍFICO, A LA ALTA CONDUCTIVIDAD TÉRMICA Y POR SU ALTO CALOR DE VAPORIZACIÓN. • EL AGUA PERMITE LA LUBRICACIÓN DE LAS ARTICULACIONES Y DE LOS SOPORTES DE ARTICULACIONES Y OTROS ÓRGANOS Y DEL SISTEMA NERVIOSO CENTRAL, EN LÍQUIDO CEREBRO-ESPINAL. • EL AGUA NO PROPORCIONA ENERGÍA, PERO POR SU GRAN VARIEDAD DE FUNCIONES, EL AGUA SE CONSIDERA COMO EL NUTRIENTE PRINCIPAL.

INTRODUCCIÓN • � EL AGUA EXTRACELULAR REPRESENTA 1/3 DEL AGUA CORPORAL TOTAL Y DE ÉSTA, UN 6% SE ENCUENTRA EN PLASMA SANGUÍNEO. • � LA MAYORÍA DEL AGUA RESTANTE APARECERÁ EN EL CONTENIDO DIGESTIVO Y EN LA ORINA. • � ANOMALÍAS FISIOLÓGICAS (FIEBRE O DIARREA) PUEDEN PROVOCAR LA DESHIDRATACIÓN ORGÁNICA O UNA RETENCIÓN EXCESIVA DE AGUA. • � EL AGUA QUE LLEGA A LOS TEJIDOS ANIMALES PROCEDE DE: A) AGUA DE BEBIDA. B) AGUA PROCEDENTE DE LOS ALIMENTOS. C) AGUA METABÓLICA POR OXIDACIÓN DE NUTRIENTES ORGÁNICOS.

PROPIEDADES FÍSICAS • TRES ESTADOS FÍSICOS • PUNTO DE EBULLICIÓN 100°C • PUNTO DE FUSIÓN 0°C • NO CONDUCTORA DE ELECTRICIDAD • SOLVENTE UNIVERSAL • TRANSPORTE DE MATERIALES (RÍO, XILEMA, VENAS Y CAPILARES) • PRINCIPAL DISOLVENTE BIOLÓGICO (RXNS BIOL)
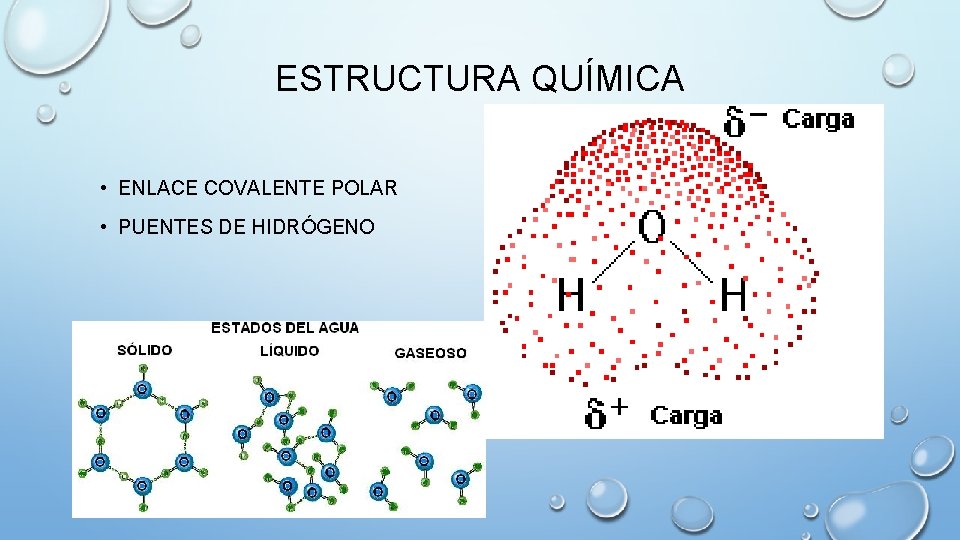
ESTRUCTURA QUÍMICA • ENLACE COVALENTE POLAR • PUENTES DE HIDRÓGENO

EL AGUA COMO DISOLVENTE BIOLÓGICO • EL AGUA ES EL MEDIO DONDE SE DESARROLLAN LA MAYORÍA DE LAS REACCIONES QUÍMICAS EN LA CÉLULA. • ES UN DIPOLO. • POR MEDIO DE LOS PUENTES DE HIDRÓGENO SE PUEDEN DISOLVER MUCHOS COMPUESTOS. • PUEDE IONIZARSE. • PUEDE COMPORTARSE COMO ÁCIDO O COMO BASE. Reacción de autoionización. (1 de cada 109 moléculas de agua)

PROCESO DE DISOCIACIÓN DEL AGUA =1. 0 x 10 -14
![PH • UNA SOLUCIÓN EN LA CUAL [H+] = [OH-] ES NEUTRA. • RECUERDA: PH • UNA SOLUCIÓN EN LA CUAL [H+] = [OH-] ES NEUTRA. • RECUERDA:](http://slidetodoc.com/presentation_image_h/ec5ec5a97feae0e40d01d625b6e617a1/image-9.jpg)
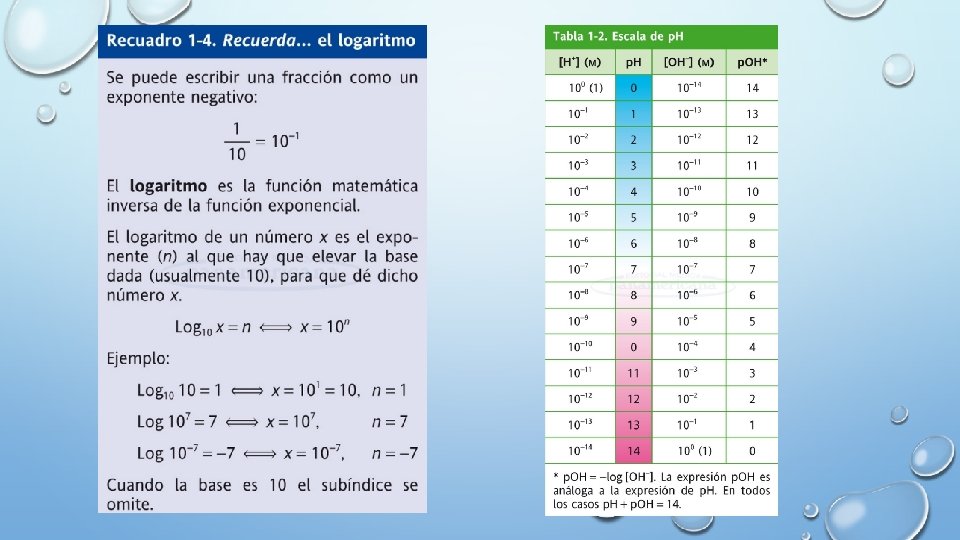
PH • UNA SOLUCIÓN EN LA CUAL [H+] = [OH-] ES NEUTRA. • RECUERDA: [H+][OH-]= 1. 0 X 10 -14 • CONFORME LA CONCENTRACIÓN DE UNO AUMENTA LA DE OTRO DISMINUYE (SIEMPRE SERÁ 1. 0 X 10 -14) • EN LAS SOLUCIONES ÁCIDAS [H+] ES MAYOR QUE [OH-]. • EN LAS SOLUCIONES BÁSICAS ES LO CONTRARIO [H+] ES MENOR QUE [OH-].
![EJERCICIO: CALCULE LOS VALORES DE [H+] Y [OH-] EN UNA SOLUCIÓN NEUTRA A 25 EJERCICIO: CALCULE LOS VALORES DE [H+] Y [OH-] EN UNA SOLUCIÓN NEUTRA A 25](http://slidetodoc.com/presentation_image_h/ec5ec5a97feae0e40d01d625b6e617a1/image-11.jpg)
EJERCICIO: CALCULE LOS VALORES DE [H+] Y [OH-] EN UNA SOLUCIÓN NEUTRA A 25 °C • RESPUESTA: POR DEFINICIÓN, EN UNA SOLUCIÓN NEUTRA [H+] ES IGUAL A [OH -]. LLAMAREMOS “X” A CADA UNA DE ESTAS ESPECIES EN SOLUCIÓN NEUTRA, POR LO QUE: • [H+][OH-]= (X)(X) = 1 X 10 -14. • X 2 = 1 X 10 -14. • X= 1 X 10 -7 • ENTONCES [H+] = [OH-] = 1 X 10 -7
![EJERCICIO: CALCULE LA CONCENTRACIÓN DE H+ EN UNA SOLUCIÓN DONDE [OH-] = A) 0. EJERCICIO: CALCULE LA CONCENTRACIÓN DE H+ EN UNA SOLUCIÓN DONDE [OH-] = A) 0.](http://slidetodoc.com/presentation_image_h/ec5ec5a97feae0e40d01d625b6e617a1/image-12.jpg)
EJERCICIO: CALCULE LA CONCENTRACIÓN DE H+ EN UNA SOLUCIÓN DONDE [OH-] = A) 0. 010 M B) 2. 0 X 10 -9 • A) 0. 010 = 10 X 10 -2 • [H+][OH-]= 1. 0 X 10 -14 • POR LO TANTO: [H+] = 1. 0 X-14/ [OH-], SUSTITUYENDO: • [H+] = 1. 0 X-14/ [0. 010] = 1. 0 X 10 -12 • 2. 0 X 10 -9 • POR LO TANTO: [H+] = 1. 0 X-14/ [OH-], SUSTITUYENDO: • [H+] = 1. 0 X-14/ 2. 0 X 10 -9 = 5. 0 X 10 -6
- Slides: 12