Ejercicios resueltos balance de ecuaciones Profesora Lissette Gmez

Ejercicios resueltos balance de ecuaciones Profesora: Lissette Gómez Curso: Primero medio

Objetivo Ø Afianzar el concepto de balance de ecuaciones químicas mediante el método de tanteo y algebraico.
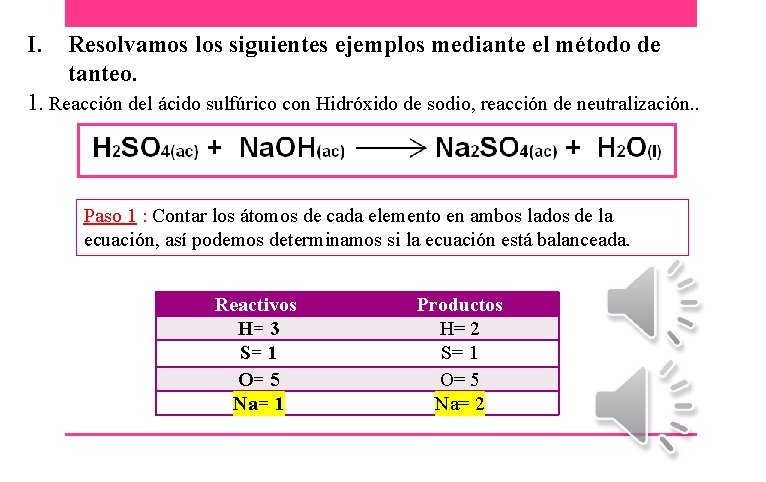
I. Resolvamos los siguientes ejemplos mediante el método de tanteo. 1. Reacción del ácido sulfúrico con Hidróxido de sodio, reacción de neutralización. . Paso 1 : Contar los átomos de cada elemento en ambos lados de la ecuación, así podemos determinamos si la ecuación está balanceada. Reactivos H= 3 S= 1 O= 5 Na= 1 Productos H= 2 S= 1 O= 5 Na= 2
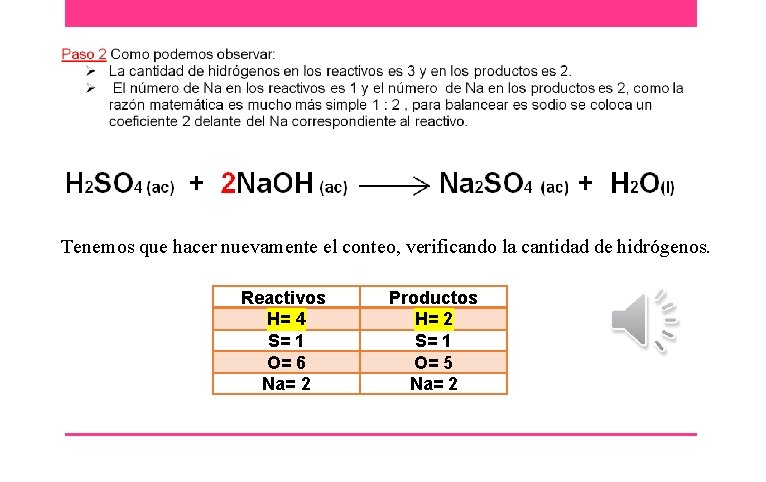
Tenemos que hacer nuevamente el conteo, verificando la cantidad de hidrógenos. Reactivos H= 4 S= 1 O= 6 Na= 2 Productos H= 2 S= 1 O= 5 Na= 2
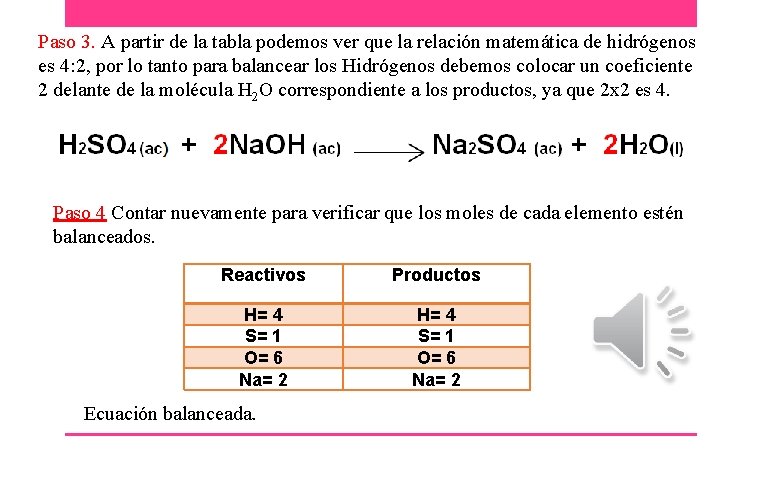
Paso 3. A partir de la tabla podemos ver que la relación matemática de hidrógenos es 4: 2, por lo tanto para balancear los Hidrógenos debemos colocar un coeficiente 2 delante de la molécula H 2 O correspondiente a los productos, ya que 2 x 2 es 4. Paso 4 Contar nuevamente para verificar que los moles de cada elemento estén balanceados. Reactivos Productos H= 4 S= 1 O= 6 Na= 2 Ecuación balanceada.
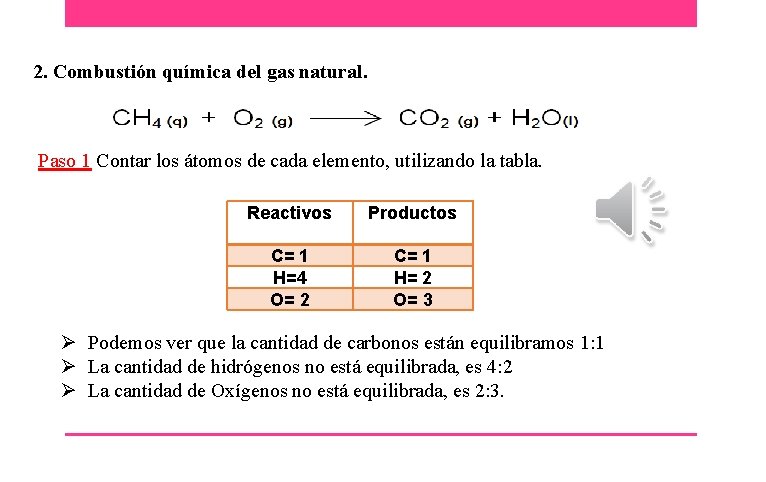
2. Combustión química del gas natural. Paso 1 Contar los átomos de cada elemento, utilizando la tabla. Reactivos Productos C= 1 H=4 O= 2 C= 1 H= 2 O= 3 Ø Podemos ver que la cantidad de carbonos están equilibramos 1: 1 Ø La cantidad de hidrógenos no está equilibrada, es 4: 2 Ø La cantidad de Oxígenos no está equilibrada, es 2: 3.

Paso 2. Primero que todo balanceamos hidrógenos, colocamos un coeficiente 2 delante de la molécula de agua, ahí tendemos los 4 hidrógenos. Ø Ahora vemos que tenemos 2 oxígenos en los reactivos y 4 en los productos, por lo tanto para balancear los oxígenos, colocamos un coeficiente 2 en el oxígeno correspondiente a los reactivos. Ø Ahora vemos que la ecuación esta balanceada, mediante el método de tanteo.

II. Método Algebraico. Determinar mediante el método algebraico, los coeficientes estequimétrico de las siguientes reacciones. 1. Oxidación de la glucosa. PASO 1. Contar los átomos de cada elemento en ambos lados de la ecuación. Reactivos C= 6 H=12 O= 8 Productos C= 1 H= 2 O= 3
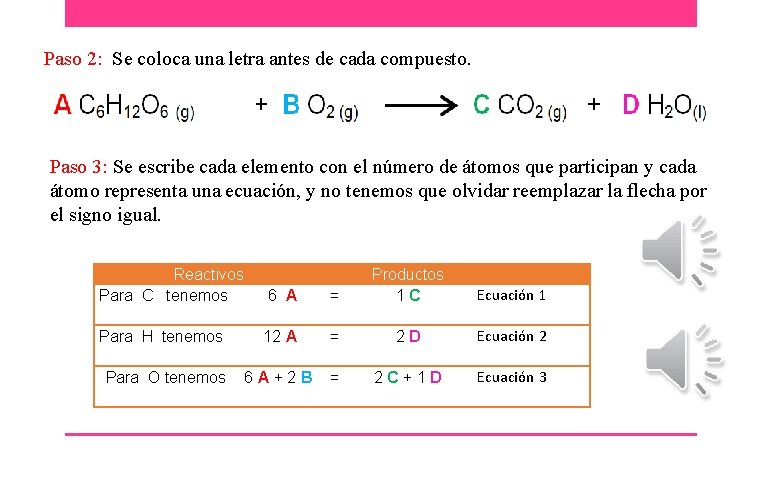
Paso 2: Se coloca una letra antes de cada compuesto. Paso 3: Se escribe cada elemento con el número de átomos que participan y cada átomo representa una ecuación, y no tenemos que olvidar reemplazar la flecha por el signo igual. Reactivos Para C tenemos = Productos 1 C 6 A Ecuación 1 Para H tenemos 12 A = 2 D Ecuación 2 Para O tenemos 6 A+2 B = 2 C+1 D Ecuación 3

Paso 4: Debe comenzar a resolver las ecuaciones químicas, de la ecuación 1 obtenemos 2 valores: Asumimos que la letra a=1, por lo tanto al reemplazar en la ecuación se tiene que: Paso 5: De la ecuación 2 se obtiene el valor de D:

Paso 6: De la ecuación 3 se obtiene el valor de B:
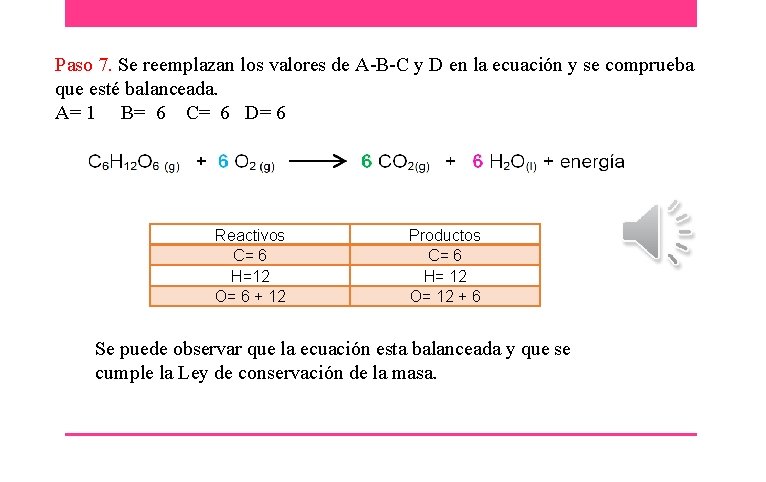
Paso 7. Se reemplazan los valores de A-B-C y D en la ecuación y se comprueba que esté balanceada. A= 1 B= 6 C= 6 D= 6 Reactivos C= 6 H=12 O= 6 + 12 Productos C= 6 H= 12 O= 12 + 6 Se puede observar que la ecuación esta balanceada y que se cumple la Ley de conservación de la masa.
- Slides: 12