EJERCICIOS ESTRUCTURA DE LEWIS Dibuje la estructura de

EJERCICIOS ESTRUCTURA DE LEWIS

Dibuje la estructura de Lewis para el NH 3 • Pasos: 2 2 s 2 2 p 3 = 5 e- de valencia N = 1 s 7 1 = 1 e- de valencia por cada hidrógeno H = 1 s 1
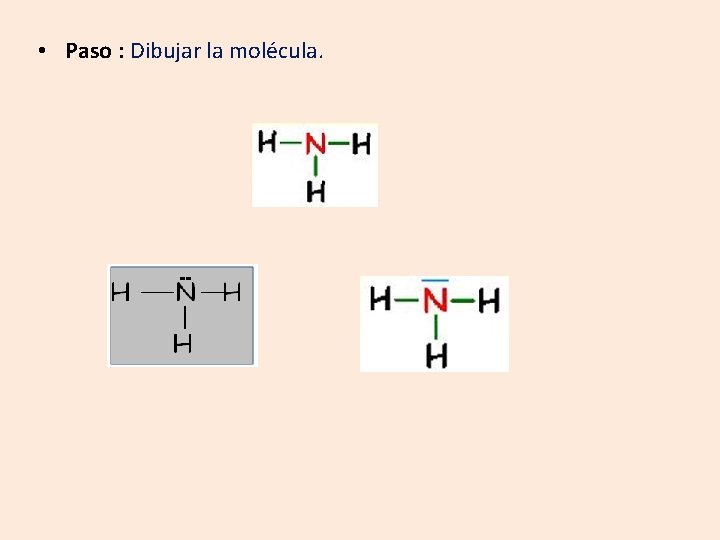
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el ión amonio NH 4 + • Pasos: 2 2 s 2 2 p 3 = 5 e- de valencia N = 1 s 7 1 = 1 e- de valencia H = 1 s 1
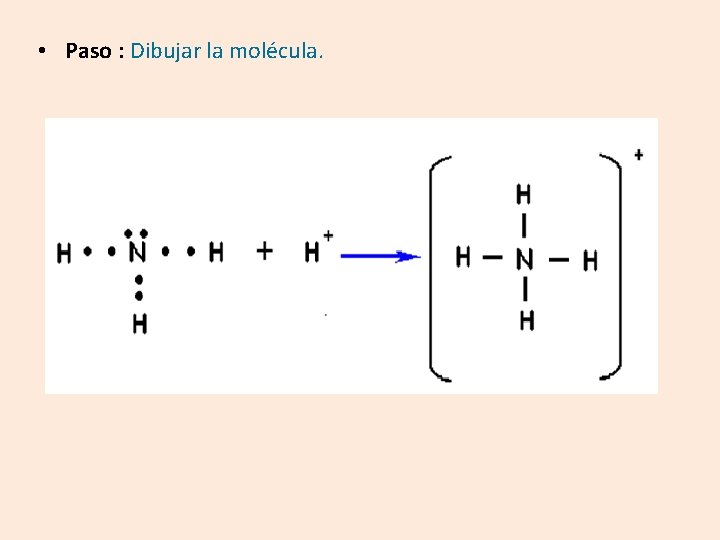
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el SO 2 • Paso 1: 2 2 s 2 2 p 6 3 s 2 3 p 4 = 6 e- de valencia S = 1 s 16 2 2 s 2 2 p 4 = 6 e- de valencia por cada O = 1 s 8 oxígeno • Paso 2: Octetos
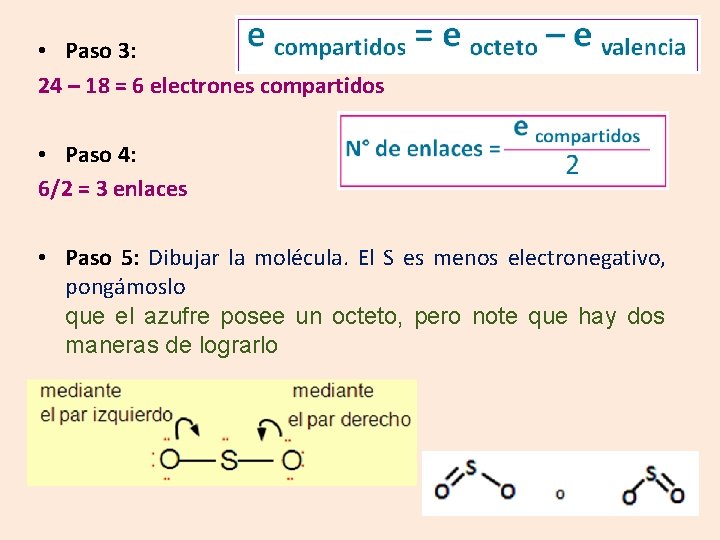
• Paso 3: 24 – 18 = 6 electrones compartidos • Paso 4: 6/2 = 3 enlaces • Paso 5: Dibujar la molécula. El S es menos electronegativo, pongámoslo que el azufre posee un octeto, pero note que hay dos maneras de lograrlo
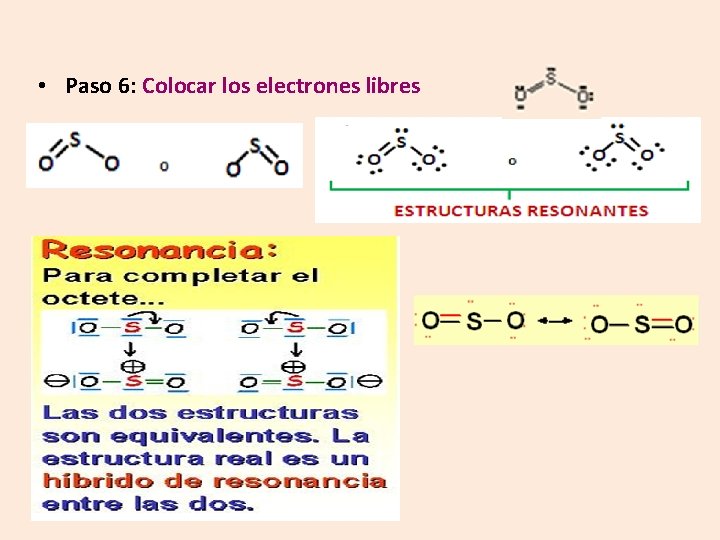
• Paso 6: Colocar los electrones libres

Dibuje la estructura de Lewis para el CO 2 • Pasos: 2 2 s 2 2 p 2 = 4 e- de valencia C = 1 s 6 2 2 s 2 2 p 4 = 6 e- de valencia por cada O = 1 s 8 oxígeno
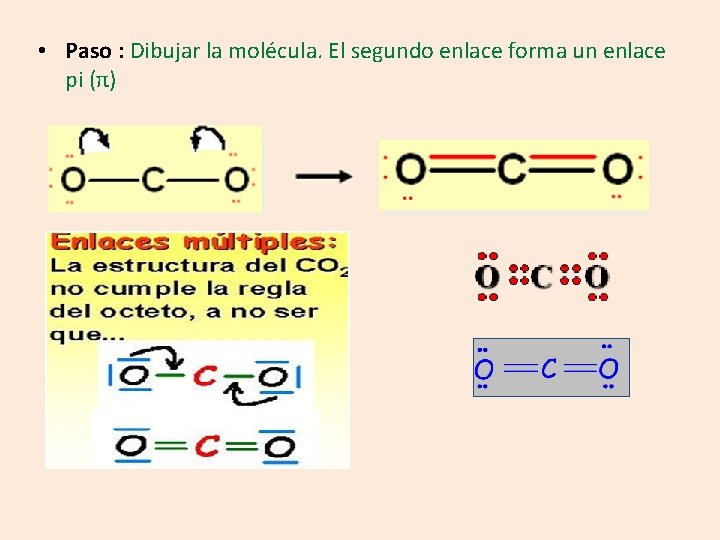
• Paso : Dibujar la molécula. El segundo enlace forma un enlace pi (π)

Dibuje la estructura de Lewis para el CH 4 • Pasos: 2 2 s 2 2 p 2 = 4 e- de valencia C = 1 s 6 1 = 1 e- de valencia por cada hidrógeno H = 1 s 1
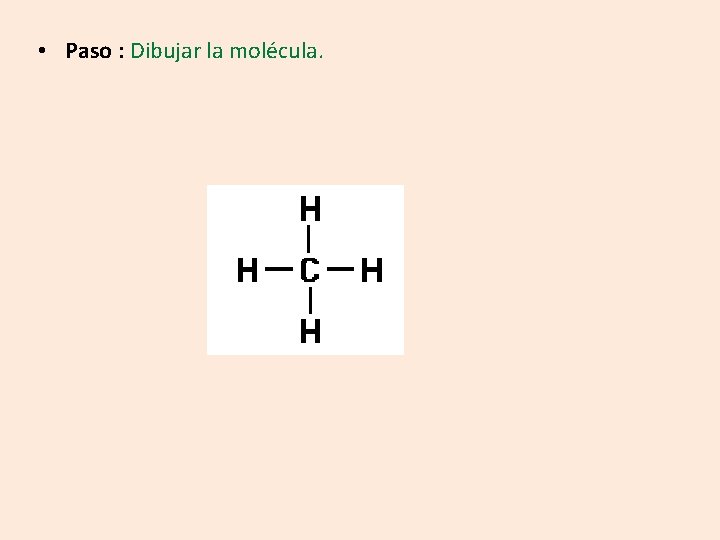
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el Be. H 2 • Pasos: 2 2 s 2 = 2 e- de valencia Be = 1 s 4 1 = 1 e- de valencia por cada hidrógeno H = 1 s 1 (Be excepción a la regla del octeto, forma cuartetos)
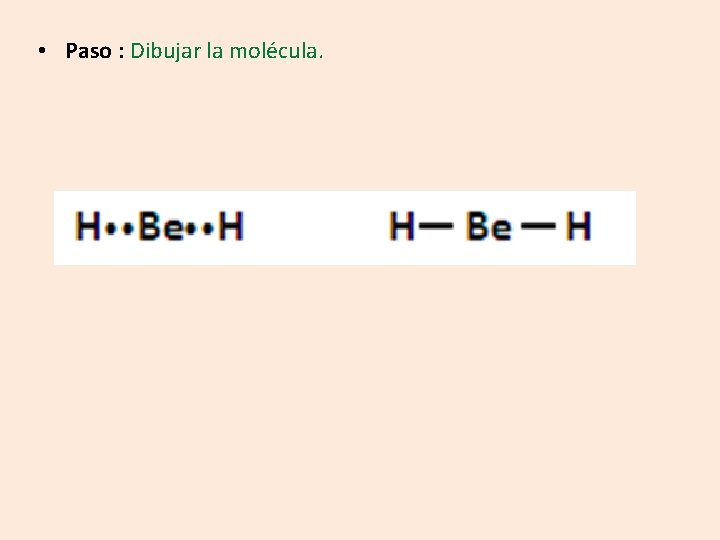
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el H 2 O • Pasos: 2 2 s 2 2 p 4 = 6 e- de valencia O = 1 s 8 1 = 1 e- de valencia por cada hidrógeno H = 1 s 1
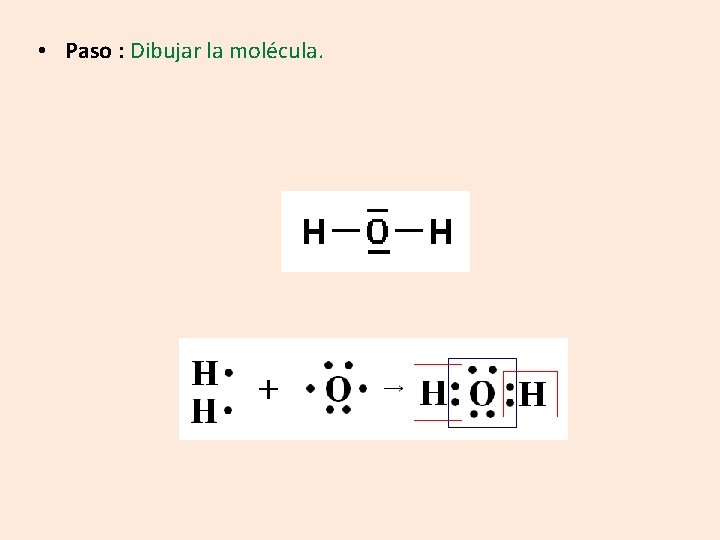
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el O 2 • Pasos: 2 2 s 2 2 p 4 = 6 e- de valencia O = 1 s 8
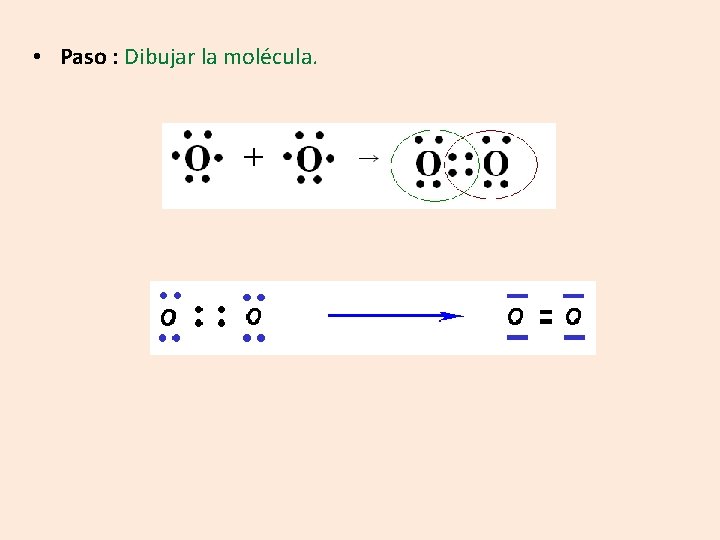
• Paso : Dibujar la molécula.
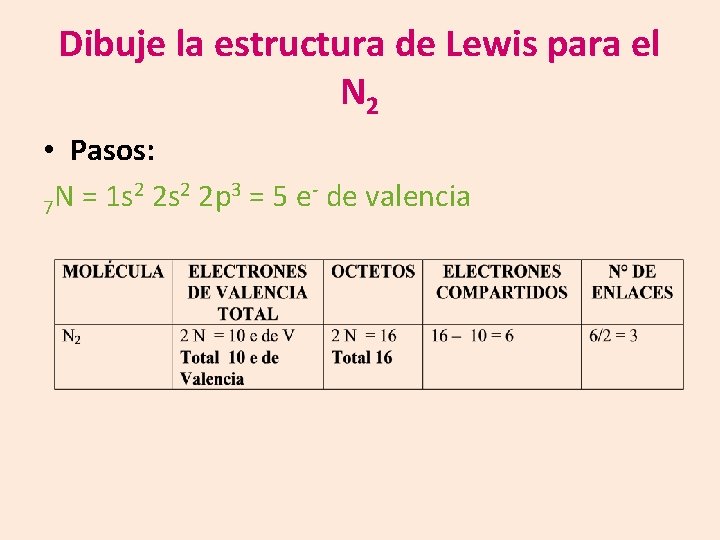
Dibuje la estructura de Lewis para el N 2 • Pasos: 2 2 s 2 2 p 3 = 5 e- de valencia N = 1 s 7
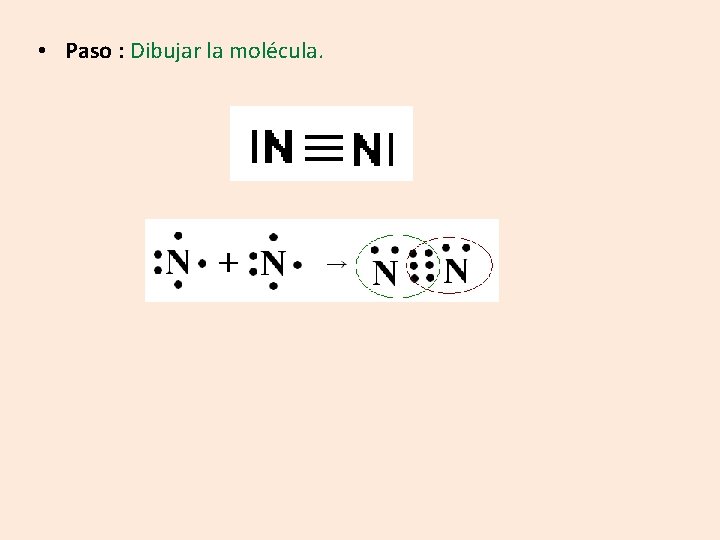
• Paso : Dibujar la molécula.

Dibuje la estructura de Lewis para el SO 3 • Pasos: 2 2 s 2 2 p 6 3 s 2 3 p 4 = 6 e- de valencia S = 1 s 16 2 2 s 2 2 p 4 = 6 e- de valencia por cada O = 1 s 8 oxígeno
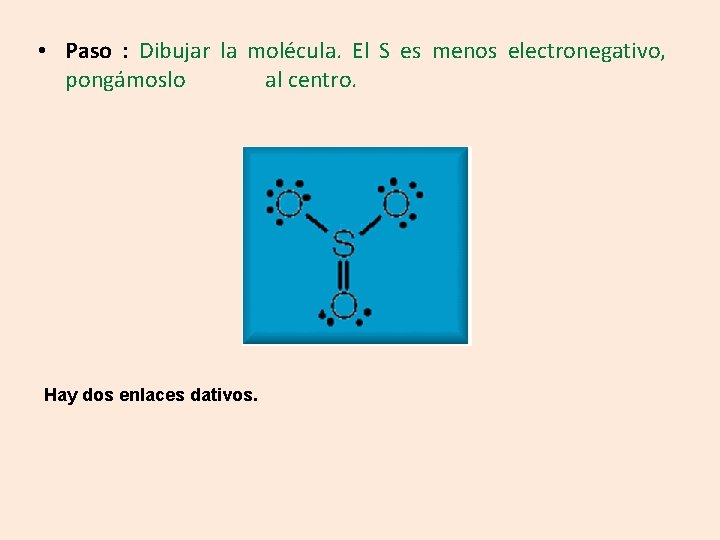
• Paso : Dibujar la molécula. El S es menos electronegativo, pongámoslo al centro. Hay dos enlaces dativos.
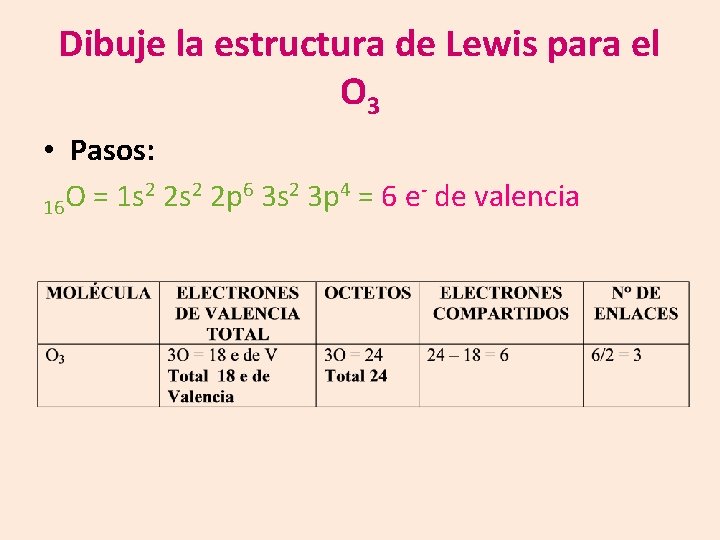
Dibuje la estructura de Lewis para el O 3 • Pasos: 2 2 s 2 2 p 6 3 s 2 3 p 4 = 6 e- de valencia O = 1 s 16
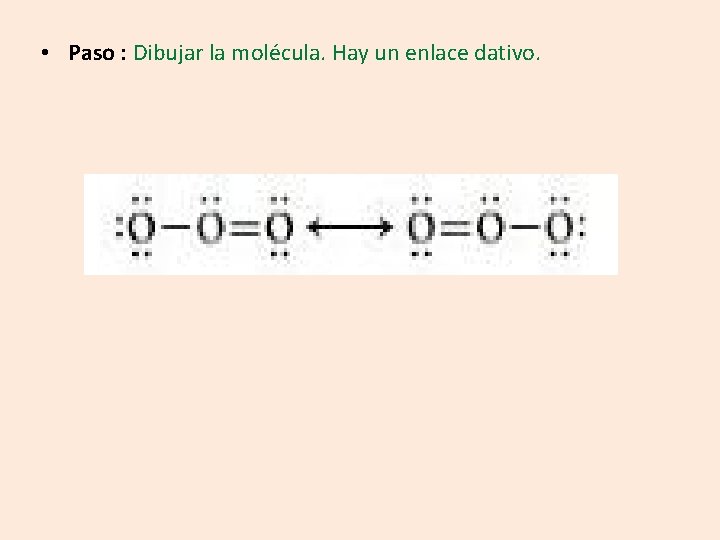
• Paso : Dibujar la molécula. Hay un enlace dativo.

Dibuje la estructura de Lewis para el CO • Pasos: 2 2 s 2 2 p 2 = 4 e- de valencia C = 1 s 6 2 2 s 2 2 p 4 = 6 e- de valencia por cada O = 1 s 8 oxígeno

• Paso : Dibujar la molécula. El que forma el triple enlace es dativo

Dibuje la estructura de Lewis para el Si. Cl 4 • Pasos: 2 2 s 2 2 p 6 3 s 2 3 p 2 = 4 e- de valencia Si = 1 s 14 2 2 s 2 2 p 6 3 s 2 3 p 5 = 7 e- de valencia por Cl = 1 s 17 cada cloro

• Paso : Dibujar la molécula. El Si al centro.

Dibuje la estructura de Lewis para el HNO 3 • Pasos: 2 2 s 2 2 p 3 = 5 e- de valencia N = 1 s 7 2 2 s 2 2 p 4 = 6 e- de valencia por cada O = 1 s 8 oxígeno 1 = 1 e- de valencia por cada hidrógeno H = 1 s 1
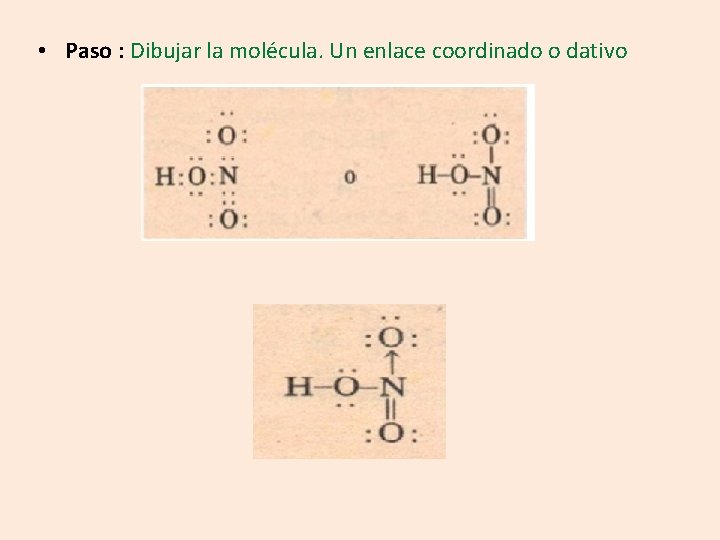
• Paso : Dibujar la molécula. Un enlace coordinado o dativo

Dibuje la estructura de Lewis para el ion clorato: Cl. O 3 • Paso 1: 2 2 s 2 2 p 6 3 s 2 3 p 5 = 7 e de valencia Cl = 1 s 17 2 2 s 2 2 p 4 = 6 e de valencia O = 1 s 8 Paso 2: Octetos
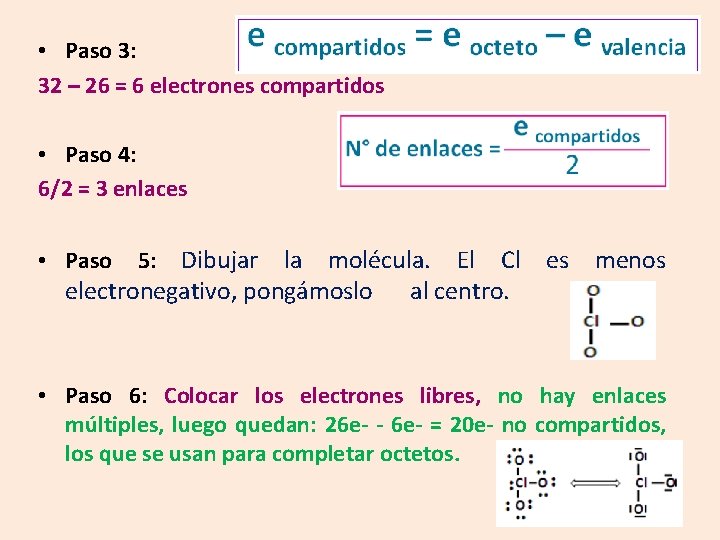
• Paso 3: 32 – 26 = 6 electrones compartidos • Paso 4: 6/2 = 3 enlaces Dibujar la molécula. El Cl es menos electronegativo, pongámoslo al centro. • Paso 5: • Paso 6: Colocar los electrones libres, no hay enlaces múltiples, luego quedan: 26 e- - 6 e- = 20 e- no compartidos, los que se usan para completar octetos.

Dibuje la estructura de Lewis para el metanol CH 3 COH • Pasos: 2 2 s 2 2 p 2 = 4 e- de valencia C = 1 s 6 1 = 1 e- de valencia H = 1 s 1 2 2 s 2 2 p 4 = 6 e- de valencia O = 1 s 8
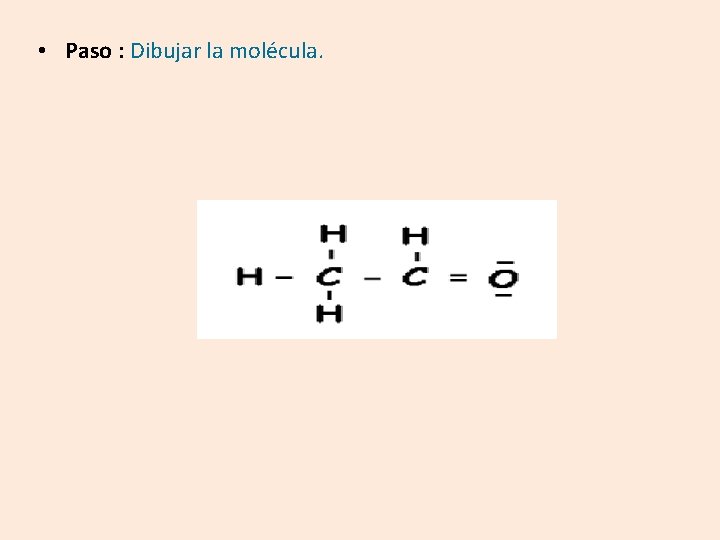
• Paso : Dibujar la molécula.
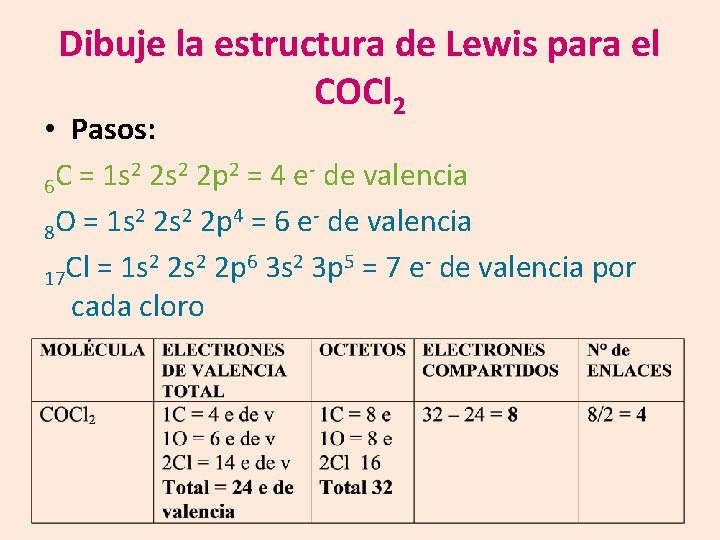
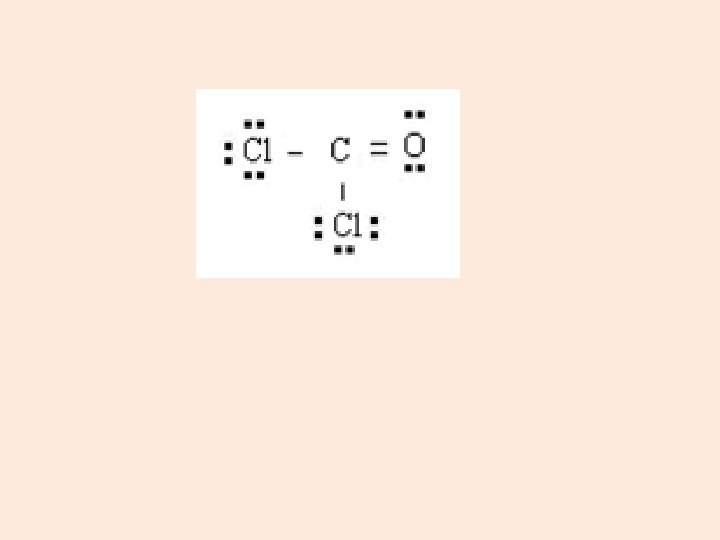
Dibuje la estructura de Lewis para el COCl 2 • Pasos: 2 2 s 2 2 p 2 = 4 e- de valencia C = 1 s 6 2 2 s 2 2 p 4 = 6 e- de valencia O = 1 s 8 2 2 s 2 2 p 6 3 s 2 3 p 5 = 7 e- de valencia por Cl = 1 s 17 cada cloro
- Slides: 36