Eigenschaften der bergangsmetalle Gliederung 1 Einfhrung 2 Eigenschaften

Eigenschaften der Übergangsmetalle

Gliederung 1. Einführung 2. Eigenschaften der Übergangsmetalle 2. 1 Oxidationsstufen 2. 2 Komplexe 2. 3 Farbige Salze 2. 4 Katalysatoren 3. Schulische Relevanz
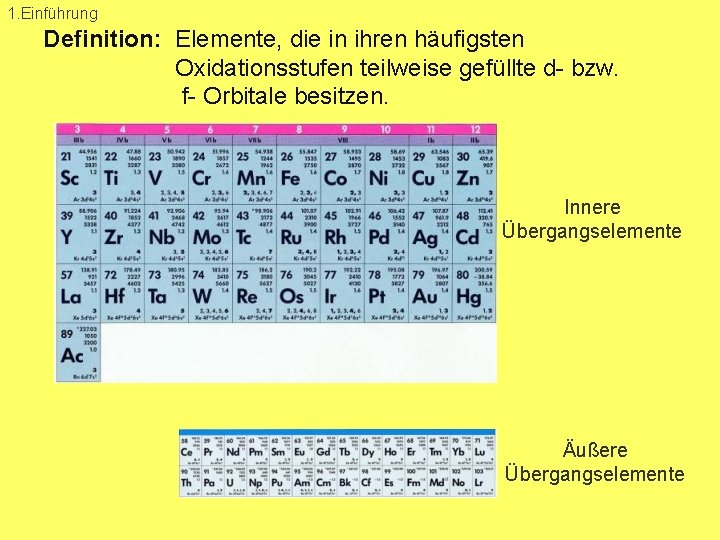
1. Einführung Definition: Elemente, die in ihren häufigsten Oxidationsstufen teilweise gefüllte d bzw. f Orbitale besitzen. Innere Übergangselemente Äußere Übergangselemente

1. Einführung Unterscheidung zwischen Übergangsmetallen und Hauptgruppen Elementen: • Hauptgruppenelemente: s und p Orbitale werden mit Elektronen besetzt • Übergangsmetalle: d bzw. f Orbitale werden mit Elektronen besetzt innere Orbital bestimmen Chemie dieser Elemente
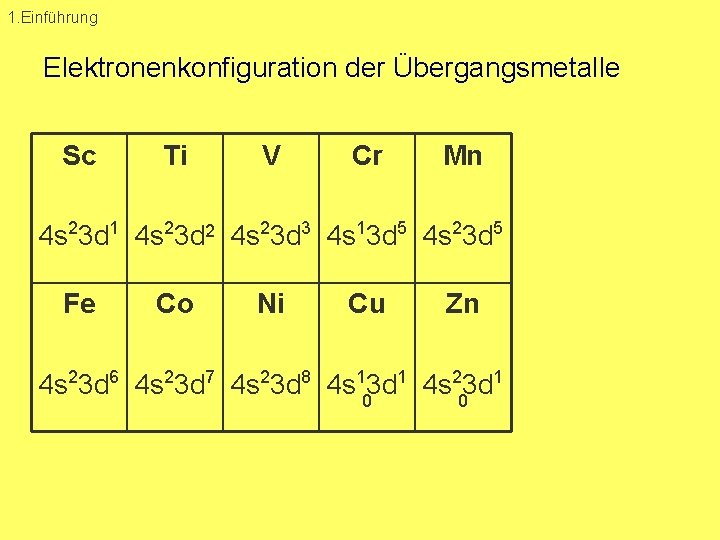
1. Einführung Elektronenkonfiguration der Übergangsmetalle Sc Ti V Cr Mn 4 s 23 d 1 4 s 23 d 2 4 s 23 d 3 4 s 13 d 5 4 s 23 d 5 Fe Co Ni Cu Zn 4 s 23 d 6 4 s 23 d 7 4 s 23 d 8 4 s 103 d 1 4 s 203 d 1

1. Einführung Physikalische Eigenschaften • Hohe Wärme und Stromleitfähigkeit • Hohe Duktilität • Zum Teil extrem hohe Schmelz und Siedepunkte (W: Smp. 3380°C, Sdp. 5500°C) • Hohe Dichten • Zum Teil hohe Beständigkeit der Metalle gegen Sauerstoff, Säuren und Basen

2. 1 Oxidationsstufen

2. 1 Oxidationsstufen Die Oxidationsstufen der Übergangsmetalle • Hauptgruppenmetalle bilden nur in einer Oxidationsstufe stabile Ionen Beispiel: Na+, Mg 2+, Al 3+ Oktettregel oder in sich um zwei Einheiten unterscheidender Oxidationsstufen stabile Ionen Beispiel: Pb 2+, Pb 4+ Inert Pair Effekt • Übergangsmetalle bilden in mehreren verschiedenen Oxidationsstufen stabile Ionen

Versuch 1: Oxidationsstufen des Mangans
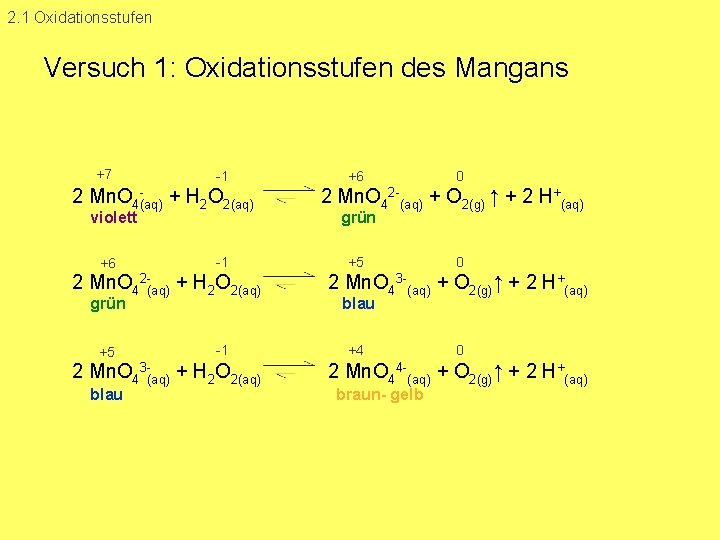
2. 1 Oxidationsstufen Versuch 1: Oxidationsstufen des Mangans +7 1 2 Mn. O 4 (aq) + H 2 O 2(aq) violett +6 1 2 Mn. O 42 (aq) + H 2 O 2(aq) grün +5 1 2 Mn. O 43 (aq) + H 2 O 2(aq) blau +6 0 2 Mn. O 42 (aq) + O 2(g) ↑ + 2 H+(aq) grün +5 0 2 Mn. O 43 (aq) + O 2(g)↑ + 2 H+(aq) blau +4 0 2 Mn. O 44 (aq) + O 2(g)↑ + 2 H+(aq) braun- gelb
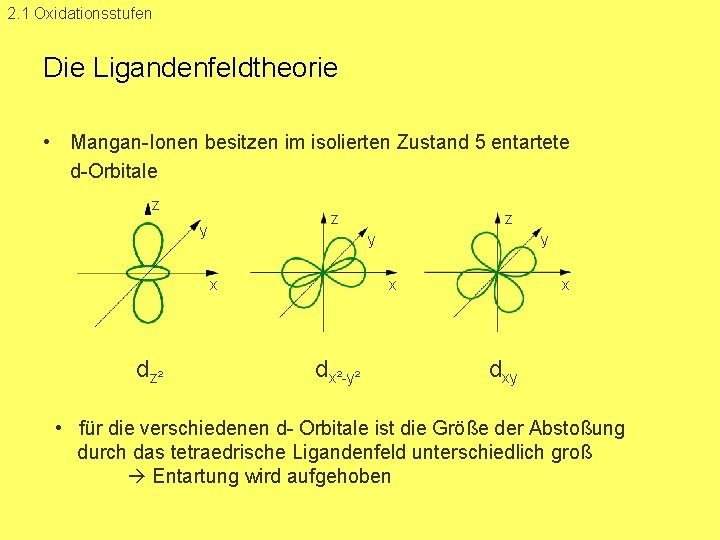
2. 1 Oxidationsstufen Die Ligandenfeldtheorie • Mangan Ionen besitzen im isolierten Zustand 5 entartete d Orbitale z z y y x dz² z y x dx² y² x dxy • für die verschiedenen d Orbitale ist die Größe der Abstoßung durch das tetraedrische Ligandenfeld unterschiedlich groß Entartung wird aufgehoben
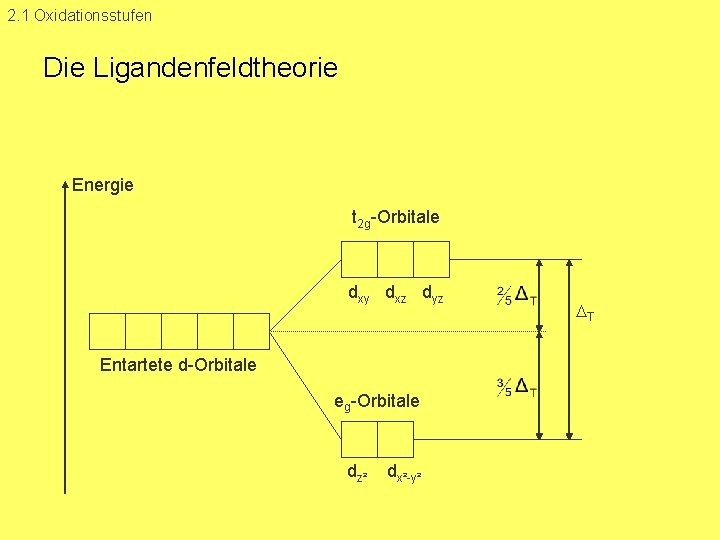
2. 1 Oxidationsstufen Die Ligandenfeldtheorie Energie t 2 g Orbitale dxy dxz dyz Entartete d Orbitale eg Orbitale dz² dx² y² T
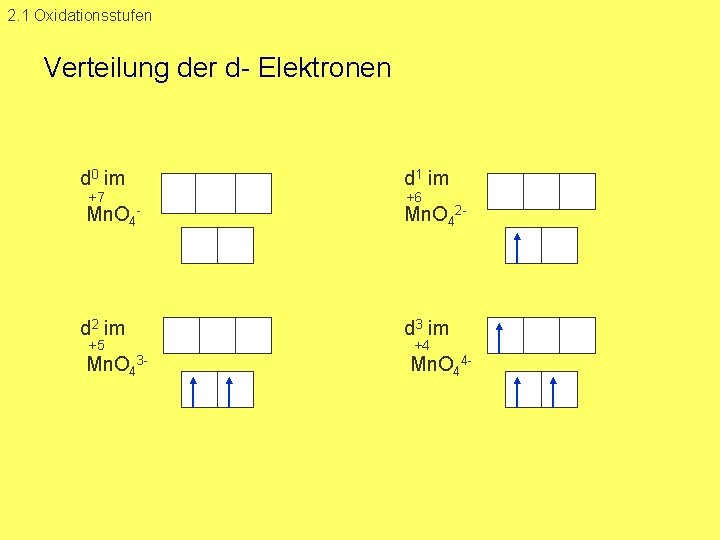
2. 1 Oxidationsstufen Verteilung der d Elektronen d 0 im +7 Mn. O 4 d 1 im +6 Mn. O 42 d 2 im d 3 im Mn. O 43 Mn. O 44 +5 +4
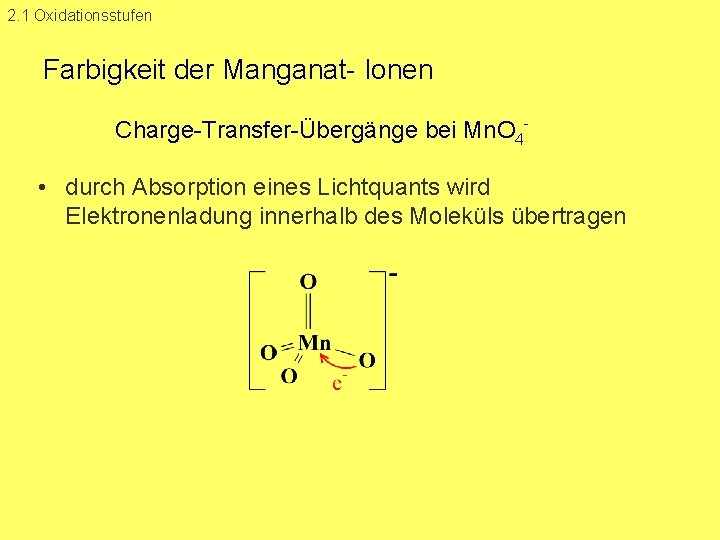
2. 1 Oxidationsstufen Farbigkeit der Manganat Ionen Charge Transfer Übergänge bei Mn. O 4 • durch Absorption eines Lichtquants wird Elektronenladung innerhalb des Moleküls übertragen
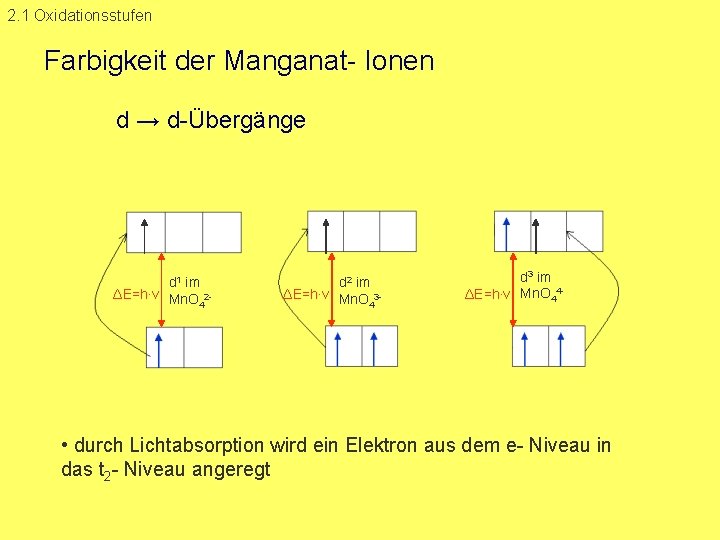
2. 1 Oxidationsstufen Farbigkeit der Manganat Ionen d → d Übergänge d 1 im ΔE=h∙ν Mn. O 2 4 d 2 im ΔE=h∙ν Mn. O 3 4 d 3 im ΔE=h∙ν Mn. O 44 • durch Lichtabsorption wird ein Elektron aus dem e Niveau in das t 2 Niveau angeregt

Demo 1: Unedel vs. Edel

2. 1 Oxidationsstufen Demo 1: Edel vs. Unedel /

2. 1 Oxidationsstufen Spannungsreihe • durch die Spannungsreihe lässt sich voraussagen, welche Redoxreaktionen möglich sind • Elemente mit einem niedrigeren Reduktionspotential (E°) geben Elektronen an die Elemente mit einem höheren Standardpotential ab E° in V Zn Zn 2+ + 2 e 0, 76 H 2 2 H+ + 2 e 0, 00 Cu Cu 2+ + 2 e + 0, 34
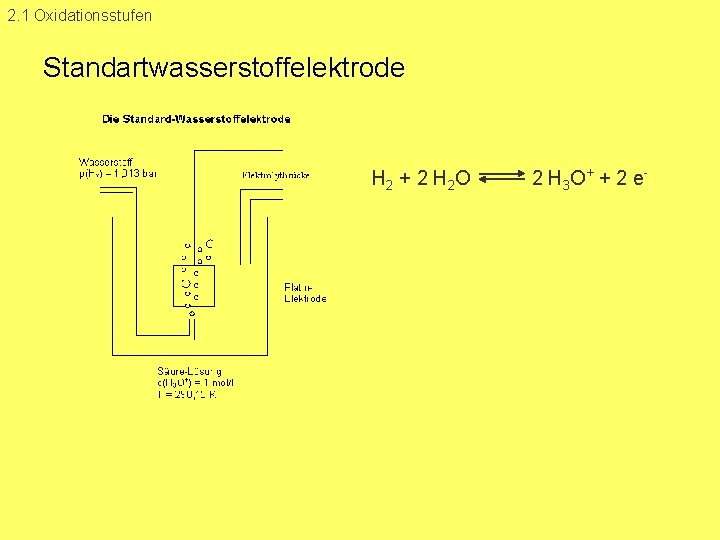
2. 1 Oxidationsstufen Standartwasserstoffelektrode H 2 + 2 H 2 O 2 H 3 O+ + 2 e

2. 2 Komplexe
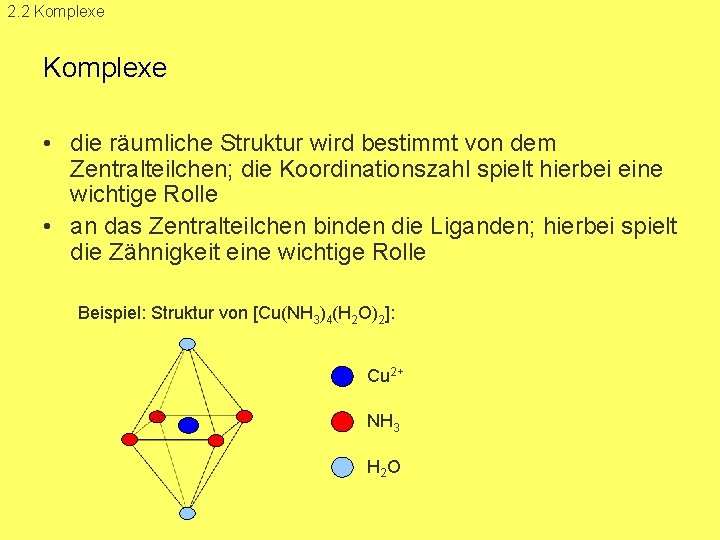
2. 2 Komplexe • die räumliche Struktur wird bestimmt von dem Zentralteilchen; die Koordinationszahl spielt hierbei eine wichtige Rolle • an das Zentralteilchen binden die Liganden; hierbei spielt die Zähnigkeit eine wichtige Rolle Beispiel: Struktur von [Cu(NH 3)4(H 2 O)2]: Cu 2+ NH 3 H 2 O
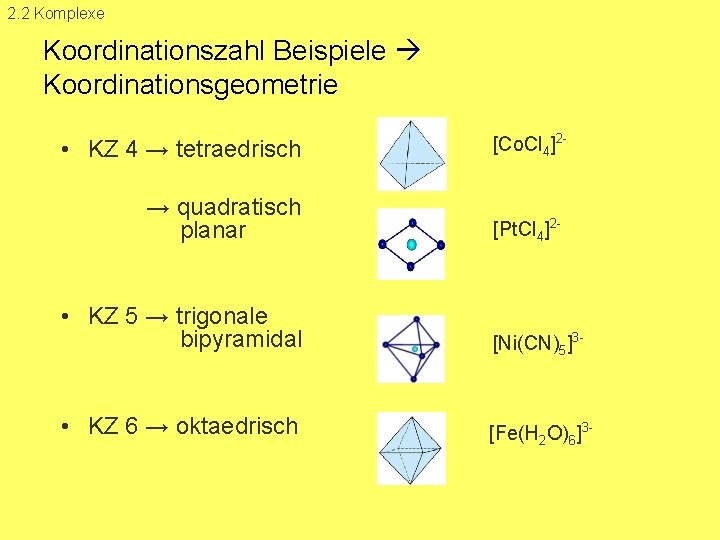
2. 2 Komplexe Koordinationszahl Beispiele Koordinationsgeometrie • KZ 4 → tetraedrisch → quadratisch planar [Co. Cl 4]2 [Pt. Cl 4]2 • KZ 5 → trigonale bipyramidal [Ni(CN)5]3 • KZ 6 → oktaedrisch [Fe(H 2 O)6]3
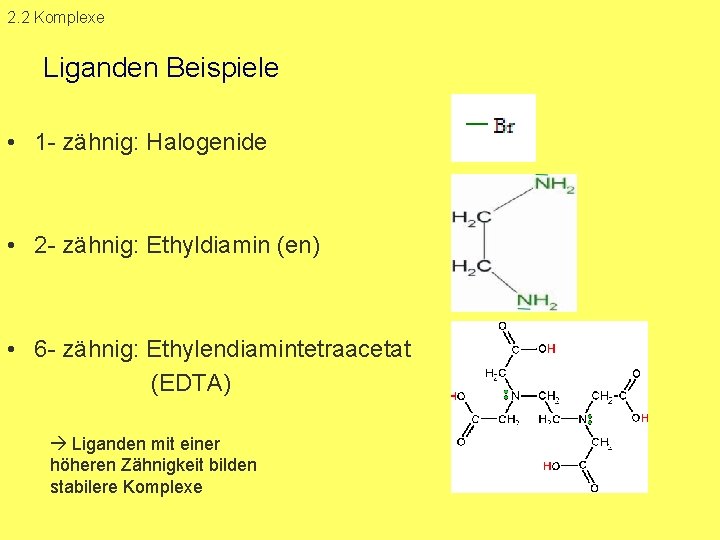
2. 2 Komplexe Liganden Beispiele • 1 zähnig: Halogenide • 2 zähnig: Ethyldiamin (en) • 6 zähnig: Ethylendiamintetraacetat (EDTA) Liganden mit einer höheren Zähnigkeit bilden stabilere Komplexe

Versuch 2: Gleichgewicht in Kupferkomplexen

2. 2 Komplexe Versuch 2: Gleichgewicht in Kupferkomplexen blaugrün himmelblaugrün hellgrün blaugrün dunkelblau
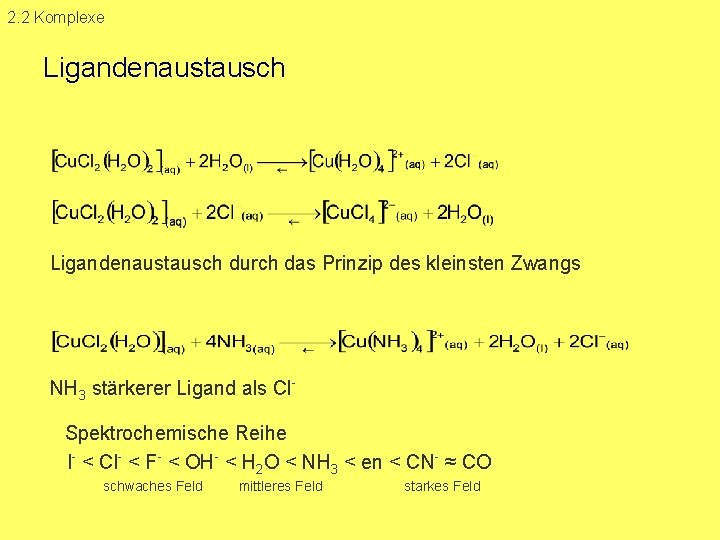
2. 2 Komplexe Ligandenaustausch durch das Prinzip des kleinsten Zwangs NH 3 stärkerer Ligand als Cl Spektrochemische Reihe I < Cl < F < OH < H 2 O < NH 3 < en < CN ≈ CO schwaches Feld mittleres Feld starkes Feld

Versuch 3: Magnetismus
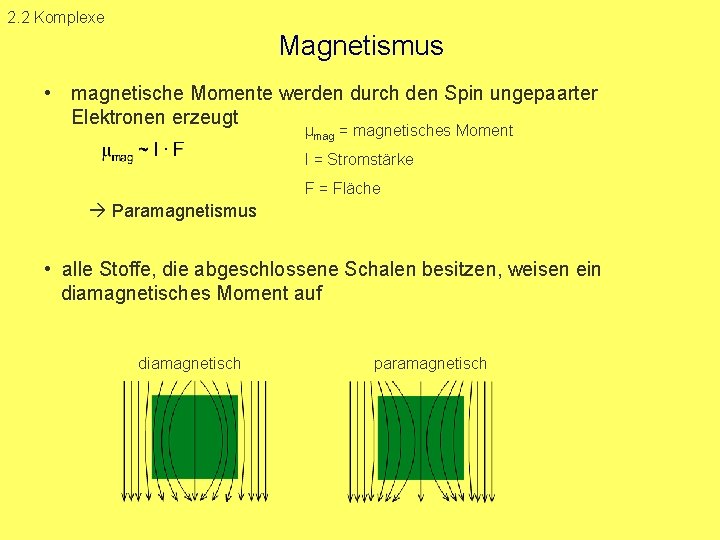
2. 2 Komplexe Magnetismus • magnetische Momente werden durch den Spin ungepaarter Elektronen erzeugt μmag = magnetisches Moment I = Stromstärke F = Fläche Paramagnetismus • alle Stoffe, die abgeschlossene Schalen besitzen, weisen ein diamagnetisches Moment auf diamagnetisch paramagnetisch
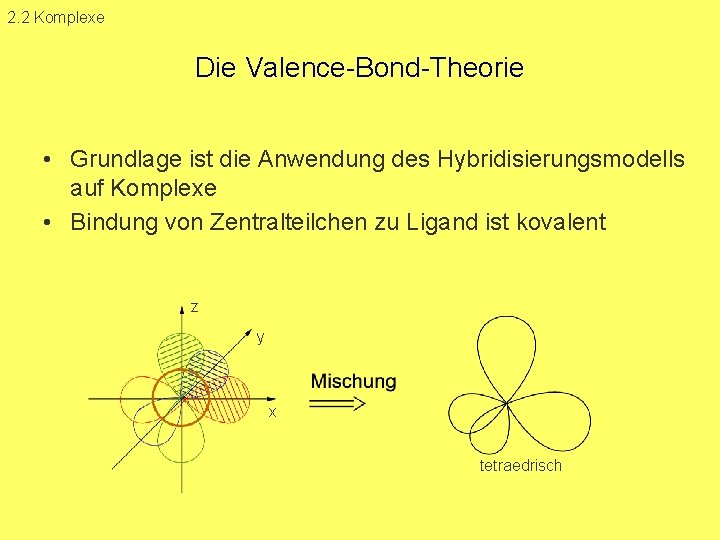
2. 2 Komplexe Die Valence Bond Theorie • Grundlage ist die Anwendung des Hybridisierungsmodells auf Komplexe • Bindung von Zentralteilchen zu Ligand ist kovalent z y x tetraedrisch
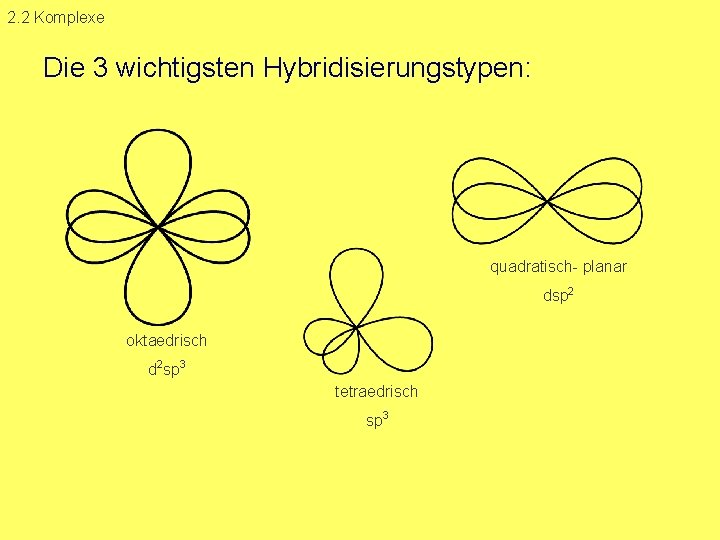
2. 2 Komplexe Die 3 wichtigsten Hybridisierungstypen: quadratisch planar dsp 2 oktaedrisch d 2 sp 3 tetraedrisch sp 3
![2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(H 2 O)6]2+ 4 s 2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(H 2 O)6]2+ 4 s](http://slidetodoc.com/presentation_image_h2/a7679fa6dbd0d17e899edd211262689e/image-31.jpg)
2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(H 2 O)6]2+ 4 s 4 p 4 d Hybridisierung Besetzung der Hybridorbitale durch Ligandenelektronen
![2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(CN)6]4 4 s 4 p 2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(CN)6]4 4 s 4 p](http://slidetodoc.com/presentation_image_h2/a7679fa6dbd0d17e899edd211262689e/image-32.jpg)
2. 2 Komplexe Magnetismus 3 d Fe 2+ im [Fe(CN)6]4 4 s 4 p Spinpaarung und Hybridisierung Besetzung der Hybridorbitale durch Ligandenelektronen Vergleich:

Versuch 4: Jahn Teller Verzerrung
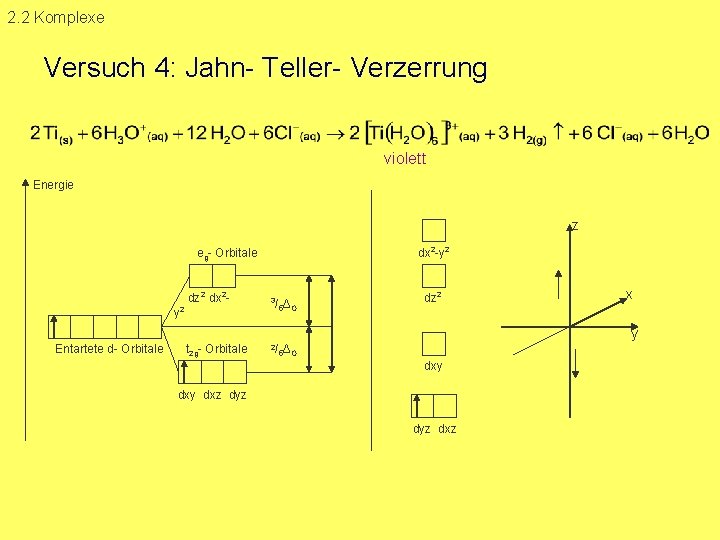
2. 2 Komplexe Versuch 4: Jahn Teller Verzerrung violett Energie z dx 2 y 2 eg Orbitale 2 dz 2 dx 2 3 t 2 g Orbitale 2/ y /5ΔO dz 2 x y Entartete d Orbitale 5ΔO dxy dxz dyz dxz

Versuch 5: 2+ Ni Nachweis
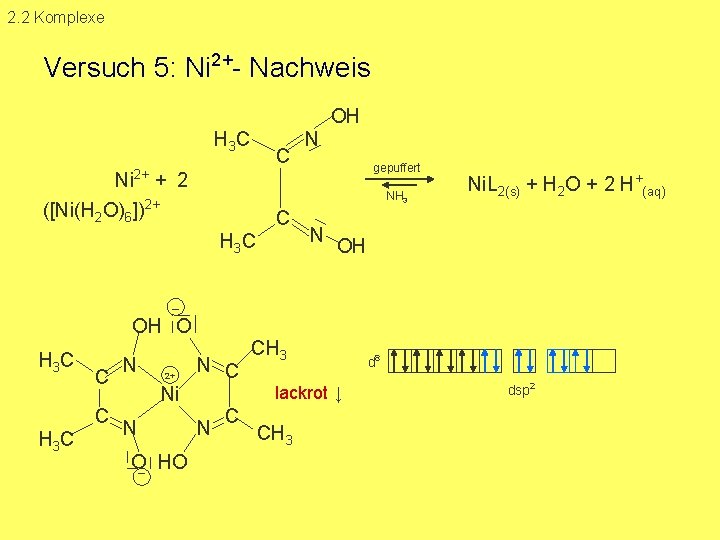
2. 2 Komplexe Versuch 5: Ni 2+ Nachweis OH H 3 C C N gepuffert 2+ Ni + 2 ([Ni(H 2 O)6])2+ NH 3 C N Ni. L 2(s) + H 2 O + 2 H+(aq) OH _ OH O H 3 C C C H 3 C N 2+ N C lackrot ↓ Ni N O_ HO CH 3 N C CH 3 d 8 dsp 2
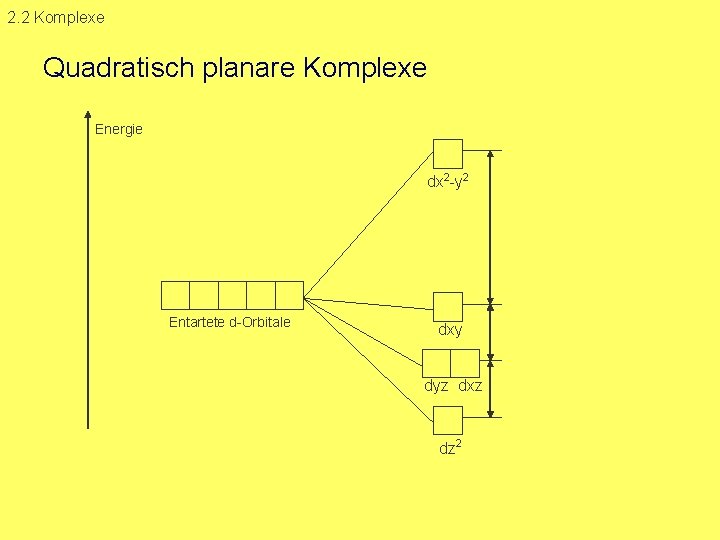
2. 2 Komplexe Quadratisch planare Komplexe Energie dx 2 y 2 Entartete d Orbitale dxy dyz dxz dz 2
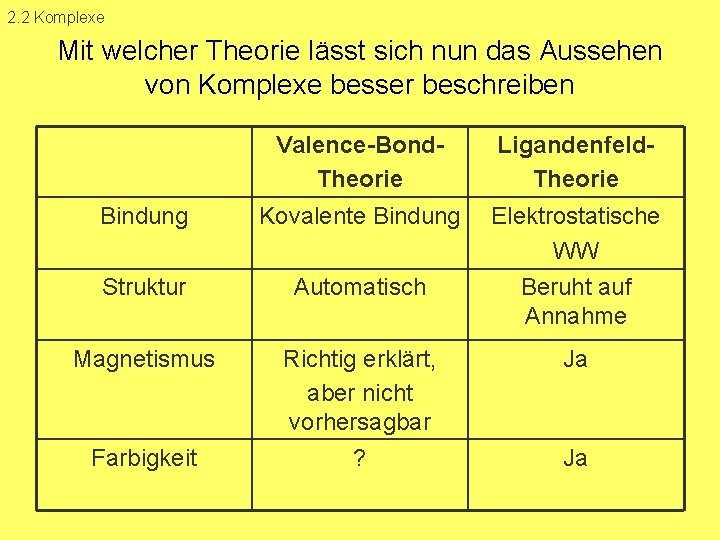
2. 2 Komplexe Mit welcher Theorie lässt sich nun das Aussehen von Komplexe besser beschreiben Valence-Bond. Theorie Ligandenfeld. Theorie Bindung Kovalente Bindung Elektrostatische WW Struktur Automatisch Beruht auf Annahme Magnetismus Richtig erklärt, aber nicht vorhersagbar Ja Farbigkeit ? Ja

2. 3 Farbige Salze

2. 3 Farbige Salze Farbige Verbindungen • die meisten Verbindungen der Hauptgruppenmetalle sind farblos bzw. weiß • Verbindungen der Übergangselemente sind dagegen oft intensiv farbig Grund: 1. d d Übergänge 2. Charge Transfer

Demo 2: Chrom Salze
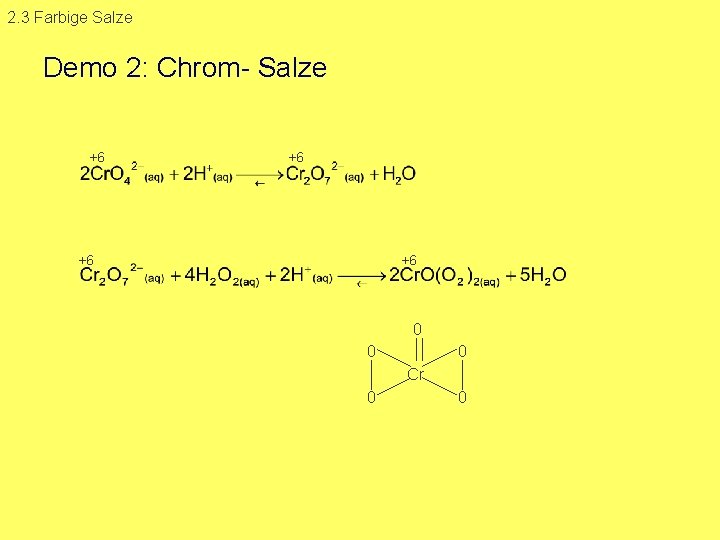
2. 3 Farbige Salze Demo 2: Chrom Salze +6 +6 0 0 0 Cr 0 0

2. 4 Katalysatoren

2. 4 Katalysatoren • • griech. katalysis = Auflösung beeinflusst die Geschwindigkeit chemischer Reaktionen ohne dabei verbraucht zu werden Veränderung der Aktivierungsenergie positive Katalysatoren setzen sie herab negative setzen diese herauf ändern die Kinetik aber nicht die Thermodynamik aber verändern nicht das Gleichgewicht einer Reaktion

2. 4 Katalysatoren Geschichte des Katalysators • schon in der Antike genutzt • erst Jöns Jakob Berzelius erkannte 1835 die Kraft der Katalysatoren und gab ihnen den Namen • Wilhelm Ostwald erforschte den Mechanismus und bekam Anfang das 20. Jahrhunderts den Nobelpreis für Chemie

2. 4 Katalysatoren Definition eines Katalysators noch W. Ostwald „Ein Katalysator ist ein Stoff, der die Geschwindigkeit einer chemischen Reaktion erhöht, ohne selbst dabei verbracht zu werden und ohne die endgültige Lage des thermodynamischen Gleichgewichts dieser Reaktion zu verändern. “

2. 4 Katalysatoren Bedeutung von Katalysatoren Lebewesen: • fast alle lebensnotwendigen Prozesse laufen katalysiert ab Autoabgaskatalysator: • unvermeidbare, giftige Gase werden in weniger gefährliche umgesetzt
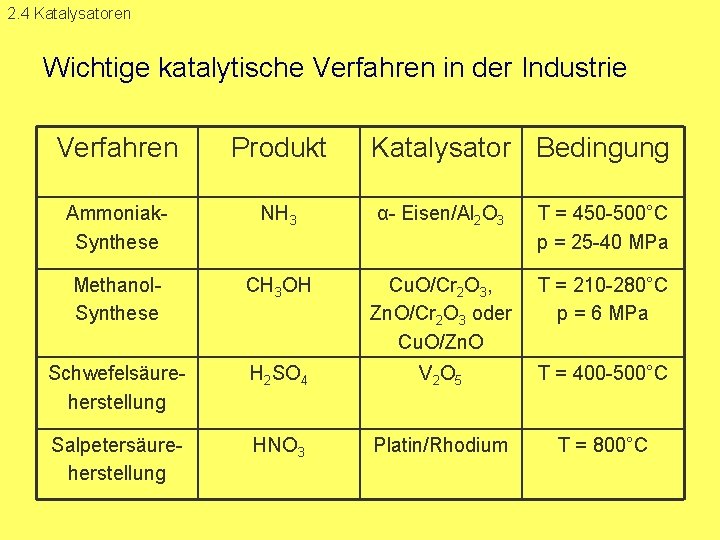
2. 4 Katalysatoren Wichtige katalytische Verfahren in der Industrie Verfahren Produkt Katalysator Bedingung Ammoniak Synthese NH 3 α Eisen/Al 2 O 3 T = 450 500°C p = 25 40 MPa Methanol Synthese CH 3 OH Cu. O/Cr 2 O 3, Zn. O/Cr 2 O 3 oder Cu. O/Zn. O T = 210 280°C p = 6 MPa Schwefelsäure herstellung H 2 SO 4 V 2 O 5 T = 400 500°C Salpetersäure herstellung HNO 3 Platin/Rhodium T = 800°C

Versuch 6: Beschleunigung des Zerfalls von H 2 O 2 durch Mn. O 2
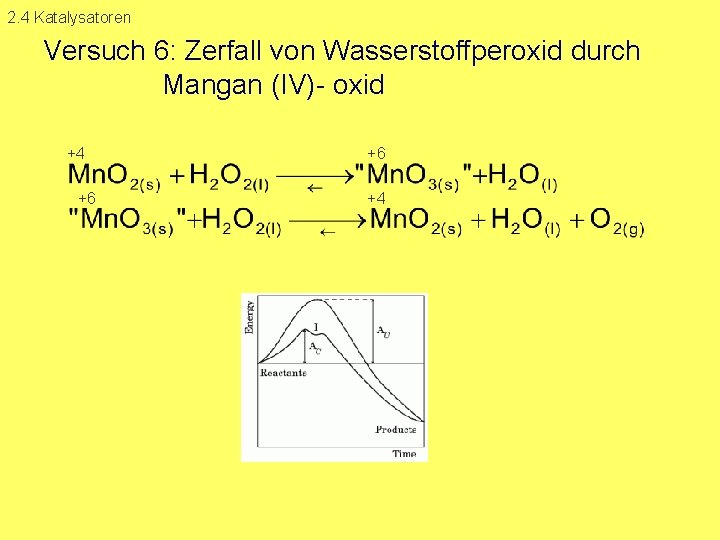
2. 4 Katalysatoren Versuch 6: Zerfall von Wasserstoffperoxid durch Mangan (IV) oxid +4 +6 +6 +4

Schulische Relevanz • Jahrgangsstufe 11: Redoxreaktionen Oxidationsstufen Standartwasserstoffelektrode • Jahrgangsstufe 13. 1 Prinzip vom Zwang Ligandenaustausch Geschwindigkeit chem. Reaktionen Katalysator • Jahrgangsstufe 13. 2 Wahlthema „Komplexchemie“ Kupferkomplexe Jahn Teller Verzerrung Ni Nachweis

Vielen Dank für Ihre Aufmerksamkeit
- Slides: 52