EGITURA ATOMIKOA ATOMOAREN EGITURA Thomsonen eredu atomikoa amaitu












- Slides: 18

EGITURA ATOMIKOA

ATOMOAREN EGITURA Thomson-en eredu atomikoa amaitu. Rutherford-en saiakuntza Masa atomikoa Hipotesia Nukleo atomikoa Rutherford-en eredu atomikoa (1911)

Thomson-en eredua amaitzen � Thomson-en plum cake teoria: = *Oso garrantzitsua izan zen atomoaren azterketa sakontzeko

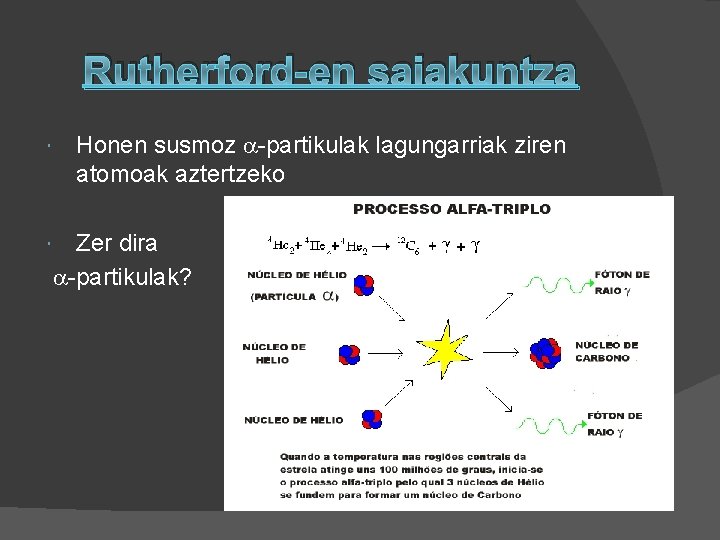
Rutherford-en saiakuntza Honen susmoz -partikulak lagungarriak ziren atomoak aztertzeko Zer dira -partikulak?

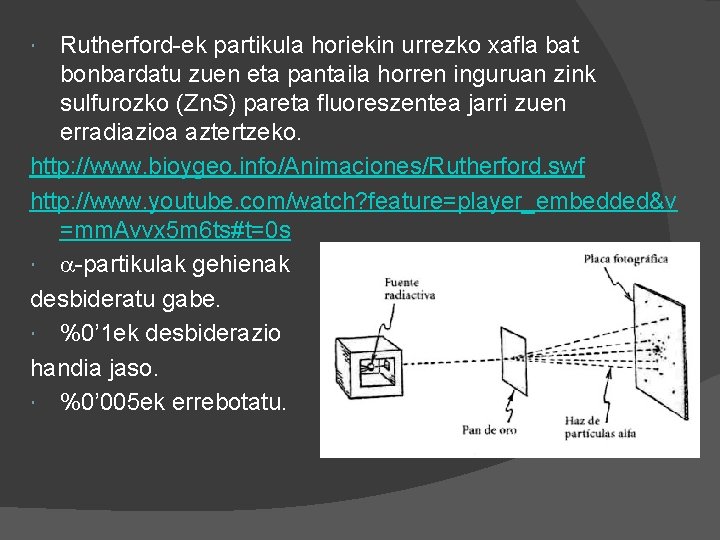
Rutherford-ek partikula horiekin urrezko xafla bat bonbardatu zuen eta pantaila horren inguruan zink sulfurozko (Zn. S) pareta fluoreszentea jarri zuen erradiazioa aztertzeko. http: //www. bioygeo. info/Animaciones/Rutherford. swf http: //www. youtube. com/watch? feature=player_embedded&v =mm. Avvx 5 m 6 ts#t=0 s -partikulak gehienak desbideratu gabe. %0’ 1 ek desbiderazio handia jaso. %0’ 005 ek errebotatu.

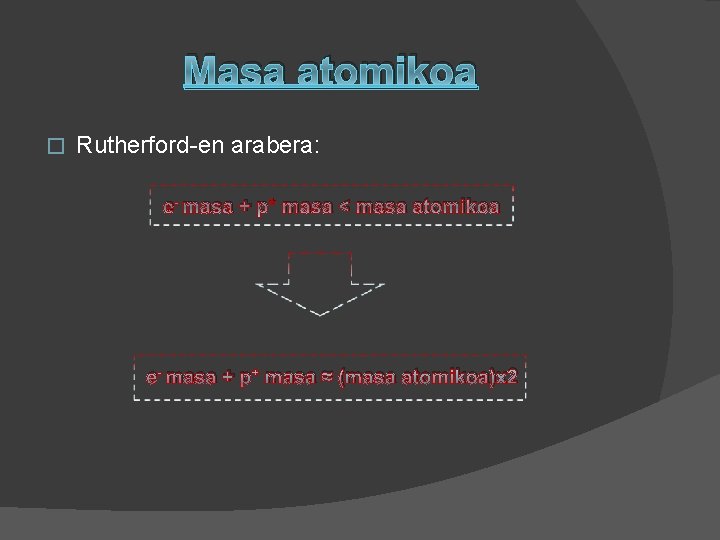
Masa atomikoa � Rutherford-en arabera: e- masa + p+ masa < masa atomikoa e- masa + p+ masa ≈ (masa atomikoa)x 2

Hipotesia � Rutherford-ek hau defendatu zuen:

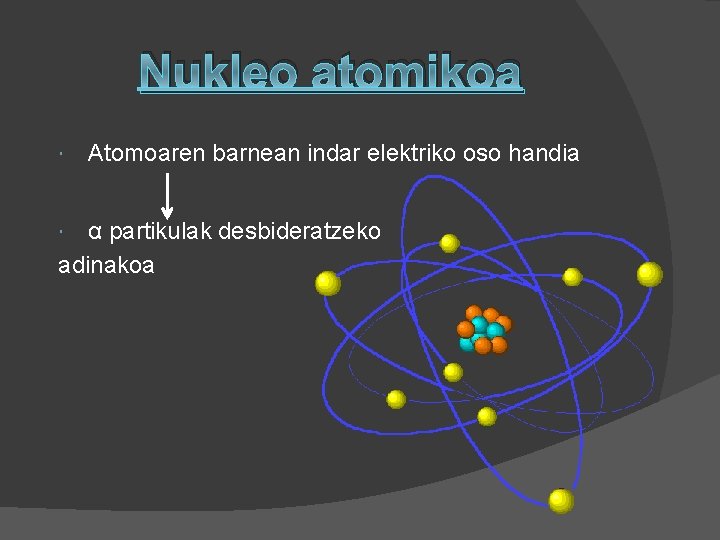
Nukleo atomikoa Atomoaren barnean indar elektriko oso handia α partikulak desbideratzeko adinakoa

ONDORIOA: -- Elektroiek atomoaren bolumen osoa bete -- Elektrizitate positiboa nukleo oso txikian kontzentraturik

Neutroia (1932) J. Chadwick fisikari ingelesak – erreakzio nuklearra NEUTROIAREN KARGA: 0 NEUTROIAREN MASA: Mn =1, 674 954 · 10 -27

Rutherford-en eredu atomikoa (1911) -Nukleoaren aurkikuntza eredu atomiko berria Rutherforden proposamena: ·MASA gehiena eta atomoaren KARGA POSITIBO guztia nukleoan ·ELEKTROIAK nukleoaren inguruan orbita zirkularrak eginez. ·Atomoa neutroa da [ elektroak, protoiak = ]

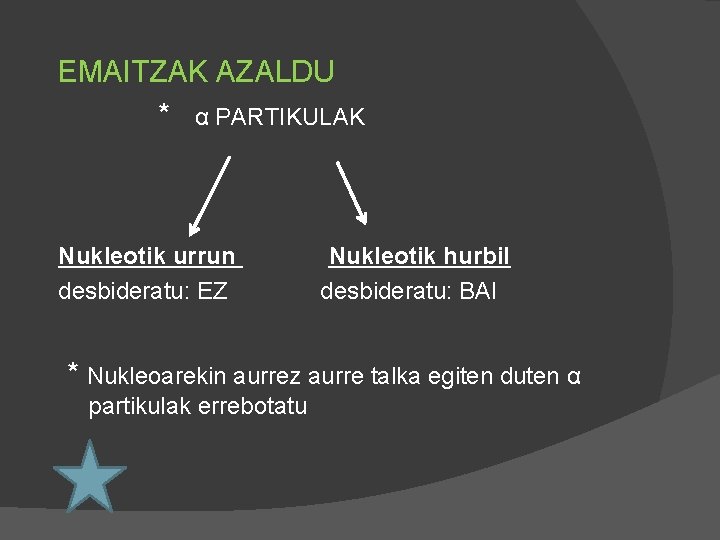
EMAITZAK AZALDU * α PARTIKULAK Nukleotik urrun desbideratu: EZ Nukleotik hurbil desbideratu: BAI * Nukleoarekin aurrez aurre talka egiten duten α partikulak errebotatu

ELEMENTU KIMIKOAK ETA ISOTOPOAK

Elementu kimikoak eta isotopoak ФElementu baten karga nuklearrari, zenbaki atomikoa deitzen zaio, Z. Ф Atomoaren nukleoan dauden nukleoien kopurua masazenbakia esaten zaio, A. A= Z+N A= neutroien eta protoien batura Z= protoien kopurua N= neutroi kopurua

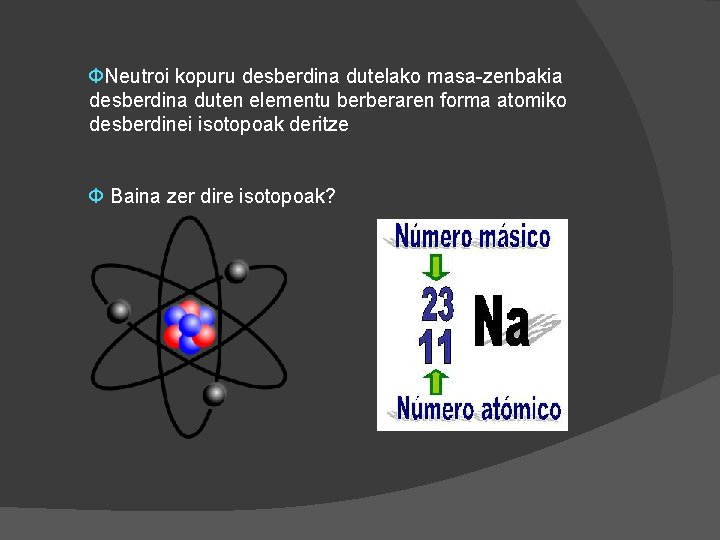
ФNeutroi kopuru desberdina dutelako masa-zenbakia desberdina duten elementu berberaren forma atomiko desberdinei isotopoak deritze Ф Baina zer dire isotopoak?

Masa atomikoa eta masa isotopikoa ФZer da masa atomikoa? Ф Nola lortu masa isotopikoa?

Elementu baten masa atomikoa lortzeko, kontuan izan behar ditugu isotopo natural guztiak. Zer da ugaritasun isotopiko erlatiboa edo ugaritasun isotopikoa? http: //www. youtube. com/watch? v=n. P 5 MHf 09 au. M&feature=related

Egileak: • Eduardo Bonilla • Ainhoa Vidal • German Velayos http: //www. youtube. com/watch? v=l v 0_OYKdmdw&feature=related