Efeito do p H sobre a ligao oxigniohemoglobina

Efeito do p. H sobre a ligação oxigêniohemoglobina e transporte do CO 2 Profa. Dra. Cínthia Pereira Machado Tabchoury Faculdade de Odontologia de Piracicaba UNICAMP

O que é p. H? • p significa “logaritmo negativo de” (- log) • Então, p. H = - log [H+] e p. OH = - log [OH-] • para H 2 O : p. H = - log 10 -7 = 7, 0 p. OH = - log 10 -7 = 7, 0 • É um artifício matemático • O p. H é inversamente proporcional à concentração de H+

Qual a origem do íon hidrogênio? • Um dos solutos mais importantes do corpo. • Pode interferir com as pontes de hidrogênio e nas forças de van der Waals. • Provenientes da separação da água. H 2 O H+ + OH • Moléculas ionizadas que liberam íons H+. Ex: CO 2 + H 2 O H 2 CO 3 H+ + HCO 3 • Somente H+ livres é que afetam a concentração de H+.

Escala de p. H • É logarítmica • Isto é, se o valor do p. H muda em uma unidade, • a concentração de H+ aumenta ou diminui em 10 vezes.
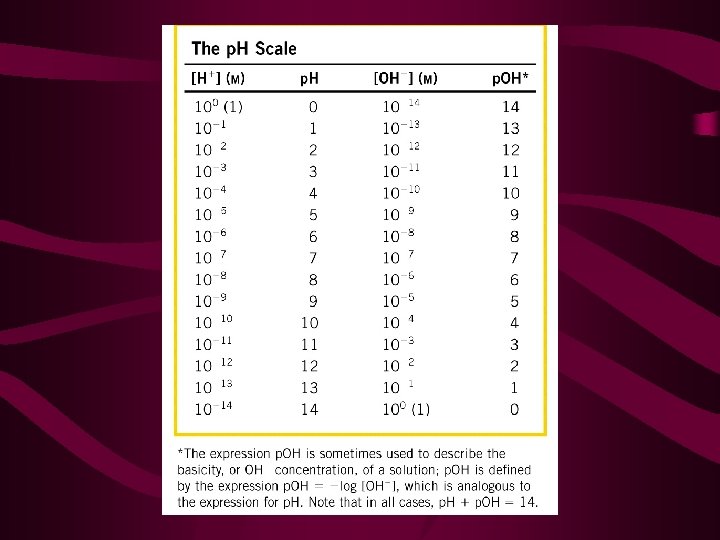
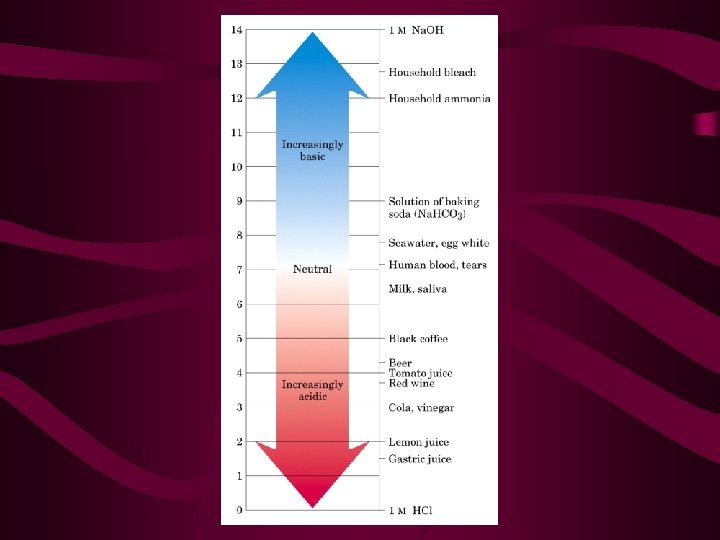

TAMPÕES • Fator-chave na capacidade do corpo em manter o p. H normal. • Solução tampão é aquela capaz de resistir às variações de p. H. • São misturas de ácidos fracos e suas bases conjugadas • Mas o que é um ácido fraco? E sua base conjugada?

ÁCIDO FRACO • Citem um exemplo de ácido forte: • Ácidos fracos são aqueles que não se ionizam completamente quando dissolvidos em água. CH 3 COOH H+ + CH 3 COO • ácido fraco: CH 3 COOH doador de prótons • base conjugada: CH 3 COO- receptor de prótons
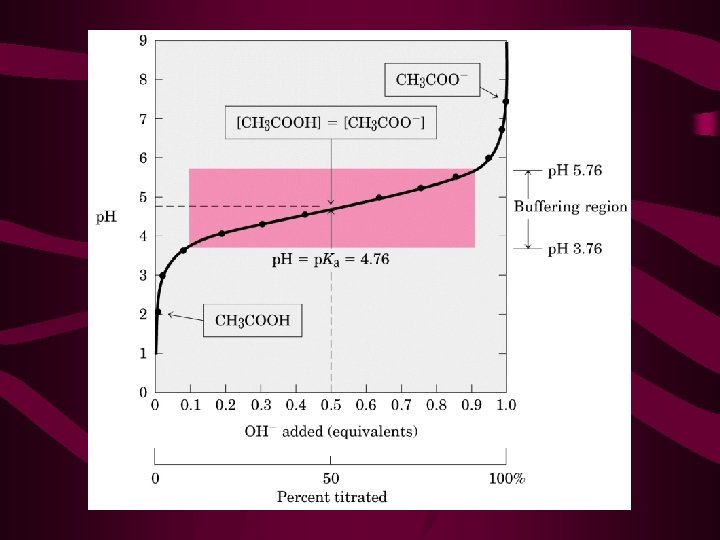
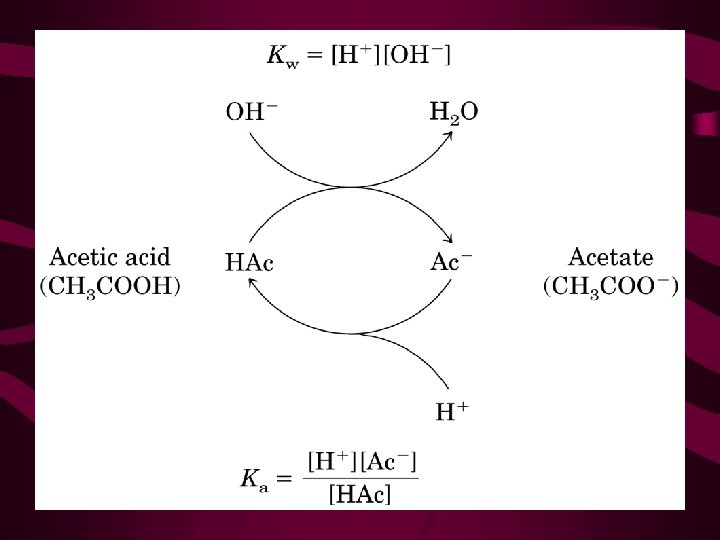
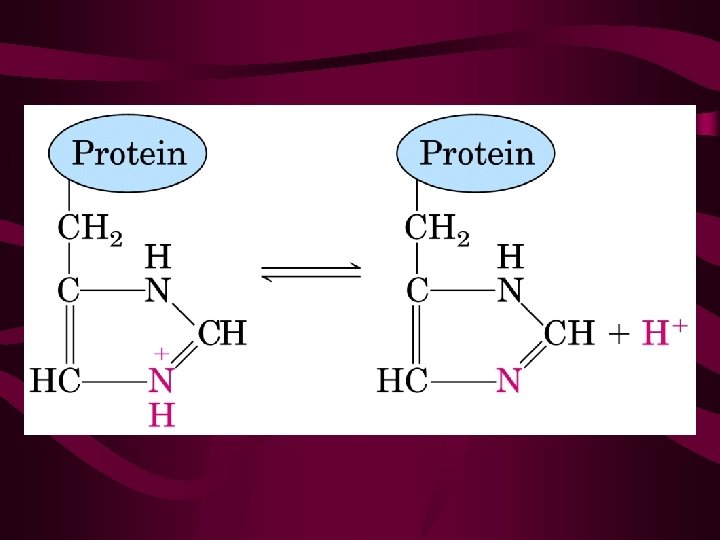

TAMPÕES BIOLÓGICOS • Bicarbonato: o mais importante na saliva e sangue • Fosfato: citoplasma das células • Proteínas

Efeito do p. H na ligação O 2 -Hb • A hemoglobina é uma proteína com 4 subunidades e um grupo heme; • Sua função é transportar O 2 para os tecidos; • Deve ligar O 2 eficientemente nos pulmões (p. O 2 – 13, 3 Kpa) e liberar O 2 nos tecidos (p. O 2 – 4 KPa). • Hemoglobina pode estar em 2 estados: T (tense) – baixa afinidade pelo O 2; R (relaxed) – alta afinidade pelo O 2.
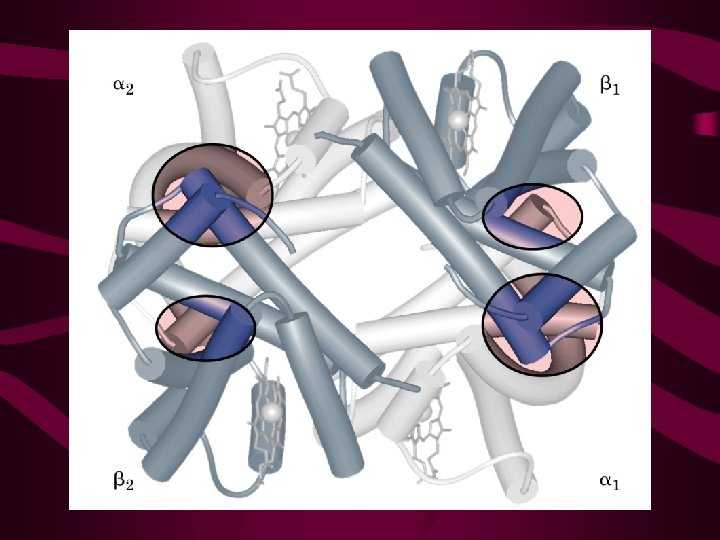
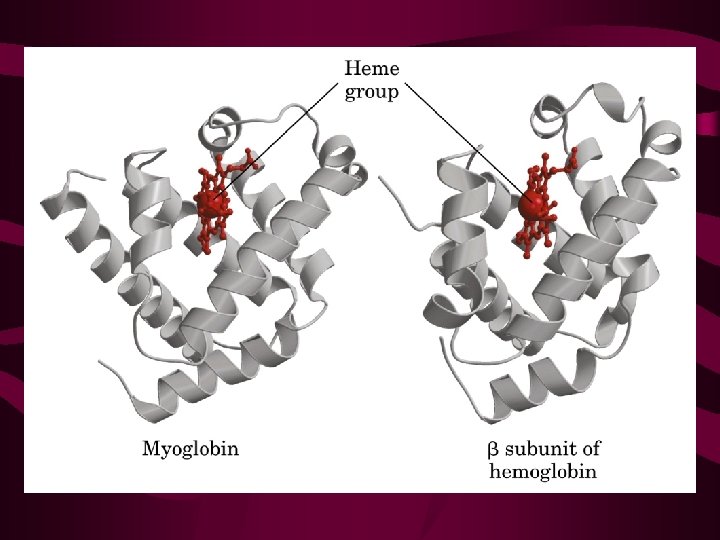
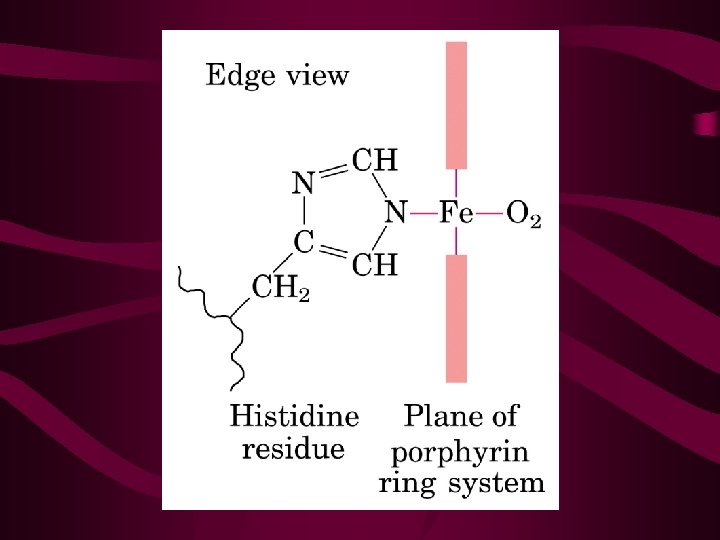
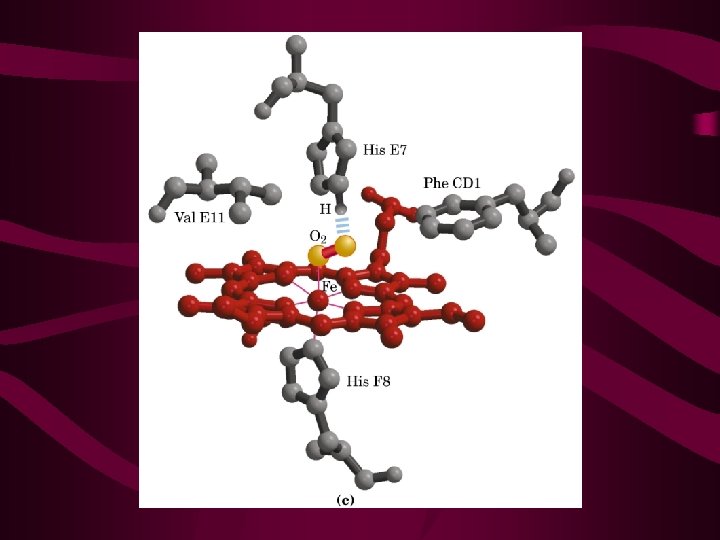
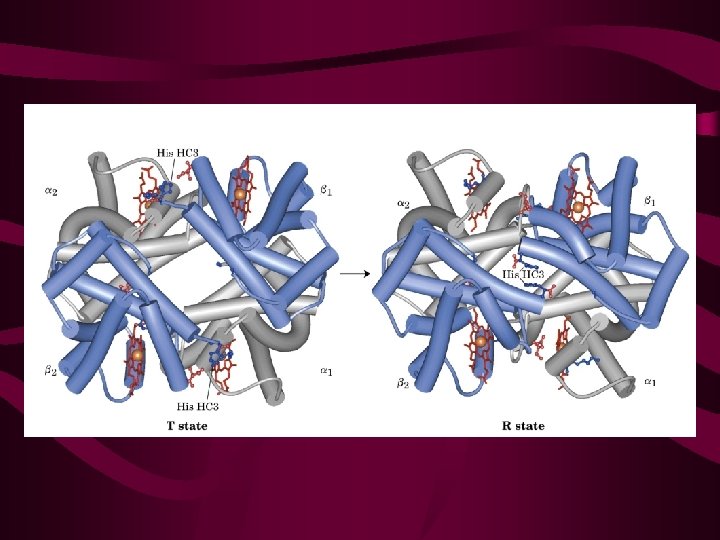

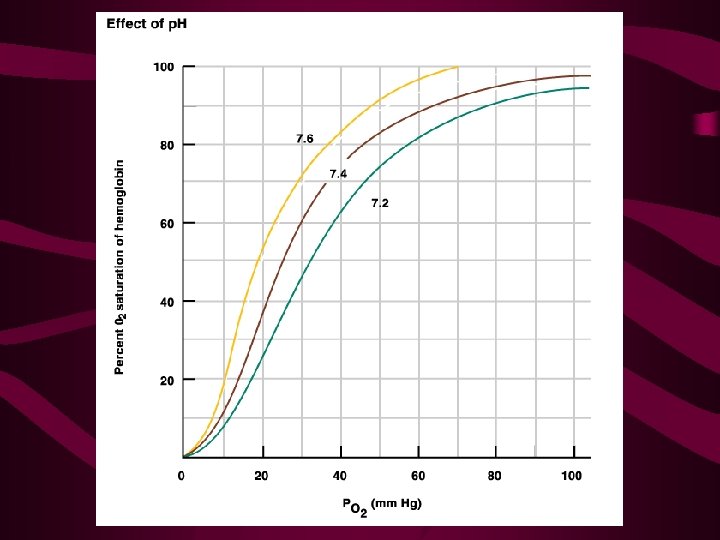
Efeito de fatores na ligação O 2 -Hb • A ligação de O 2 pela Hb é profundamente influenciada pelo p. H e pela concentração de CO 2; • Em baixo p. H e alta [ ] de CO 2 dos tecidos periféricos, a afinidade da Hb por O 2 diminui e O 2 é liberado para os tecidos; • Este efeito do p. H e [ ] de CO 2 na ligação e liberação de O 2 pela Hb é chamado de efeito Bohr.

Efeito do p. H na ligação O 2 -Hb • A diminuição do p. H diminui a afinidade da Hb pelo O 2 e muda a curva de dissociação O 2 -Hb; • O transporte de O 2 para os tecidos pode ser alterado de modo significativo. • Em p. H 7, 2, as moléculas de hemoglobina liberam 15% mais de O 2 do que em p. H 7, 4; • Durante exercício anaeróbio, há produção de ácido láctico, que libera H+ para dentro do citoplasma e para o fluido extracelular, levando à diminuição do p. H.

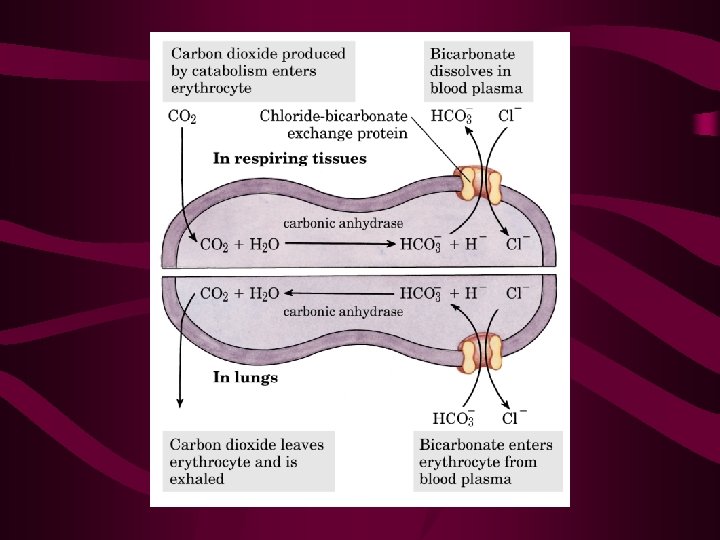
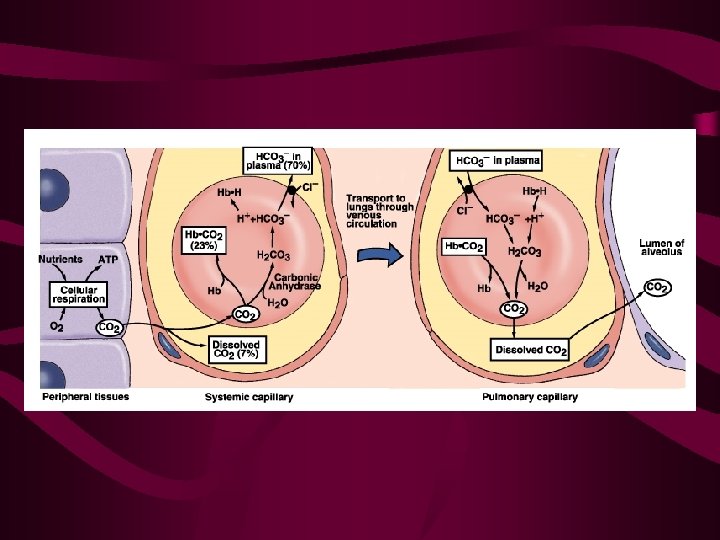
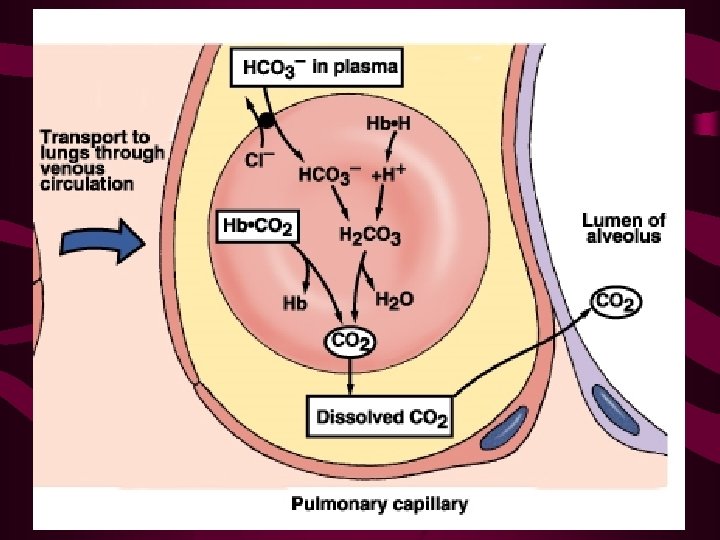
Transporte de dióxido de carbono • A remoção do CO 2 é essencial para a entrada de O 2; • CO 2 - 7% é transportado pelo sangue venoso na forma dissolvida 93% difunde-se para dentro das hemácias 70% é convertido em íon bicarbonato dissolvido no plasma 23% liga-se à hemoglobina (Hb. CO 2)

Transporte de dióxido de carbono Esta conversão de CO 2 em bicarbonato tem 2 propósitos: 1 – meio adicional para o CO 2 ser transportado das células para os pulmões; 2 – bicarbonato (HCO 3 -) está disponível para atuar como tampão.
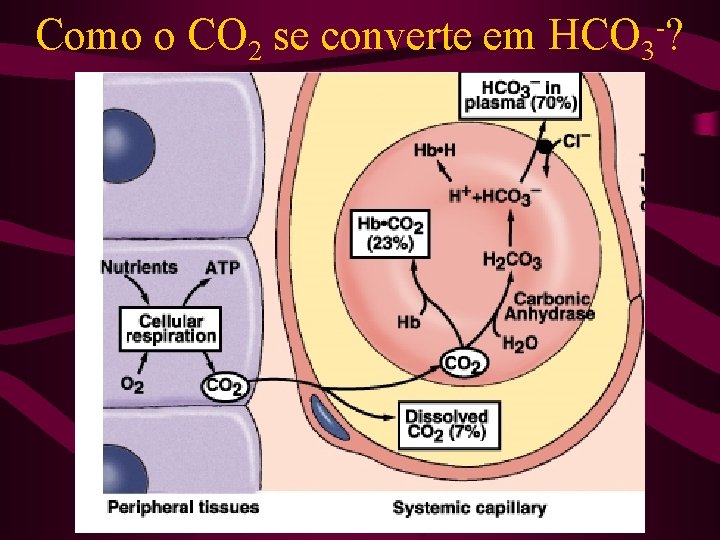
Como o CO 2 se converte em HCO 3 -?

Referências Bibliográficas NELSON, D. L. , COX, M. M. Lehninger Principles of Biochemistry. 3 a edição, 2000, capítulo 7, pág. 204 a 221. SILVERTHORN, DU. Fisiologia Humana. 2 a edição, Manole 2003, pág. 525 -529.
- Slides: 29