ECHEC THERAPEUTIQUE Changement de traitement Pr O Bouchaud

ECHEC THERAPEUTIQUE Changement de traitement Pr O. Bouchaud juin 2011

Causes de changements de traitement: n échec clinique, et/ou biologique n Effets indésirables n (allègement d’une combinaison) souci d’épargne thérapeutique Prévention des effets secondaires de long terme

Définition OMS de l’échec : évaluation initiale à 6 mois clinique Nouvelle manifestation ou récurrence du grpe 3 ou 4 Sd reconstitution immunitaire immunologique baisse au niveau pré TTT baisse de 50 % /pic sous TTT persistance < 50 (100) CD 4 < seuil virologique charge virale > 5000 Ou < 400 ? copies : ?

2 situations échec après une première ligne n n Nombre limité de mutations de résistance Rares cas de résistance primaire Échec chez patients déjà traités n Nombre +/- important de mutations de résistance d’autant plus important que multitraités

Analyse de la situation d’échec virologique Type d’échec virologique: 1. 2. 3. Réduction non-optimale de la charge virale Échappement virologique Absence de réponse ( diminution CV < 0, 5 log) Moment de l’échec virologique Niveau de l’échec virologique 1. 2. Intensité de l’échec (valeur absolue de la CV) Durée de l’échec virologique

Analyse de la situation d’échec virologique vérifier l’adéquation du traitement n posologie, inter-actions…. Évaluer l’adhésion et l’observance du patient n vérifier l’adéquation du traitement Préciser l’antériorité thérapeutique Évaluer la résistance du virus: tests génotypiques bilan des résistances acquises Évaluer les concentrations plasmatiques des ARV (IP et INN)

Chronologie de l’échec D’abord échec virologique par n n RESISTANCE Non prise du traitement ARV Puis échec immunologique Puis échec clinique
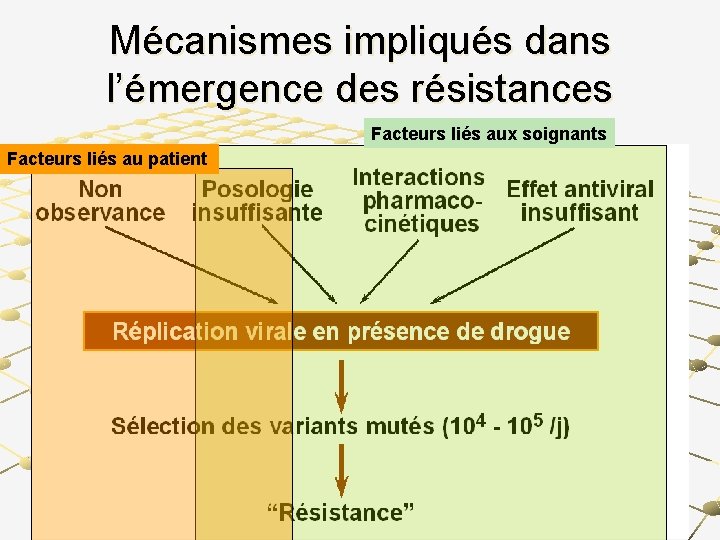
Mécanismes impliqués dans l’émergence des résistances Facteurs liés aux soignants Facteurs liés au patient

Il ne peut y avoir de résistance que si il y a en même temps dans le sang des virus VIH ET des médicaments ARVs
Notion de quasi-espèces
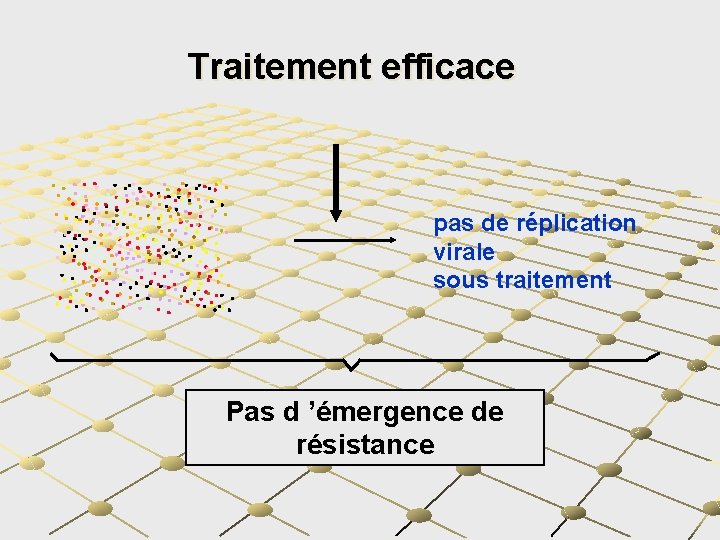
Traitement efficace pas de réplication virale sous traitement Pas d ’émergence de résistance
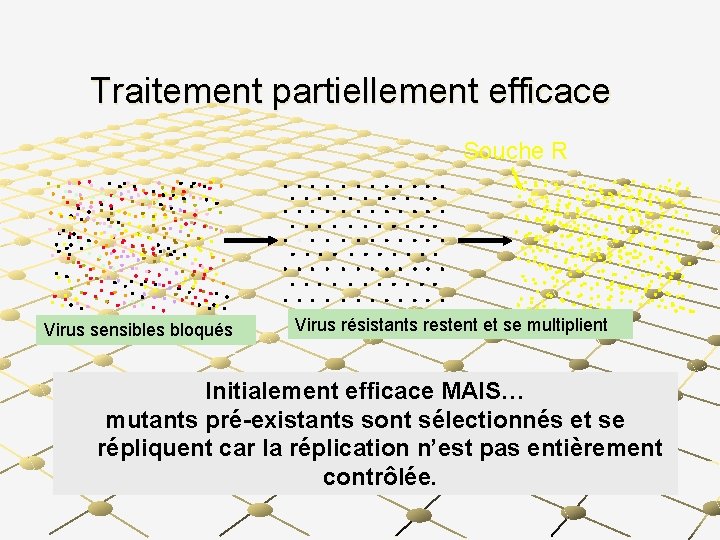
Traitement partiellement efficace Souche R Virus sensibles bloqués Virus résistants restent et se multiplient Initialement efficace MAIS… mutants pré-existants sont sélectionnés et se répliquent car la réplication n’est pas entièrement contrôlée.
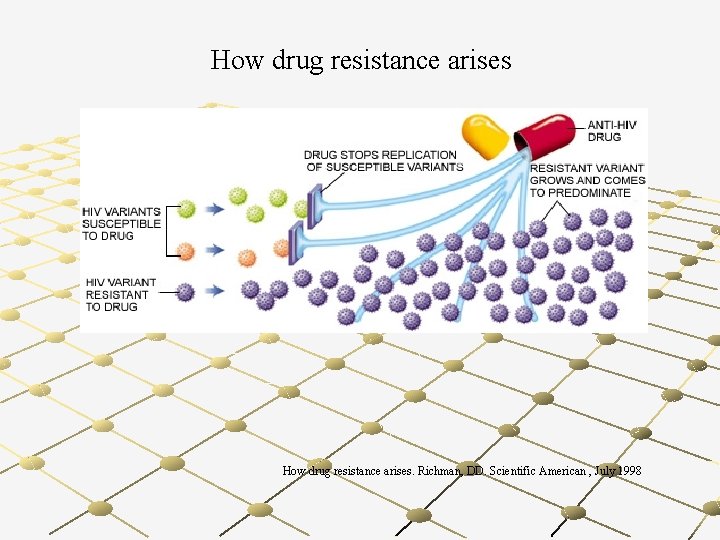
How drug resistance arises. Richman, DD. Scientific American , July 1998

« résistance » à la résistance Certains ARVs « résistent » mieux à la résistance que d’autres Nombre et effet des mutations: n Si 1 mutation (= 1 erreur) suffit pour la induire la résistance, elle apparaît facilement n n C’est le cas des NNUC (EFZ et NVP) S’il faut 8 mutations pour induire la résistance, elle apparaît plus difficilement n C’est le cas de certains IP comme le Kalétra Concentration des ARVs (CMI)
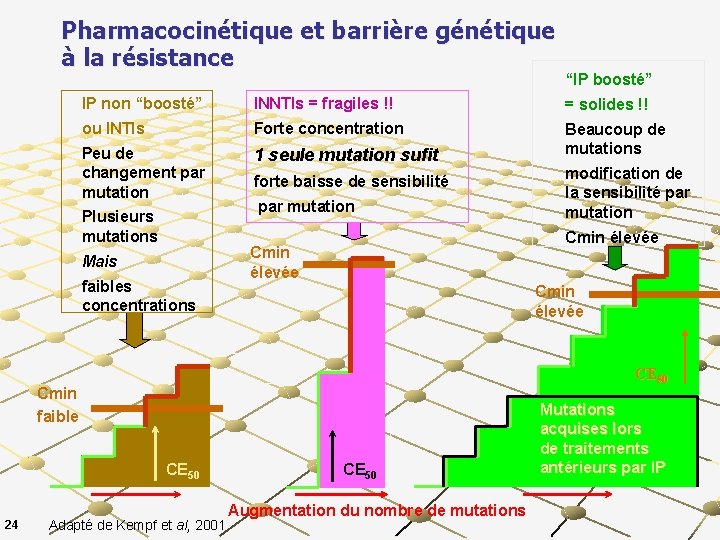
Pharmacocinétique et barrière génétique à la résistance IP non “boosté” INNTIs = fragiles !! = solides !! ou INTIs Forte concentration Peu de changement par mutation 1 seule mutation sufit Beaucoup de mutations Plusieurs mutations Mais faibles concentrations forte baisse de sensibilité par mutation modification de la sensibilité par mutation Cmin élevée CE 50 Cmin faible CE 50 24 “IP boosté” Adapté de Kempf et al, 2001 CE 50 Augmentation du nombre de mutations Mutations acquises lors de traitements antérieurs par IP
CAS 1 Patient , stade 4, cachexie Examens de laboratoire: Hb 7. 9 g/dl, Lymphocytes totaux: 600 Début ARV: 3 TC/D 4 T/NVP
CAS 1, 6 mois plus tard Gain pondéral: + 8 kg Pas de nouvelle IO LT = 1500 HB: 11 g/dl SUCCÈS? ECHEC?
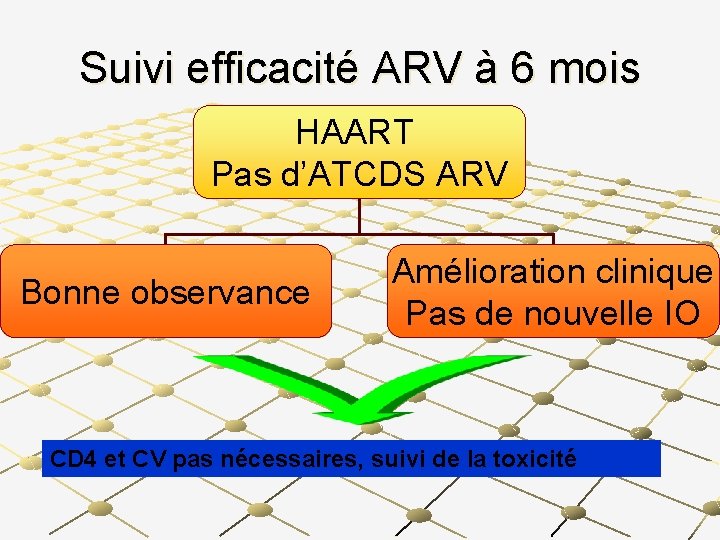
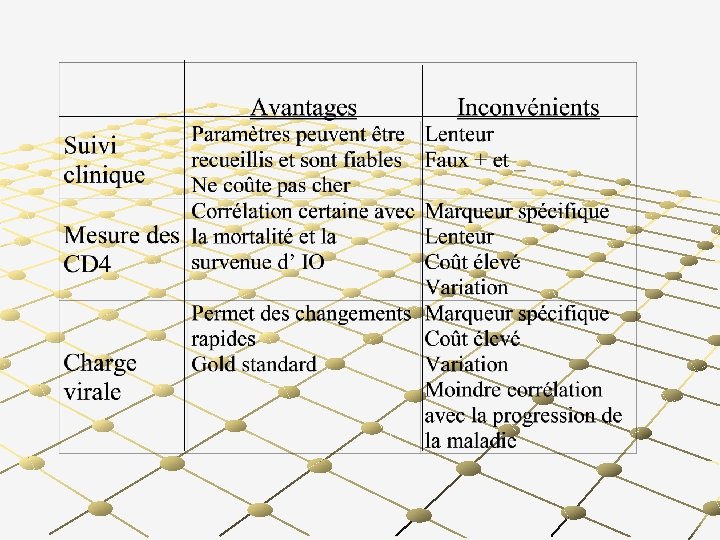
Suivi efficacité ARV à 6 mois HAART Pas d’ATCDS ARV Bonne observance Amélioration clinique Pas de nouvelle IO CD 4 et CV pas nécessaires, suivi de la toxicité

CAS 2 Patient, HIV (+), stade 3 OMS CD 4 : 180/mm³ Combinaison: 3 TC/AZT/NVP A 6 mois: pas de nouvelle IO, gain pondéral de 2 kg, et CD 4 à 200/mm³

Cas 2, 1 année plus tard Amaigrissement, candidose orale, fièvre intermittente CD 4 = 180/mm³ Le patient reconnaît avoir été traité dans une clinique privée avec DUOVIR (AZT/3 TC) mais il a arrêté son traitement par manque de moyens financiers SUCCÈS? ECHEC?
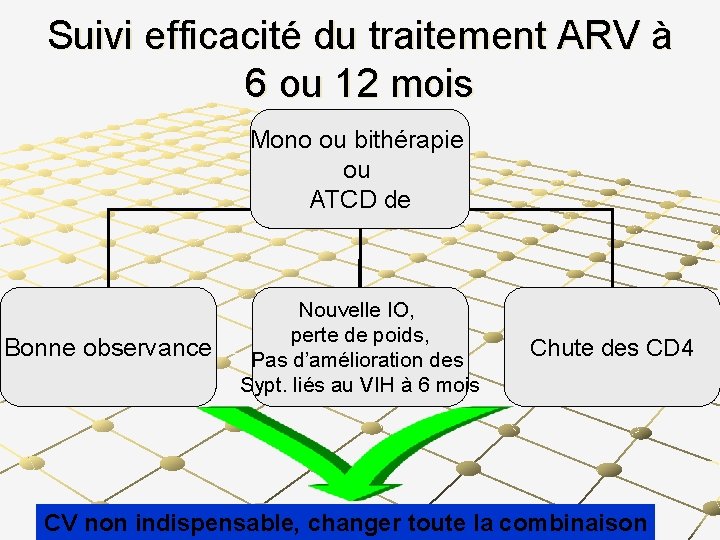
Suivi efficacité du traitement ARV à 6 ou 12 mois Mono ou bithérapie ou ATCD de Bonne observance Nouvelle IO, perte de poids, Pas d’amélioration des Sypt. liés au VIH à 6 mois Chute des CD 4 CV non indispensable, changer toute la combinaison

Cas 3 Un homme âgé de 44 ans marié, père de 4 enfants Depuis 7 mois présente une éruption papulaire et prurigineuse (PPE) Douleurs abdominales et diarrhée depuis 1 mois Candidose oro-pharyngée

Cas 3 CD 4 : 2/mm 3 GB: 2. 300, lymphocytes totaux: 800 Hb: 7. 8 g/dl Examen de selles: pas de parasites isolés Traité avec fluconazole, metronidazole, cetrizine et co-trimoxazole.

Une semaine plus tard Diarrhée a cessé, mais persistance de prurigo et douleurs abdominales Patient commence les ARVs après conseil (AZT, 3 TC, NVP) Sur une période de 4 mois suivant le début du traitement, le prurigo s’estompe progressivement mais le patient a des poussées récurrentes de candidoses buccales,

Au 6ème mois Prurigo nocturne reprend Patient a gagné 9 kg depuis le début du traitement Observance très bonne aux ARV et au Cotrimoxazole

Examens de laboratoire à M 6 CD 4 : 5/mm 3 GB: 2. 3 x 103/µl Lymphocytes totaux : 0. 5 x 103/µl Hb: 7. 9 g/dl
Résumé: Cas 3 Bonne observance, Amélioration clinique, mais récurrence de la candidose orale pendant les premiers mois de traitement. Pas de changement du nombre des CD 4. Échec de la combinaison thérapeutique? CV ?
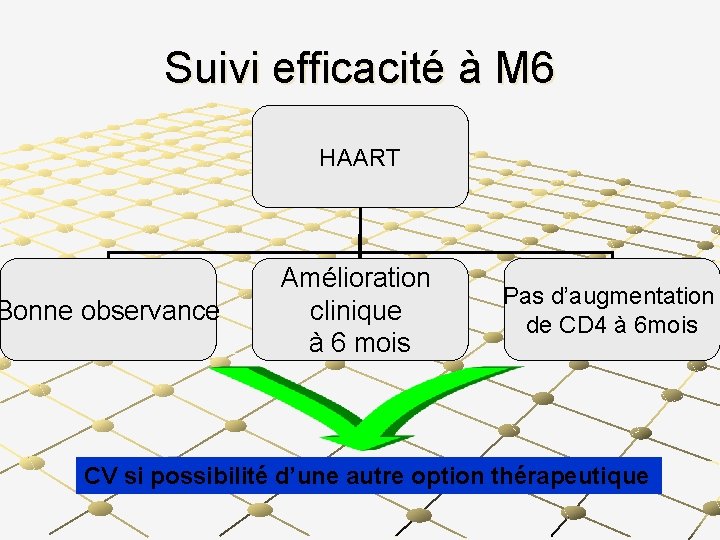
Suivi efficacité à M 6 HAART Bonne observance Amélioration clinique à 6 mois Pas d’augmentation de CD 4 à 6 mois CV si possibilité d’une autre option thérapeutique
Suivi efficacité du traitement ARV ATCDS de prise de traitement Régime actuel Bonne observance ? - mesure? - depuis quand? État clinique

Effets attendus du traitement Patients naïfs Avec bonne observance 70 - 80% auront une CV indétectable à 48 semaines de traitement. Facteur déterminant?
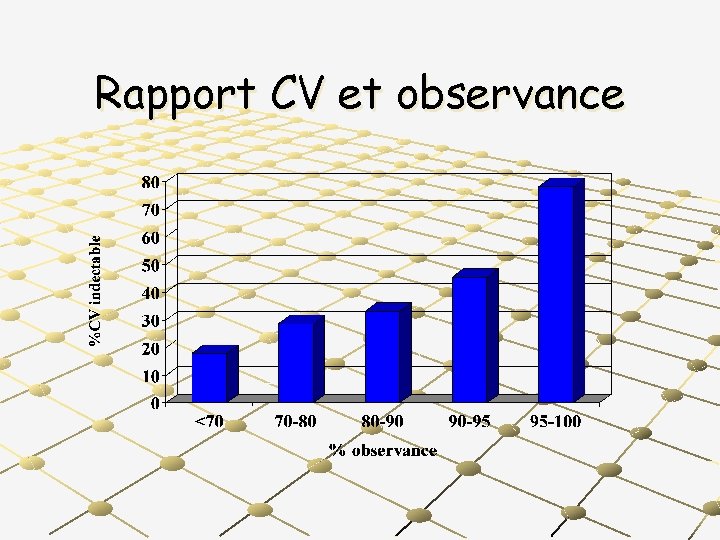
Rapport CV et observance

95 % d’observance minimum impératif = sur 100 prises : maximum 3 à 4 oublis possibles !!!!! = pas d’excès sur le respect des heures de prise

Observance et efficacité 110 patients sous AZT+3 TC+IDV(800 x 3) Évaluation succès (CV<50) à 24 semaines adhésion N= 68 CV<50 70, 6% >90%doses >1 oubli/j, +repas 25 40% <90%doses 17 35, 3% >90% doses <1 oubli/j

Seconde ligne de traitement pour adultes et adolescents en cas d’échec de la première ligne de traitement Cas 1 (Reco 2010 Burundi) AZT + 3 TC + NVP ou EFZ ABC + TDF* ou DDI + LPV/r ou ATZ/r * TDF si Ag Hb. S On peut laisser EN PLUS le 3 TC pour son effet sur sensibilité AZT/D 4 T + frein du fitness Tests de résistance en routine en cas d’échec n’ont pas de sens si il existe une seule deuxième ligne de ttt
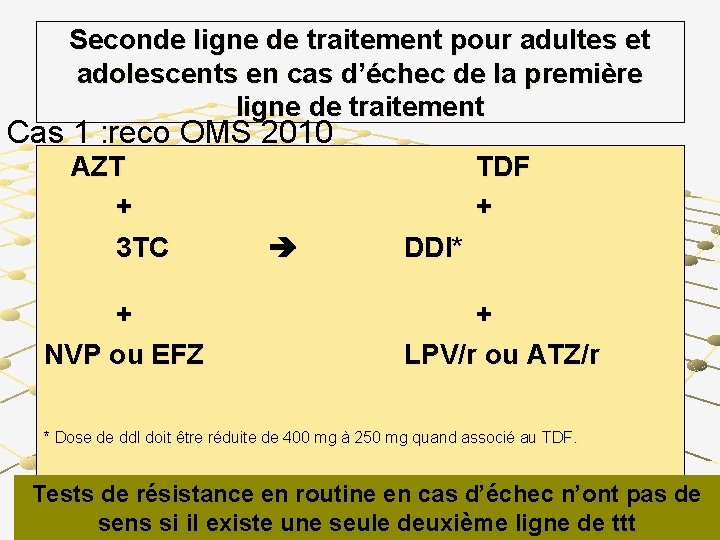
Seconde ligne de traitement pour adultes et adolescents en cas d’échec de la première ligne de traitement Cas 1 : reco OMS 2010 AZT + 3 TC + NVP ou EFZ TDF + DDI* + LPV/r ou ATZ/r * Dose de dd. I doit être réduite de 400 mg à 250 mg quand associé au TDF. On peut laisser EN PLUS le 3 TC pour son effet sur sensibilité AZT/D 4 T + frein du fitness Tests de résistance en routine en cas d’échec n’ont pas de sens si il existe une seule deuxième ligne de ttt
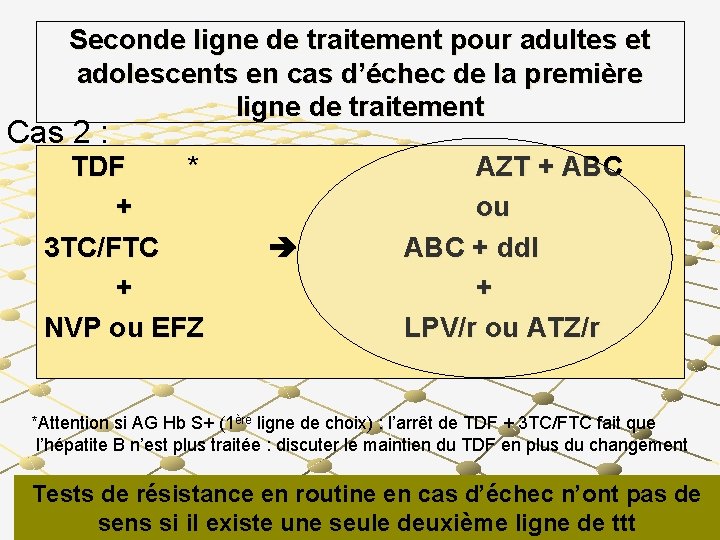
Seconde ligne de traitement pour adultes et adolescents en cas d’échec de la première ligne de traitement Cas 2 : TDF * + 3 TC/FTC + NVP ou EFZ AZT + ABC ou ABC + dd. I + LPV/r ou ATZ/r *Attention si AG Hb S+ (1ère ligne de choix) : l’arrêt de TDF + 3 TC/FTC fait que l’hépatite B n’est plus traitée : discuter le maintien du TDF en plus du changement Tests de résistance en routine en cas d’échec n’ont pas de sens si il existe une seule deuxième ligne de ttt
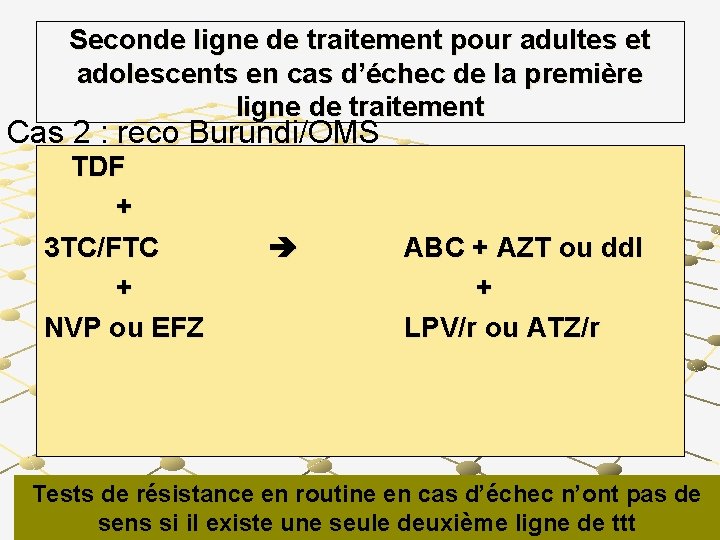
Seconde ligne de traitement pour adultes et adolescents en cas d’échec de la première ligne de traitement Cas 2 : reco Burundi/OMS TDF + 3 TC/FTC + NVP ou EFZ ABC + AZT ou dd. I + LPV/r ou ATZ/r Tests de résistance en routine en cas d’échec n’ont pas de sens si il existe une seule deuxième ligne de ttt
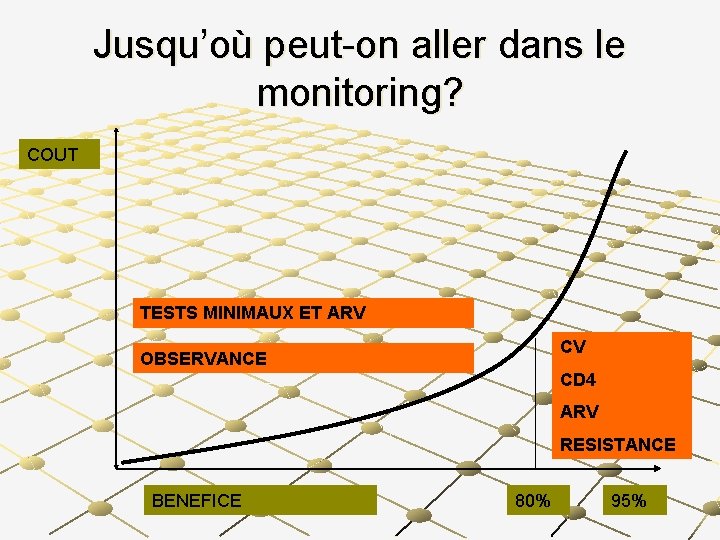
Jusqu’où peut-on aller dans le monitoring? COUT TESTS MINIMAUX ET ARV CV OBSERVANCE CD 4 ARV RESISTANCE BENEFICE 80% 95%
- Slides: 39