Dvidas denuccigdenucci com Arquivo Biodisponibilidade e Bioequivalncia O

Dúvidas denucci@gdenucci. com Arquivo Biodisponibilidade e Bioequivalência: O mercado de genéricos no Brasil e no mundo Site www. gdenucci. com
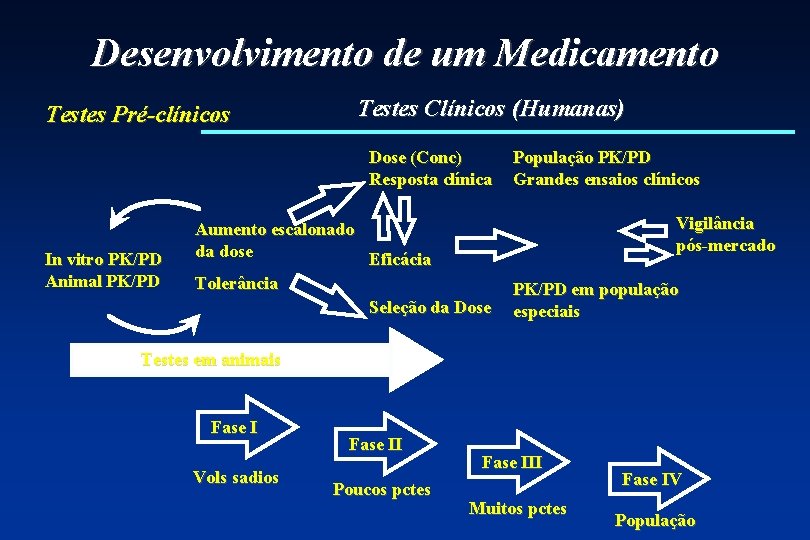
Desenvolvimento de um Medicamento Testes Pré-clínicos Testes Clínicos (Humanas) Dose (Conc) Resposta clínica In vitro PK/PD Animal PK/PD Aumento escalonado da dose Eficácia Tolerância Seleção da Dose População PK/PD Grandes ensaios clínicos Vigilância pós-mercado PK/PD em população especiais Testes em animais Fase I Vols sadios Fase II Poucos pctes Fase III Muitos pctes Fase IV População

Organização do Mercado Farmacêutico no Brasil 1999 1996 Medicamentos: • Inovadores – com marca; com ou sem patente • Similares üPatenteados üNão-patenteados • Similares – com marca; cópias não testadas e não intercambiáveis • Genéricos – sem marca; cópias testadas e intercambiáveis Lei 9279 (Lei de Propriedade Industrial) Lei 9787 (Lei dos Genéricos)

Tipos de Medicamentos no Brasil Inovador (referência) Similar Genérico

Medicamento - Prozac 3 Princípio ativo - fluoxetina 3 Forma farmacêutica - comprimido 3 Apresentação - caixa com 14 comprimidos 3 Classe terapêutica - antidepressivo

Medicamento Referência É aquele produzido pelo laboratório inovador (geralmente multinacional), goza de monopólio comercial por período de tempo determinado (patente). Vendido com marca comercial (Prozac ).

Medicamento Similar É aquele que contém o mesmo princípio ativo - na mesma dose mas não necessariamente na mesma forma farmacêutica - do medicamento de referência. Atualmente necessitará de estudos de equivalência farmacêutica e/ou bioequivalência para renovação do registro. Vendido com marca comercial (Psiquial ).


Medicamento Genérico É aquele que contém o mesmo princípio ativo - na mesma dose e forma farmacêutica - de um medicamento de referência. Apresenta a mesma eficácia que o medicamento de referência, visto ter sido avaliado através de equivalência farmacêutica e/ou bioequivalência. Vendido sem marca comercial, apenas pelo nome do princípio ativo (fluoxetina).

Tipos de Medicamentos no Brasil Referência - Prozac Similar - Psiquial Genérico - Fluoxetina

Tipos de Medicamentos no Brasil Referência - Viagra Similar - não existe (devido a patente) Genérico - não existe (devido a patente)

Medicamento Genérico Apresenta a mesma eficácia que o medicamento de referência, visto ter sido avaliado através de equivalência farmacêutica e/ou bioequivalência.

Equivalência Farmacêutica São testes in vitro que avaliam: 3 Teor de princípio ativo 3 Características físicas da formulação 3 Perfil de dissolução em meios aquosos

Bioequivalência São testes realizados em humanos para avaliar a biodisponibilidade de 2 ou mais formulações

Premissa Básica da Bioequivalência Se dois medicamentos são bioequivalentes, eles apresentam a mesma eficácia terapêutica, e portanto são intercambiáveis.

Bioequivalência Em uma ocasião o voluntário ou o paciente toma uma formulação (medicamento referência por exemplo) e em outra ocasião ele toma a outra formulação (formulação teste)

Determinação da Bioequivalência 3 Concentração da droga ativa ou metabólito(s) em fluidos biológicos em função do tempo. 3 Excreção urinária da droga metabólito(s) em função do tempo. 3 Qualquer efeito apropriado. farmacológico ativa ou agudo

Determinação da Bioequivalência 3 Em 99. 9% dos casos, a avaliação da bioequivalência é feita através da determinação da concentração da droga ativa ou metabólito(s) em fluidos biológicos (plasma) em função do tempo. 3 Este estudo é feito em voluntários sadios de ambos os sexos, tratando-se de estudo clínico aberto, cruzado de duas fases e aleatorizado.

Parâmetros para estabelecimento de bioequivalência • ASC - extensão da absorção • Cmax - pico da absorção
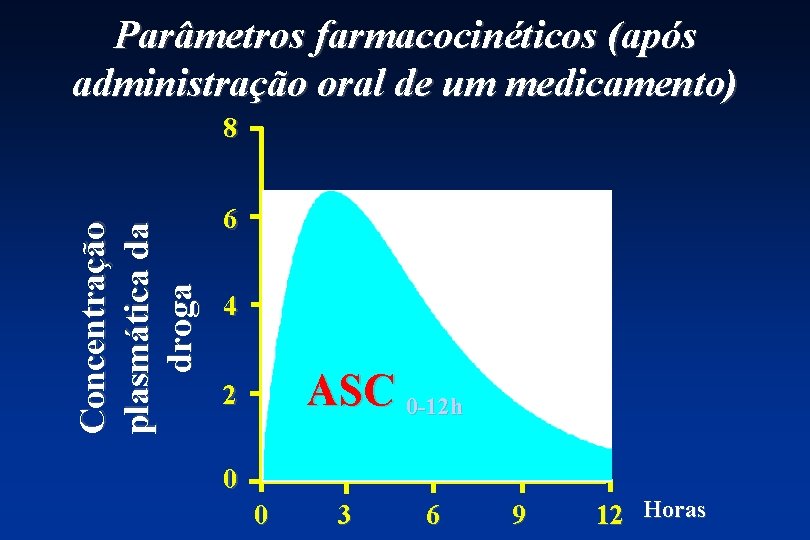
Parâmetros farmacocinéticos (após administração oral de um medicamento) Concentração plasmática da droga 8 6 4 ASC 0 -12 h 2 0 0 3 6 9 12 Horas
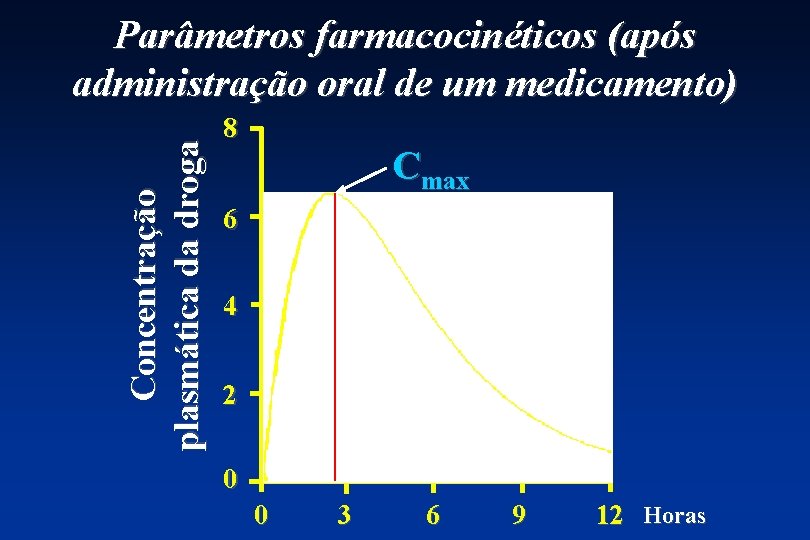
Concentração plasmática da droga Parâmetros farmacocinéticos (após administração oral de um medicamento) 8 Cmax 6 4 2 tmax 0 0 3 6 9 12 Horas

Análise estatística para bioequivalência 3 Razões da AUC e Cmax log-transformadas 3 Análise Paramétrica ou não-paramétrica

Análise estatística para bioequivalência 3 Calcular intervalos de confiança (90%). 3 Os intervalos de confiança devem variar entre 0. 8 -1. 25 (corresponde a + 20%)
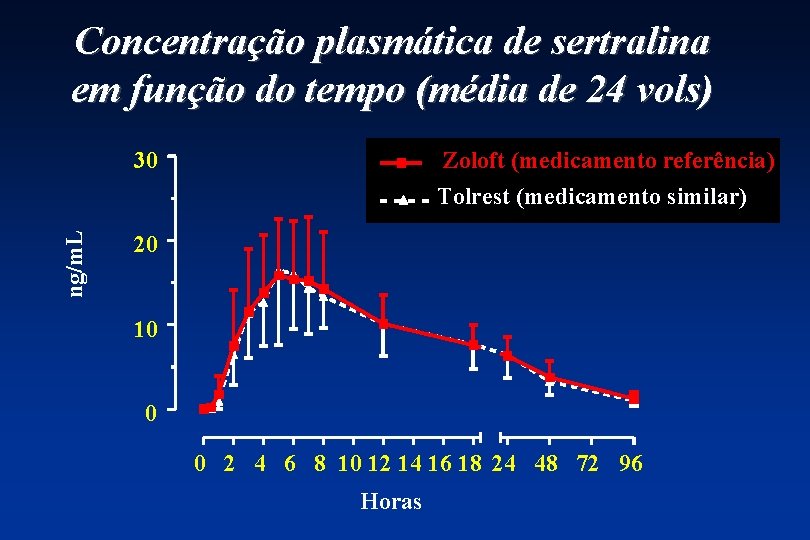
Concentração plasmática de sertralina em função do tempo (média de 24 vols) ng/m. L 30 Zoloft (medicamento referência) Tolrest (medicamento similar) 20 10 0 0 2 4 6 8 10 12 14 16 18 24 48 72 96 Horas
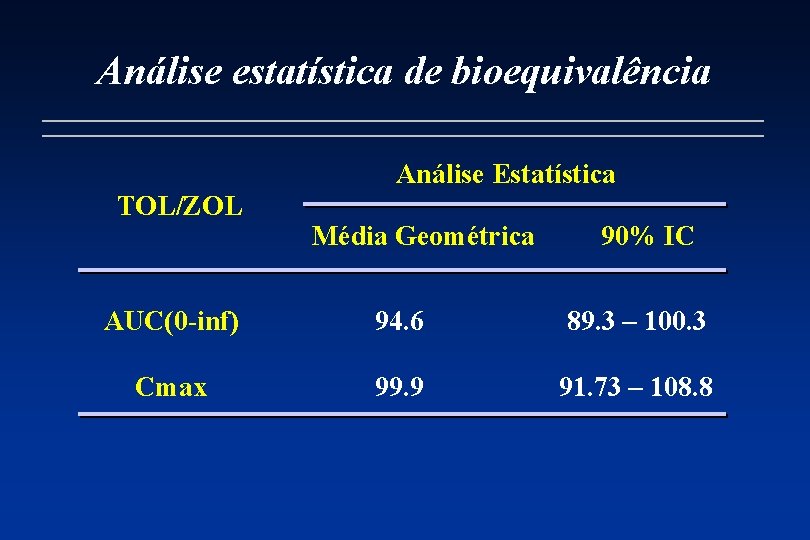
Análise estatística de bioequivalência Análise Estatística TOL/ZOL Média Geométrica 90% IC AUC(0 -inf) 94. 6 89. 3 – 100. 3 Cmax 99. 9 91. 73 – 108. 8

Por que Genéricos? Reduzem os custos!!

Medicamento genérico no Brasil Controle governamental de preços ü Controle de preço prévio ao registro (CMED) – preço de lançamento do genérico no mínimo 35% menor que o do medicamento de referência ü Concorrência do mercado – na prática, genérico em média 45% mais barato que o referência, podendo chegar a 70%
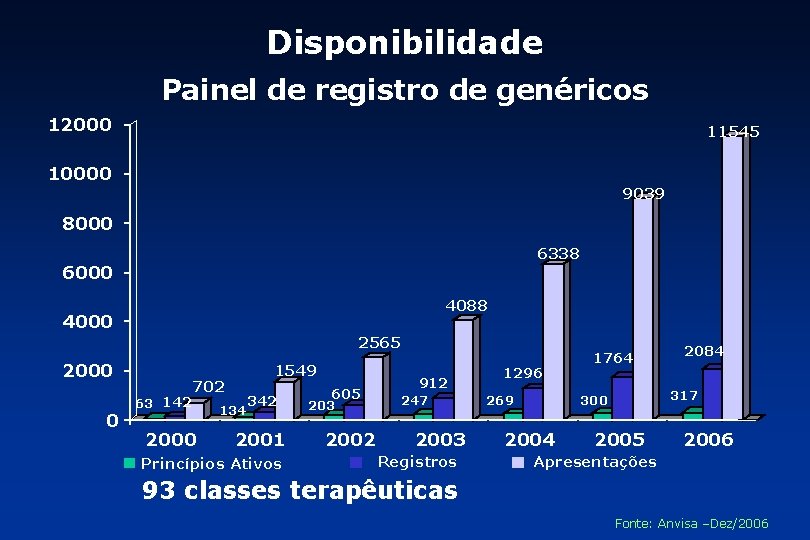
Disponibilidade Painel de registro de genéricos 12000 11545 10000 9039 8000 6338 6000 4088 4000 2565 2000 0 63 142 1549 702 2000 134 342 2001 Princípios Ativos 605 203 2002 912 247 2003 Registros 1296 1764 317 300 269 2004 2084 2005 2006 Apresentações 93 classes terapêuticas Fonte: Anvisa –Dez/2006
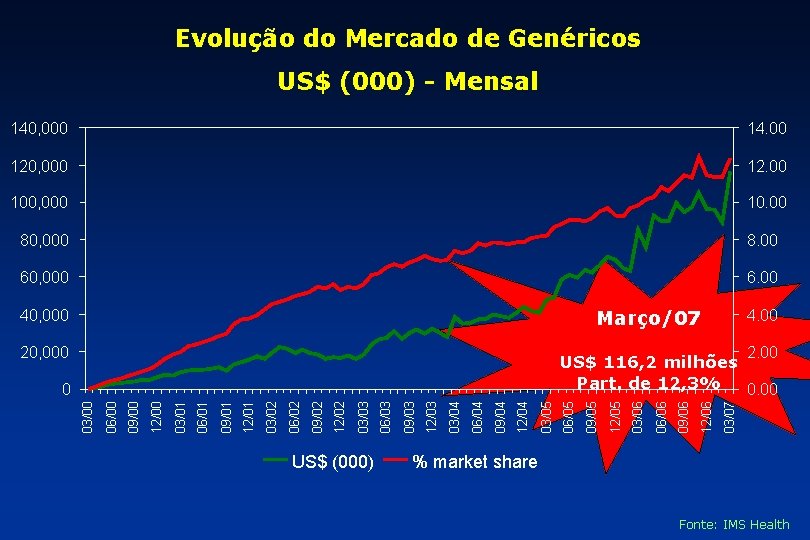
Evolução do Mercado de Genéricos US$ (000) - Mensal 140, 000 14. 00 120, 000 12. 00 100, 000 10. 00 80, 000 8. 00 60, 000 6. 00 Março/07 40, 000 20, 000 4. 00 2. 00 US$ (000) 03/07 12/06 09/06 06/06 03/06 12/05 09/05 03/05 12/04 09/04 06/04 03/04 12/03 09/03 06/03 03/03 12/02 09/02 06/02 03/02 12/01 09/01 06/01 03/01 12/00 09/00 06/00 03/00 0 06/05 US$ 116, 2 milhões Part. de 12, 3% 0. 00 % market share Fonte: IMS Health
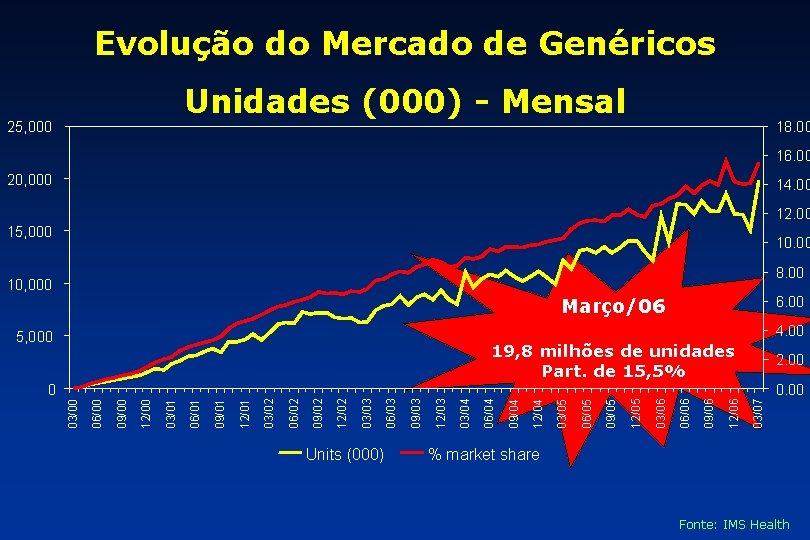
Evolução do Mercado de Genéricos Unidades (000) - Mensal 25, 000 18. 00 16. 00 20, 000 14. 00 12. 00 15, 000 10. 00 8. 00 10, 000 6. 00 Março/06 4. 00 5, 000 19, 8 milhões de unidades Part. de 15, 5% 2. 00 Units (000) 03/07 12/06 09/06 06/06 03/06 12/05 09/05 06/05 03/05 12/04 09/04 06/04 03/04 12/03 09/03 06/03 03/03 12/02 09/02 06/02 03/02 12/01 09/01 06/01 03/01 12/00 09/00 06/00 03/00 0 % market share Fonte: IMS Health
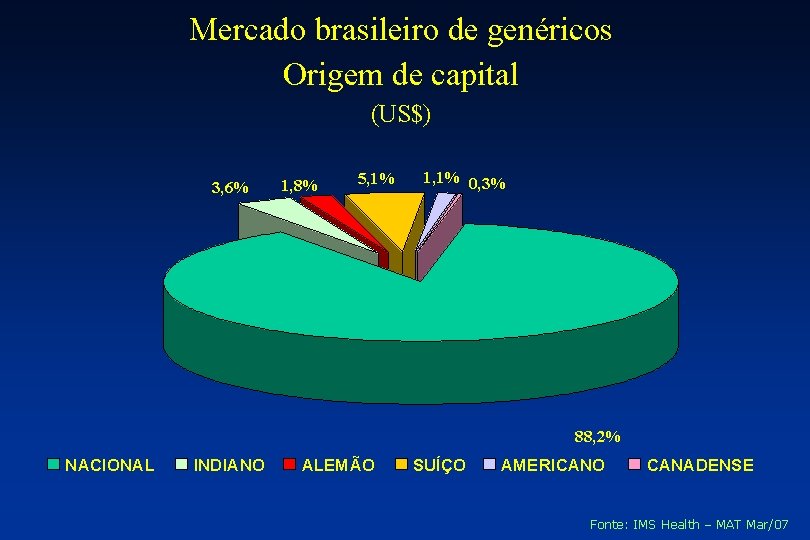
Mercado brasileiro de genéricos Origem de capital (US$) 3, 6% 1, 8% 5, 1% 1, 1% 0, 3% 88, 2% NACIONAL INDIANO ALEMÃO SUÍÇO AMERICANO CANADENSE Fonte: IMS Health – MAT Mar/07

Atenolol + 63% 10, 88 milhões Unidades x 1000 6, 69 milhões Mix 2003 54% Mix 2007 69% 8% 19% 23% 27% Genérico até 63% mais barato que o referência (Atenol®) Fonte: IMS Health – MAT março Impacto dos Genéricos Aumento de Acesso - Hipertensão
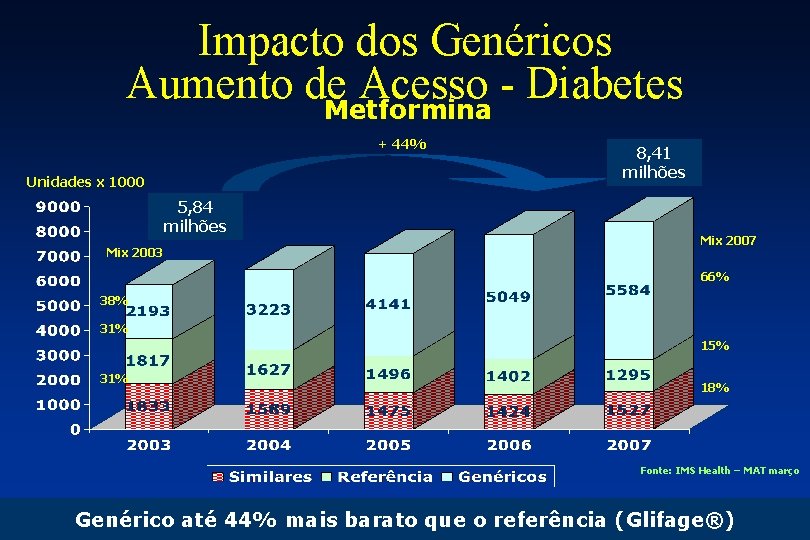
Impacto dos Genéricos Aumento de Acesso Diabetes Metformina + 44% Unidades x 1000 5, 84 milhões Mix 2003 8, 41 milhões Mix 2007 66% 38% 31% 15% 31% 18% Fonte: IMS Health – MAT março Genérico até 44% mais barato que o referência (Glifage®)
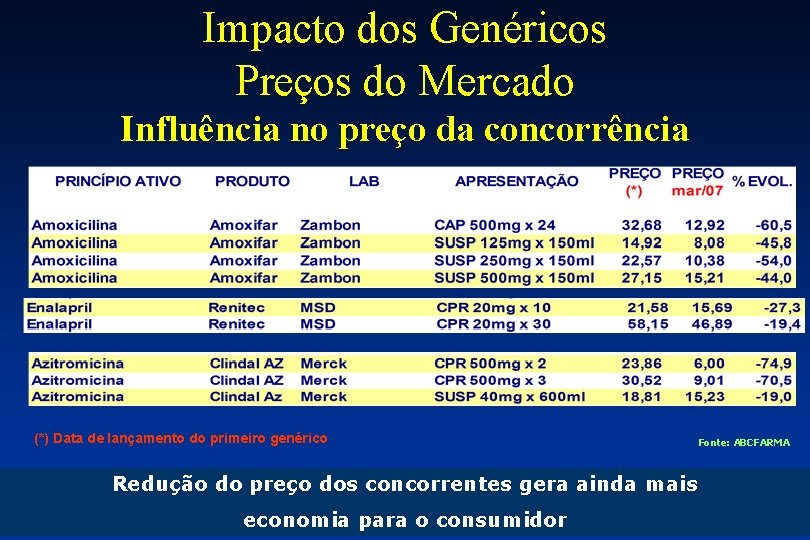
Impacto dos Genéricos Preços do Mercado Influência no preço da concorrência (*) Data de lançamento do primeiro genérico Redução do preço dos concorrentes gera ainda mais economia para o consumidor Fonte: ABCFARMA

Impacto dos Genéricos Economia para o consumidor R$ (milhões) Genéricos propiciaram em 6 anos uma economia estimada de R$ 5, 374 bilhões à população brasileira Fonte: Pró Genéricos - valores acumulados, com base no IMS Health

Impacto dos Genéricos Economia nas compras governamentais Ciclosporina 100 mg (preço por cápsula) R$ Redução de preço propiciou economia estimada de 67% Fonte: Secretaria de Saúde do Estado de São Paulo

MEDICAMENTOS NO BRASIL Gastos públicos e privados O desafio do acesso

Gastos públicos com medicamentos (R$ bil. ) 115% 147% Medicamentos de alto custo já representam 29% dos gastos públicos com medicamentos Fonte: Ministério da Saúde – SCTIE – Dpto. de Assist. Farm. e Insumos Estratégicos

Gastos com medicamentos no orçamento do Ministério da Saúde Fonte: Ministério da Saúde – SCTIE – Dpto. de Assist. Farm. e Insumos Estratégicos
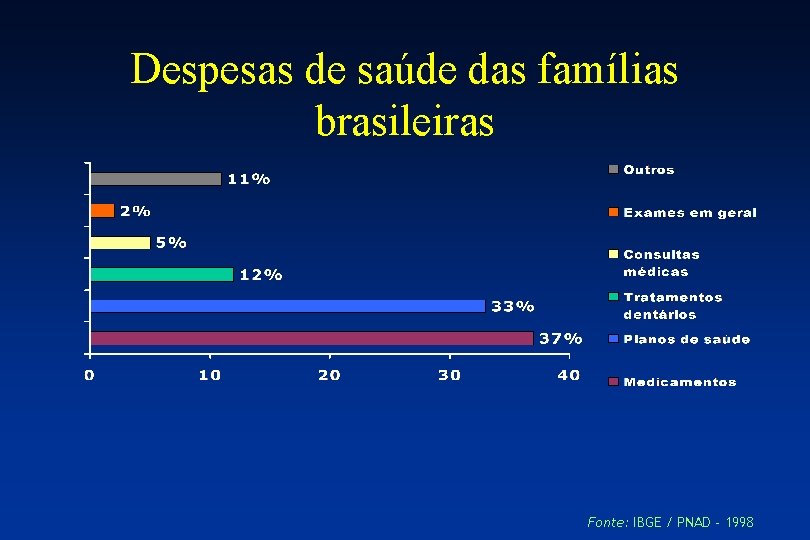
Despesas de saúde das famílias brasileiras Fonte: IBGE / PNAD - 1998

Acesso a medicamentos • 51, 7% dos brasileiros abandonam o tratamento médico por falta de dinheiro para comprar os medicamentos prescritos • 59% da população brasileira ganha até 2 salários mínimos Estimativa de 50 milhões de brasileiros sem acesso a medicamentos Fonte: CONASS (disponível em http: //portal. saude. gov. br/portal/saude/visualizar_texto. cfm? idtxt=25060&janela=1) e IBGE

Propriedade Intelectual: principais aspectos com impacto para os genéricos

Propriedade Intelectual no Brasil Aspectos de relevância • 1996 – Lei de Propriedade Industrial • Previsão do dispositivo de Patentes pipeline – graciosidade para patentes que já haviam sido concedidas no exterior, desde que seu objeto não tivesse sido colocado em qualquer mercado, com respeito ao prazo de vigência da patente prioridade • Prazo para depósito: maio de 1996 a maio de 1997 • LPI embasou o pedido de 1197 patentes pipeline no Brasil • A lei brasileira não prevê - nem para pipelines nem para patentes regulares extensões de prazo

Propriedade Intelectual no Brasil Aspectos de relevância • Tem havido pedidos de extensão de patentes pipeline, com base em extensões concedidas nos países de origem • INPI tem negado os pedidos, devido à falta de previsão legal • Empresas iniciam processo judicial contra o INPI • Tramitam no Judiciário mais de 100 processos relacionados a patentes pipeline

Exemplos de patentes pipeline com pedidos de extensão na Justiça Preços para o consumidor Fonte: revista Kairos – out/06 (preços ICMS 19%)
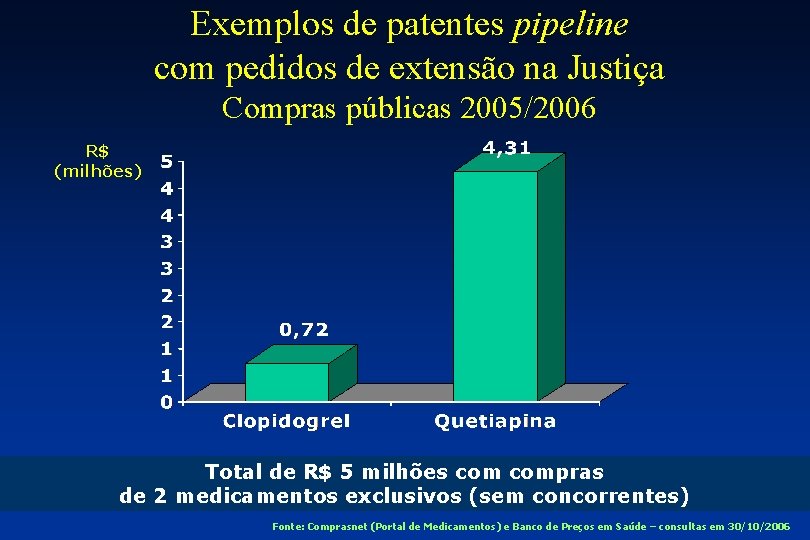
Exemplos de patentes pipeline com pedidos de extensão na Justiça Compras públicas 2005/2006 R$ (milhões) Total de R$ 5 milhões compras de 2 medicamentos exclusivos (sem concorrentes) Fonte: Comprasnet (Portal de Medicamentos) e Banco de Preços em Saúde – consultas em 30/10/2006

Pedidos de extensão de patentes pipeline: efeito prático imediato Inibição do desenvolvimento de genéricos Cronograma de lançamento de um genérico 2005 Início do desenvolvimento do genérico 2006 Início do processo de registro do genérico 2007 Expiração da patente pipeline Lançamento do genérico Ø Obtido o registro do genérico, a empresa tem que iniciar a comercialização em até 6 meses
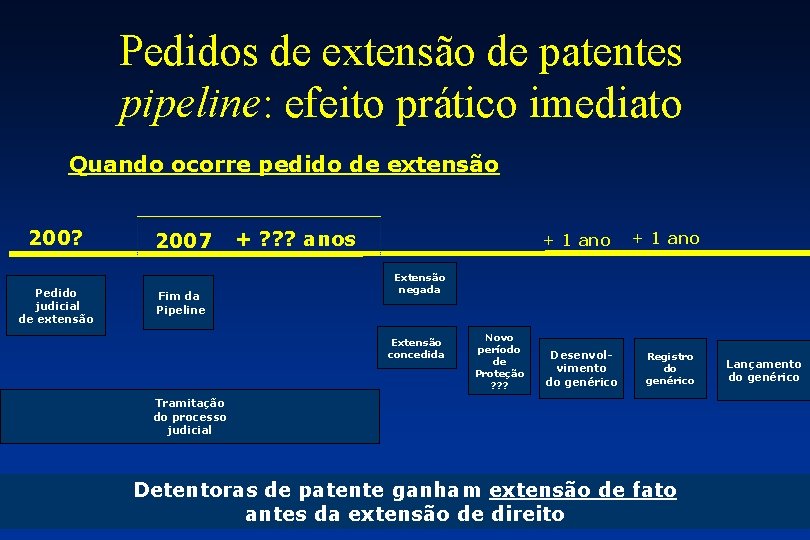
Pedidos de extensão de patentes pipeline: efeito prático imediato Quando ocorre pedido de extensão 200? Pedido judicial de extensão 2007 Fim da Pipeline + ? ? ? anos + 1 ano Extensão negada Extensão concedida Novo período de Proteção ? ? ? Desenvolvimento do genérico Registro do genérico Tramitação do processo judicial Detentoras de patente ganham extensão de fato antes da extensão de direito Lançamento do genérico

Pedidos de extensão de patentes pipeline: efeito prático imediato Exemplo do Orlistate (Xenical®) Ø Expiração da patente pipeline = 2003 Ø Pedido de extensão para 2009 tramita na Justiça Ø Se a extensão fosse negada hoje, na prática já teria ganho 5 anos adicionais de exclusividade (3 anos já passados da vigência original + 2 anos para desenvolvimento e registro do genérico)
- Slides: 50