DTG TAFFTC vs DTG TDFFTC vs EFVTDFFTC ADVANCE



- Slides: 11

DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC § ADVANCE

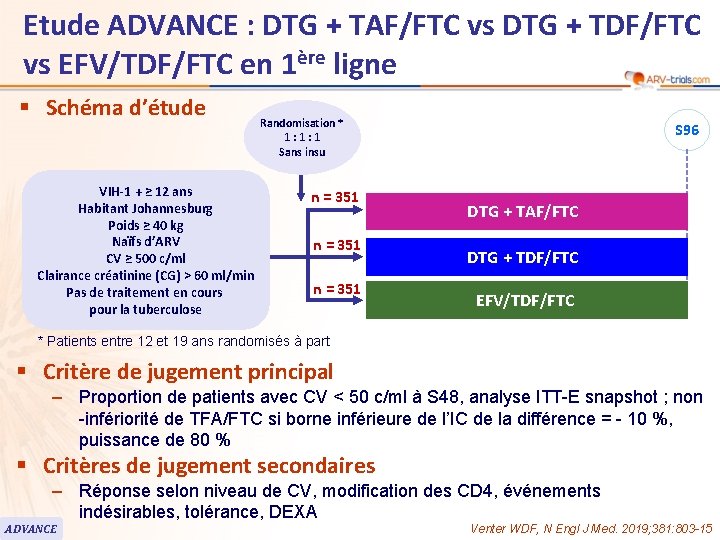
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne § Schéma d’étude VIH-1 + ≥ 12 ans Habitant Johannesburg Poids ≥ 40 kg Naïfs d’ARV CV ≥ 500 c/ml Clairance créatinine (CG) > 60 ml/min Pas de traitement en cours pour la tuberculose Randomisation * 1: 1: 1 Sans insu n = 351 S 96 DTG + TAF/FTC DTG + TDF/FTC EFV/TDF/FTC * Patients entre 12 et 19 ans randomisés à part § Critère de jugement principal – Proportion de patients avec CV < 50 c/ml à S 48, analyse ITT-E snapshot ; non -infériorité de TFA/FTC si borne inférieure de l’IC de la différence = - 10 %, puissance de 80 % § Critères de jugement secondaires – Réponse selon niveau de CV, modification des CD 4, événements indésirables, tolérance, DEXA ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15

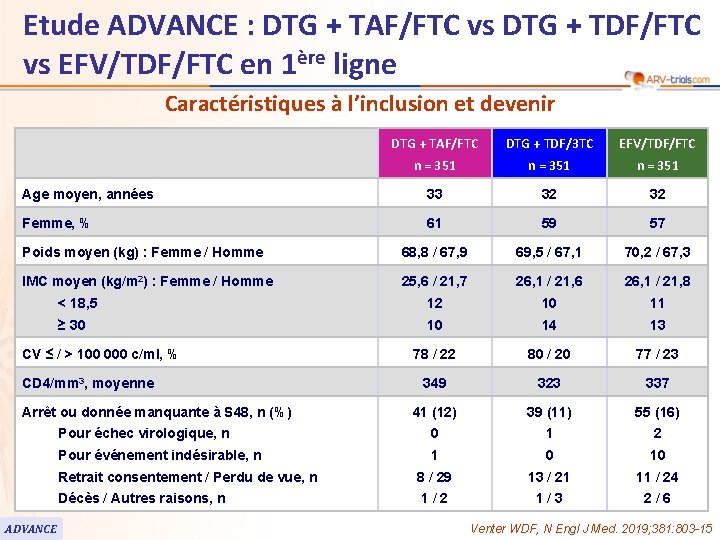
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne Caractéristiques à l’inclusion et devenir DTG + TAF/FTC DTG + TDF/3 TC EFV/TDF/FTC n = 351 Age moyen, années 33 32 32 Femme, % 61 59 57 Poids moyen (kg) : Femme / Homme 68, 8 / 67, 9 69, 5 / 67, 1 70, 2 / 67, 3 IMC moyen (kg/m 2) : Femme / Homme 25, 6 / 21, 7 26, 1 / 21, 6 26, 1 / 21, 8 < 18, 5 12 10 11 ≥ 30 10 14 13 78 / 22 80 / 20 77 / 23 349 323 337 41 (12) 39 (11) 55 (16) Pour échec virologique, n 0 1 2 Pour événement indésirable, n 1 0 10 Retrait consentement / Perdu de vue, n 8 / 29 13 / 21 11 / 24 Décès / Autres raisons, n 1/2 1/3 2/6 CV ≤ / > 100 000 c/ml, % CD 4/mm 3, moyenne Arrêt ou donnée manquante à S 48, n (%) ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15

Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne 100 CV < 50 c/ml % 90 DTG + TDF/FTC = 85 % DTG + TAF/FTC = 84 % EFV/TDF/FTC = 79 % 80 70 Différence ajustée, % (IC 98, 3 %) 60 -1, 1 50 TAF/FTC vs TDF/FTC 40 5, 4 -7, 7 DTG + TDF/FTC vs EFV/TDF/FTC -0, 7 DTG + TAF/FTC vs EFV/TDF/FTC -1, 9 6, 3 13, 2 30 20 -10 10 -6 12, 2 5, 1 -2 0 2 6 10 20 0 0 ADVANCE 4 12 24 Semaines 36 48 Venter WDF, N Engl J Med. 2019; 381: 803 -15

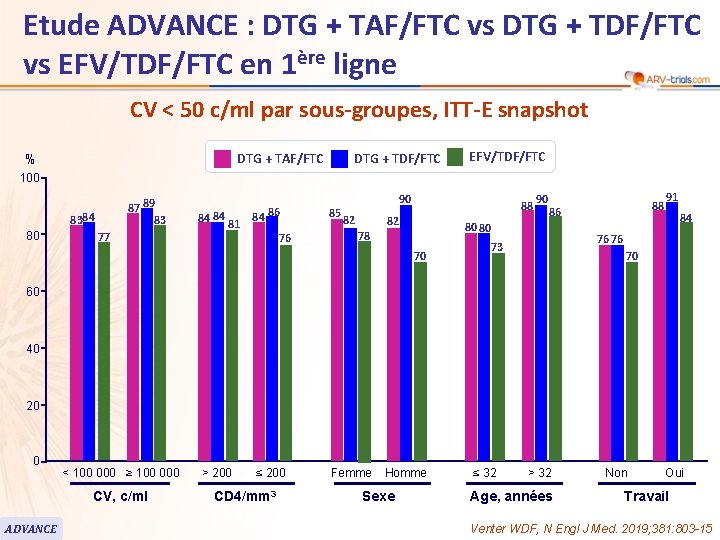
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne 76 CV < 50 c/ml par sous-groupes, ITT-E snapshot DTG + TDF/FTC DTG + TAF/FTC % EFV/TDF/FTC 100 87 89 83 8384 80 77 84 84 81 84 86 76 85 90 82 88 82 90 80 80 78 70 88 86 91 84 76 76 73 70 60 40 20 0 < 100 000 ≥ 100 000 CV, c/ml ADVANCE > 200 ≤ 200 CD 4/mm 3 Femme Homme Sexe ≤ 32 > 32 Age, années Non Oui Travail Venter WDF, N Engl J Med. 2019; 381: 803 -15

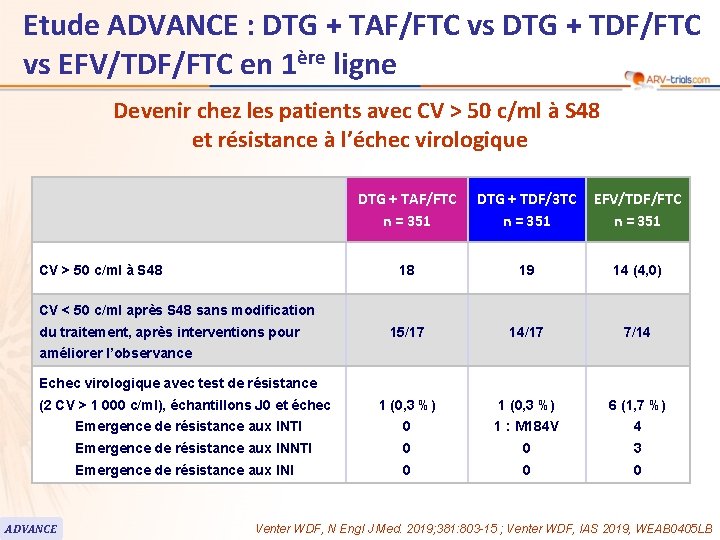
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne Devenir chez les patients avec CV > 50 c/ml à S 48 et résistance à l’échec virologique DTG + TAF/FTC n = 351 DTG + TDF/3 TC n = 351 EFV/TDF/FTC n = 351 18 19 14 (4, 0) 15/17 14/17 7/14 (2 CV > 1 000 c/ml), échantillons J 0 et échec 1 (0, 3 %) 6 (1, 7 %) Emergence de résistance aux INTI 0 1 : M 184 V 4 Emergence de résistance aux INNTI 0 0 3 Emergence de résistance aux INI 0 0 0 CV > 50 c/ml à S 48 CV < 50 c/ml après S 48 sans modification du traitement, après interventions pour améliorer l’observance Echec virologique avec test de résistance ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15 ; Venter WDF, IAS 2019, WEAB 0405 LB

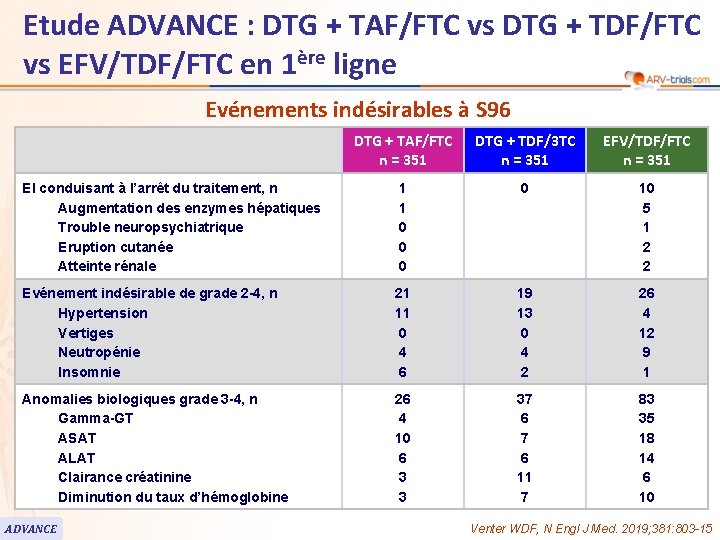
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne Evénements indésirables à S 96 DTG + TAF/FTC n = 351 DTG + TDF/3 TC n = 351 EFV/TDF/FTC n = 351 EI conduisant à l’arrêt du traitement, n Augmentation des enzymes hépatiques Trouble neuropsychiatrique Eruption cutanée Atteinte rénale 1 1 0 0 10 5 1 2 2 Evénement indésirable de grade 2 -4, n Hypertension Vertiges Neutropénie Insomnie 21 11 0 4 6 19 13 0 4 2 26 4 12 9 1 Anomalies biologiques grade 3 -4, n Gamma-GT ASAT ALAT Clairance créatinine Diminution du taux d’hémoglobine 26 4 10 6 3 3 37 6 11 7 83 35 18 14 6 10 ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15

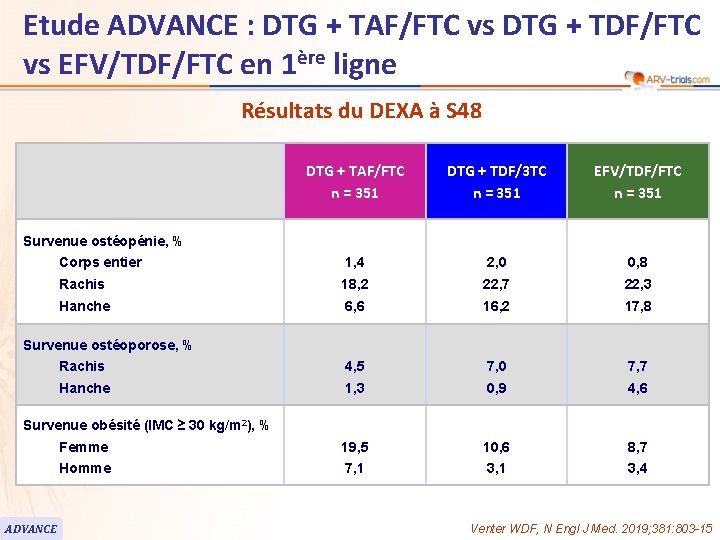
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne Résultats du DEXA à S 48 DTG + TAF/FTC n = 351 DTG + TDF/3 TC n = 351 EFV/TDF/FTC n = 351 Corps entier 1, 4 2, 0 0, 8 Rachis 18, 2 22, 7 22, 3 Hanche 6, 6 16, 2 17, 8 Rachis 4, 5 7, 0 7, 7 Hanche 1, 3 0, 9 4, 6 Femme 19, 5 10, 6 8, 7 Homme 7, 1 3, 4 Survenue ostéopénie, % Survenue ostéoporose, % Survenue obésité (IMC ≥ 30 kg/m 2), % ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15

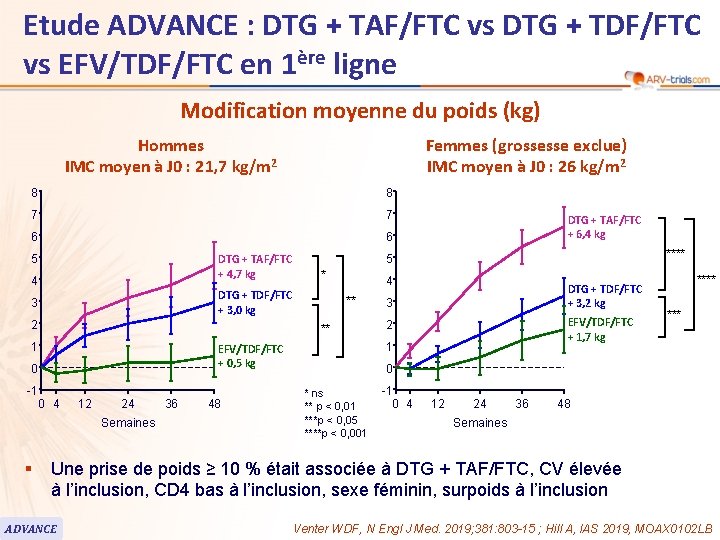
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne 99 Modification moyenne du poids (kg) Hommes IMC moyen à J 0 : 21, 7 kg/m 2 Femmes (grossesse exclue) IMC moyen à J 0 : 26 kg/m 2 8 8 7 7 6 6 DTG + TAF/FTC + 4, 7 kg 5 4 2 0 4 12 24 Semaines § 4 ** 36 48 DTG + TDF/FTC + 3, 2 kg 3 EFV/TDF/FTC + 1, 7 kg 2 1 EFV/TDF/FTC + 0, 5 kg 0 -1 * ** 1 **** 5 DTG + TDF/FTC + 3, 0 kg 3 DTG + TAF/FTC + 6, 4 kg **** 0 * ns ** p < 0, 01 ***p < 0, 05 ****p < 0, 001 -1 0 4 12 24 36 48 Semaines Une prise de poids ≥ 10 % était associée à DTG + TAF/FTC, CV élevée à l’inclusion, CD 4 bas à l’inclusion, sexe féminin, surpoids à l’inclusion ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15 ; Hill A, IAS 2019, MOAX 0102 LB

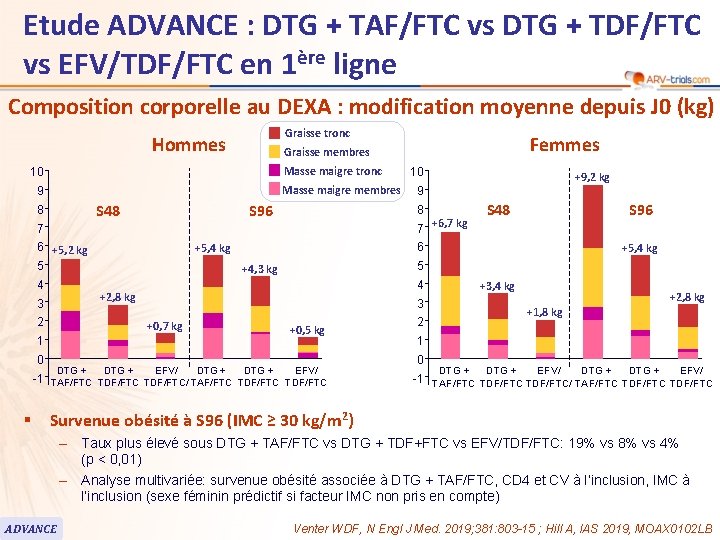
Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne 100 Composition corporelle au DEXA : modification moyenne depuis J 0 (kg) Graisse tronc Hommes Masse maigre tronc 10 Masse maigre membres 9 S 48 8 S 96 4 2 +5, 4 kg 0 -1 § S 48 S 96 6 +5, 4 kg 5 +4, 3 kg 4 +3, 4 kg 3 +0, 7 kg 1 +9, 2 kg 9 7 +6, 7 kg +2, 8 kg 3 10 8 7 6 +5, 2 kg 5 Femmes Graisse membres +0, 5 kg DTG + EFV/ TAF/FTC TDF/FTC/ TAF/FTC TDF/FTC +2, 8 kg +1, 8 kg 2 1 0 DTG + EFV/ -1 TAF/FTC TDF/FTC/ TAF/FTC TDF/FTC Survenue obésité à S 96 (IMC ≥ 30 kg/m 2) – Taux plus élevé sous DTG + TAF/FTC vs DTG + TDF+FTC vs EFV/TDF/FTC: 19% vs 8% vs 4% (p < 0, 01) – Analyse multivariée: survenue obésité associée à DTG + TAF/FTC, CD 4 et CV à l’inclusion, IMC à l’inclusion (sexe féminin prédictif si facteur IMC non pris en compte) ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15 ; Hill A, IAS 2019, MOAX 0102 LB

Etude ADVANCE : DTG + TAF/FTC vs DTG + TDF/FTC vs EFV/TDF/FTC en 1ère ligne § Conclusion – Le traitement par DTG associé à FTC et l’une ou l’autre des 2 prodrogues de ténofovir (TAF et TDF) avait une efficacité non inférieure à celle du traitement standard par EFV/TDF/FTC – La prise de poids était significativement plus élevée sous traitement avec DTG, en particulier en association avec TAF, que sous traitement standard – Les craintes concernant la tératogénicité de DTG et l’absence de données de sécurité sur l’utilisation du TAF en cours de conception ou de grossesse constituent une problématique complexe pour les cliniciens des pays à revenu faible ou modéré qui dépendent d’options thérapeutiques limitées, en particulier chez les femmes – Le risque accru de prise de poids avec les 2 schémas à base de DTG et l’absence donnée sur le TAF en cours de grossesse doivent être mis en balance avec l’amélioration du profil de tolérance et d’observance, l’obtention légèrement plus rapide de la suppression virologique et les bénéfices sur la densité minérale osseuse et la fonction rénale ADVANCE Venter WDF, N Engl J Med. 2019; 381: 803 -15