Dsordres acidobasiques Le lactate en ranimation Dr Thomas

- Désordres acido-basiques - Le lactate en réanimation Dr Thomas Rimmelé thomas. rimmele@chu-lyon. fr Département d’Anesthésie-Réanimation Pavillon P Réanimation Hôpital Edouard Herriot, Lyon Janvier 2007

Plan Désordres acido-basiques - Acidose métabolique - Acidose respiratoire - Alcalose métabolique - Alcalose respiratoire - Troubles mixtes Le lactate en réanimation - Métabolisme du lactate - Dosage du lactate - Hyperlactatémie : facteur pronostique ? - Hyperlactatémie : marqueur d’hypoxie et de métabolisme anaérobie ? - Classification des hyperlactatémies - Hyperlactatémie : facteur de protection ? - Traitement des acidoses lactiques

Introduction - Désordres acido-basiques très fréquents en réanimation - Nombreuses erreurs d’interprétation ! - Lactatémie prescrite tous les jours en réanimation - Nombreuses « idées reçues » sur le lactate - LE lactate !

Désordres acido-basiques

Prélèvement : la gazométrie artérielle • Pas de bulle d’air pour éviter la perte de CO 2 par dissipation • Seringue héparinisée • Glace jusqu’au laboratoire • Pas plus d’une heure de conservation avant analyse

Définitions • Trouble de l’équilibre acido-basique : trouble affectant la charge acide, c’est à dire la quantité d’ions H+ présents dans les liquides de l’organisme • Acidose : augmentation de la charge en ions H+ de l’organisme • Acidémie : diminution du p. H sanguin exprimant une augmentation de la concentration H+ dans le sang • Alcalose : diminution de la charge en ions H+ de l’organisme • Alcalémie : augmentation du p. H sanguin exprimant une diminution de la concentration H+ dans le sang

Conséquences de l’acidose Cardiovasculaires : - Baisse de la contractilité et de la réponse aux amines - Vasodilatation artérielle, veinoconstriction, HTAP - Baisse du DC, de la PA, des flux sanguins rénal et hépatique - Arythmies Respiratoires (variable selon étiologie métabolique ou respiratoire) : - Hyperventilation, dyspnée - Fatigue musculaire Métaboliques - Augmentation des besoins métaboliques, insulinorésistance - Inhibition de la glycolyse anaérobie - Diminution de la synthèse d’ATP - Hyperkaliémie - Catabolisme protéique Cérébrales - Inhibition du métabolisme, coma NEJM 1998

Conséquences de l’alcalose Cardiovasculaires : - Vasoconstriction artérielle - Baisse de la perfusion coronaire - Arythmies Respiratoires (variable selon étiologie métabolique ou respiratoire) : - Hypoventilation, hypercapnie - Hypoxémie Métaboliques : - Stimulation de la glycolyse anaérobie - Hypokaliémie, hypomagnésémie, hypophosphorémie - Baisse du calcium ionisé Cérébrales : - Baisse du flux sanguin cérébral - Convulsions, délire NEJM 1998
![Le p. H = Potentiel Hydrogène • [ ] sanguine en ions H+ très Le p. H = Potentiel Hydrogène • [ ] sanguine en ions H+ très](http://slidetodoc.com/presentation_image_h/0f5fb1f3a4df685ec15baa9c3e23d53b/image-9.jpg)
Le p. H = Potentiel Hydrogène • [ ] sanguine en ions H+ très faible : 40 nmol/L p. H = - log [H+] • Limites de la normale étroites : • Limites compatibles avec la vie : 7, 38 à 7, 42 6, 60 à 7, 70 • [H+] stable indispensable au bon fonctionnement cellulaire et enzymatique • Production de H+ par l’organisme : 50 à 100 mmol / jour !!! Tendance à l’accumulation d’ions H+

Les systèmes tampons Neutralisation de l’excès de H+ par 2 systèmes de défense : - L’un immédiat, physicochimique : les sytèmes tampons - L’autre, plus lent, constitué par 2 organes excréteurs de H+ : le rein et le poumon les systèmes tampons : -Système des bicarbonates (tampon extracellulaire le + important) -Hémoglobine -Protéines cellulaires et plasmatiques -Phosphates inorganiques -L’ammonium

• Tamponnement par les bicarbonates : H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 • p. H = 6, 1 + log [HCO 3 -] / [H 2 CO 3] • p. H = 6, 1 + log [HCO 3 -] / 0, 03. Pa. CO 2 • Bicarbonates régulés par le rein • Ac. carbonique régulé par poumon via la Pa. CO 2 • Pour maintenir p. H normal, variation du numérateur et dénominateur dans le même sens.

• Les variations de H+ (et donc du p. H) sont induites par des altérations de la Pa. CO 2 ou de la [ ] plasmatique de HCO 3 -. • Les anomalies primitives de la Pa. CO 2 sont responsables d’acidose ou d’alcalose dites « respiratoires » . • Les anomalies primitives de HCO 3 - sont responsables d’acidose ou d’alcalose dites « métaboliques » .

• Dans chacun de ces désordres acido-basiques, des réponses compensatoires rénales ou respiratoires sont mises en jeu afin de minimiser les variations de p. H en minimisant les variations du rapport HCO 3 - / Pa. CO 2. • Les réponses compensatrices vont toujours dans le même sens que l’anomalie primitive.

Acidose métabolique Défaut primitif - Baisse des bicarbonates Compensation - Hyperventilation pour Pa. CO 2 Etiologies - Acidose lactique, acidocétose du diabétique, insuffisance rénale, intoxications (aspirine, éthylène glycol). - Fuites digestives de bicarbonates (diarrhée, fistule digestive), acidoses tubulaires rénales, remplissage vasculaire. TTT - étiologique, hyperventilation, très rarement bicarbonates, parfois EER.

Acidose métabolique Profil p. H < 7. 38 Bicar < 23 mmol/L Pa. CO 2 < 5 k. Pa Remarque KPa mm Hg (× 7. 5)

Acidose métabolique Le trou anionique Principe: plasma = électroneutralité = correspondance des charges électriques portées par les anions(-) et par les cations(+) 2 anions sont dosés couramment dans le plasma (HCO 3 - et Cl-) = 85% des anions. 15% restants = anions indosés = protéines plasmatiques (albumine), phosphates, sulfates, acides organiques…

Acidose métabolique Valeur normale du TA : (Na+ + K+) – (Cl- + HCO 3 -) = 16 ± 2 2 situations : 1) Si perte rénale ou digestive de HCO 3 -, la baisse de HCO 3 - est compensée par une augmentation proportionnelle de Cl-. Le TA ne change pas et cette forme d’acidose métabolique = acidose métabolique hyperchlorémique (TA normal)

Acidose métabolique 2) Inversement, lorsque l’acidose est produite par l’addition d’un acide autre que HCl, l’acidose s’accompagne d’un TA excessif parce que HCO 3 - est abaissé et remplacé par un anion indosé. Donc TA = utile pour le diagnostic différentiel d’une acidose métabolique !

Acidoses métaboliques hyperchlorémiques à TA normal Le TA urinaire : Na+ + K+ - Cl- = 0 à -20 Si TA u > 0 Acidose tubulaire rénale Si TA u < -20 Pertes digestives de bicarbonates

Acidose métabolique hyperchlorémique et remplissage vasculaire Pas seulement avec certains cristalloïdes ! 2 hypothèses physiopathologiques : - Acidose de dilution : Approche traditionnelle d’Henderson Hasselbach - Apport de [ ] élevées en Cl- : approche de Stewart

Acidose de dilution : • Henderson-Hasselbach • Diminution des bicarbonates plasmatiques secondaire à l’expansion volémique Garella et al. Am J Physiol 1973. Effect of isotonic volume expansion on extracellular bicarbonate stores in normal dogs.

• Modèle de Stewart (1978) : Respect de 3 principes physico-chimiques fondamentaux : - Equilibre de dissociation électrochimique - Conservation de masse - Electroneutralité Stewart PA. Resp Physiol 1978. Independant and dependent variables of acid-base control.

• p. H et HCO 3 - sont dépendants de 3 variables distinctes : - Le Strong ion difference (SID) = différence entre cations et anions fortement dissociés: (Na+ + K+) – (Cl- + lactate) - Pa. CO 2 - Acides faibles (albumine, phosphore inorganique)
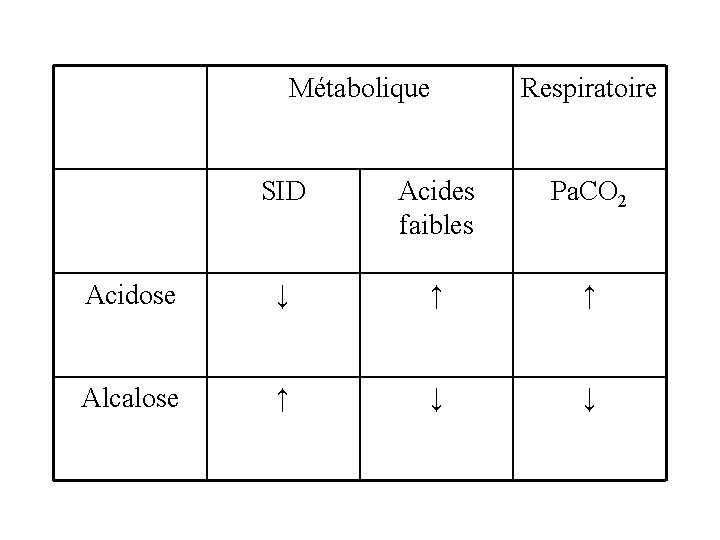
Métabolique Respiratoire SID Acides faibles Pa. CO 2 Acidose ↓ ↑ ↑ Alcalose ↑ ↓ ↓

L’ hypoalbuminémie entraîne une alcalose métabolique. Quelques réf sur acidose hyperchlorémique : Scheingraber S et al. Anesthesiology 1999. Rapid saline infusion produces hyperchloremic acidosis in patients undergoing gynecologic surgery. Blanloeil Y et al. Ann Fr Anesth Réanim 2002. Acidose hyperchlorémique lors du remplissage vasculaire. Waters JH et al. Crit Care Med 1999. Cause of metabolic acidosis in prolonged surgery.

Place des bicarbonates dans le traitement d’une acidose métabolique Effets néfastes des bicarbonates : 1) Augmentation de la production de CO 2 HCO 3 - + H+ H 20 + CO 2 Nécessité d’augmenter le travail ventilatoire pour épurer le CO 2. Peut même aboutir à des acidoses respiratoires ! 2) Acidose intracellulaire paradoxale par diffusion dans la cellule du CO 2 (acidose gazeuse intracellulaire). Ritter et al. Lancet 1990 Effet inotrope négatif si acidification des cellules cardiaques !

3) Acidification du LCR 4) Alcalose métabolique secondaire Rappel : alcalose + grave que acidose ! 5) Hypokaliémie 6) Hypernatrémie et hyperosmolarité

Les indications des bicarbonates : Persistantes : Acidose métabolique par fuite digestive ou urinaire de bicarbonates = acidose métabolique hyperchlorémique à TA normal Discutées : Acidose métabolique très sévère (p. H < 6, 90) Action des amines ? ? Abandonnées : - Acidose métabolique par gain d’acide = acidose métabolique normochlorémique à TA augmenté. - Réanimation de l’arrêt cardiocirculatoire Correction de l’acidose métabolique en réanimation. Conférence consensus Juin 1999

Remarque sur l’acidose au cours d’un arrêt cardiocirculatoire : Acidose mixte avec grosse part « respiratoire » par défaut d’épuration du CO 2 donc prescription de bicarbonates illogique. Risque d’aggravation de l’acidose tissulaire si bicarbonates

Précautions d’utilisation si administration de bicarbonates : - Administration lente et régulière (< 2 mmol/kg/H) diminue l’acidose intracellulaire et LCR diminue la production de CO 2 - Utiliser solutés hypoosmolaires (1, 4 %) - Augmenter ventilation minute si ventilation mécanique - Prévenir l’hypokaliémie - Limiter les quantités

Acidose respiratoire Défaut primitif Augmentation de la Pa. CO 2 = Hypercapnie Compensation Réabsorption rénale des bicarbonates augmentée Etiologies Toutes les causes d’ hypoventilation alvéolaire = paralysies respiratoires neurologiques ou musculaires (Guillain-Barré, myopathies), comas, effets secondaires des morphiniques, BPCO décompensée…

Acidose respiratoire TTT Etiologique, augmenter la ventilation alvéolaire Profil p. H < 7. 38 Bicar > 26 mmol/L Pa. CO 2 > 5. 6 KPa

Alcalose métabolique Défaut primitif - Elévation des bicarbonates Compensation - Hypoventilation alvéolaire Etiologies - Hypovolémie, diurétiques (contraction du volume extra-cellulaire réabsorption proximale de bicarbonates) = alcalose de contraction - Pertes de H+ : Vomissements - perfusions excessives de bicarbonates

Alcalose métabolique TTT - Normalisation de la volémie, ttt étiologique, parfois acétazolamide (favorise excrétion rénale des bicar) Profil p. H > 7, 42 Bicar > 26 mmol/L Pa. CO 2 > 5, 6 KPa

Alcalose respiratoire Défaut primitif - Baisse de la Pa. CO 2 Compensation - Baisse des bicarbonates (réduction de la réabsorption rénale) Etiologies Hyperventilation alvéolaire par hyperpnée - centrale (psychiatrie, AVC, tumeurs cérébrales) - réflexe à une hypoxie (EP, pneumothorax, anémie) - respirateur de réa mal réglé

Alcalose respiratoire TTT - étiologique, O 2 si besoin, diminuer la ventilation Profil : alcalose respiratoire avec alcalémie p. H > 7, 42 Bicar < 23 mmol/L Pa. CO 2 < 5 KPa

Remarque : • On peut avoir une acidose métabolique sans acidémie (= compensée) - Bicar diminués (trouble primitif) - Pa. CO 2 diminuée - p. H normal • Mais attention : même profil que alcalose respiratoire sans alcalémie !! • Acidose respiratoire sans acidémie ou compensée : cas fréquent au cours des insuffisances respiratoires chroniques
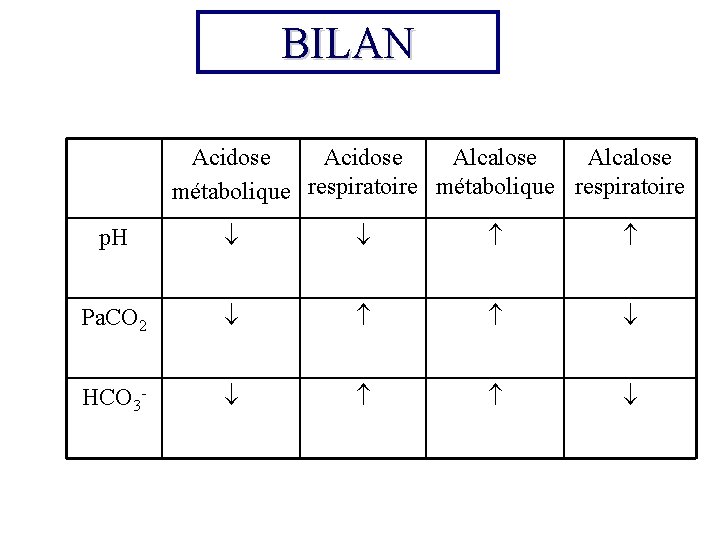
BILAN Acidose Alcalose métabolique respiratoire p. H Pa. CO 2 HCO 3 -

Quelques précisions… • Nous venons de voir les troubles acido-basiques simples ! • Il existe (fréquemment en réanimation) des troubles acidobasiques complexes ou mixtes… • Ces derniers surviennent quand la compensation rénale ou respiratoire ne peut pas s’effectuer correctement. Ex : administration massive de bicarbonates à un malade soumis à une ventilation mécanique avec ventilation minute trop élevée Alcalose mixte !

BILAN des troubles mixtes Acidose mixte Alcalose mixte p. H Pa. CO 2 HCO 3 -

Quelques précisions… • Enfin, de manière générale, pour éviter les erreurs, ne jamais interpréter une gazométrie artérielle de façon isolée. Il faut systématiquement s’aider de : -l’anamnèse -L’examen clinique -La biologie (ionogramme, ac. lactique…)

Conclusion L’analyse d’un trouble acido-basique n’est pas compliquée si - Rigueur de raisonnement (identifier défaut primitif…) - Prise en compte des paramètres anamnestiques, cliniques et biologiques associés

Le lactate en réanimation

Métabolisme du lactate Lactatémie = concentration qui résulte à la fois du flux de production et du flux d’élimination du lactate Le lactate est formé dans le cytosol à partir du pyruvate qui est réduit grâce à une enzyme, la lacticodeshydrogénase (LDH) : Pyruvate + NADH + H+ LDH Lactate + NAD Donc la concentration cellulaire de lactate dépend de : - Concentration en pyruvate - Rapport NADH/NAD - Concentration en ion H+

Concentration cellulaire en pyruvate : Le lactate augmente quand la production de pyruvate dans le cytosol excède son utilisation Le pyruvate est issu essentiellement de la glycolyse
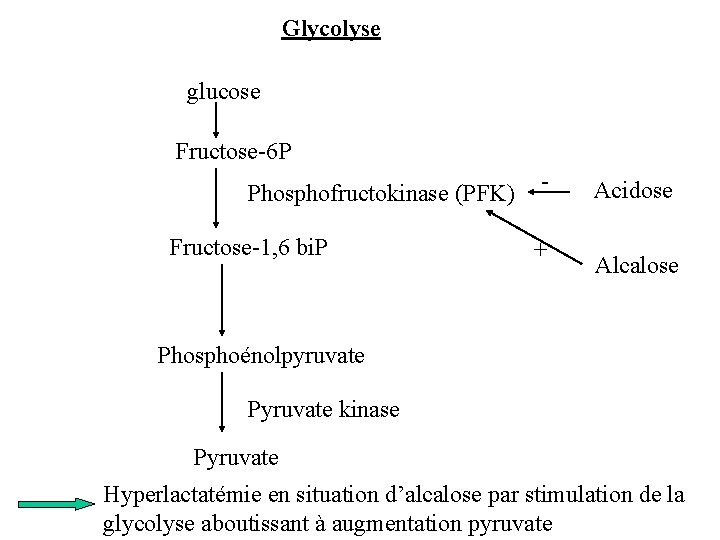
Glycolyse glucose Fructose-6 P Phosphofructokinase (PFK) Fructose-1, 6 bi. P + Acidose Alcalose Phosphoénolpyruvate Pyruvate kinase Pyruvate Hyperlactatémie en situation d’alcalose par stimulation de la glycolyse aboutissant à augmentation pyruvate

Le pyruvate 4 voies métaboliques : 2 intramitochondriales 2 cytosoliques 1) Oxydation aérobique intramitochondriale via le cycle de Krebs catalysée par la pyruvate deshydrogénase (PDH) 36 ATP 2) Transformation en oxaloacétate 3) Donner du glucose par la néoglucogénèse 4) Donner alanine par transamination
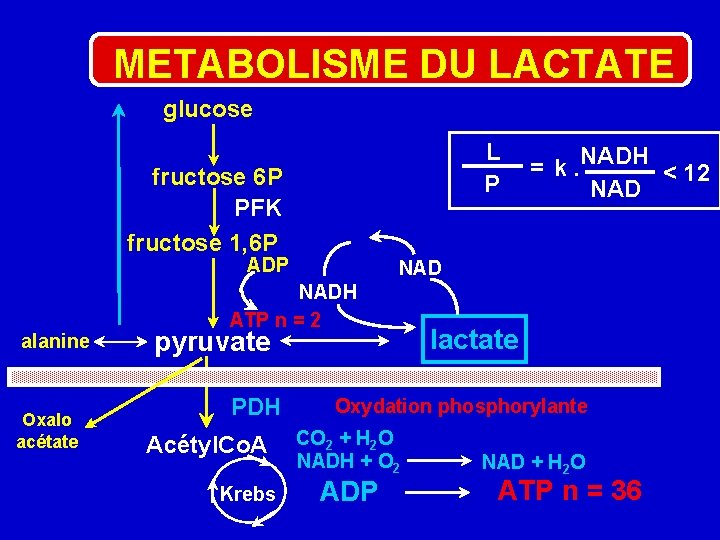
METABOLISME DU LACTATE glucose L P fructose 6 P PFK fructose 1, 6 P ADP alanine Oxalo acétate NADH ATP n = 2 pyruvate PDH Acétyl. Co. A Krebs NADH = k. < 12 NAD lactate Oxydation phosphorylante CO 2 + H 2 O NADH + O 2 ADP NAD + H 2 O ATP n = 36
![Le potentiel Redox (NADH/NAD) Contrôle étroitement la [] cellulaire en pyruvate en régulant : Le potentiel Redox (NADH/NAD) Contrôle étroitement la [] cellulaire en pyruvate en régulant :](http://slidetodoc.com/presentation_image_h/0f5fb1f3a4df685ec15baa9c3e23d53b/image-49.jpg)
Le potentiel Redox (NADH/NAD) Contrôle étroitement la [] cellulaire en pyruvate en régulant : - La glycolyse et l’oxydation du pyruvate en acétylco. A via la PDH Pyruvate + Co. A PDH NAD Acétyl. Co. A + CO 2 NADH + H+ - La réduction du pyruvate en lactate via la LDH Pyruvate + NADH + H+ Lactate + NAD LDH
![Les variations de la [H+] ou p. H L’acidose favorise la transformation du pyruvate Les variations de la [H+] ou p. H L’acidose favorise la transformation du pyruvate](http://slidetodoc.com/presentation_image_h/0f5fb1f3a4df685ec15baa9c3e23d53b/image-50.jpg)
Les variations de la [H+] ou p. H L’acidose favorise la transformation du pyruvate en lactate. L’acidose diminue la production de pyruvate en inhibant l’activité de la PFK.
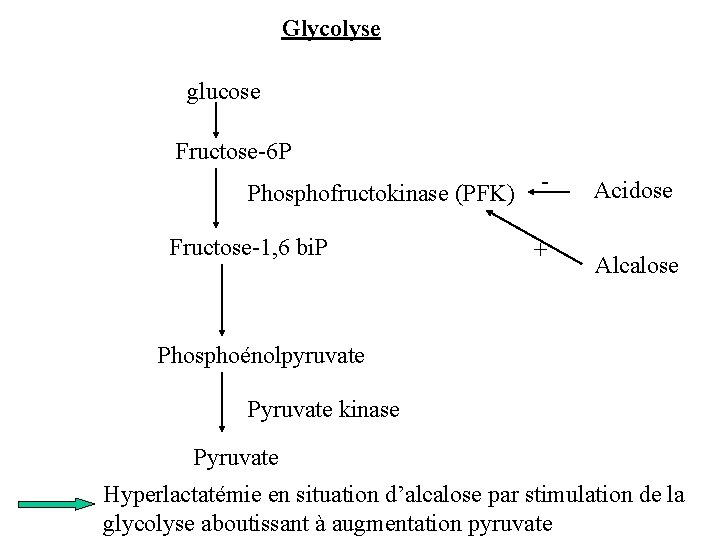
Glycolyse glucose Fructose-6 P Phosphofructokinase (PFK) Fructose-1, 6 bi. P + Acidose Alcalose Phosphoénolpyruvate Pyruvate kinase Pyruvate Hyperlactatémie en situation d’alcalose par stimulation de la glycolyse aboutissant à augmentation pyruvate

Turnover du lactate - La production de lactate correspond donc à un travail anaérobie ne nécessitant pas d’O 2 - Production globale : 1500 mmol/j - Organes producteurs : érythrocytes, intestin, cerveau, peau et muscle surtout lors de exercice physique - En situation normale, cette production est compensée par une métabolisation par organes métaboliseurs (foie +++ , rein, cœur) Baisse importante du débit sanguin hépatique, cirrhose Diminution de la clairance hépatique du lactate Augmentation de sa demi-vie

En fait, le turn over du lactate est très complexe ! - Les organes métaboliseurs peuvent devenir producteurs (foie, rein) - Les producteurs peuvent devenir métaboliseurs (cerveau, muscle) - En situation normale, production = élimination d’où lactatémie stable de 0, 5 à 1, 5 mmol/L avec ½ vie plasmatique de 10 minutes. - Lactatémie ne reflète donc pas le turn over ou métabolisme : on peut avoir lactatémie normale avec un métabolisme du lactate multiplié par 3 - Hyperlactatémie = déséquilibre entre production et élimination Remarque : Lactatémie et HDFVVC : - fiable il y a 10 ans - aujourd’hui ?
![Relation production de lactate et [H+] La théorie : Il existe une relation Relation production de lactate et [H+] La théorie : Il existe une relation](http://slidetodoc.com/presentation_image_h/0f5fb1f3a4df685ec15baa9c3e23d53b/image-54.jpg)
Relation production de lactate et [H+] La théorie : Il existe une relation directe entre lactate et acidose car : l’acide lactique est un acide fort (p. K = 3, 9) donc complètement dissocié de façon équimolaire en anion lactate- et H+ à p. H plasmatique physiologique

Concept de Stewart : le p. H n’est pas une valeur contrôlante mais Contrôlée par 3 variables qui sont : -la différence ionique constituée par les ions fortement dissociés (SID) -la Pa. CO 2 -les acides faiblement dissociés Ces 3 paramètres définissent le degré de dissociation des molécules d’eau et donc le p. H. Le lactate est un anion, réduisant le SID et avec pour conséquence d’augmenter la dissociation de l’eau et donc la génèse de protons entraînant l’acidose
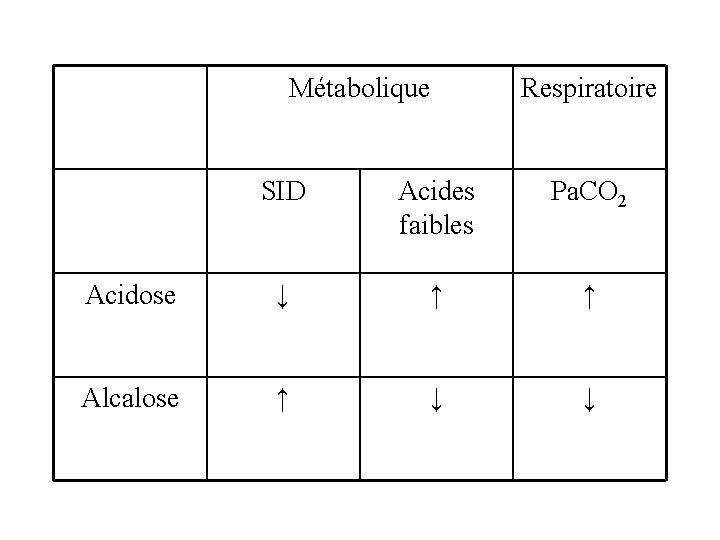
Métabolique Respiratoire SID Acides faibles Pa. CO 2 Acidose ↓ ↑ ↑ Alcalose ↑ ↓ ↓

La réalité : Il existe des hyperlactatémies sans acidose ou même avec des alcaloses !!

1) La production de lactate à partir du glucose n’aboutit ni à une production, ni à une consommation d’ion H+ Glycolyse : glucose + 2 ADP + 2 Pi 2 lactate + 2 ATP 2) Hydrolyse de l’ATP : 2 ATP 2 ADP + 2 Pi + 2 H+ + énergie 3) Si apport d’O 2 est insuffisant, les métabolites de l’ATP sont recyclés dans la mitochondrie et les ions H+ sont tamponnés par les HCO 3 La lactatémie cytosolique peut augmenter sans développement d’une acidose 4) L’acidose inhibe fortement la glycolyse baisse de la production de lactate
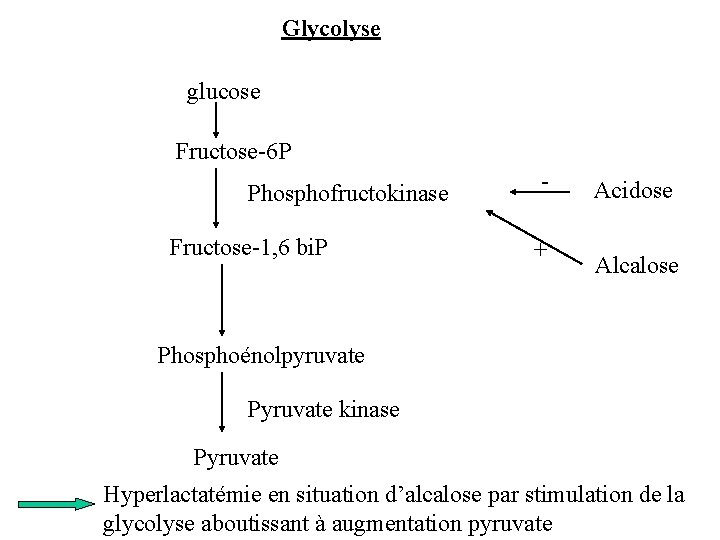
Glycolyse glucose Fructose-6 P Phosphofructokinase Fructose-1, 6 bi. P + Acidose Alcalose Phosphoénolpyruvate Pyruvate kinase Pyruvate Hyperlactatémie en situation d’alcalose par stimulation de la glycolyse aboutissant à augmentation pyruvate
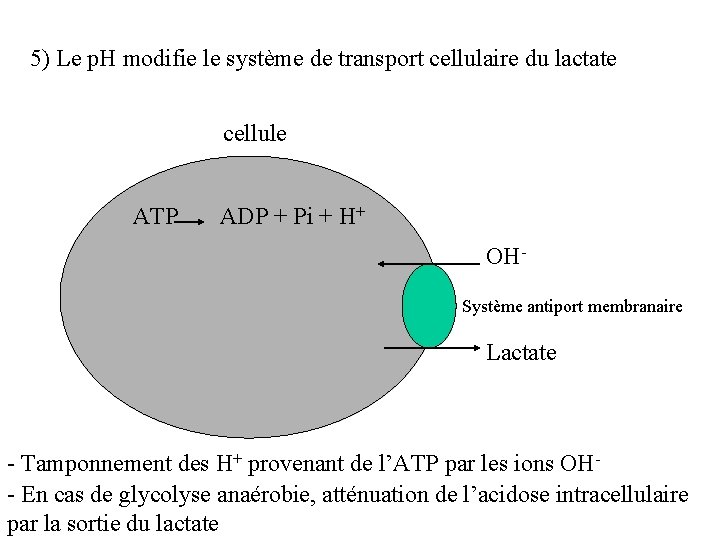
5) Le p. H modifie le système de transport cellulaire du lactate cellule ATP ADP + Pi + H+ OHSystème antiport membranaire Lactate - Tamponnement des H+ provenant de l’ATP par les ions OH- En cas de glycolyse anaérobie, atténuation de l’acidose intracellulaire par la sortie du lactate

Au total, les voies métaboliques du lactate et des H+ sont différentes. Hyperlactatémie == Acidose lactique !

Dosage du lactate - Prélèvement artériel = reflet global du lactate de l’organisme - Prélèvement veineux périphérique = surestime la lactatémie, en particulier lors d’une instabilité hémodynamique Jackson et al. CCM 1997 - Prélever lentement afin de limiter l’hémolyse sur un tube contenant un anticoagulant et mettre dans glace - Centrifuger rapidement de façon à limiter la glycolyse in vitro des hématies qui augmente artificiellement la lactatémie - Surestimation de la lactatémie si perfusion rapide de Ringer lactate - Hyperlactatémie = élévation de la concentration sanguine en lactate > 2 mmol/L

Lactatémie et trou anionique (TA) plasmatique - L’acidose lactique est une acidose métabolique à TA élevé - Delta TA = Delta HCO 3 - Peut on suspecter une hyperlactatémie devant un TA élevé ? Oui mais : - 35 % de faux positifs (élévation du TA sans augmentation d’ac. organiques) Hypoalbuminémie, variation des volumes de distribution des cations et anions, tampons non bicarbonates… - On peut aussi avoir hyperlactatémie modérée et TA normal ! La fiabilité du TA pour le Dg d’hyperlactatémie est donc médiocre Doser directement le lactate !

Hyperlactatémie : facteur pronostique ? Relation indiscutable entre sévérité de l’hyperlactatémie et morbi-mortalité des patients de réanimation Lactate > 5 mmol/L à l’admission en réa Mortalité à 3 j : 60 % Mortalité à 30 j : 83 % Stacpoole et al. Am J Med 1994 Durée de l’acidose lactique +++ Répétition des dosages

Hyperlactatémie : marqueur d’hypoxie et de métabolisme anaérobie ? Energie cellulaire stockée sous forme d’ATP Hydrolyse de l’ATP : ATP ADP + Pi + H+ + énergie Physiologiquement chez l’homme, le métabolisme énergétique repose pour 90 % sur la production aérobie d’ATP et 10 % sur la production anaérobie d’ATP Pour produire de l’ATP en l’absence d’oxygène, la seule voie possible est la glycolyse qui consomme du glucose et produit du lactate. (voie de la créatinine-kinase utilisant la phosphocréatine anecdotique) L’hyperlactatémie marqueur de déficit énergétique dans toutes les mentalités depuis des dizaines d’années.

Les mécanismes de surproduction de lactate en situation d’hypoxie sont complexes : - Blocage de l’oxydation phosphorylante mitochondriale - Baisse du rapport ATP/ADP - Elévation du rapport NADH/NAD - Augmentation de la prod de pyruvate via la glycolyse suite à baisse du rapport ATP/ADP (stimulation de la PFK) - Diminution de l’utilisation du pyruvate vers la voie de l’oxaloacétate - Accumulation de pyruvate via Inhibition de la pyruvate deshydrogénase via élévation du rapport NADH/NAD Au total, l’accumulation de lactate résulte de accumulation de pyruvate et surtout des modif du potentiel redox avec majoration de pyr lact Pyruvate + NADH + H+ Lactate + NAD Utile car seule voie de régénération de NAD permettant de poursuivre la glycolyse

Au total, le métabolisme anaérobie se caractérise par : - Hyperlactatémie - Élévation du rapport Lactate/Pyruvate - Utilisation accrue de glucose - Absence de respiration cellulaire - Déficit oxydatif avec élévation du rapport NADH/NAD

L’hyperlactatémie n’est pas synonyme d’hypoxie tissulaire : Hyperlactatémie et exercice musculaire : - Acidose lactique sévère en qq min (p. H <7 , lactatémie > 20 mmol/L) - Activation de la glycolyse en situation aérobie - Baisse de la clairance hépatique par baisse du débit sanguin hépatique et/ou l’acidose accompagnant l’hyperlactatémie - Idem pour crise convulsive généralisée Déséquilibre entre production et élimination du lactate

Hyperlactatémie et sepsis : De nombreux travaux cliniques et expérimentaux remettent en cause l’origine hypoxique de l’hyperlactatémie observée au cours du sepsis. Absence d’hypoxie tissulaire au cours du sepsis - Accélération du flux glycolytique liée à des cytokines - Diminution de l’activité de la PDH par les cytokines Blocage de l’entrée du pyruvate dans le cycle de Krebs - Modification de certaines activités enzymatiques induisant une surproduction de pyruvate et donc de lactate - Stimulation de la glycolyse par les catécholamines

- Altération de la clairance hépatique au cours du sepsis (baisse du débit hépatique? Altération fonction métabolique hépatique ? ) Hyperlactatémie au cours du sepsis = conséquence d’un métabolisme aérobie plus qu’anaérobie. Déséquilibre entre production et élimination du lactate

Marqueur fiable d’hypoxie tissulaire : le rapport lactate/pyruvate A l’équilibre, 10 fois plus de lactate que de pyruvate En situation anaérobie, l’oxydation phosphorylante mitochondriale est bloquée entraînant accumulation de l’équivalent réduit NADH, favorisant ainsi la formation de lactate, régénérant ainsi le NAD nécessaire à la poursuite de la glycolyse et donc la formation d’ATP Rapport L/P >> 10 L/P = bon indicateur du passage d’un métabolisme aérobie à métabolisme anaérobie

2 types d’hyperlactatémies : - Hyperlactatémie sans acidose sévère dites hyperlactatémie de stress qui sont en rapport avec une accélération aérobie de la glycolyse et/ou un dysfonctionnement de la PDH avec un rapport L/P normal. Ex : sepsis, exercice musculaire, administration d’amines. Traduisent une modification métabolique et non une hypoperfusion tissulaire - Hyperlactatémie avec acidose sévère. Rapport L/P élevé suggérant métabolisme anaérobie Remarque : dosage du pyruvate très difficile en pratique courante

Classification des hyperlactatémies -Formes congénitales rares (anomalies génétiques métaboliques) -Acidoses lactiques acquises : type A : dues à défaut d’oxygénation tissulaire type B : dues à défaut de métabolisation


Classification très schématique car pratiquement toujours excès de production + défaut d’élimination du lactate (exemple du sepsis avec altération de la clairance hépatique du lactate) Intoxications : - Inhibition de la chaîne respiratoire mitochondriale au niveau de la cytochrome oxydase par effet toxique direct (cyanure) ou effet indirect de compétition entre O 2 et CO ou NO. Production d’équivalents réduits - Intoxications aux alcools Elévation du potentiel redox Pyruvate Lactate

Cancers : - Hyperlactatémie sans acidose voire avec alcalose ! - Hyperproduction (défaut de perfusion de la tumeur) + défaut de clairance hépatique (chimiothérapie) - Rôle de l’hexokinase sur l’accélération de la glycolyse ? Hyperlactatémies au cours des alcaloses : - Sous estimée - Excès de production par activation de la PFK en rapport avec le p. H alcalin
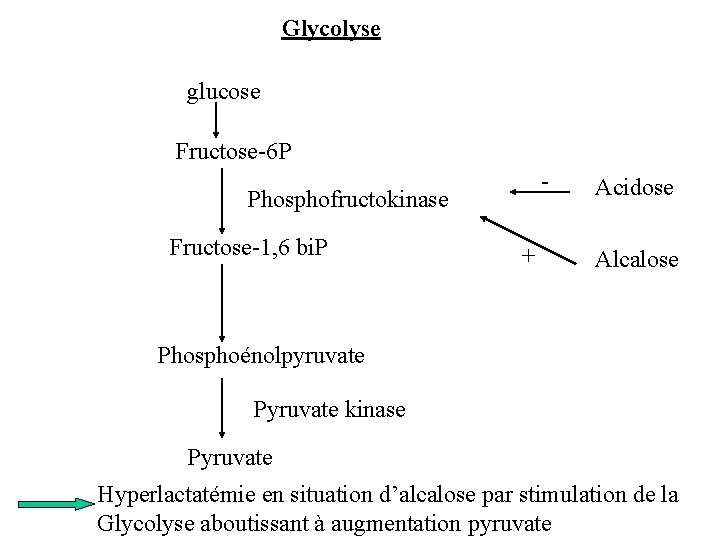
Glycolyse glucose Fructose-6 P - Phosphofructokinase Fructose-1, 6 bi. P + Acidose Alcalose Phosphoénolpyruvate Pyruvate kinase Pyruvate Hyperlactatémie en situation d’alcalose par stimulation de la Glycolyse aboutissant à augmentation pyruvate
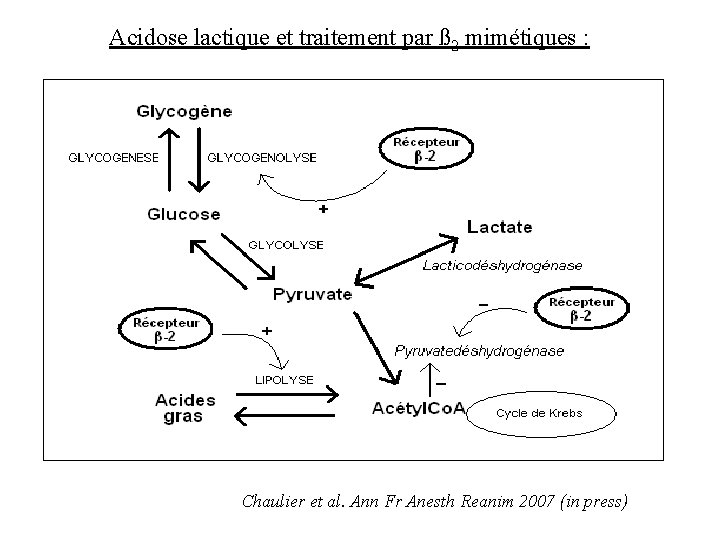
Acidose lactique et traitement par ß 2 mimétiques : Chaulier et al. Ann Fr Anesth Reanim 2007 (in press)

Au total, classification très simpliste et artificielle car : - L’hyperlactatémie résulte en général de plusieurs modifications métaboliques potentialisatrices - Intéractions de mécanismes biochimiques complexes - Probablement encore bcp d’inconnues

Hyperlactatémie : facteur de protection ? Aucune preuve de la toxicité du lactate Acidose lactique et effort musculaire intense, perfusions de lactate pas d’effets délétères Réponse adaptée, mécanisme de protection, mécanisme de défense face à des situations de déficit énergétique ?
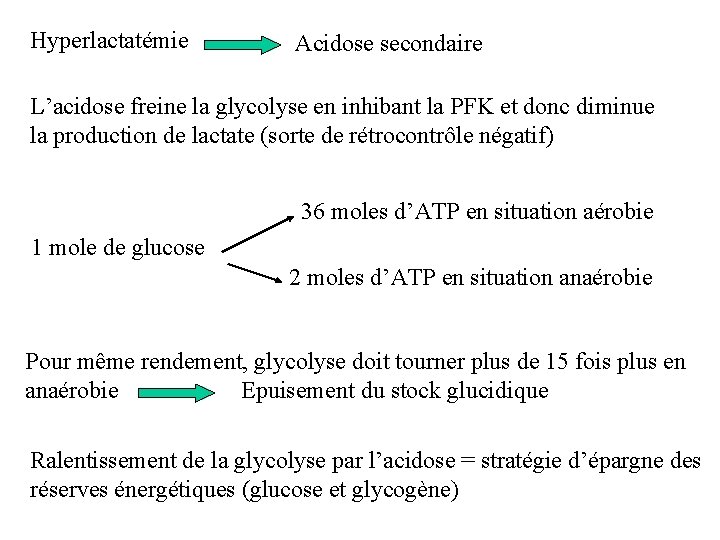
Hyperlactatémie Acidose secondaire L’acidose freine la glycolyse en inhibant la PFK et donc diminue la production de lactate (sorte de rétrocontrôle négatif) 36 moles d’ATP en situation aérobie 1 mole de glucose 2 moles d’ATP en situation anaérobie Pour même rendement, glycolyse doit tourner plus de 15 fois plus en anaérobie Epuisement du stock glucidique Ralentissement de la glycolyse par l’acidose = stratégie d’épargne des réserves énergétiques (glucose et glycogène)

Effet protecteur cellulaire de l’acidose face à l’hypoxie L’augmentation du p. H chez des patients en acidose n’améliore pas La survie

Couple lactate-pyruvate = navette redox Chaque organe ne fonctionne pas indépendamment des autres. Il existe des échanges inter et même intraorganes Le lactate produit dans un organe peut être oxydé dans d’autres organes ou cellules du même organe selon les besoins et les situations physiopathologiques Navette redox lactate-pyruvate Exemples : 1) Cycle de Cori entre foie et globule rouge 2) Agression pulmonaire Elévation de la prod de lactate par poumon Lacatémie reste normale car augmentation du recaptage par foie et rein

Lactate = substrat énergétique Oxydation du lactate issu des tissus hypoxiques par les tissus aérobies Baisse du métabolisme du glucose dans les tissus aérobies Epargne de glucose pour la production anaérobie d’ATP via la glycolyse dans les tissus anaérobies

L’hyperlactatémie entraîne certaines voies métaboliques vers une économie de substrats énergétiques (glucose, glycogène) qui sont ainsi réservés aux organes ou cellules en situation anaérobie. « Brain lactate production is not a suicide, it is a survival kit » Schurr et al. Dev Neurosci 1998

Importance qualitative de la production d’ATP anaérobie Le métabolisme énergétique de la cellule est compartimenté : les activités des pompes membranaires ATPase sont surtout dépendantes de l’ATP glycolytique. = autre effet protecteur de l’ATP glycolytique Leverve. Réanimation 2003

Traitement des acidoses lactiques 1) Faut-il traiter l’acidose ? 2) Faut-il traiter l’hyperlactatémie ?

Faut-il traiter l’acidose ? Il faut traiter la cause sous-jacente de survenue de l’acidose lactique. Ex : rétablir un apport suffisant d’O 2 aux tissus en optimisant l’Hb et la Pa 02. Corriger l’acidose en elle-même par des solutés tampons tels que le bicarbonate de sodium n’a montré aucun bénéfice. Il existe des effets protecteurs de l’acidose en cas de déficit énergétique donc il est illogique de préconiser un ttt actif de l’acidose par hyperlactatémie.

Faut-il traiter l’hyperlactatémie ? Le lactate n’est pas toxique Aucun intérêt à corriger l’hyperlactatémie simplement pour normaliser le chiffre de lactate L’administration de dichloroacétate diminue la lactatémie via la stimulation de la PDH mais n’améliore pas la survie des patients. Stacpoole et al. Ann Intern Med 1998

Conclusion Hypoxie tissulaire Déficit énergétique Hyperlactatémie Acidose lactique en réanimation = lourde mortalité et morbidité Hyperlactatémie == Acidose lactique Hyperlactatémie == Hypoxie tissulaire Le plus souvent, déséquilibre entre production et élimination du lactate

- Métabolite majeur, indispensable à la vie, situé au carrefour des grandes voies métaboliques - Absence de toxicité du lactate - Utilité du lactate pour économiser d’autres réserves énergétiques - Garant de la coopération énergétique entre les différents organes (navette redox lactate/pyruvate)

- Son élévation doit être considéré comme un signal d’alerte correspondant à des phénomènes énergétiques adaptatifs qu’il importe d’analyser et de comprendre. - Encore beaucoup d’inconnues mais cette réponse métabolique semble intégrée à tout l’organisme avec une hiérarchisation des priorités et une redistribution métabolique entre les organes.

« Primum non nocere » Hippocrate (- 400 AVJC)
- Slides: 93