Druhy vazby oktetov pravidlo Vazba iontov polrn Vazba

Druhy vazby oktetové pravidlo • • Vazba iontová polární • • Vazba v kovech • Mezimolekulární interakce kovalentní
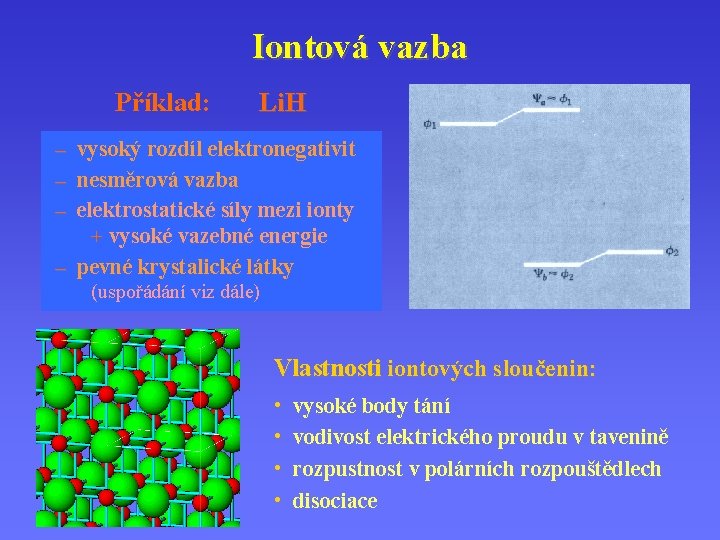
Iontová vazba Příklad: Li. H – vysoký rozdíl elektronegativit – nesměrová vazba – elektrostatické síly mezi ionty + vysoké vazebné energie – pevné krystalické látky (uspořádání viz dále) Vlastnosti iontových sloučenin: • • vysoké body tání vodivost elektrického proudu v tavenině rozpustnost v polárních rozpouštědlech disociace
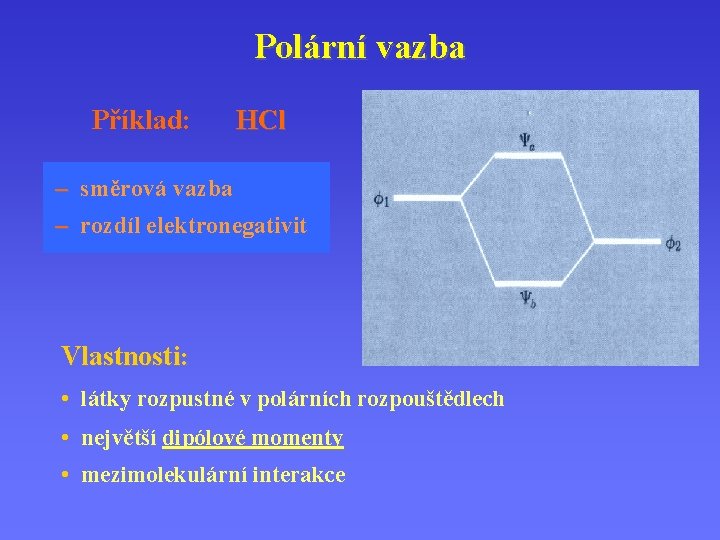
Polární vazba Příklad: HCl – směrová vazba – rozdíl elektronegativit Vlastnosti: • látky rozpustné v polárních rozpouštědlech • největší dipólové momenty • mezimolekulární interakce
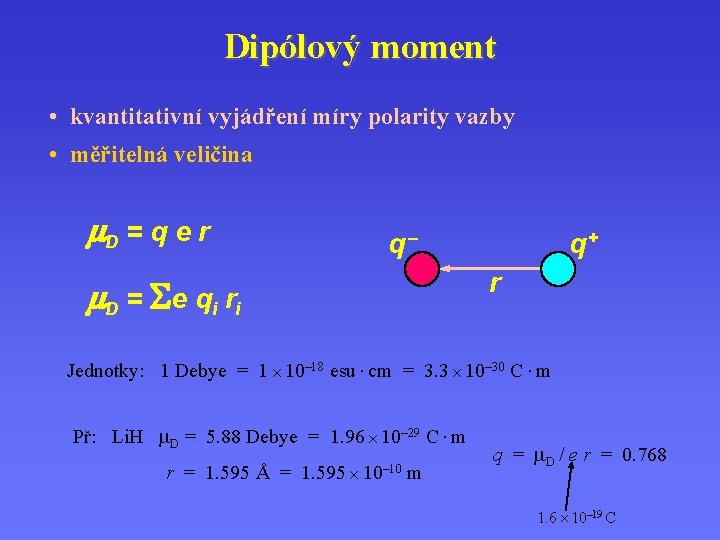
Dipólový moment • kvantitativní vyjádření míry polarity vazby • měřitelná veličina m. D = q e r q– q+ r m. D = S e q i r i Jednotky: 1 Debye = 1 10– 18 esu · cm = 3. 3 10– 30 C · m Př: Li. H m. D = 5. 88 Debye = 1. 96 10– 29 C · m r = 1. 595 Å = 1. 595 10– 10 m q = m. D / e r = 0. 768 1. 6 10– 19 C
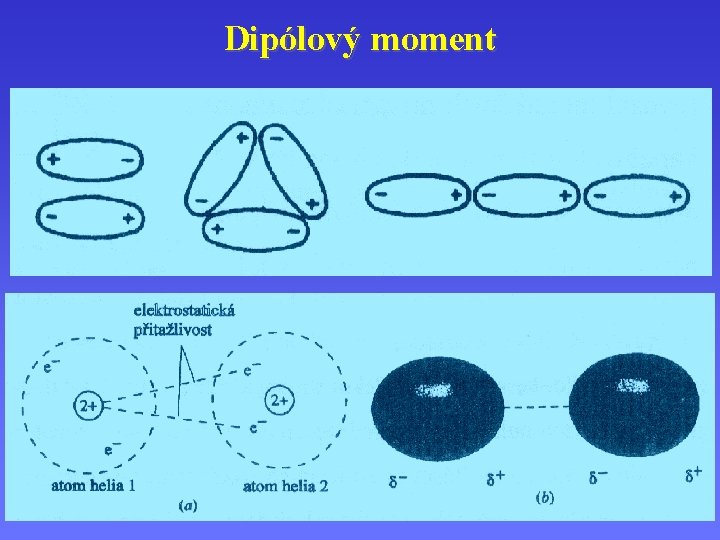
Dipólový moment

Dipólové momenty p některých molekul (v jednotkách D; 1 D = 3, 34 · 10– 30 C·m) molekula p HF 1, 82 H 2 0 HCl 1, 08 CO 2 0 HBr 0, 82 CS 2 0 HI 0, 44 CH 4 0 NH 3 1, 34 Li. H 5, 88 NF 3 0, 23 KF 8, 60 H 2 O 1, 84 KI 10, 44
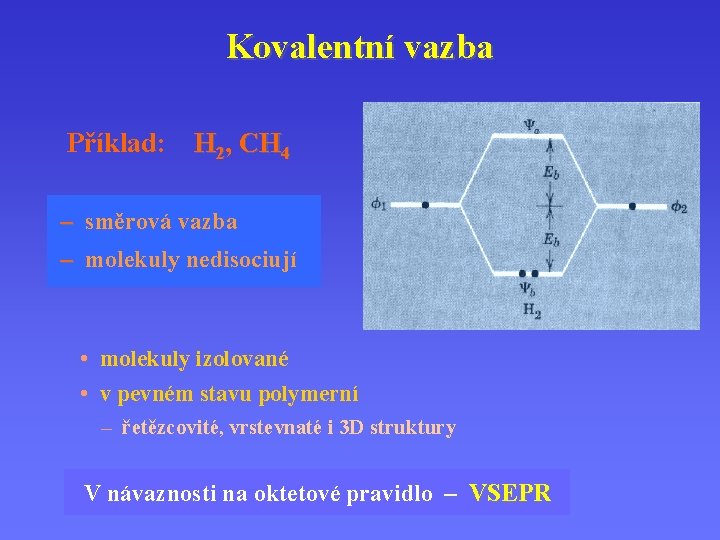
Kovalentní vazba Příklad: H 2, CH 4 – směrová vazba – molekuly nedisociují • molekuly izolované • v pevném stavu polymerní – řetězcovité, vrstevnaté i 3 D struktury V návaznosti na oktetové pravidlo – VSEPR
- Slides: 7