Dr Niko Radulovi vanredni profesor Dr Polina Blagojevi

Dr Niko Radulović, vanredni profesor Dr Polina Blagojević, vanredni profesor Dipl. hem. Marija Denić, asistent Dipl. hem. Miljana Đorđević, saradnik Dipl. hem. Dragan Zlatković, saradnik ORGANSKA HEMIJA II
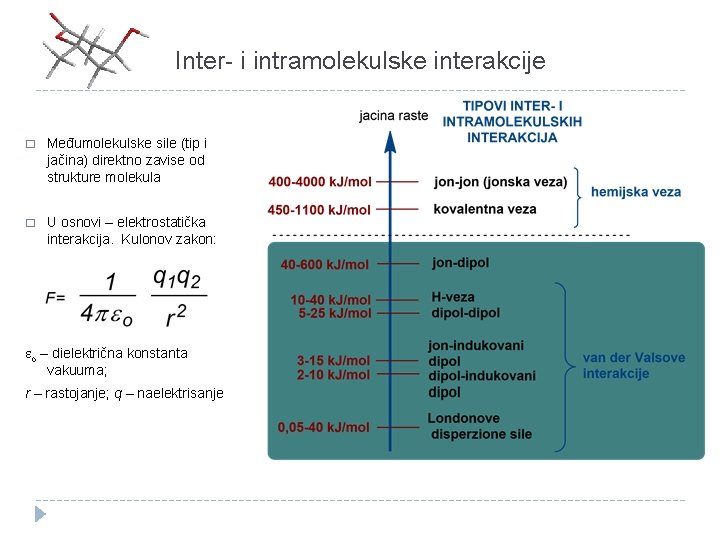
Inter- i intramolekulske interakcije � Međumolekulske sile (tip i jačina) direktno zavise od strukture molekula � U osnovi – elektrostatička interakcija. Kulonov zakon: eo – dielektrična konstanta vakuuma; r – rastojanje; q – naelektrisanje
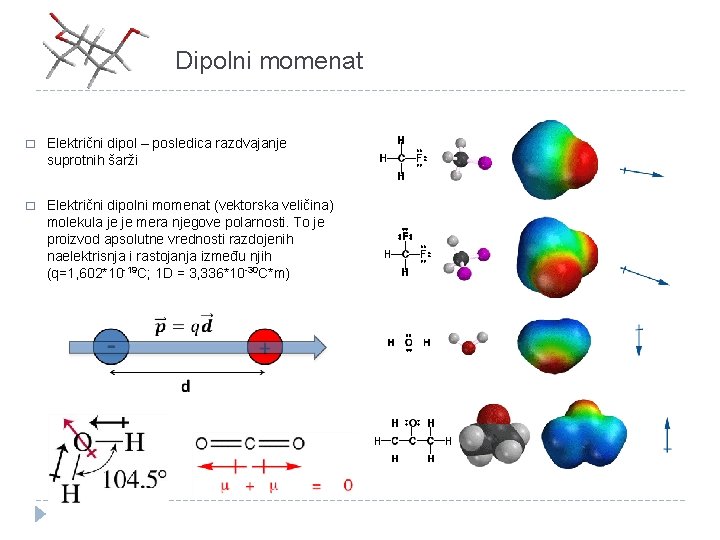
Dipolni momenat � Električni dipol – posledica razdvajanje suprotnih šarži � Električni dipolni momenat (vektorska veličina) molekula je je mera njegove polarnosti. To je proizvod apsolutne vrednosti razdojenih naelektrisnja i rastojanja između njih (q=1, 602*10 -19 C; 1 D = 3, 336*10 -30 C*m)
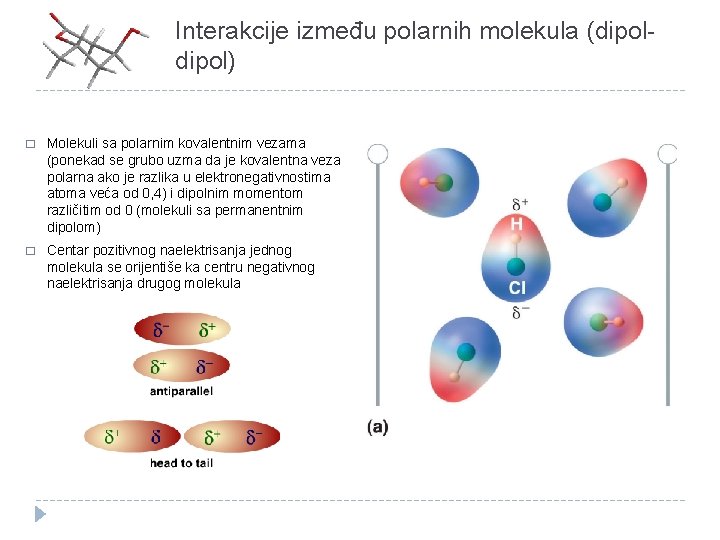
Interakcije između polarnih molekula (dipol) � Molekuli sa polarnim kovalentnim vezama (ponekad se grubo uzma da je kovalentna veza polarna ako je razlika u elektronegativnostima atoma veća od 0, 4) i dipolnim momentom različitim od 0 (molekuli sa permanentnim dipolom) � Centar pozitivnog naelektrisanja jednog molekula se orijentiše ka centru negativnog naelektrisanja drugog molekula
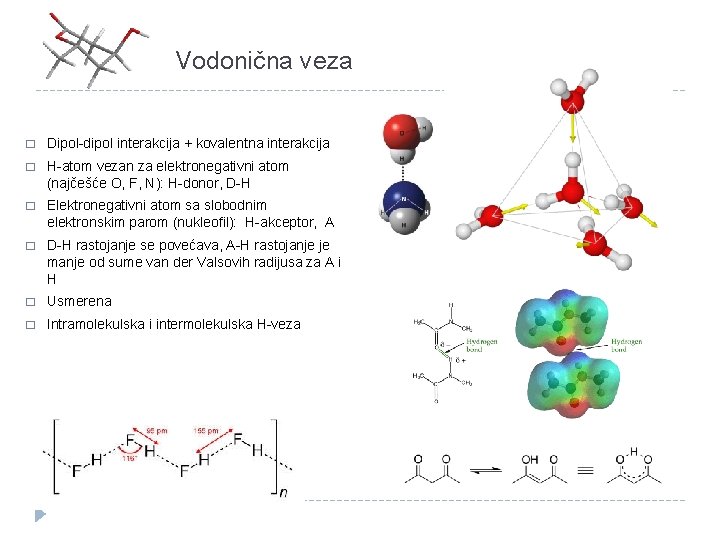
Vodonična veza � Dipol-dipol interakcija + kovalentna interakcija � H-atom vezan za elektronegativni atom (najčešće O, F, N): H-donor, D-H � Elektronegativni atom sa slobodnim elektronskim parom (nukleofil): H-akceptor, A � D-H rastojanje se povećava, A-H rastojanje je manje od sume van der Valsovih radijusa za A i H � Usmerena � Intramolekulska i intermolekulska H-veza
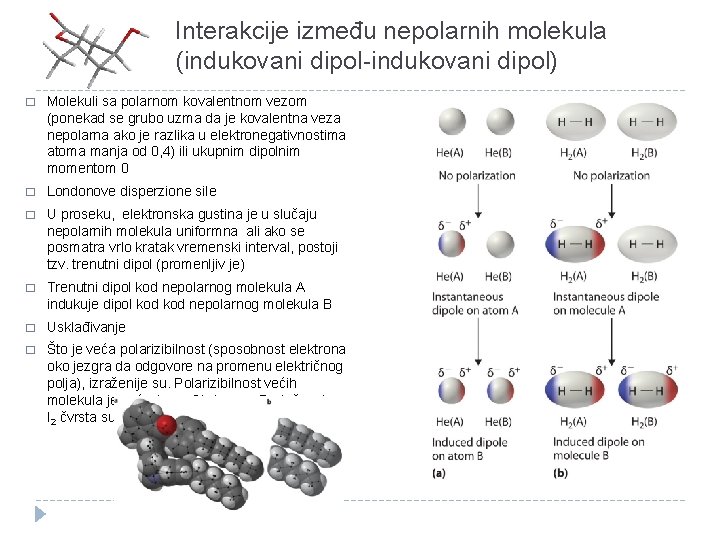
Interakcije između nepolarnih molekula (indukovani dipol-indukovani dipol) � Molekuli sa polarnom kovalentnom vezom (ponekad se grubo uzma da je kovalentna veza nepolarna ako je razlika u elektronegativnostima atoma manja od 0, 4) ili ukupnim dipolnim momentom 0 � Londonove disperzione sile � U proseku, elektronska gustina je u slučaju nepolarnih molekula uniformna ali ako se posmatra vrlo kratak vremenski interval, postoji tzv. trenutni dipol (promenljiv je) � Trenutni dipol kod nepolarnog molekula A indukuje dipol kod nepolarnog molekula B � Usklađivanje � Što je veća polarizibilnost (sposobnost elektrona oko jezgra da odgovore na promenu električnog polja), izraženije su. Polarizibilnost većih molekula je veća (npr. Cl 2 je gas, Br 2 tečnost a I 2 čvrsta supstanca)
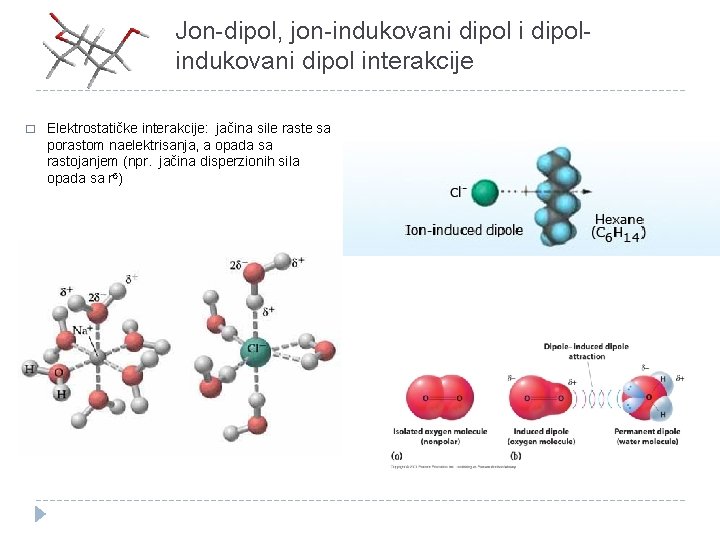
Jon-dipol, jon-indukovani dipolindukovani dipol interakcije � Elektrostatičke interakcije: jačina sile raste sa porastom naelektrisanja, a opada sa rastojanjem (npr. jačina disperzionih sila opada sa r 6)
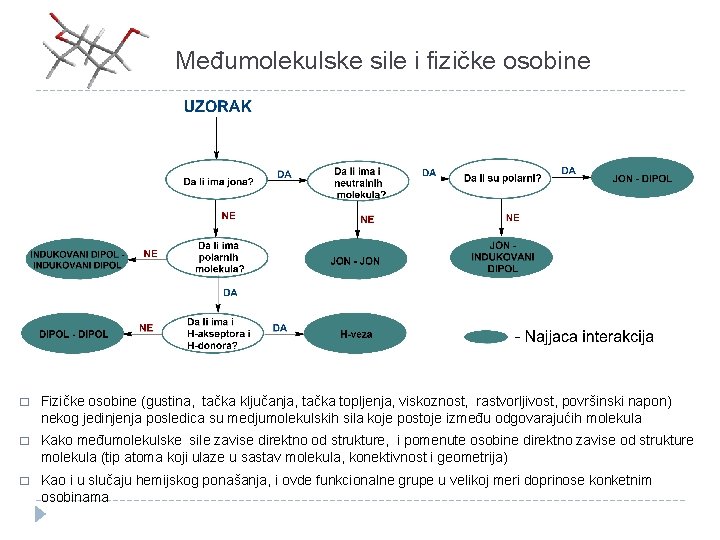
Međumolekulske sile i fizičke osobine � Fizičke osobine (gustina, tačka ključanja, tačka topljenja, viskoznost, rastvorljivost, površinski napon) nekog jedinjenja posledica su medjumolekulskih sila koje postoje između odgovarajućih molekula � Kako međumolekulske sile zavise direktno od strukture, i pomenute osobine direktno zavise od strukture molekula (tip atoma koji ulaze u sastav molekula, konektivnost i geometrija) � Kao i u slučaju hemijskog ponašanja, i ovde funkcionalne grupe u velikoj meri doprinose konketnim osobinama
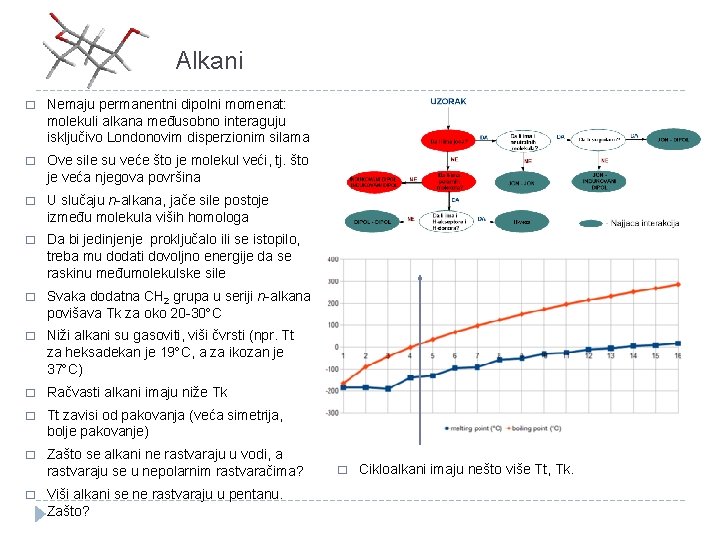
Alkani � Nemaju permanentni dipolni momenat: molekuli alkana međusobno interaguju isključivo Londonovim disperzionim silama � Ove sile su veće što je molekul veći, tj. što je veća njegova površina � U slučaju n-alkana, jače sile postoje između molekula viših homologa � Da bi jedinjenje proključalo ili se istopilo, treba mu dodati dovoljno energije da se raskinu međumolekulske sile � Svaka dodatna CH 2 grupa u seriji n-alkana povišava Tk za oko 20 -30 C � Niži alkani su gasoviti, viši čvrsti (npr. Tt za heksadekan je 19 C, a za ikozan je 37 C) � Račvasti alkani imaju niže Tk � Tt zavisi od pakovanja (veća simetrija, bolje pakovanje) � Zašto se alkani ne rastvaraju u vodi, a rastvaraju se u nepolarnim rastvaračima? � Viši alkani se ne rastvaraju u pentanu. Zašto? � Cikloalkani imaju nešto više Tt, Tk.
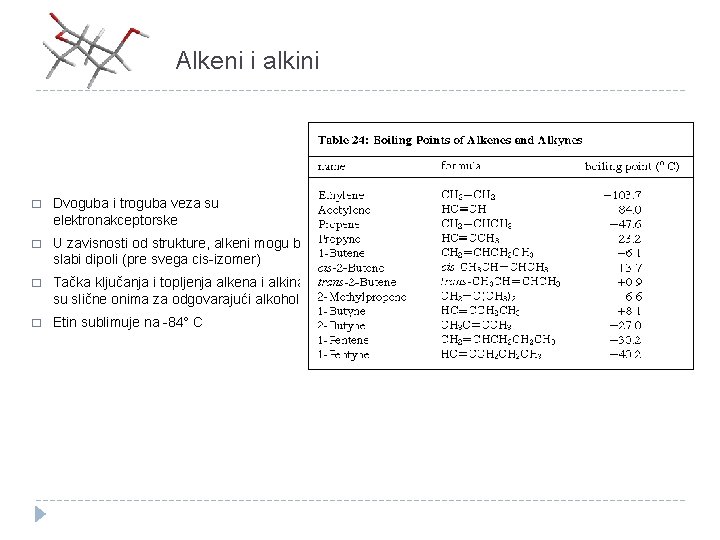
Alkeni i alkini � Dvoguba i troguba veza su elektronakceptorske � U zavisnosti od strukture, alkeni mogu biti slabi dipoli (pre svega cis-izomer) � Tačka ključanja i topljenja alkena i alkina su slične onima za odgovarajući alkohol � Etin sublimuje na -84 C
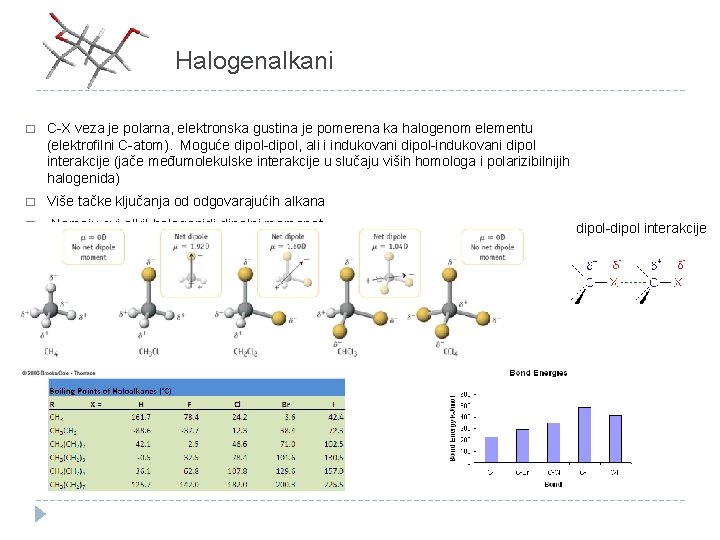
Halogenalkani � C-X veza je polarna, elektronska gustina je pomerena ka halogenom elementu (elektrofilni C-atom). Moguće dipol-dipol, ali i indukovani dipol-indukovani dipol interakcije (jače međumolekulske interakcije u slučaju viših homologa i polarizibilnijih halogenida) � Više tačke ključanja od odgovarajućih alkana � Nemaju svi alkil-halogenidi dipolni momenat dipol-dipol interakcije
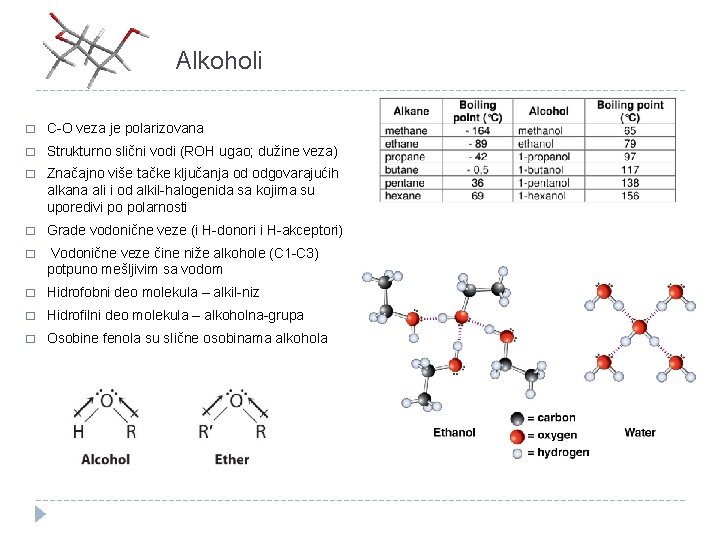
Alkoholi � C-O veza je polarizovana � Strukturno slični vodi (ROH ugao; dužine veza) � Značajno više tačke ključanja od odgovarajućih alkana ali i od alkil-halogenida sa kojima su uporedivi po polarnosti � Grade vodonične veze (i H-donori i H-akceptori) � Vodonične veze čine niže alkohole (C 1 -C 3) potpuno mešljivim sa vodom � Hidrofobni deo molekula – alkil-niz � Hidrofilni deo molekula – alkoholna-grupa � Osobine fenola su slične osobinama alkohola
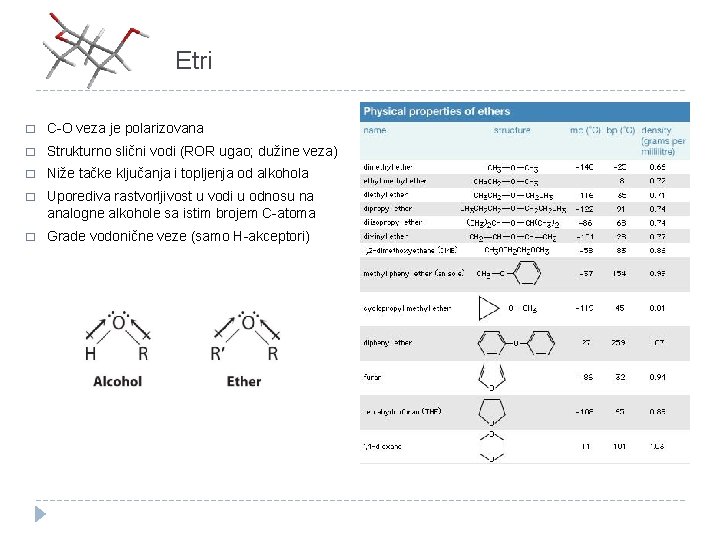
Etri � C-O veza je polarizovana � Strukturno slični vodi (ROR ugao; dužine veza) � Niže tačke ključanja i topljenja od alkohola � Uporediva rastvorljivost u vodi u odnosu na analogne alkohole sa istim brojem C-atoma � Grade vodonične veze (samo H-akceptori)
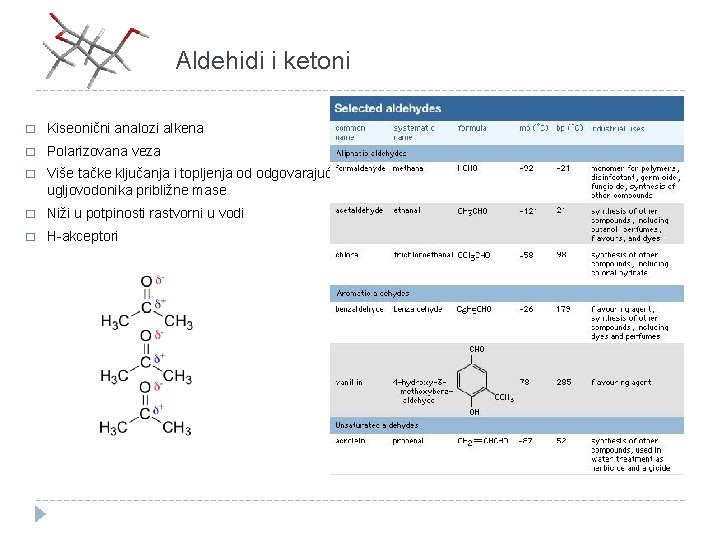
Aldehidi i ketoni � Kiseonični analozi alkena � Polarizovana veza � Više tačke ključanja i topljenja od odgovarajućih ugljovodonika približne mase � Niži u potpinosti rastvorni u vodi � H-akceptori
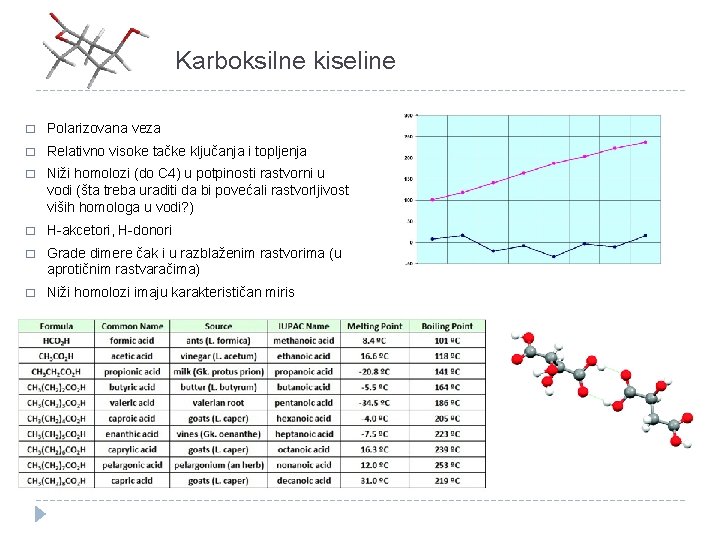
Karboksilne kiseline � Polarizovana veza � Relativno visoke tačke ključanja i topljenja � Niži homolozi (do C 4) u potpinosti rastvorni u vodi (šta treba uraditi da bi povećali rastvorljivost viših homologa u vodi? ) � H-akcetori, H-donori � Grade dimere čak i u razblaženim rastvorima (u aprotičnim rastvaračima) � Niži homolozi imaju karakterističan miris
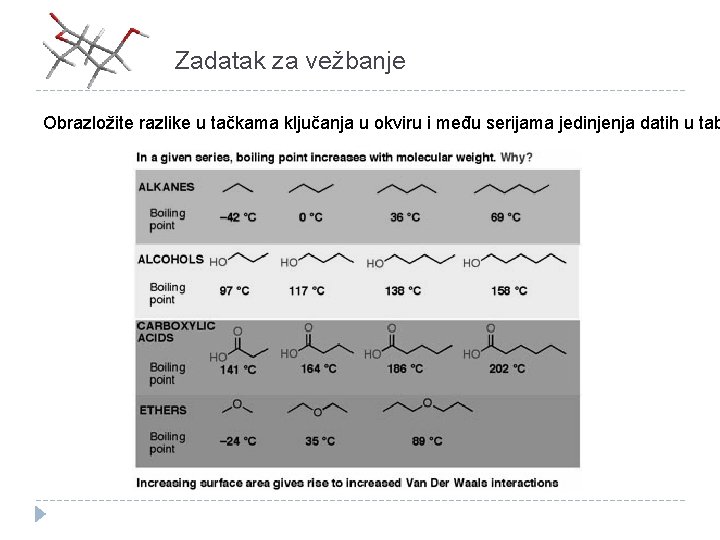
Zadatak za vežbanje Obrazložite razlike u tačkama ključanja u okviru i među serijama jedinjenja datih u tab

OSNOVNO ZNANJE ! � � � Tipovi interakcija Kako se menjaju osobine molekula koji pripadaju istoj homologoj seriji Kako se razlikuju osobine odgovarajućih predstavnika različitih klasa jedinjenja (isti skelet, različita funkcionalna grupa)
- Slides: 17