Dr Jose Luis Gorriz Hospital Universitario Dr Peset






























- Slides: 49

Dr Jose Luis Gorriz Hospital Universitario Dr Peset Valencia

¿L@s nefrólog@s hacen algo mas que dializar? ¿Los nefrólog@s hacen algo especial que no puedan hacer otros médicos?

¿Qué actitudes realiza el nefrólogo en el paciente con enfermedad renal crónica? • Control estricto de la presión arterial • Tratamiento de la anemia • Tratamiento de las alteraciones del metab oseo mineral • Tratamiento de la acidosis metabólica e hiperpotasemia • Tratamiento de la dislipemia • Otros: evitar el tabaquismo y el sobrepeso • Preparación para terapias sustitutivas renales

Factores de progresión de la enfermedad renal • NO MODIFICABLES: – – – – Sexo varón Edad Raza (afro-am) Genéticos-hered. Bajo peso al nacer nº de nefronas Historia familiar de ERC Taal & Brenner. Kidney Int 2006 • MODIFICABLES: – – – HTA Proteinuria Hiperfiltración-obesidad Tabaquismo Control glucémico (DM) Otros: • • Anemia Alt metab Ca-P Estrés oxidativo Inflamación

AHA: Cardiovascular risk factors in patients with CKD include anemia Cardiovascular risk factors in CKD Traditional risk factors Non-traditional risk factors §Increasing age §Male sex §Hypertension §Higher LDL §Lower LDL §Diabetes §Smoking §Physical inactivity §Menopause §Family hustory of CVD §Left ventricular hyperthrophy • Albuminuria • Homocysteine • Lipoprotein (a) • ANEMIA • Abnormal Calcium/phosphate metabolism • Extracellular fluid volume overload • Electrolyte imbalance • Ixidative stress • Inflamation (C reactive protein) • Malnutrition • Thrombogenic factors • Altered nitric oxide/endothelin balance Sharnak, Circulation 2003; 108; 2154 -2169

Guias • ERC: anemia por déficit de EPO. • Exclusión de causas diferentes (deficit férrico, B 12, folico). • Hb > 11 g/dl. • Tto con AAEE cuando: – Ferritina > 100 ng/ml – IST > 20 %.

Anemia de la ERC • Anemia normocítica normocrómica. • Si no se trata: – oxigenación y utilización del O 2 (tejidos). – ↑ Gasto cardiaco. – HVI – ICC – agudeza mental y cognitiva.

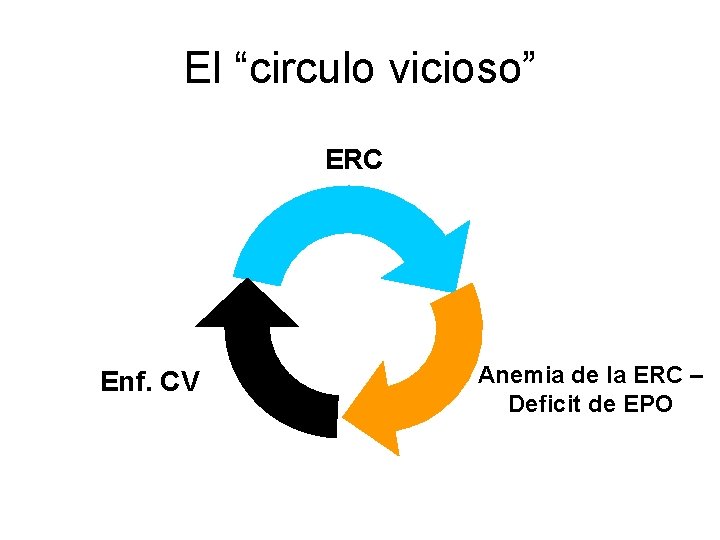
El “circulo vicioso” ERC Enf. CV Anemia de la ERC – Deficit de EPO

¿La anemia incrementa la mortalidad por ICC? • En 54 (96 %) de 56 estudios en pacientes con ICC, la anemia se asoció a un incremento de la mortalidad: • • • SOLVD ELITE Val-He. FT ATLAS IN-CHF • • • OPTIMUS COPERNICUS RENAISSANCE OPTIMAAL PRAISE POR CADA 3% HTO 1. 08 RR AJUSTADO de MUERTE POR CADA 0. 1 mg/dl Cr 1. 06 RR AJUSTADO de MUERTE JACC 2002; 39: 955; JASN 2002; 13: 1928. Cir 2003; 107: 223

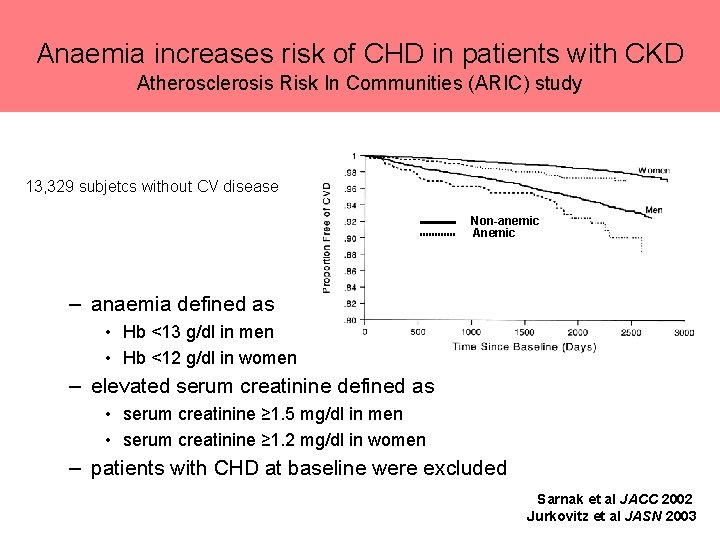
Anaemia increases risk of CHD in patients with CKD Atherosclerosis Risk In Communities (ARIC) study 13, 329 subjetcs without CV disease Non-anemic Anemic – anaemia defined as • Hb <13 g/dl in men • Hb <12 g/dl in women – elevated serum creatinine defined as • serum creatinine ≥ 1. 5 mg/dl in men • serum creatinine ≥ 1. 2 mg/dl in women – patients with CHD at baseline were excluded Sarnak et al JACC 2002 Jurkovitz et al JASN 2003

¿La anemia incrementa la hospitalización y severidad de la ICC? • En 17 de 17 estudios en pacientes con ICC, la anemia se asoció a mayor nº de días de hospitalización. • En 14 (82 %) de 17 estudios en pacientes con ICC, la anemia se asoció a mayor severidad de la ICC (mayor grado NYHA). Silverberg DS Clinical Nephrology 2003; 60 (suppl 1) S 9

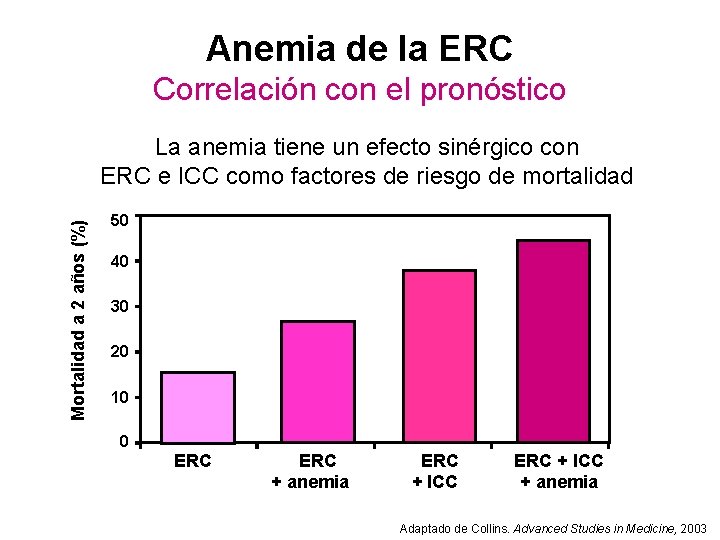
Anemia de la ERC Correlación con el pronóstico Mortalidad a 2 años (%) La anemia tiene un efecto sinérgico con ERC e ICC como factores de riesgo de mortalidad 50 40 30 20 10 0 ERC + anemia ERC + ICC + anemia Adaptado de Collins. Advanced Studies in Medicine, 2003

Tto de la anemia en la ERC • Mejora la supervivencia 1. • mortalidad 2. • ↑ calidad de vida 3. • Quedan todavía algunas cuestiones por resolver, como el nivel objetivo de Hb en una población heterogenea de pacientes con ERC. 1. - Grutzmacher Pet al. Contrib Nephrol 1988; 66: 176 -84. 2. - Evans RW et al. JAMA 1990; 263: 825 -30. 3. - Delano BG et al. Am J Kidney Dis 1989; 14 (Suppl 1): 14 -8.

CHOIR • Hb 13, 5 vs Hb 11, 3 • 1342 ptes ERC • Los niveles objetivo de Hb de 13, 5 g/d. L (respecto de 11, 3 g/d. L) se asociaron con un aumento del riesgo cardiovascular”. • 125 epidodios en Hb alta y 97 en Hb baja. • Alta tasa de abandono • Diferencias en las caracteristicas basales (edad, comorbilidad, IMC, …) Singh et al. NEJM 2006; 355: 2085

CREATE • • 603 pacientes ERC (FG 15 -35). Hb 11 vs 12. 5 g/dl. 58 eventos en grupo 1 vs 47 en grupo 2. La correcciontemprana de la anemia no reduce el riesgo CV. • Tasa de episodios más baja de la esperada (6% frente a 15% ) Drueque NEJM 2006; 355: 2071

Comentarios a ambos estudios • No parece defendible normalizar totalmente la Hb en todos los pacientes, especialmente en pacientes con alto riesgo CV. • Evitar unos niveles superiores a 13 g/dl y 12 en pacientes de alto rtiesgo CV, probablemente pueda reducir la morbimortalidad CV de estos pacientes. • Se requieren mas estudios. • Individualización.

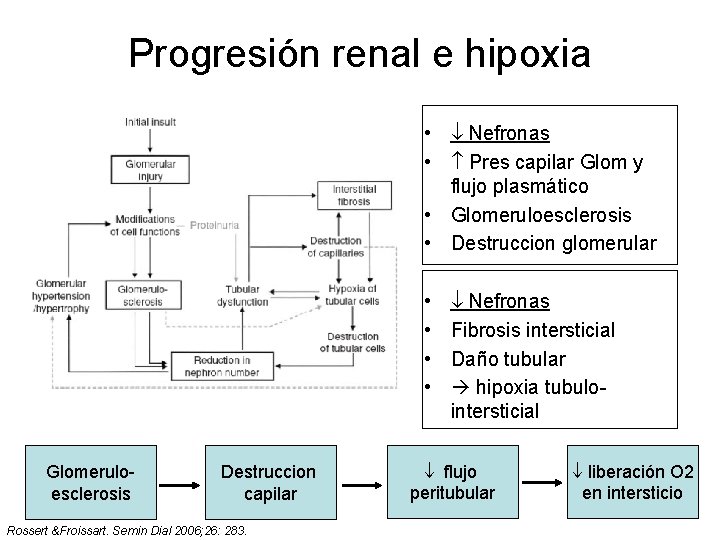
Anemia y progresión renal • Hipótesis basada en datos experimentales. • Mecanismos de lesión: – Hipoxia células tubulares. – Daño intersticial • Patogenia – Eritrocitos: Principal componente antioxidante de la sangre. – Estrés oxidativo Glomeruloesclerosis y daño tubulo intersticial.

Progresión renal e hipoxia • Nefronas • Pres capilar Glom y flujo plasmático • Glomeruloesclerosis • Destruccion glomerular • • Glomeruloesclerosis Destruccion capilar Rossert &Froissart. Semin Dial 2006; 26: 283. Nefronas Fibrosis intersticial Daño tubular hipoxia tubulointersticial flujo peritubular liberación O 2 en intersticio

Estudios clínicos que relacionan la anemia y la progresión renal • Revisión CARI Guidelines. – Nivel de evidencia II. – 7 RCT (escaso numero de pacientes): • 5 no efecto AAEE en progresión. • 2 EPO retrasa la progresión renal en no diabéticos (Jungers 2001; NDT 16: 307 -12; Gouva 2004; KI 66: 753). • Otros: – – RENAAL (Brenner NEJM 2001; 345: 861) Rosing et al (Kidney Int 2004; 66: 1596) Ravani et al (JASN 2005; 16: 2449) Iseki NDT (2003; 18: 899)

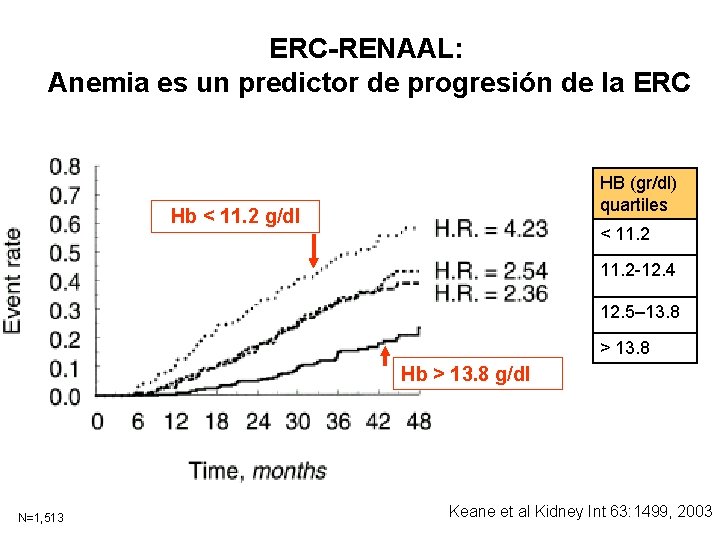
ERC-RENAAL: Anemia es un predictor de progresión de la ERC HB (gr/dl) quartiles Hb < 11. 2 g/dl < 11. 2 -12. 4 12. 5– 13. 8 > 13. 8 Hb > 13. 8 g/dl N=1, 513 Keane et al Kidney Int 63: 1499, 2003

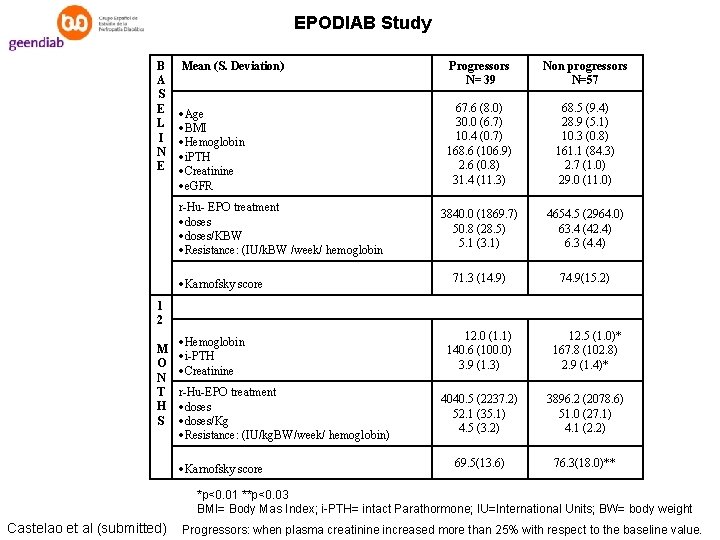
EPODIAB Study B A S E L I N E Mean (S. Deviation) Progressors N= 39 Non progressors N=57 Age BMI Hemoglobin i. PTH Creatinine e. GFR 67. 6 (8. 0) 30. 0 (6. 7) 10. 4 (0. 7) 168. 6 (106. 9) 2. 6 (0. 8) 31. 4 (11. 3) 68. 5 (9. 4) 28. 9 (5. 1) 10. 3 (0. 8) 161. 1 (84. 3) 2. 7 (1. 0) 29. 0 (11. 0) 3840. 0 (1869. 7) 50. 8 (28. 5) 5. 1 (3. 1) 4654. 5 (2964. 0) 63. 4 (42. 4) 6. 3 (4. 4) 71. 3 (14. 9) 74. 9(15. 2) 12. 0 (1. 1) 140. 6 (100. 0) 3. 9 (1. 3) 12. 5 (1. 0)* 167. 8 (102. 8) 2. 9 (1. 4)* 4040. 5 (2237. 2) 52. 1 (35. 1) 4. 5 (3. 2) 3896. 2 (2078. 6) 51. 0 (27. 1) 4. 1 (2. 2) 69. 5(13. 6) 76. 3(18. 0)** r-Hu- EPO treatment doses/KBW Resistance: (IU/k. BW /week/ hemoglobin Karnofsky score 1 2 Hemoglobin M i-PTH O Creatinine N T r-Hu-EPO treatment H doses S doses/Kg Resistance: (IU/kg. BW/week/ hemoglobin) Karnofsky score *p<0. 01 **p<0. 03 BMI= Body Mas Index; i-PTH= intact Parathormone; IU=International Units; BW= body weight Castelao et al (submitted) Progressors: when plasma creatinine increased more than 25% with respect to the baseline value.

Corrección de la anemia y progresión renal • La hipótesis de que la corrección de la anemia con AAEE puede retrasar la progresión de la enfermedad renal es posible basada en los resultados obtenidos de estudios de cohortes y pequeños ensayos clínicos sugieren la necesidad de un gran estudio prospectivo.

Alteraciones del metabolismo oseomineral y morbimortalidad CV

Preguntas • ¿Las alteraciones del metabolismo óseo-mineral se asocian a una mayor morbimortalidad cardiovascular? • ¿Su corrección mejora la morbimortalidad CV? • ¿Su corrección reatrasa la progresion renal?

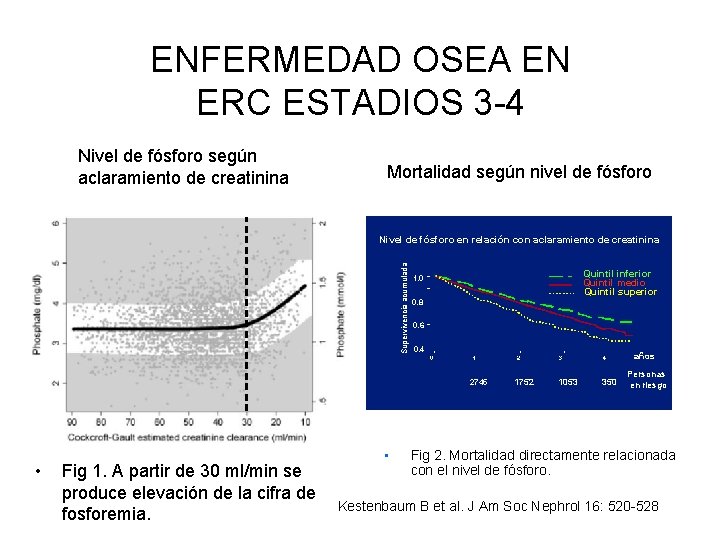
ENFERMEDAD OSEA EN ERC ESTADIOS 3 -4 Nivel de fósforo según aclaramiento de creatinina Mortalidad según nivel de fósforo Supervivencia acumulada Nivel de fósforo en relación con aclaramiento de creatinina Quintil inferior Quintil medio Quintil superior 1. 0 0. 8 0. 6 0. 4 años 2745 • Fig 1. A partir de 30 ml/min se produce elevación de la cifra de fosforemia. • 1752 1053 350 Personas en riesgo Fig 2. Mortalidad directamente relacionada con el nivel de fósforo. Kestenbaum B et al. J Am Soc Nephrol 16: 520 -528

Efectos cardiovasculares del fósforo • Grosor íntima-media. • Rigidez arterial. • Trastornos hemodinámicos: – PA, FC, PP, velocidad onda de pulso. • Fibrosis cardiaca y enf microvascular. • Calcificación – Coronaria, vascular y miocárdica. Qunibi et al. Kidney Int 2004

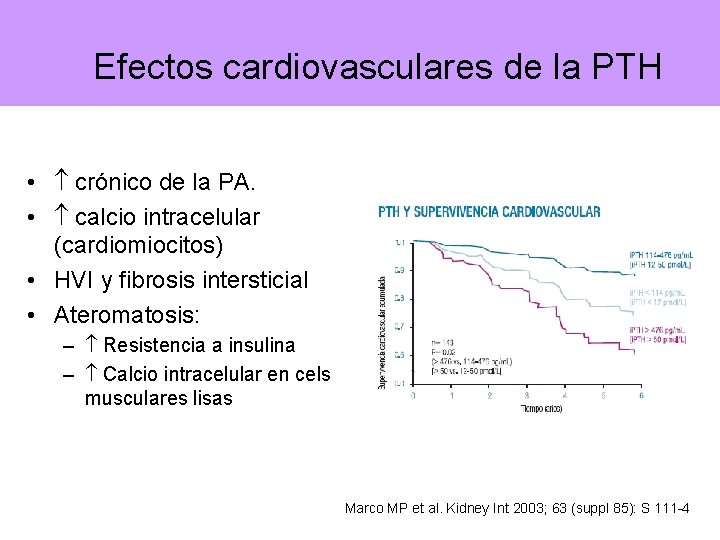
Efectos cardiovasculares de la PTH • crónico de la PA. • calcio intracelular (cardiomiocitos) • HVI y fibrosis intersticial • Ateromatosis: – Resistencia a insulina – Calcio intracelular en cels musculares lisas Marco MP et al. Kidney Int 2003; 63 (suppl 85): S 111 -4

Efectos cardiovasculares de la vitamina D • Pared vascular (efecto antiproliferativo): – Las células endoteliales y del musculo liso vascular poseen receptores para la vit D. – Vit D: papel protector en ateromatosis (modula las metaloproteinasas). • Supresión de la renina (bloqueo SRAA). • Inhibición de la inflamación (papel en AE). Levin A , Li YC. Kidney Int 2005; 68: 1973 -81

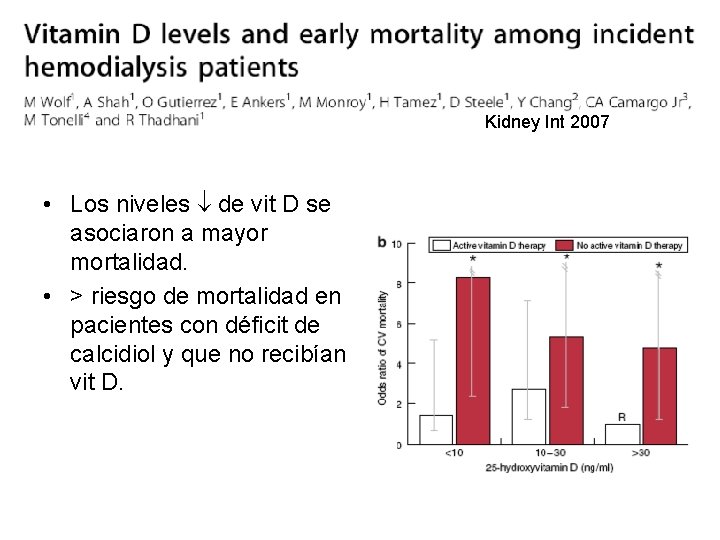
Kidney Int 2007 • Los niveles de vit D se asociaron a mayor mortalidad. • > riesgo de mortalidad en pacientes con déficit de calcidiol y que no recibían vit D.

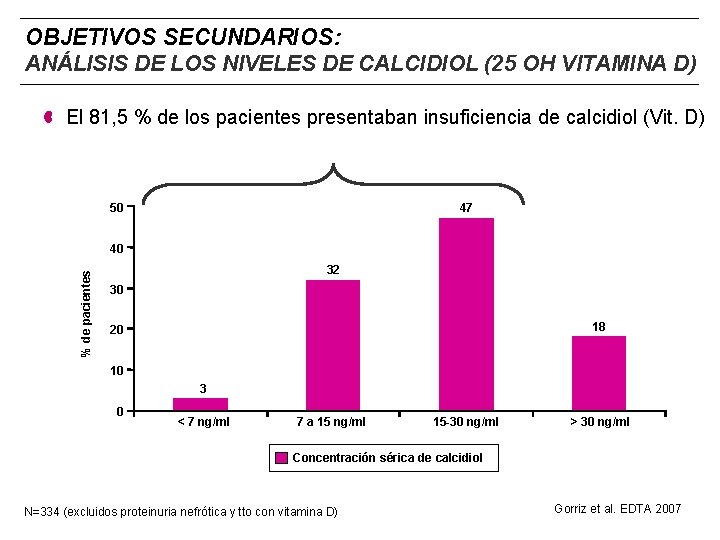
OBJETIVOS SECUNDARIOS: ANÁLISIS DE LOS NIVELES DE CALCIDIOL (25 OH VITAMINA D) El 81, 5 % de los pacientes presentaban insuficiencia de calcidiol (Vit. D) 50 47 % de pacientes 40 32 30 18 20 10 3 0 < 7 ng/ml 7 a 15 ng/ml 15 -30 ng/ml > 30 ng/ml Concentración sérica de calcidiol N=334 (excluidos proteinuria nefrótica y tto con vitamina D) Gorriz et al. EDTA 2007

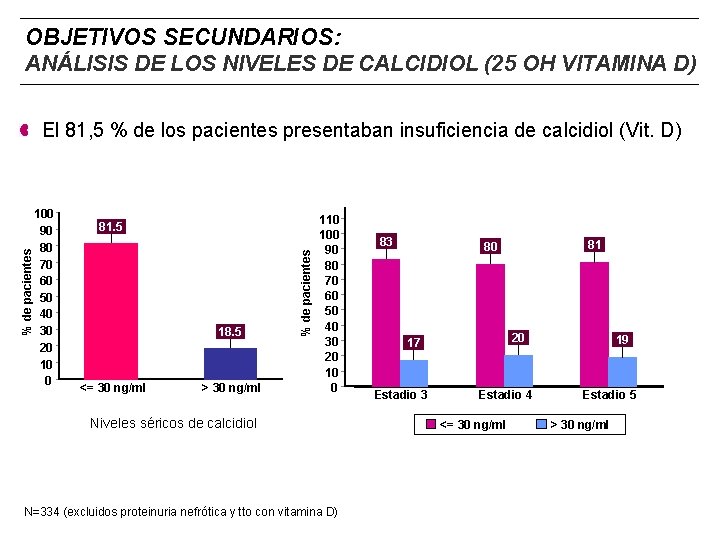
OBJETIVOS SECUNDARIOS: ANÁLISIS DE LOS NIVELES DE CALCIDIOL (25 OH VITAMINA D) 100 90 80 70 60 50 40 30 20 10 0 81. 5 18. 5 <= 30 ng/ml > 30 ng/ml % de pacientes El 81, 5 % de los pacientes presentaban insuficiencia de calcidiol (Vit. D) 110 100 90 80 70 60 50 40 30 20 10 0 Niveles séricos de calcidiol N=334 (excluidos proteinuria nefrótica y tto con vitamina D) 83 81 80 20 17 Estadio 3 Estadio 4 <= 30 ng/ml 19 Estadio 5 > 30 ng/ml

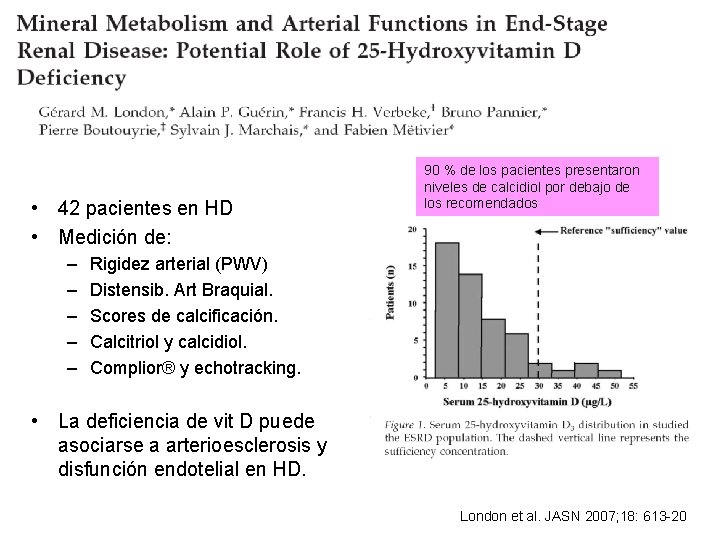
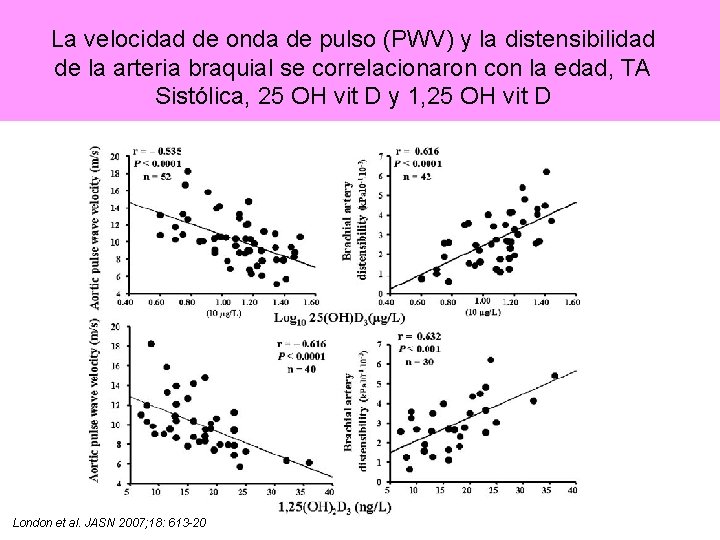
• 42 pacientes en HD • Medición de: – – – 90 % de los pacientes presentaron niveles de calcidiol por debajo de los recomendados Rigidez arterial (PWV) Distensib. Art Braquial. Scores de calcificación. Calcitriol y calcidiol. Complior® y echotracking. • La deficiencia de vit D puede asociarse a arterioesclerosis y disfunción endotelial en HD. London et al. JASN 2007; 18: 613 -20

La velocidad de onda de pulso (PWV) y la distensibilidad de la arteria braquial se correlacionaron con la edad, TA Sistólica, 25 OH vit D y 1, 25 OH vit D London et al. JASN 2007; 18: 613 -20

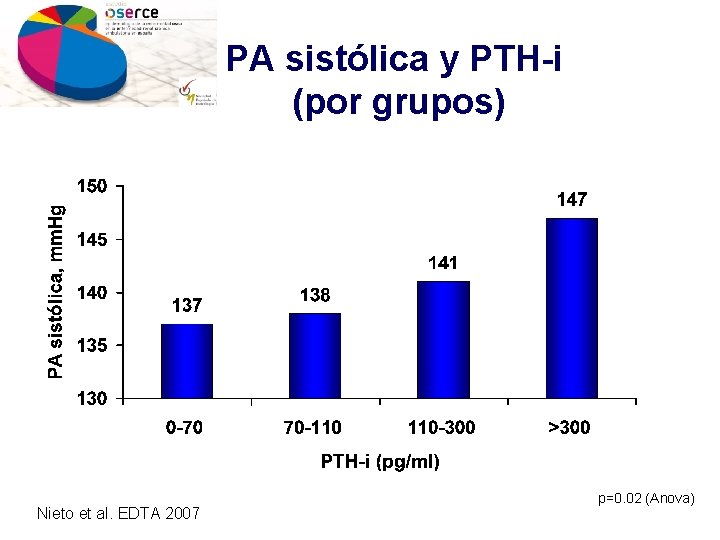
PA sistólica y PTH-i (por grupos) Nieto et al. EDTA 2007 p=0. 02 (Anova)

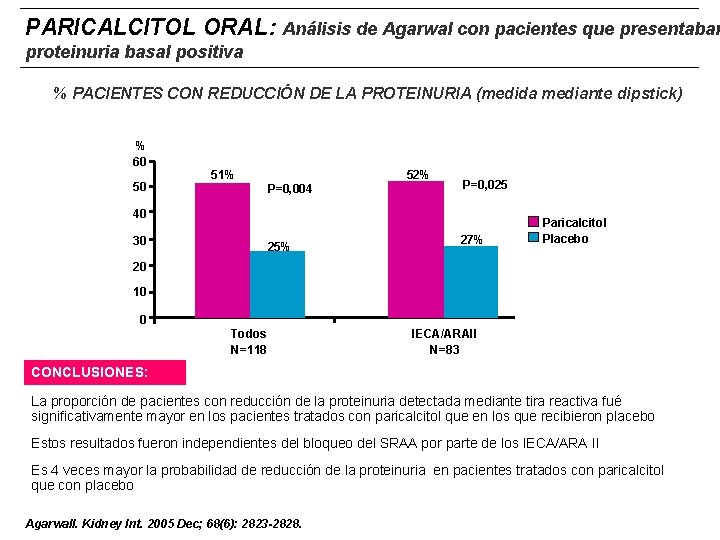
PARICALCITOL ORAL: Análisis de Agarwal con pacientes que presentaban proteinuria basal positiva % PACIENTES CON REDUCCIÓN DE LA PROTEINURIA (medida mediante dipstick) % 60 50 51% P=0, 004 52% P=0, 025 40 30 25% 27% Paricalcitol Placebo 20 10 0 Todos N=118 IECA/ARAII N=83 CONCLUSIONES: La proporción de pacientes con reducción de la proteinuria detectada mediante tira reactiva fué significativamente mayor en los pacientes tratados con paricalcitol que en los que recibieron placebo Estos resultados fueron independientes del bloqueo del SRAA por parte de los IECA/ARA II Es 4 veces mayor la probabilidad de reducción de la proteinuria en pacientes tratados con paricalcitol que con placebo Agarwall. Kidney Int. 2005 Dec; 68(6): 2823 -2828.

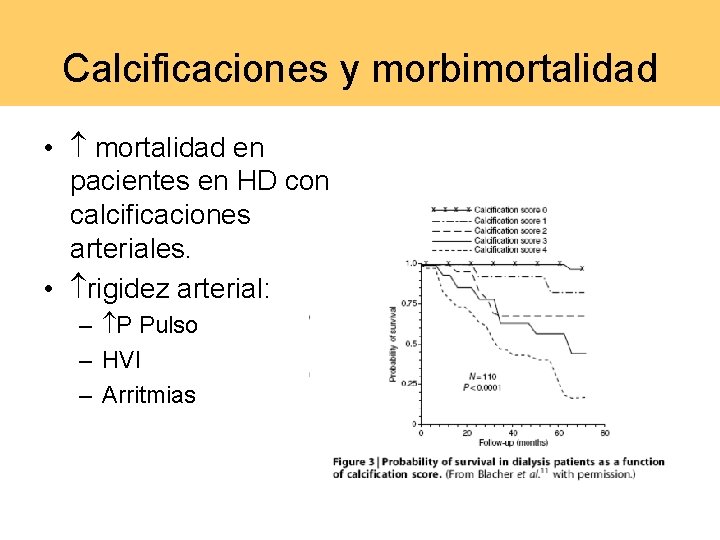
Calcificaciones y morbimortalidad • mortalidad en pacientes en HD con calcificaciones arteriales. • rigidez arterial: – P Pulso – HVI – Arritmias

Calcificaciones y morbimortalidad • Las calcificaciones ya se detectan en estadios precoces de la ERC -estadios 3 -4 - (Kramer H. JASN 2005; 16: 507 -13). • Activacion de VDRs con vitamina D inhiben las proteinas necesarias para la calcificación. • Exceso de calcio y calcitriol pueden producir calcificacion. • Potenciales inductores de calcificación: – – – – Fosforo PTH Uremia BMP-2 IL 1, IL 6 TGF Estrés oxidativo Hipercalcemia (x vit D)

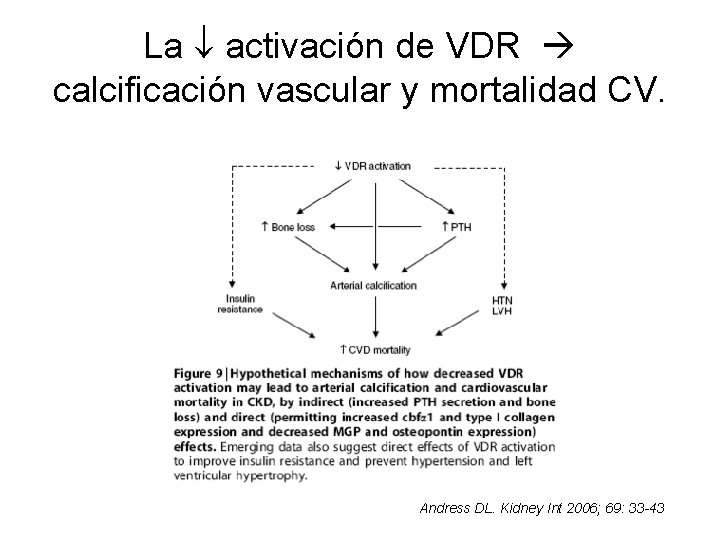
La activación de VDR calcificación vascular y mortalidad CV. Andress DL. Kidney Int 2006; 69: 33 -43

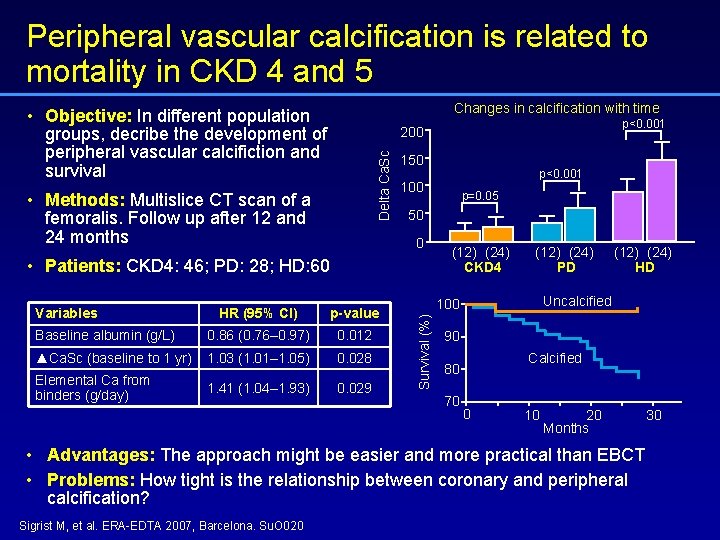
Peripheral vascular calcification is related to mortality in CKD 4 and 5 Changes in calcification with time • Objective: In different population groups, decribe the development of peripheral vascular calcifiction and survival Delta Ca. Sc • Methods: Multislice CT scan of a femoralis. Follow up after 12 and 24 months 150 Baseline albumin (g/L) 0. 86 (0. 76– 0. 97) 0. 012 ▲Ca. Sc (baseline to 1 yr) 1. 03 (1. 01– 1. 05) 0. 028 Elemental Ca from binders (g/day) 1. 41 (1. 04– 1. 93) 0. 029 (12) (24) CKD 4 (12) (24) PD (12) (24) HD Uncalcified 100 Survival (%) p-value p=0. 05 50 0 HR (95% CI) p<0. 001 100 • Patients: CKD 4: 46; PD: 28; HD: 60 Variables p<0. 001 200 90 Calcified 80 70 0 10 20 Months • Advantages: The approach might be easier and more practical than EBCT • Problems: How tight is the relationship between coronary and peripheral calcification? Sigrist M, et al. ERA-EDTA 2007, Barcelona. Su. O 020 30

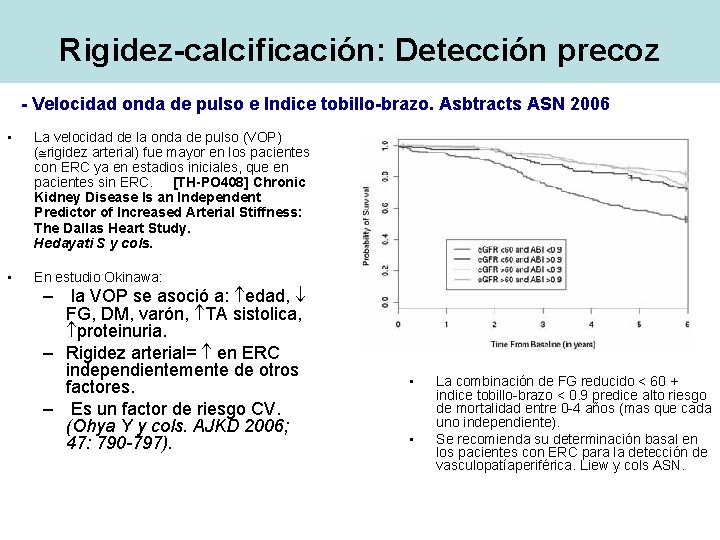
Rigidez-calcificación: Detección precoz - Velocidad onda de pulso e Indice tobillo-brazo. Asbtracts ASN 2006 • La velocidad de la onda de pulso (VOP) ( rigidez arterial) fue mayor en los pacientes con ERC ya en estadios iniciales, que en pacientes sin ERC. [TH-PO 408] Chronic Kidney Disease Is an Independent Predictor of Increased Arterial Stiffness: The Dallas Heart Study. Hedayati S y cols. • En estudio Okinawa: – la VOP se asoció a: edad, FG, DM, varón, TA sistolica, proteinuria. – Rigidez arterial= en ERC independientemente de otros factores. – Es un factor de riesgo CV. (Ohya Y y cols. AJKD 2006; 47: 790 -797). • • La combinación de FG reducido < 60 + indice tobillo-brazo < 0. 9 predice alto riesgo de mortalidad entre 0 -4 años (mas que cada uno independiente). Se recomienda su determinación basal en los pacientes con ERC para la detección de vasculopatíaperiférica. Liew y cols ASN. • Hedayati S y cols. , Ohya Y y cols. AJKD 2006; 47: 790 -797. Liew y cols ASN.

Fósforo y progresión renal

Fósforo y progresión renal • Asociación directa entre fosfatemia, deterioro renal y cambios morfológicos en modelo de rata (Neves KR et al Kidney Int 2004; 66: 2237 -2244). • Datos clínicos: • • 448 ptes estadio 4 (< 20 ml/min/1. 73 m 2). Media: 7 determinaciones /año Por cada mg/dl la tasa de deterioro renal se incrementó en 0. 154 ml/min/mes (IC: 0. 071 -0. 237) Voormolen NDT 2007

Patogenia (en modelos animales) • Hipótesis precipitación-calcificación: – En animales con dieta fosforo depósito de cristales de fosfato cálcico en mitocondria de cels tubulares daño tubulo intersticial (Khan SR. Clin Exp Nephrol 2004; 8: 75 -88). – Tras administrar quelantes del P • depósitos de fosfato calcico • fibrosis intersticial • deterioro renal (Koizumi T Biochem Biophys Res Commun 2002; 295: 917 -921). Voormolen NDT 2007

Patogenia (en humanos) • Incapacidad de adaptación a los altos niveles de fosfato Deterioro renal (Ketteler M NDT 2005; 20: 673 -677). • Asociación entre fosforo y mortalidad CV (por morbilidad CV). • Pacientes con hiperfosforemia calcificaciones arteriales (Goodman AJKD 2004; 43: 572 -9): – Defecto in gen klotho y FGF 23 (fibroblast growth factor 23). – En ratones con defecto en gen klotho: • Dieta fosforo calcificación vascular pacientes en dialisis. • Dieta sin fósforo: el defecto del gen klotho se normaliza – FGF 23: importante determinante en la reabsorción de P por el riñón. Voormolen NDT 2007

Actitudes en alt MMO • Normalización de niveles de vitamina D (vitamina D natural). • Ergocalciferol muestra un benefiio en los niveles de PTH si el tto consigue normalizar los niveles de calicidiol, siendo mas evidente en estadio 3. Am J Kidney Dis 2007; 50: 59 -68. • Ergocalciferol muestra un beneficio en los niveles de PTH si el tto consigue normalizar los niveles de calcidiol, siendo mas evidente en estadio 3. Causa absorción P (menos con paricalcitol). • Limitar la ingesta de calcio (< 2 g/dia) (< 1500 mg de calcio elemento) (prevenir calcificaciones).

Prevención cardiovascular y alteraciones metabolismo mineral-oseo Recomendaciones prácticas • Carbonato cálcico (0, 5 -1, 5 g/dia) (↑Ca, PTH). • Medir 25 OH D 3 (déficit < 30 pg/ml). – Corregir deficit si está presente. • Si PTH↑ ( y Ca-P =): – – Análogos vit D (calcitriol, 1, 25 g/d o -calcidol). Activ selectivos Vit D: paricalcitol Riesgo de hipercalcemia (dosis > 1, 25 g/d de calcitriol) Contraindicación calcitriol: • Si hipercalcemia o hiperfosforemia. – Monitorización periódica.

Conclusiones • La ERC precisa un abordaje multidisciplinario por la interacción de la mayoria de sus complicaciones (anemia, alt MMO, enf cardiovascular) • La anemia es un factor de riesgo independiente para la aparición de acontecimientos cardiovasculares, y probablemente para la progresion de la ERC. Estudios retrospectivos muestran que el tratamiento precoz de la anemia reduce el riesgo CV. Estos datos deberán ser confirmados en estudios randomizados • El nivel objetivo de Hb debe ser clarificado no existiendo datos contundentes que nos indican un nivel objetivo determinado.

Conclusiones • Dado el importante numero de pacientes con ERC y enf CV y su posible relación con las alt MMO, es importante la monitorización de los niveles de vitamina D, Ca, P y PTH así como su corrección. • En los pacientes con ERC , la hiperfosforemia no es solo un factor de riesgo de mortalidad sino que tambien actua como factor de progresión renal importancia de mantener P en rango normal. • Se necesitan estudios prospectivos para conocer exactamente su peso pronóstico de todos estos factores en la morbimortalidad CV.

Desde un abordaje multidisciplinar y conjunto, los nefrólog@s podemos reducir claramente la morbimortalidad de los pacientes con ERC