Dpto Ingeniera Qumica TEMA 4 Clculo del equilibrio
Dpto. Ingeniería Química TEMA 4 Cálculo del equilibrio líquido-vapor. Diagramas de equilibrio OBJETIVOS • Conocer las fuentes bibliográficas de datos de equilibrio líquido-vapor • Conocer y entender los distintos diagramas de equilibrio • Conocer los tipos de cálculo implicados en la resolución de problemas de equilibrio líquido-vapor, correlación de datos y predicción. 1

TEMA 4: EQUILIBRIO LÍQUIDO VAPOR - "Ingeniería Química 5. Transferencia de materia. 1ª p. ". E. Costa Novella. Vol. 5, Ed. Alhambra Universidad. 1988. - "Separation Processes". C. J. King. Ed. Mc. Graw Hill, Chemical Engineering Series, 2ª ed. Nueva York, 1988. - "Operaciones de Separación por etapas de equilibrio en Ingeniería Química". E. J. Henley y J. D. Seader. Ed. Reverté, Barcelona, 1998 -2000. - "Chemical Engineering. II. V. Unit Operations". J. M. Coulson y J. F. Richardson. Ed. Reverté, Barcelona, 1979 -1981. - “Termodinámica Molecular de los Equilibrios entre Fases”. Prausnitz, Lichtenthaler y Gomes de Azevedo, (2000). -“Introducción a la Termodinámica en Ingeniería Química”. Smith, Van Ness y Abbott, (1997). - “Phase Equilibrium in Process Design”. Null, Harold R. Ed. Wiley Interscience, 1970. - “Multicomponent Distillation”. Holland, C. D. , Prentice Hall. Englewood Cliff. Nueva Jersey, 1963. - “Distillation”. Van Winkle, Ed. Mc. Graw Hill, Nueva York, 1968. -“Calcul sur Ordinateur des Equilibres Liquide-Vapeur et Liquide-Liquide”. Renon, H. , Asselineau, L. , Cohen, G. y Rimbault, Technip, Paris, 1971. - "Introducción a las operaciones de separación. Cálculo por etapas de equilibrio" A. Marcilla, Publicaciones de la Universidad de Alicante, 1998. (Edición digital: http: //publicaciones. ua. es) Programas comerciales CHEMCAD HYSYS ASPEN PLUS. . . 2

TEMA 4: EQUILIBRIO LÍQUIDO VAPOR REGLA DE LAS FASES L=C+2 -F Ley de equilibrio: f(xi, yi, T, P)=0 Mezclas binarias: (C=2, F=2) L=2 Tipos de diagramas composición vs. temperatura composición vs. presión vs. temperatura composición del vapor vs. composición del líquido 3
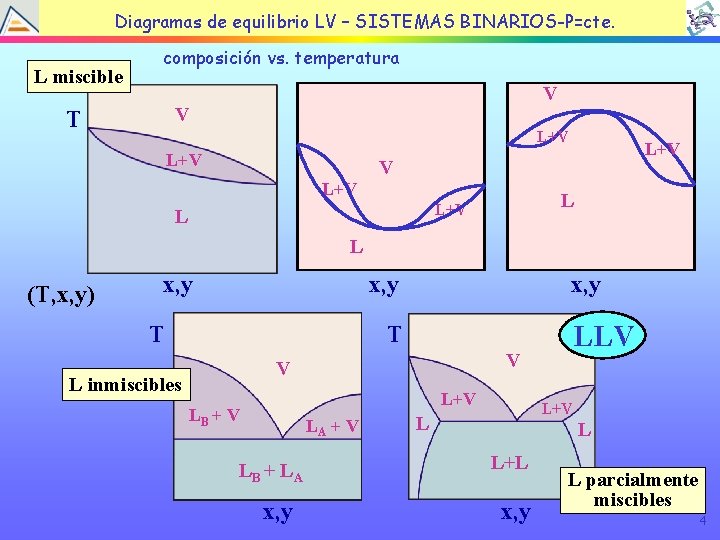
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS L miscible composición vs. temperatura V V T L+V L+V L L (T, x, y) x, y T x, y LLV T V V L inmiscibles L+V LB + V LA + V LB + L A x, y L+V L L L+L x, y L parcialmente miscibles 4
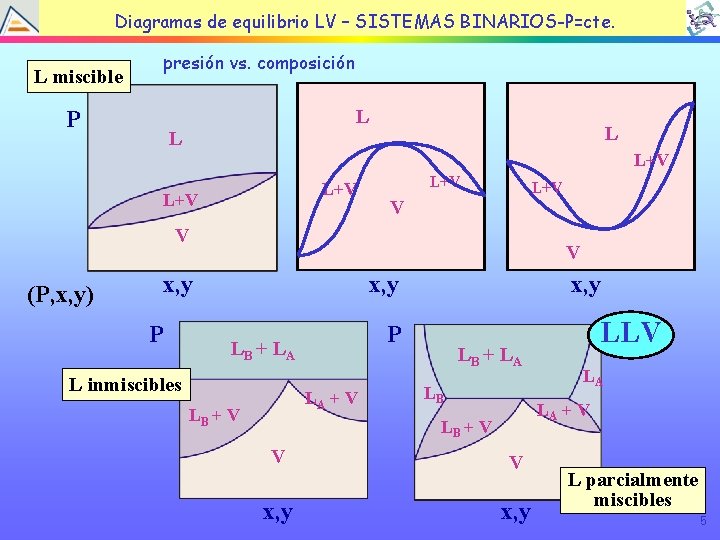
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS L miscible presión vs. composición L P L L L+V L+V L+V V x, y (P, x, y) P x, y P LB + L A L inmiscibles LA + V LB + V x, y LB + L A LB x, y LA LA + V LB + V V LLV V x, y L parcialmente miscibles 5
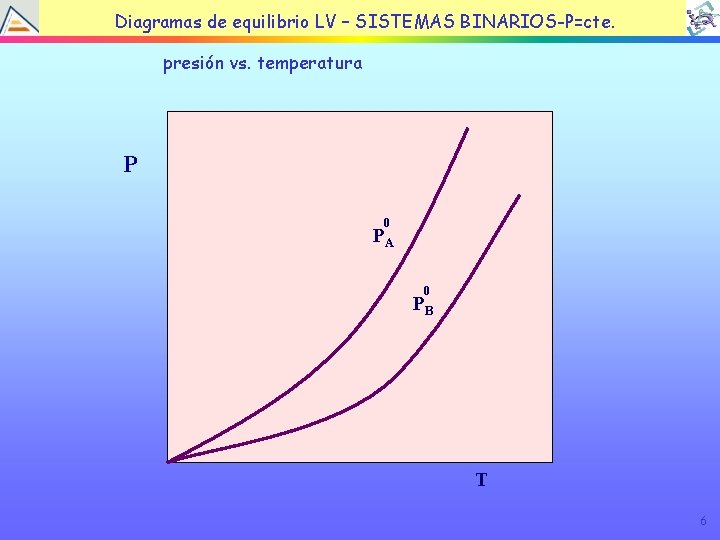
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS presión vs. temperatura P 0 PA 0 PB T 6
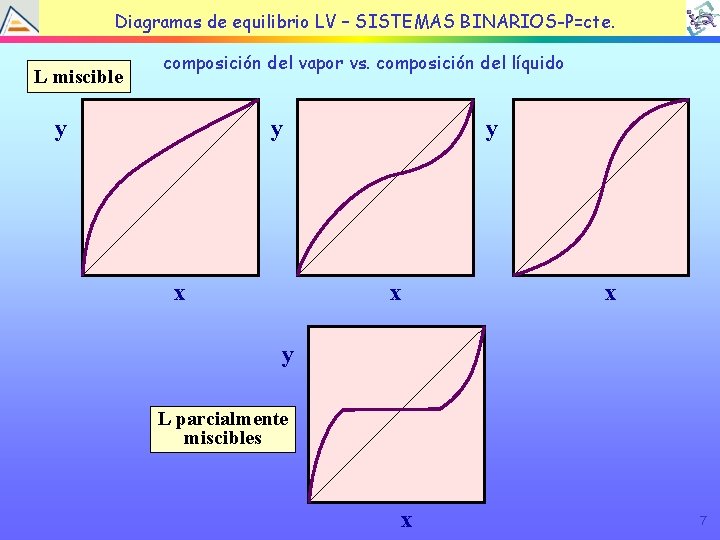
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS L miscible composición del vapor vs. composición del líquido y y x x y L parcialmente miscibles x 7
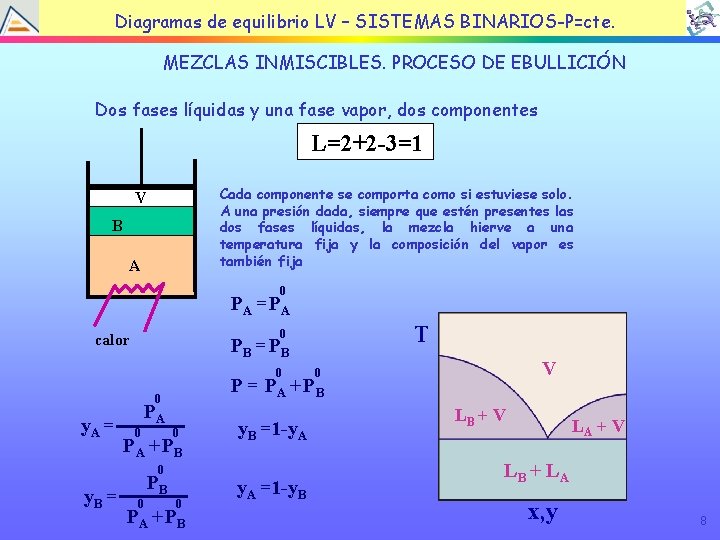
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS MEZCLAS INMISCIBLES. PROCESO DE EBULLICIÓN Dos fases líquidas y una fase vapor, dos componentes L=2+2 -3=1 Cada componente se comporta como si estuviese solo. A una presión dada, siempre que estén presentes las dos fases líquidas, la mezcla hierve a una temperatura fija y la composición del vapor es también fija V B A 0 PA = PA PB = PB 0 PA 0 0 PA + PB 0 y. B = PB 0 V 0 P = PA + PB 0 y. A = T 0 calor 0 PA + PB y. B =1 -y. A =1 -y. B LB + V LA + V LB + L A x, y 8
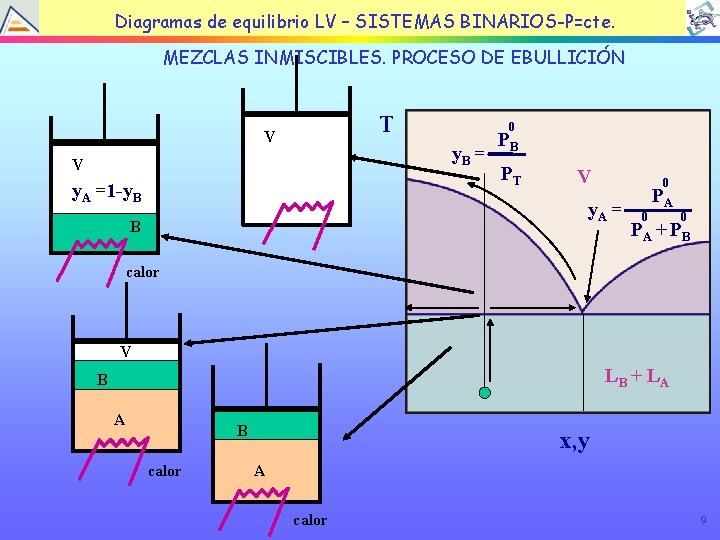
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS MEZCLAS INMISCIBLES. PROCESO DE EBULLICIÓN T V 0 y. B = V y. A =1 -y. B PB PT V 0 y. A = B PA 0 0 PA + PB calor V LB + L A B calor x, y A calor 9
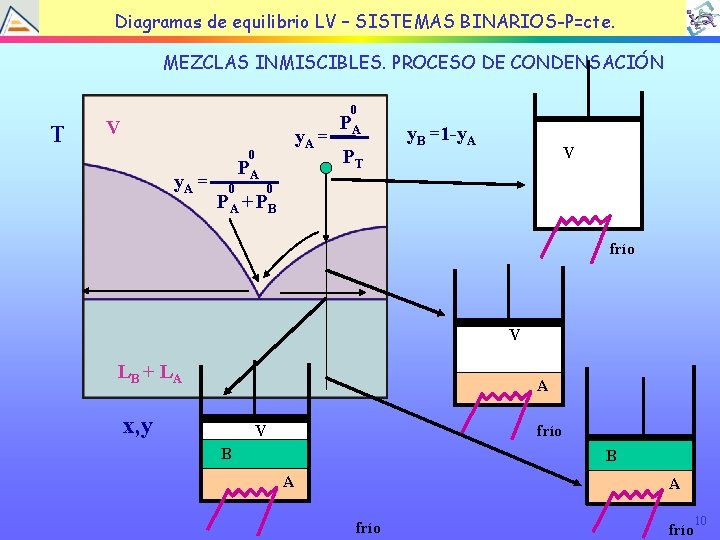
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS MEZCLAS INMISCIBLES. PROCESO DE CONDENSACIÓN T 0 V y. A = 0 y. A = PA 0 PA PT y. B =1 -y. A V 0 PA + PB frío V LB + L A A x, y V frío B B A A frío 10
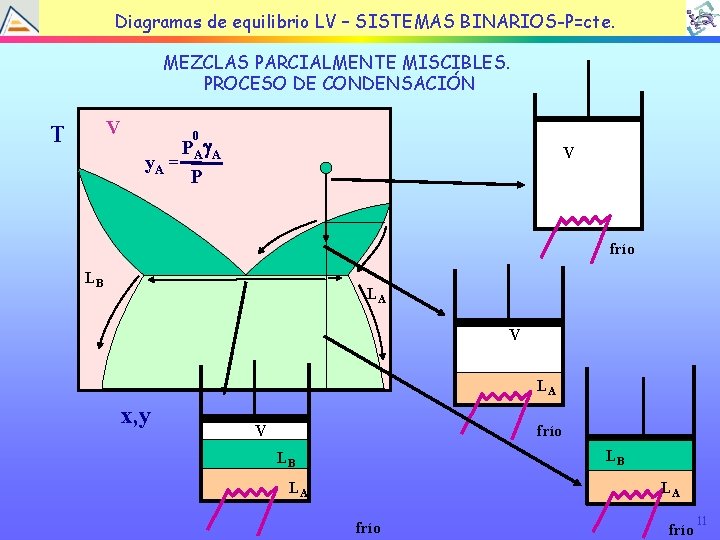
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS MEZCLAS PARCIALMENTE MISCIBLES. PROCESO DE CONDENSACIÓN V T 0 PAg. A y. A = P V frío LB LA V LA x, y V frío LB LB LA LA frío 11
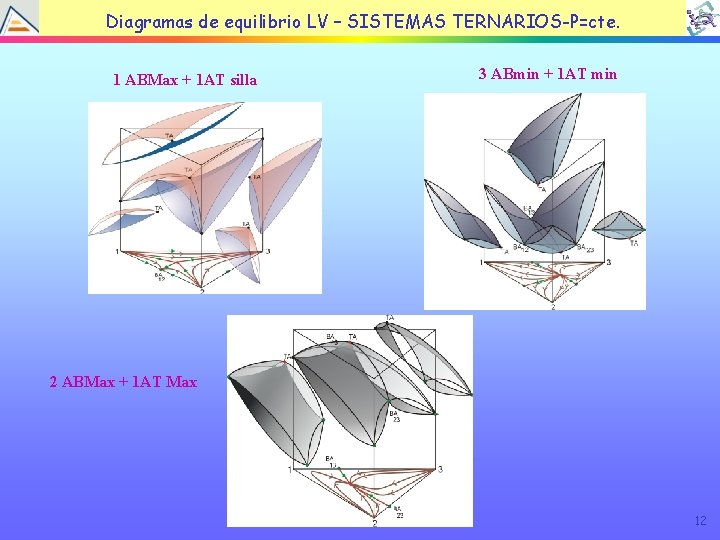
Diagramas de equilibrio LV – SISTEMAS TERNARIOS-P=cte. 1 ABMax + 1 AT silla 3 ABmin + 1 AT min 2 ABMax + 1 AT Max 12
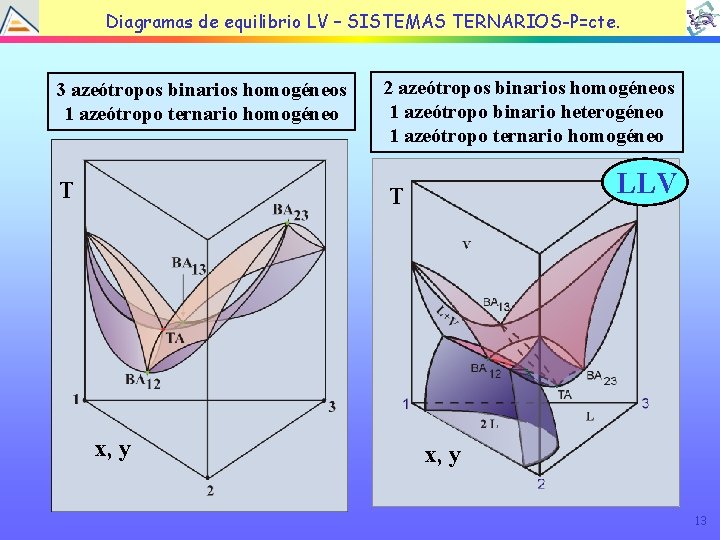
Diagramas de equilibrio LV – SISTEMAS TERNARIOS-P=cte. 3 azeótropos binarios homogéneos 1 azeótropo ternario homogéneo 2 azeótropos binarios homogéneos 1 azeótropo binario heterogéneo 1 azeótropo ternario homogéneo T T x, y LLV x, y 13
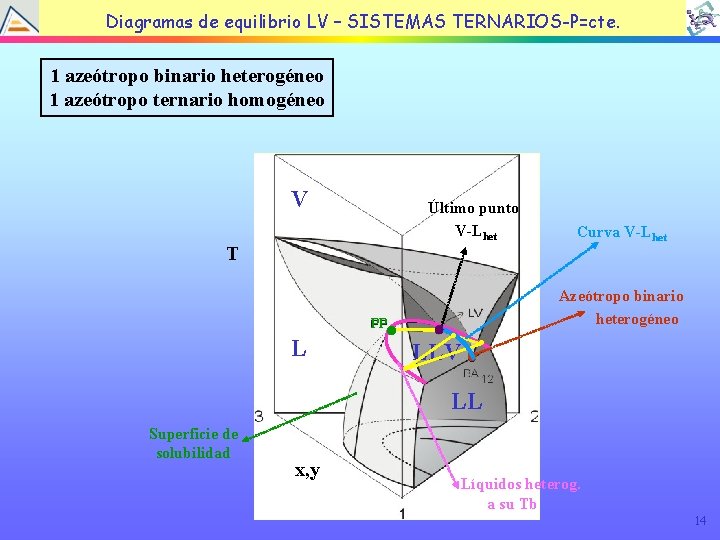
Diagramas de equilibrio LV – SISTEMAS TERNARIOS-P=cte. 1 azeótropo binario heterogéneo 1 azeótropo ternario homogéneo V Último punto V-Lhet T PP L . . . LLV Curva V-Lhet Azeótropo binario heterogéneo LL Superficie de solubilidad x, y Líquidos heterog. a su Tb 14
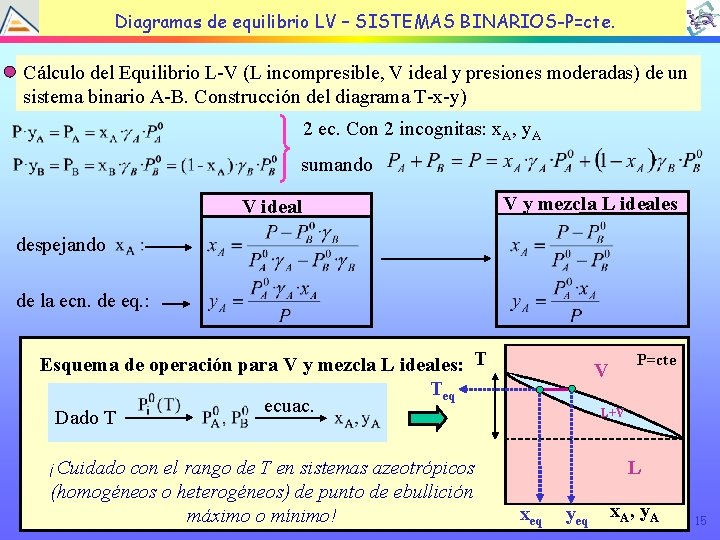
TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS Cálculo del Equilibrio L-V (L incompresible, V ideal y presiones moderadas) de un sistema binario A-B. Construcción del diagrama T-x-y) 2 ec. Con 2 incognitas: x. A, y. A sumando V ideal V y mezcla L ideales despejando de la ecn. de eq. : Esquema de operación para V y mezcla L ideales: T Teq ecuac. Dado T ¡Cuidado con el rango de T en sistemas azeotrópicos (homogéneos o heterogéneos) de punto de ebullición máximo o mínimo! P=cte V L+V L xeq yeq x. A, y. A 15
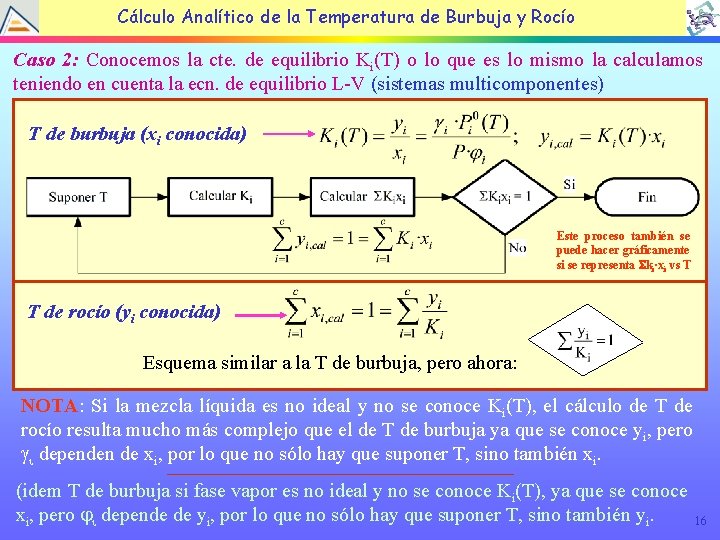
Cálculo Analítico de la Temperatura de Burbuja y Rocío Caso 2: Conocemos la cte. de equilibrio Ki(T) o lo que es lo mismo la calculamos teniendo en cuenta la ecn. de equilibrio L-V (sistemas multicomponentes) T de burbuja (xi conocida) Este proceso también se puede hacer gráficamente si se representa Ski·xi vs T T de rocío (yi conocida) Esquema similar a la T de burbuja, pero ahora: NOTA: Si la mezcla líquida es no ideal y no se conoce Ki(T), el cálculo de T de rocío resulta mucho más complejo que el de T de burbuja ya que se conoce yi, pero gi dependen de xi, por lo que no sólo hay que suponer T, sino también xi. (idem T de burbuja si fase vapor es no ideal y no se conoce Ki(T), ya que se conoce xi, pero i depende de yi, por lo que no sólo hay que suponer T, sino también yi. 16
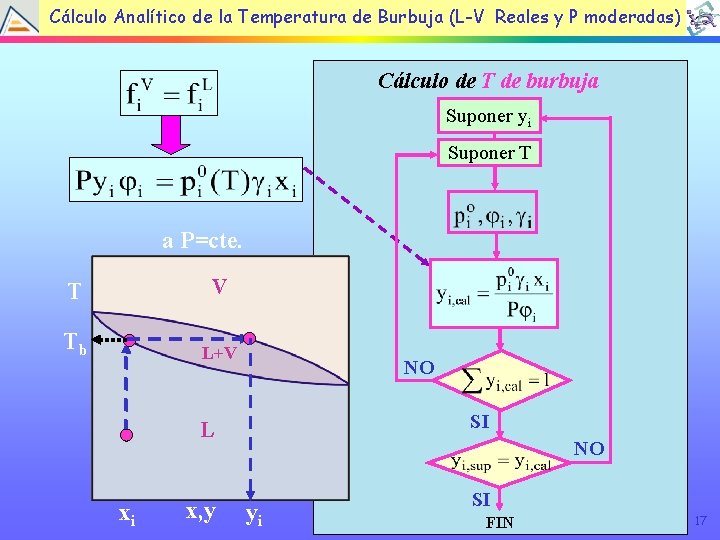
Cálculo Analítico de la Temperatura de Burbuja (L-V Reales y P moderadas) Cálculo de T de burbuja Suponer yi Suponer T a P=cte. T V Tb L+V NO SI L xi x, y NO yi SI FIN 17
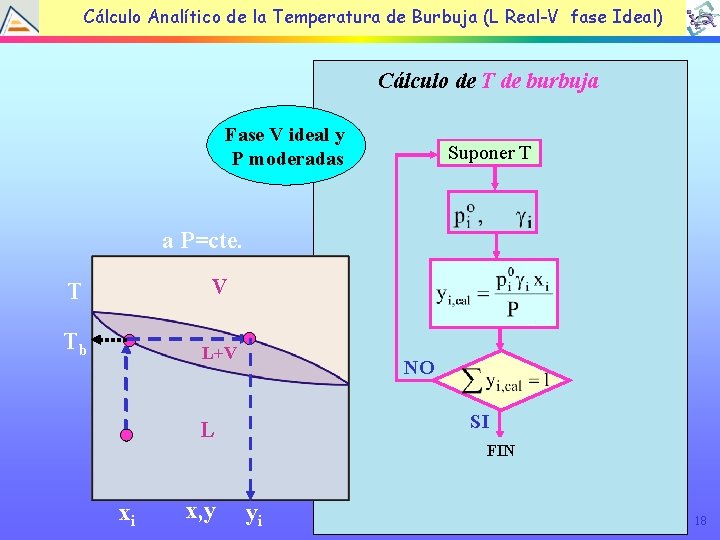
Cálculo Analítico de la Temperatura de Burbuja (L Real-V fase Ideal) Cálculo de T de burbuja Suponer yi Fase V ideal y P moderadas Suponer T a P=cte. T V Tb L+V NO SI L FIN xi x, y yi NO SI 18
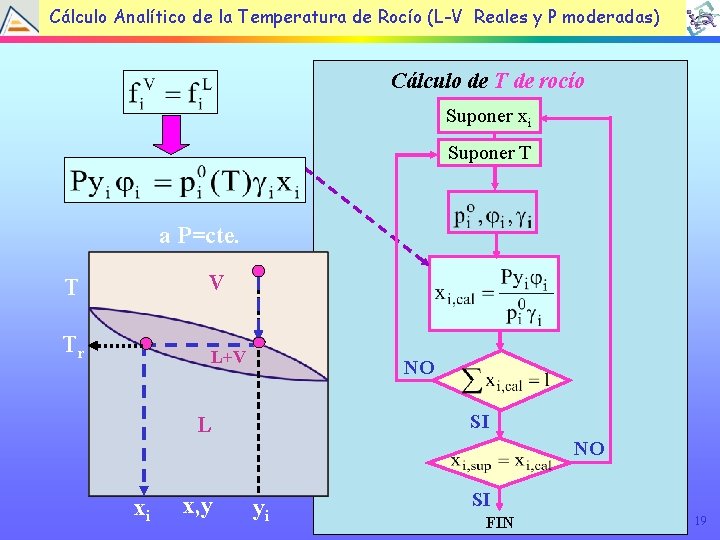
Cálculo Analítico de la Temperatura de Rocío (L-V Reales y P moderadas) Cálculo de T de rocío Suponer xi Suponer T a P=cte. T V Tr L+V NO SI L xi x, y NO yi SI FIN 19

TEMA EQUILIBRIO LÍQUIDOBINARIOS-P=cte. VAPOR Diagramas de 4: equilibrio LV – SISTEMAS Concepto de VOLATILIDAD Volatilidad absoluta de A ( A): cociente entre la presión parcial del componente A en la fase gas y su fracción molar en la fase líquida. la volatilidad de A coincide con su presión de vapor a T Si A comp. puro o mezcla liq. ideal Volatilidad relativa de A respecto a B ( AB): cociente entre las volatilidades absolutas de A y B. Si mezcla L ideal Influencia de la volatilidad sobre el equilibrio: aplicamos la ecuación de equilibrio a cada uno de los componentes de una mezcla binaria y luego dividimos y sustituimos la definición de volatilidad relativa. Separable por destilación si si si aprox. 1 Separación difícil Separación imposible por destilación simple (azeótropos) 20

Relaciones Termodinámicas del Equilibrio entre 2 Fases Cálculo del equilibrio con ayuda de la volatilidad relativa (sistemas binarios): dando valores a xi se obtiene yi Si derivamos respecto x. A: b’ Si x. A= 0 y. A Si x. A= 1 b en muchas ocasiones la variación de la volatilidad relativa con T y composición es pequeña por lo que puede utilizarse una volatilidad x. A relativa media en todo el diagrama ( m. AB) Además, la simetría de la curva de equilibrio indica: -Constancia en el valor de la volatilidad relativa media. -Idealidad del vapor. 21

Relaciones Termodinámicas del Equilibrio entre 2 Fases CÁLCULO ANALÍTICO de la T de BURBUJA y de ROCÍO Caso 1: Conocemos la volatilidad relativa media (Mezcla binaria; fase V ideal) Datos: a. AB, P, x. A (si Tburbuja) o y. A(si Trocío), función T de burbuja (conocida x. A se despeja y. A y se opera) T burbuja T de rocío (conocida y. A se despeja x. A y se opera) T rocío 22

Relaciones Termodinámicas del Equilibrio entre 2 Fases Cálculo del equilibrio con ayuda de la volatilidad relativa media (sistemas multicomponentes): 23
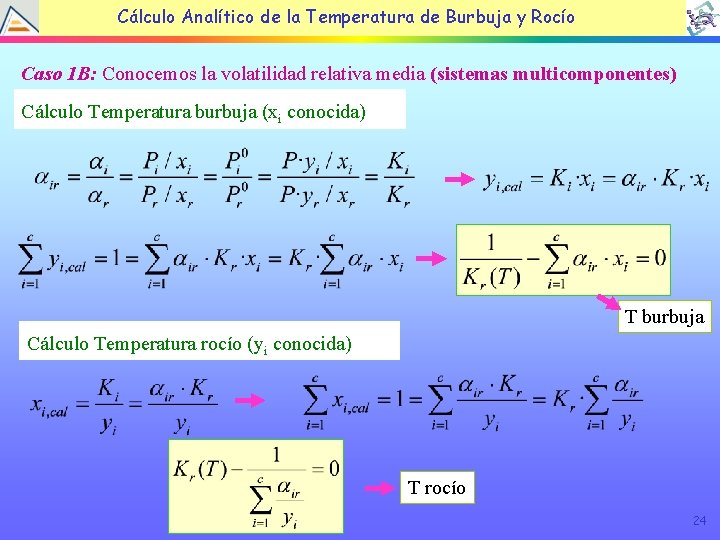
Cálculo Analítico de la Temperatura de Burbuja y Rocío Caso 1 B: Conocemos la volatilidad relativa media (sistemas multicomponentes) Cálculo Temperatura burbuja (xi conocida) T burbuja Cálculo Temperatura rocío (yi conocida) T rocío 24

Condiciones termodinámicas del equilibrio EQUILIBRIO LÍQUIDO-VAPOR ENTALPÍA LIBRE DE MEZCLA DEL LÍQUIDO EN FUNCIÓN DE LA COMPOSICIÓN. Por definición: Si tomamos como referencia el líquido, y restamos a GML/RT, podemos escribir
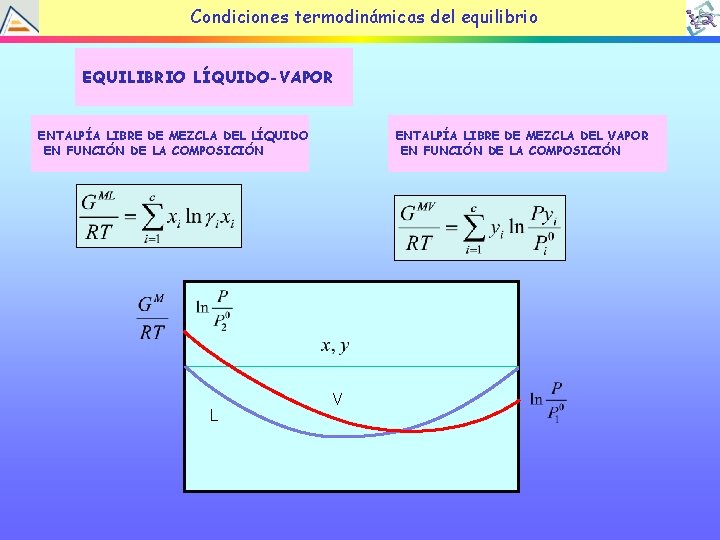
Condiciones termodinámicas del equilibrio EQUILIBRIO LÍQUIDO-VAPOR ENTALPÍA LIBRE DE MEZCLA DEL LÍQUIDO EN FUNCIÓN DE LA COMPOSICIÓN L ENTALPÍA LIBRE DE MEZCLA DEL VAPOR EN FUNCIÓN DE LA COMPOSICIÓN V
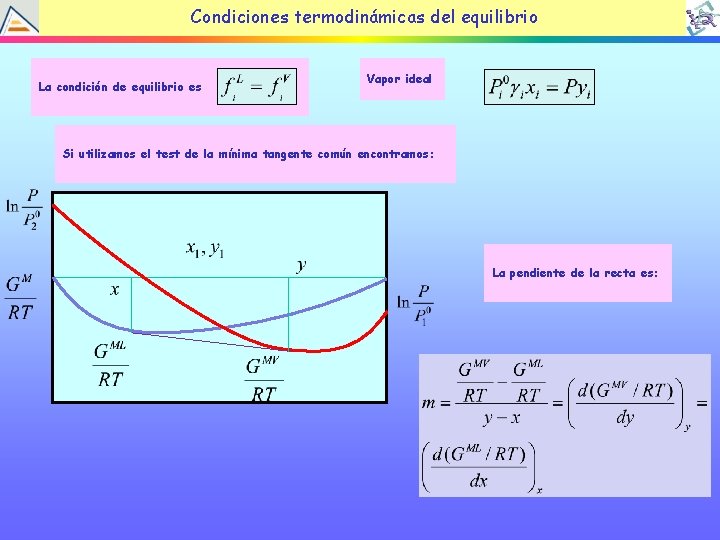
Condiciones termodinámicas del equilibrio La condición de equilibrio es Vapor ideal Si utilizamos el test de la mínima tangente común encontramos: La pendiente de la recta es:
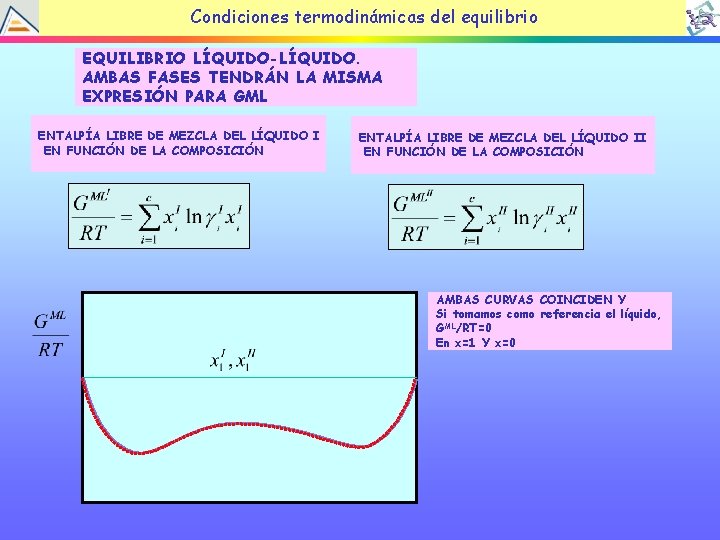
Condiciones termodinámicas del equilibrio EQUILIBRIO LÍQUIDO-LÍQUIDO. AMBAS FASES TENDRÁN LA MISMA EXPRESIÓN PARA GML ENTALPÍA LIBRE DE MEZCLA DEL LÍQUIDO I EN FUNCIÓN DE LA COMPOSICIÓN ENTALPÍA LIBRE DE MEZCLA DEL LÍQUIDO II EN FUNCIÓN DE LA COMPOSICIÓN AMBAS CURVAS COINCIDEN Y Si tomamos como referencia el líquido, GML/RT=0 En x=1 Y x=0
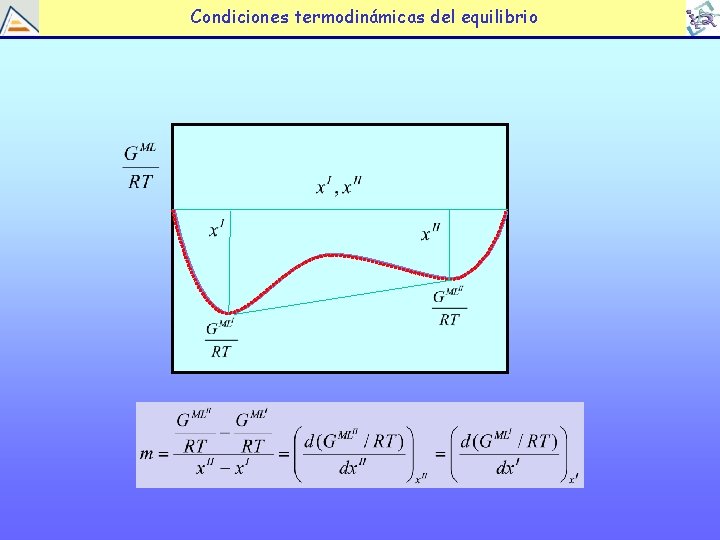
Condiciones termodinámicas del equilibrio
- Slides: 29