Dorudan gen aktarm teknikleri ile bitkilere gen aktarm

Doğrudan gen aktarım teknikleri ile bitkilere gen aktarımı Sebahattin ÖZCAN l a. Biyolistik (Partikül Tabancası) l b. Mikroenjeksiyon l c. Protoplastlara Gen Aktarımı i. Kimyasal Yöntemler l ii. Elektroparosyon l

Biyolistik (Partikül Tabancası) l Bu yöntemin esası, yüksek derecede hızlandırılmış mikro-taşıyıcı adı verilen 1 -2 m çapındaki metal (çoğunlukla altın ya da tungsten) partiküller aracılığıyla, bir ateşleme mekanizmasından yararlanılarak DNA’nın hedef dokulara aktarılmasıdır

Biyolistik (Partikül Tabancası) Mikro-taşıyıcılar makro-taşıyıcı olarak adlandırılan plastik bir silindir üzerinden hedef dokulara doğru bir helyum gazı basncı ile hızlandırılır. l Ateşleme gerek mikro-taşıyıcıların sürtünmesinden doğan sürüklenmeyi, gerekse yüksek basınçlı gaz şokundan doğabilecek hücre parçalanmasını ve sesi engellemek için vakum altında yapılır. l

Biyolistik yönteminde gen aktarım frekansını etkileyen faktörler l l Partikül hızlandırmada kullanılan helyum gazının basıncı: Gaz hızlandırma tüpündeki helyum basıncı, mikro-partiküllerin hızının belirlenmesinde etkilidir. Partikülü hızlandırmak amacıyla, kullanılan dokunun özelliğine bağlı olarak 450 ile 2200 psi basınç uygulanır. Ancak, çoğu hücre tipi için optimal basınç 1000 psi olarak belirlenmiştir. Bu değerden daha yüksek basınçlarda hücrelerde yaralanma düzeyi artar ve gen aktarım frekansı düşer. Mikro-taşıyıcının boyutu, tipi ve sayısı: Tungsten partiküllerin ortalama çapları 0. 5 -2. 0 m olup, optimum boyut hedef hücrelerin çapı ile ilişkilidir. Ancak 1. 0 m çaplı partiküllerin, başarılı geçici ve stabil transformasyonlar için uygun olduğu saptanmıştır. Tungsten partiküllerinin kullanımının dezavantajları; düzensiz şekil ve boyutta olmaları, belli hücre tipleri için toksik etki göstermeleri ve DNA çökelmesi ile sonuçlanabilecek yüzey oksidasyonuna neden olmalarıdır. Uniform boyutta olan (1 -3 m) altın partikülleri ise tungstenden daha pahalı olmalarına karşın daha az toksik etkiye sahiplerdir.

Biyolistik yönteminde gen aktarım frekansını etkileyen faktörler l l Makro-taşıyıcı ile hedef doku arasındaki uzaklık: Maksimum etkinlikte transformasyon elde etmek için makro-taşıyıcı ile hedef doku arasındaki uzaklık (uçuş mesafesi) önemli bir parametredir. Her hücre tipi için bu mesafenin deneme yoluyla belirlenmesi gerekmekle birlikte, pek çok örnekte 10 mm’lik uçuş mesafesi kullanılarak yüksek transformasyon frekansı elde edilmiştir. DNA’nın mikro-taşıyıcı partiküllere yapışması için kullanılan spermidin ve Ca. Cl 2’ün konsantrasyonu.

Biyolistik yönteminin başlıca üstünlükleri l l l Kullanım kolaylığı, Her ateşlemede mikro-taşıyıcıların birden fazla hücreye ulaşabilmesi, Mikro-taşıyıcılara bağlı genlerin biyolojik aktivitelerinin bozulmaması, Polen, hücre kültürleri, bitki organları, meristemler, kallus, olgunlaşmamış embriyo, olgun embriyo parçaları, yaprak parçaları, mikrosporlar gibi çeşitli hedef dokulara uygulanabilmesi, Mikro-taşıyıcıların derin hücre katmanlarına ulaşabilmesidir.
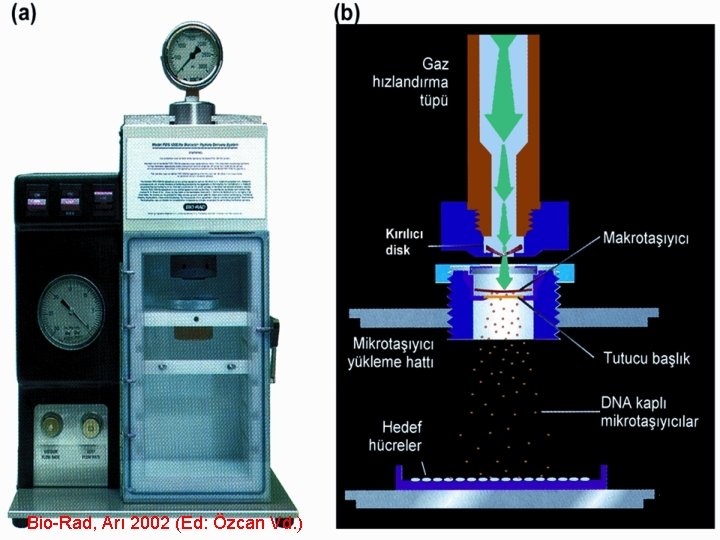
Bio-Rad, Arı 2002 (Ed: Özcan Vd. )

Ye vd. 1997, Arı 2002 (Ed: Özcan Vd. )

Mikroenjeksiyon l l Doğrudan gen aktarımı yöntemleri arasında en kesin biçimde hücrenin istenilen bölmesine DNA’nın enjekte edilmesini sağlayan mikroenjeksiyon, kapiller mikropipetler yardımıyla ve mikroskop altında gerçekleştirilir. Mikro-enjeksiyonla protoplastlara, izole edilmiş hücrelere, kallus, meristemler, zigotik ve mikrospor türevli proembriyolar gibi çok hücreli dokulara DNA aktarımı mümkündür.

Mikroenjeksiyon Alıcı hücreler veya dokular sodyum alginat, agaroz veya poli-L-lisin ile ya da kapiler sistem kullanılarak sabitlenir. l DNA mikromanipülatör sistemine bağlı kapiler bir mikropipet aracılığı ile doğrudan hücrenin çekirdeğine aktarılır. l

Mikroenjeksiyon yönteminin avantajları l l l Aktarılan DNA’nın miktarı optimize edilebilir. İstenilen hücreye DNA aktarılabilir. İstenilen hücre kısmına DNA aktarımı görsel olarak kontrol edilebilir. Mikrosporlar ya da birkaç hücreli proembriyolar gibi küçük boyutlu hedef dokular kullanılabilir. Zigotik embriyo kültürü ve mikro-enjeksiyon yöntemleri birlikte kullanılarak her bitki türüne gen aktarımı yapabilmek mümkün olabilir.
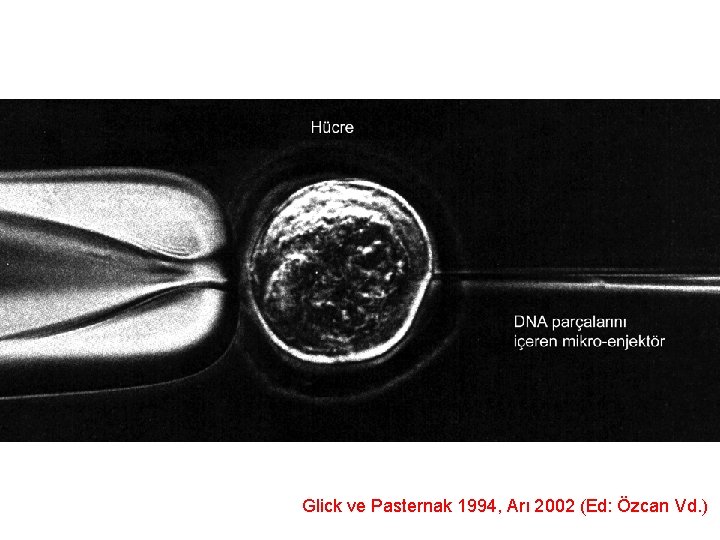
Glick ve Pasternak 1994, Arı 2002 (Ed: Özcan Vd. )

Protoplastlara Gen Aktarımı l l Enzimatik yollarla hücre duvarları uzaklaştırılmış bitki hücreleri, yani protoplastlar hücre süspansiyon kültürü, kallus kültürü ve farklılaşmış bitki dokularından izole edilebilir Kimyasal maddeler yardımıyla veya membran geçirgenliğinin elektrik akımı ile değiştirilmesi (elektroporasyon) sonucunda protoplastlar gen aktarımında kullanılabilmektedir.

Protoplastların ideal eksplant olarak kullanılmalarının nedenleri l l Hücre zarı ile çevrili olduklarından deneysel olarak belirlenmiş konsantrasyonlardaki DNA’yı içlerine almaları kolaydır. Enzimatik veya mekanik yolla yapılan izolasyon işlemleri aynı zamanda hücre yaralanmalarını artırmakta, bu durum hücrelerin rejenerasyon yeteneğini ve entegratif transformasyonu teşvik edebilmektedir. Hücrelerin DNA molekülleri ile teması kolay olduğundan transgenik bitki elde etme şansı fazladır. Gen transferi için biyolojik vektör kullanılmadığından DNA’nın hücre içine alınması fiziksel bir süreçtir ve bu da konukçu sınırı engelini ortadan kaldırmaktadır.

Kimyasal yöntemlerle protoplastlara gen aktarımı l l l Polietilen glikol (PEG), polivinil alkol veya kalsiyum fosfat gibi kimyasal maddelerle protoplastların hücre zarlarının geçirgenlikleri geri dönüşümlü olarak artırılabilir. Genetik transformasyon için protoplastlar, DNA ve kimyasal maddeler ile birlikte inkübe edilir. Bitki türü, kültür koşulları, protoplast kaynağı ve izolasyon için kullanılan yöntemlerin yanısıra, transformasyon için kullanılan tampon ve katyonla, taşıyıcı DNA’nın varlığı ve konsantrasyonu, plazmid ve taşıyıcı DNA formu, hücre döngüsü, PEG gibi gen aktarımına yardımcı kimyasal maddelerin konsantrasyonu kimyasal yöntemlerle protoplastlara gen aktarımını önemli ölçüde etkilemektedir.

Elektroporasyon ile protoplastlara gen aktarımı l l Süspansiyon halindeki protoplastlara yüksek voltajlı elektrik akımı uygulandığında hücre zarının geçirgenliği geri dönüşümlü olarak artar ve mikroporlar oluşur. Elektroporasyon sırasında protoplastların bulunduğu solüsyonda DNA da bulunduğundan membranda açılan porlardan DNA hücre içine girer porlar kapanarak hücrenin bütünlüğü sağlanır.

Elektroporasyon ile protoplastlara gen aktarımı l l l Elektroporasyonda elektrik akımı hücre canlılığına zarar vermeyecek şiddette seçilmelidir. Bu kritik noktanın üzerine çıkıldığında hücre zarları tamamen parçalanabilir, altındaki akım şiddetlerinde ise por oluşumu gerçekleşmeyebilir. Genellikle kullanılan elektroporasyon sistemleri ya düşük voltaj/uzun süreli elektrik akımı (pulse), ya da yüksek voltaj/kısa süreli elektrik akımı şeklindedir. Tütün mezofil hücreleri için tipik değerler düşük voltaj/uzun akım için 300 -400 V/cm ve 10 -50 s, yüksek voltaj/kısa akım için ise 1. 000 -15. 000 V/cm ve 10 s’dir.

Elektroporasyon ile protoplastlara gen aktarımı l Elektroporasyon ile gen aktarım frekansı plazmid konsantrasyonu, elektriksel koşullar, protoplast boyutu ve yoğunluğu ile protoplastların fizyolojik özelliklerine bağlıdır. Düşük voltaj/uzun akım genellikle geçici gen ifadesine, yüksek voltaj/kısa akım ise yüksek düzeyde stabil entegrasyona neden olmaktadır.
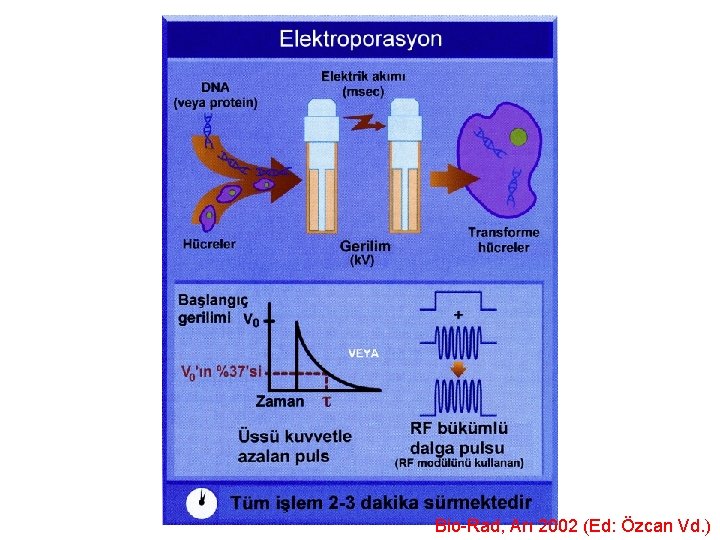
Bio-Rad, Arı 2002 (Ed: Özcan Vd. )

Gen aktarımında karşılaştırılması. yaygın olarak kullanılan yöntemlerin Avantajları Dezavantajları Agrobacterium 1. Yüksek derece etkinlik 2. Uzun DNA dizilerinin aktarılabilmesi 3. Çoğunlukla tek ya da az sayıda T -DNA entegrasyonu 4. Uygulama için özel bir donanıma ihtiyaç olmaması 1. Sınırlı konukçu alanı 2. Genetik bilginin sadece T-DNA aracılığıyla aktarımı • Kimyasal Yöntemler ve Elektroporasyon 1. Basit kullanım 2. Tek denemede birçok örneğe uygulanabilirlik 3. Kimyasal yöntemler için özel bir donanıma ihtiyaç duyulmaması 1. Aktarılan DNA’da yüksek derecede yeni düzenlemeler görülmesi ve çok sayıda kopyanın entegrasyonu 2. Kimyasal yöntemlerde transgenik bitki üretimi için protoplast kültürü ve rejenerasyon sistemlerinin kurulması 3. Somoklonal varyasyonda artış Mikro-enjeksiyon 1. Genotipten bağımsız olarak kullanım 2. Çok çeşitli hedef hücre ve dokulara uygulanabilirlik 3. Uygulamada görsel kontrol olanağı 1. Kompleks ve pahalı donanım gereksinimi 2. Başarı için deneyim gerekliliği Biyolistik 1. Genotipten bağımsız kullanım 2. Farklı hedef hücre ve dokulara uygulanabilirlik 3. Transgenik tahıl elde etmek için güçlü bir yöntem olması 1. Kompleks ve pahalı donanım gereksinimi 2. Aktarılan DNA’da yüksek derecede yeni düzenlemeler görülmesi ve çok Bio-Rad, Arı 2002 (Ed: Özcan sayıda kopyanın integrasyonu. Yöntem Vd. )
- Slides: 20