Distrbios do equilbrio cidobsico Leandro Carvalho R 3

Distúrbios do equilíbrio ácido-básico Leandro Carvalho - R 3 TI setembro/2015

Introdução �Função bioquímica e fisiológica requer que o p. H extracelular seja mantido dentro de um intervalo adequado. �Os valores normais de p. H no sangue arterial (extracelular) variam entre 7, 35 e 7, 45 e, no intracelular, varia entre 7 e 7, 2.

Introdução �Função bioquímica e fisiológica requer que o p. H extracelular seja mantido dentro de um intervalo adequado. �Os valores normais de p. H no sangue arterial (extracelular) variam entre 7, 35 e 7, 45 e, no intracelular, varia entre 7 e 7, 2.

Introdução �Função bioquímica e fisiológica requer que o p. H extracelular seja mantido dentro de um intervalo adequado. �Os valores normais de p. H no sangue arterial (extracelular) variam entre 7, 35 e 7, 45 e, no intracelular, varia entre 7 e 7, 2.

Introdução �Função bioquímica e fisiológica requer que o p. H extracelular seja mantido dentro de um intervalo adequado. �Os valores normais de p. H no sangue arterial (extracelular) variam entre 7, 35 e 7, 45 e, no intracelular, varia entre 7 e 7, 2.

�A relação entre o p. H e a concentração de + H é feita em escala logarítmica, de modo que variações discretas nos valores de p. H expressam grandes oscilações na + concentração de H �Equilíbrio ácido-básico depende da cooperação de pelo menos dois órgãos vitais: os pulmões e os rins.

p. H x homeostasia Homeostasia é a constância do meio interno o Equilíbrio entre a entrada ou produção de íons hidrogênio e a livre remoção desses íons do organismo. o O organismo dispõe de mecanismos para manter a [H+] e, conseqüentemente o p. H sangüineo, dentro da normalidade, ou seja manter a homeostasia. p. H do Sangue Arterial p. H normal Acidose Alcalose 7, 8 7, 4 6, 8 Faixa de sobrevida

Sistemas Primários Reguladores do p. H

�Para manter a homeostase em seu diversos compartimentos, o organismo trabalha com sistemas-tampão. Aumentos de hidrogênio permite que a equação se desloque para a esquerda, e do mesmo modo, queda nessas concentrações levam ao desvio para a direita.

Tampões são substâncias capazes de remover ou de restituir íons hidrogênio de acordo com a necessidade, � mantendo a composição do líquido extracelular e impedindo variações abruptas no p. H. Para manter a homeostase em seu diversos compartimentos, o organismo trabalha com sistemas-tampão. Geralmente são formados por um ácido fraco e seu respectivo sal, ou por uma base fraca e seu respectivo sal. O sistema bicarbonato-CO 2 é o principal tampão presente no líquido extracelular. Aumentos de hidrogênio permite que a equação se desloque para a esquerda, e do mesmo modo, queda nessas concentrações levam ao desvio para a direita.

�Para manter a homeostase em seu diversos compartimentos, o organismo trabalha com sistemas-tampão. Aumentos de hidrogênio permite que a equação se desloque para a esquerda, e do mesmo modo, queda nessas concentrações levam ao desvio para a direita.

Eficiência de um tampão Quanto maior o número de moles que é necessário adicionar a um meio contendo um sistema tampão, de modo a alterar significativamente a concentração de H+, mais eficiente é o tampão. Pela equação de Handerson-Hasselbalch, p. H = p. Ka + log ([A-]/[HA]) o O p. H depende das concentrações do ácido (HA) e da base (A-). o O sistema tampão será mais eficiente quando [A-]=[HA], ou seja, quando o p. H = p. Ka. o O tampão se liga aos íons H+ e estabiliza o p. H.

Eficiência de um tampão Quanto maior o número de moles que é necessário adicionar a um meio contendo um sistema tampão, de modo a alterar significativamente a concentração de H+, mais eficiente é o tampão. Pela equação de Handerson-Hasselbalch, p. H = p. Ka + log ([A-]/[HA]) o O p. H depende das concentrações do ácido (HA) e da base (A-). o O sistema tampão será mais eficiente quando [A-]=[HA], ou seja, quando o p. H = p. Ka. o O tampão se liga aos íons H+ e estabiliza o p. H.
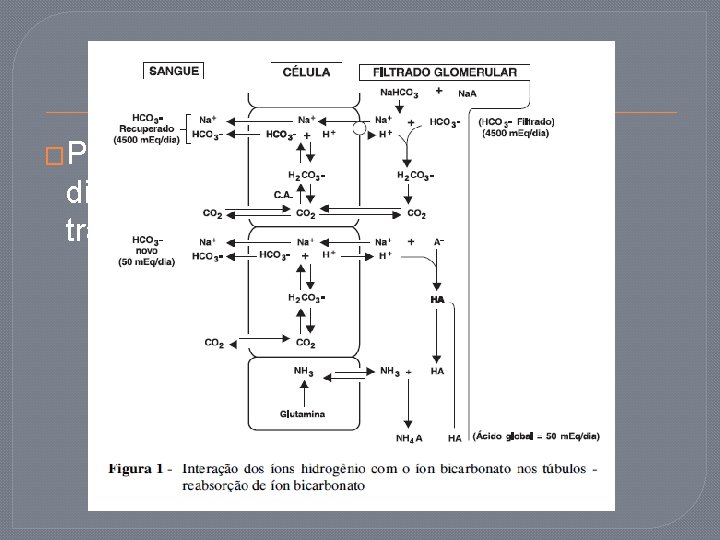
�Para manter a homeostase em seu diversos compartimentos, o organismo trabalha com sistemas-tampão. Aumentos de hidrogênio permite que a equação se desloque para a esquerda, e do mesmo modo, queda nessas concentrações levam ao desvio para a direita.
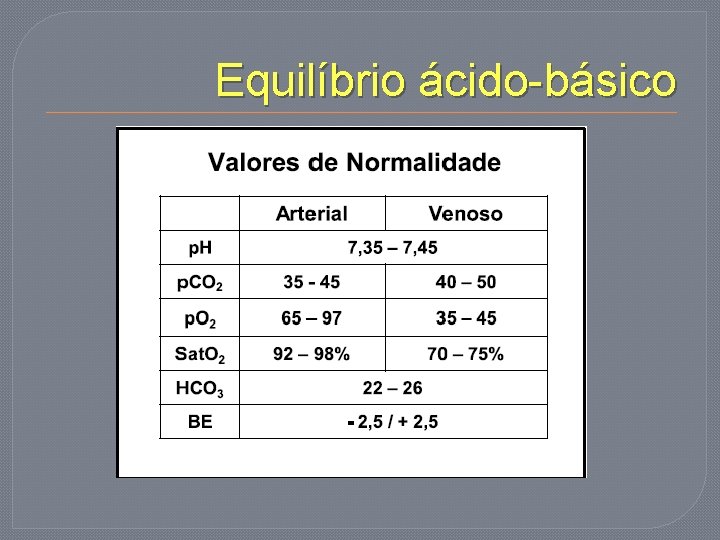
Equilíbrio ácido-básico

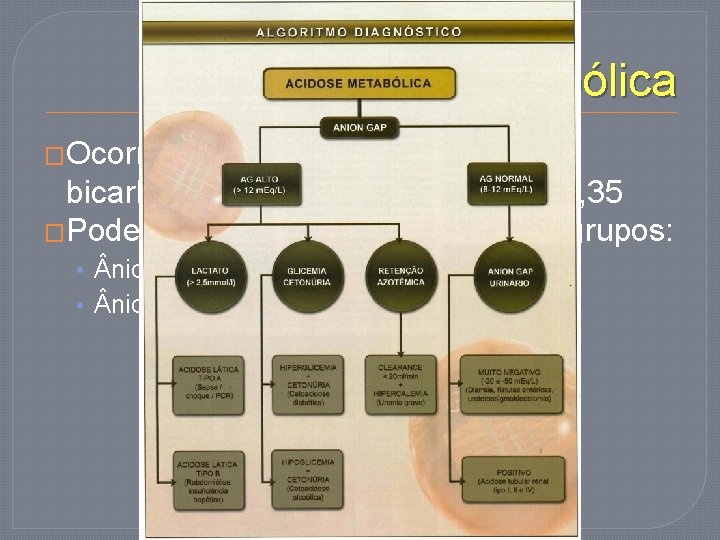
Acidose metabólica �Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 �Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Acidose metabólica O anion gap é a diferença entre os cátions e os ânions presentes no � plasma e deve ser calculado em todos os casos de suspeita de distúrbio ácido-base. Um aumento do anion Gap significa elevação de anions plasmáticos não mensuráveis, incluindo lactato e são mais preocupantes � Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12
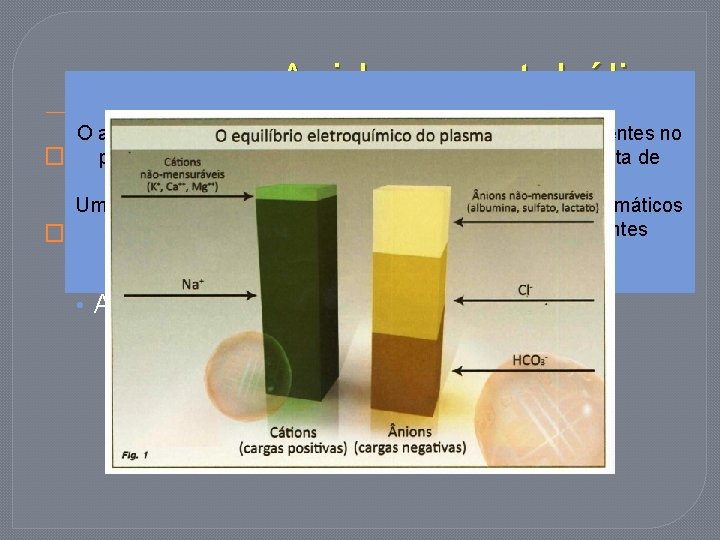
Acidose metabólica O anion gap é a diferença entre os cátions e os ânions presentes no � plasma e deve ser calculado em todos os casos de suspeita de distúrbio ácido-base. Um aumento do anion Gap significa elevação de anions plasmáticos não mensuráveis, incluindo lactato e são mais preocupantes � Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Acidose metabólica O anion gap é a diferença entre os cátions e os ânions presentes no � plasma e deve ser calculado em todos os casos de suspeita de distúrbio ácido-base. Um aumento do anion Gap significa elevação de anions plasmáticos não mensuráveis, incluindo lactato são mais preocupantes � Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Acidose metabólica �Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 �Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Acidose metabólica �Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 �Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Acidose metabólica �Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 �Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Anion gap urinário �O íon amônio (NH+4) é o principal cátion excretado na urina. � Na acidose metabólica a excreção de NH+4 aumenta drasticamente, resultando em negativação do AG urinário (-20 a -50 m. Eq/L). � Entretanto, se existe algum defeito na acidificação renal (eg. acidose tubular renal), a excreção de NH+4 é diminuída, resultando em anion gap urinário positivo.
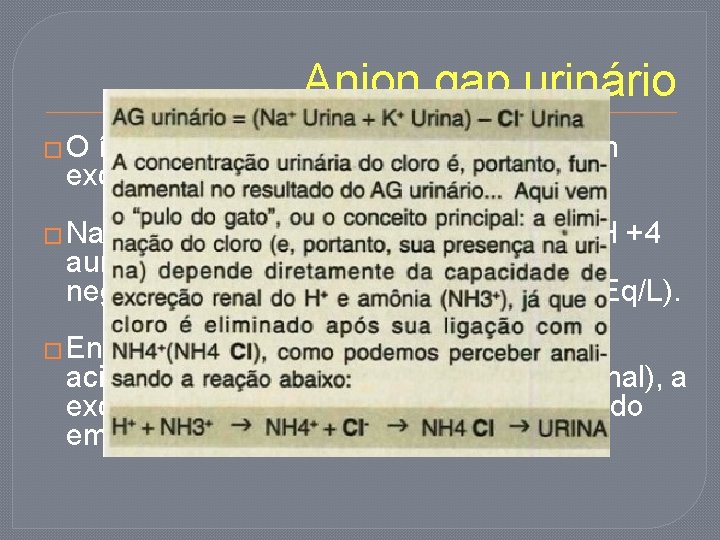
Anion gap urinário �O íon amônia (NH +4) é o principal cátion excretado na urina. � Na acidose metabólica a excreção de NH +4 aumenta drasticamente, resultando em negativação do AG urinário (-20 a -50 m. Eq/L). � Entretanto, se existe algum defeito na acidificação renal (eg. acidose tubular renal), a excreção de NH +4 é diminuída, resultando em anion gap urinário positivo.
Acidose metabólica �Ocorre queda dos níveis séricos de bicarbonato (<22 mm. Hg) e um p. H<7, 35 �Podem ser divididas em 2 grandes grupos: • nion-Gap alto • nion-Gap normal – hiperclorêmica O valor normal fica entre 8 -12

Tratamento acidose metabólica �É fundamental e mandatório o diagnóstico etiológico. �A dosagem do cloreto e cálculo do ânion Gap são passos cruciais na investigação.

Reposição de bases �A mais utilizada é o bicarbonato de sódio (Na. HCO 3) �A indicação depende de causa da acidose metabólica e de sua gravidade. �Acidoses hiperclorêmicas: está indicada na IRC e ATRs, com exceção na ATR IV e o hipoaldosteronismo.

�Acidoses com Anion-Gap alto: não está indicada de rotina, somente em casos muito graves e refratários. �Está indicada, por outro lado, na uremia grave e nas intoxicações exógenas por salicilatos, metanol e etilenoglicol.

�Acidoses com Anion-Gap alto: não está indicada de rotina, somente em casos muito graves e refratários. �Está indicada, por outro lado, na uremia grave e nas intoxicações exógenas por salicilatos, metanol e etilenoglicol.

�Acidoses com Anion-Gap alto: não está indicada de rotina, somente em casos muito graves e refratários. �Está indicada, por outro lado, na uremia grave e nas intoxicações exógenas por salicilatos, metanol e etilenoglicol.

�Quais os riscos de administrar Na. HCO 3: o Edema agudo de pulmão: 50 ml da solução de Na. HCO 3 a 8, 4% é equivalente a 4, 5 g de Na. Cl. o Hipernatremia o Redução do cálcio ionizado o Redução do p. H intracelular

Alcalose metabólica �É definida por um HCO 3 - >26 m. Eq/l e um p. H>7, 45. �Tem como principais causas os vômitos e o uso de diuréticos tiazídicos ou de alça. �Se associa frequentemente a hipocalemia.
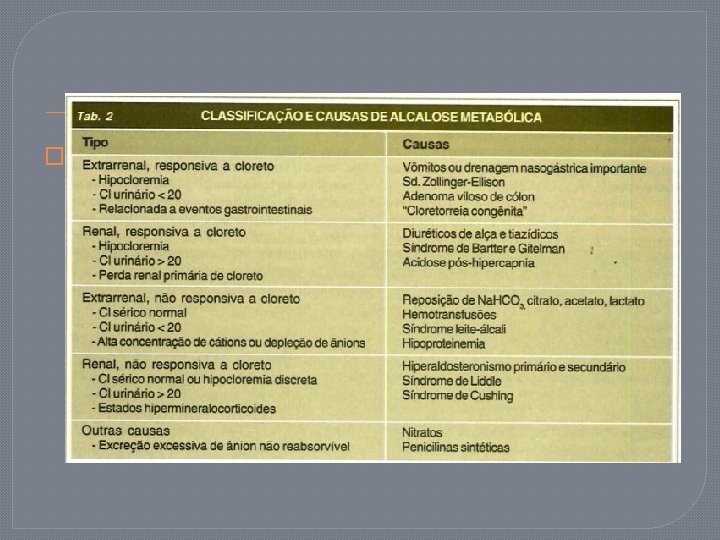
�Quadro do medcurso

Tratamento das alcalose metabólicas � Porquê tratar? o Cálcio ionizado o Encefalopatia hepática � Alcalose com depleção de volume e cloreto: SF 0, 9% + KCL (VO ou EV) � Hipervolemia: Acetazolamida****; nos pctes com hiperaldosteronismo ou hipercortisolismo – reposição K e diuréticos poupadoes de K.

Acidose Respiratória �Definida como PCO 2> 45 mm. Hg e um p. H<7, 35, o H+ que se acumula, é derivado do CO 2. �Aguda: Mecanismo só pode ser hipoventilação – geralmente decorrente de uma patologia pulmonar grave, que já levou à fadiga da musculatura respiratória, ou obstrução de vias aéreas.

�Lesões de SNC ou uso de medicações que inibem o centro respiratório �Doenças da medula espinhal que comprometem níveis cervicais altos (C 2, C 3), �Doenças dos nervos periféricos – frênico musculares ou neuromusculares que acometem o diafragma.

�Crônica: Retentores crônicos de CO 2 – DPOC, S. Pickwick �Estes pacientes têm níveis de CO 2 elevados, mas o p. H está apenas tocado para baixo ou normal, pois existe um aumento compensatório importante de bicarbonato, devido a retenção renal.

Tratamento acidose respiratória �Deve ser prontamente revertida, pois suas consequências clínicas podem ser graves – SÍNDROME DA CARBONARCOSE. �IOT e VM, trazendo a PCO 2 para o valor normal ou prévio e, principalmente, o p. H para a faixa normal.

Tratamento acidose respiratória �Deve ser prontamente revertida, pois suas consequências clínicas podem ser graves – SÍNDROMECO 2 DA CARBONARCOSE. o Vasodilatação cerebral, queda do p. H liquórico e cerebral o Alteração do sensório (confusão mental, agitação, convulsões, torpor, coma) o Papiledema e distúrbios hemodinâmicos (choque, arrtimias ventriculares malignas, PCR)

Tratamento acidose respiratória �Deve ser prontamente revertida, pois suas consequências clínicas podem ser graves – SÍNDROME DA CARBONARCOSE. �IOT e VM, trazendo a PCO 2 para o valor normal ou prévio e, principalmente, o p. H para a faixa normal.

�Acidose respiratória crônica não precisa ser tratada, quando no estado compensado. Apenas o tratamento da doença de base. �Quando estes pacientes descompensam, devem sempre ser intubados se houver alteração do sensório, fadiga respiratória ou p. H<7, 25 na gasometria.

Alcalose respiratória � Definida �O por PCO 2<35 mm. Hg e um PH>7, 45. mecanismo só pode ser hiperventilação • Psicogênica: crise de ansiedade ou angústia • Patologia pulmonar aguda: crise asmática, pneumonia, TEP, etc. �O consumo de H+ é consequente a perda de CO 2.

Tratamento da alcalose respiratória �Deve ser rápido, pois leva a vasoconstrição e hipofluxo cerebral. �Tetania pode ser desencadeada por pela redução do cálcio ionizável. �A princípio se trata a causa base; casos graves e refratários faz-se o uso de bolsas coletoras; se em VM aumenta-se o espaço morto.
- Slides: 43