Displasia broncopulmonar doena pulmonar crnica da infncia e

Displasia broncopulmonar: doença pulmonar crônica da infância e resultados a longo prazo Bronchopulmonary Dysplasia: Chronic Lung Disease of Infancy and Long-Term Pulmonary Outcomes. Davidson LM, Berkelhamer SK. J Clin Med. 2017 Jan 6; 6(1). pii: E 4. doi: 10. 3390/jcm 6010004. Review. PMID: 28067830 Similar articles Artigo Livre! Apresentação: Lara Ramos Pereira R 3 NEONATOLOGIA/HMIB/SES/DF Coordenação: Evely Mirela www. paulomargotto. com. br Brasília, 16 de dezembro de 2017

INTRODUÇÃO A displasia broncopulmonar (DBP) é a doença pulmonar crônica mais comum em lactentes prematuros que necessitaram de ventilação mecânica e oxigenoterapia para doenças respiratórias agudas, mas também pode ocorrer em neonatos que tiveram um quadro respiratório menos grave [1 -3]. A DBP foi descrita pela primeira vez em 1967, por Northway et al [1], em um grupo de prematuros que desenvolveram doenças pulmonares crônicas após receber ventilação e oxigênio suprafisiológico para tratar insuficiência respiratória aguda.

INTRODUÇÃO Embora os avanços nos cuidados neonatais tenham resultado em melhores taxas de sobrevivência de bebês prematuros, foram feitos progressos limitados na redução das taxas de DBP. No entanto, várias séries identificaram que os bebês sofrem de doença menos grave com menor risco de mortalidade do que o observado originalmente e descrito por Northway [4, 5]. A introdução de esteróides pré-natais, surfactante pósnatal, cuidados respiratórios modernos e nutrição adequada resultaram em seqüelas pulmonares mais leves com menos fibrose pulmonar, mas evidências histopatológicas de desenvolvimento pulmonar preso, referido por alguns como a “nova Displasia” [4, 6– 8].

INTRODUÇÃO Apesar dos esforços generalizados para proteger o vulnerável pulmão do prematuro contra lesões, a DBP continua sendo o resultado adverso mais freqüente em bebês nascidos com menos de 30 semanas de idade gestacional e a doença pulmonar crônica mais comum na infância[9]. Outros estudos identificaram que DBP e a prematuridade tem impactos a longo prazo sobre a função pulmonar e podem aumentar o risco de morbidade pulmonar tardia, o que levanta preocupações de que os sobreviventes da UTI neonatal representam uma emergente carga e desafio futuro para os sistemas de saúde.

INTRODUÇÃO • • • Prevalência da DPB: A incidência de DBP em bebês sobreviventes com IG <ou = a 28 semanas foi de aproximadamente 40% ao longo das últimas décadas [5, 10 -12]. Apesar do uso rotineiro de corticóide pré-natal nos trabalhos de parto prematuro e do uso do surfactante nos prematuros com síndrome do desconforto respiratório (SDR) terem muito impactado na sobrevivência de bebês prematuros, esses avanços não parecem ter traduzido taxas decrescentes de DBP [16, 17]. O progresso é dificultado pela falta de terapias efetivas para prevenir lesões pulmonares neonatais e doenças crônicas. As estratégias atuais para proteção pulmonar que estão sendo encorajadas incluem: o uso da ventilação volumétrica e não invasiva, hipercapnia permissiva e uso direcionado de esteróides, além de cafeína e vitamina A.

INTRODUÇÃO Definição de DBP: Historicamente, falta uniformidade nos critérios para definir DBP. A primeira definição clínica de DBP foi limitada a necessidade de oxigênio aos 28 dias de vida com alterações radiológicas consistentes. Estes foram originalmente modificados para incluir necessidade contínua de oxigenoterapia com 36 semanas de idade pós-concepcional(Ig. PC)[3, 18]. A definição atual leva em consideração a duração total da suplementação de oxigênio, requisitos de pressão positiva e idade gestacional, além da dependência de oxigênio com 36 semanas de Ig. PC. (Tabela 1)


INTRODUÇÃO À medida que a população de sobreviventes da UTIN cresce, é provável que as manifestações a longo prazo de lesões pulmonares crônicas da DBP representem um ônus maior para os sistemas de saúde. Este artigo procura rever a fisiopatologia da DBP, as estratégias de gestão recentes e o que é conhecido atualmente sobre os resultados pulmonares a longo prazo em sobreviventes com DBP.

FISIOPATOLOGIA DA DISPLASIA BRONCOPULMONAR O fenótipo visto com DBP é o resultado final de um processo multifatorial complexo no qual vários fatores pré e pós-natais comprometem o desenvolvimento normal no pulmão imaturo. (Figura 1) O tempo e a duração específicos das exposições influenciam o padrão de danos pulmonares que pode ocorrer [25]. Notavelmente, a prevalência de DBP em crianças em ventilação mecânica está inversamente relacionada à idade gestacional e ao peso ao nascer, apoiando o fato de que o desenvolvimento incompleto dos pulmões ou lesões durante uma janela crítica do desenvolvimento pulmonar influenciam o desenvolvimento de DBP [4]. Além disso, para a prematuridade, vários outros fatores podem contribuir para a ruptura do crescimento alveolar e para o desenvolvimento vascular pulmonar, incluindo, entre outros, ventilação mecânica, toxicidade de oxigênio, infecção pré/ pós-natal, inflamação e restrição de crescimento ou déficits nutricionais. A predisposição genética é reconhecida por modificar ainda mais o risco de doença.
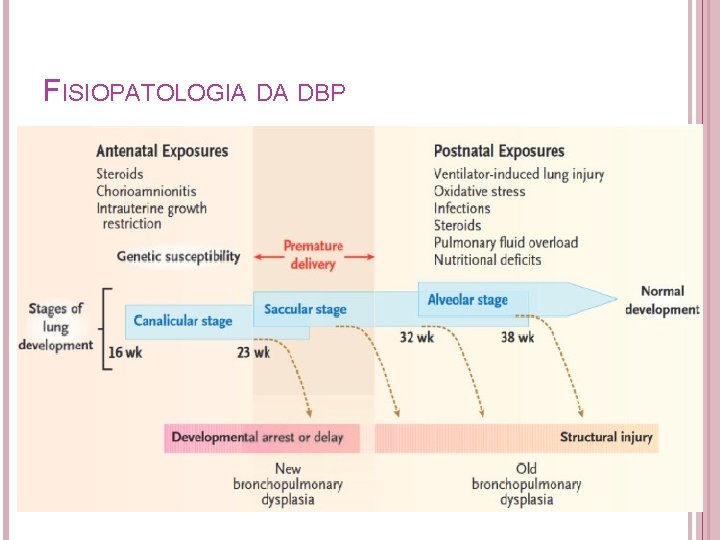
FISIOPATOLOGIA DA DBP

FISIOPATOLOGIA DA DBP • • TRAUMA MEC NICO: A DBP ocorre quase que exclusivamente em recém-nascidos prematuros que receberam ventilação de pressão positiva sugerindo que a hiperinsuflação pulmonar e o alongamento alveolar desempenham um papel crítico na patogênese da DBP. A mecânica pulmonar ineficaz resulta em necessidade de assistência ventilatória no nascimento. Dados recentes sugerem que 65% dos recém nascidos prematuros nascidos de 22 a 28 semanas de idade gestacional são intubado na sala de parto, que diminuiu desde 1993, quando 80% dessa população foi intubado imediatamente após o parto [26]. O pulmão prematuro é difícil de ventilar devido a deficiência de surfactante, resultando em diminuição da complacência e dificuldade para manter a capacidade residual funcional (CRF) [27, 28]. A deficiência de surfactante contribui ainda mais para a expansão pulmonar não uniforme, com áreas de hiperinsuflação e atelectasia [27, 29]. Pressão positiva e excesso de volume na ventilação mecânica pode causar lesão no pulmão imaturo por uma insuflação adicional de alvéolos, levando a geração de lesões celulares, inflamação e espécies reativas de oxigênio, assim ampliando a lesão pré-existente associada à inflamação pré-natal [9, 30].

FISIOPATOLOGIA DA DBP • • • TOXICIDADE DO OXIGÊNIO: Estudos em numerosos modelos animais identificaram que a exposição ao oxigênio suprafisiológico isolada induz um fenótipo comparável ao observado na DBP, incluindo desenvolvimento alveolar comprometido e remodelamento vascular pulmonar [31]. Estudos clínicos paralelam esses achados com algumas evidências de diminuição da inflamação pulmonar e das taxas de DBP com uso restrito de oxigênio ou menores alvos de saturação [32, 33]. Oxigênio suprafisiológico resulta em aumento da geração de Espécies Reativas de Oxigênio mitocondrial com susceptibilidade única ao estresse oxidativo e lesão das células alveolares no pulmão em desenvolvimento, em parte atribuível a deficiências de antioxidantes e defesas imaturas[35 -37]. Modelos de animais sugerem que mesmo exposições breves a altas concentrações de oxigênio podem resultar em alterações morfológicas e funcionais a longo prazo no pulmão [38]. Dados clínicos sugerem que mesmo uma exposição breve ao oxigênio suprafisiológico durante a ressuscitação aumenta o risco de DBP [33].

FISIOPATOLOGIA DA DBP • • • INFECÇÃO E INFLAMAÇÃO: Existe controvérsia quanto a contribuição da corioamnionite e da inflamação pré-natal com o risco de desenvolver DBP [41]. Estudos clínicos e experimentais sugeriram que a corioamnionite induz a maturação precoce do pulmão com aumento da produção de surfactante e diminui o risco de síndrome do desconforto respiratório (SDR)[42, 43]. No entanto, estudos também suscitaram preocupações com lesões pulmonares associadas e diminuição da alveolarização. A administração da endotoxina Escherichia coli às ovelhas grávidas resultou em inflamação amplificada com ventilação dos cordeiros prematuros expostos, incluindo evidência de apoptose celular e desenvolvimento alveolar comprometido [44, 45]. Embora vários estudos clínicos tenham relatado uma associação entre corioamnionite e DBP, uma metanálise com 59 estudos e mais de 15. 000 crianças sugeriu que existia uma associação limitada entre corioamnionite e DBP quando foram feitos ajustes para idade gestacional [43]. Este estudo, também levantou preocupações com a publicação de viés e concluiu que a corioamnionite não pode ser definitivamente considerada um risco para DBP [41]. A controvérsia existe, uma vez que as variáveis definições foram usadas para classificar a corioamnionite e esse termo pode representar uma variedade de patologias.

FISIOPATOLOGIA DA DBP • • • INFECÇÃO E INFLAMAÇÃO: Análise recente de dados de uma coorte de mais de 25 anos, com mais de 1600 lactentes com muito baixo peso ao nascer concluíram que a sepse, e não a corioamnionite, aumentava os riscos de desenvolvimento de DBP moderada ou grave [46]. Existe pouca controvérsia quanto a contribuição da inflamação pós-natal ou infecção nosocomial para o aumento do risco de desenvolver DBP [47, 48]. Novitsky et al. identificaram que bebês prematuros com DBP eram mais propensos a receber cursos prolongados de antibióticos na primeira semana de vida e de ter evidencia de resistência a bacilos gram negativos no tubo orotraqueal (TOT)[49]. Preocupa-se que a presença de organismos resistentes pode resultar em infecção mais grave, o que justifica o uso criterioso de antibióticos em lactentes prematuros em risco. Exposições não infecciosas como o oxigênio e ventilação mecânica, causam mais lesões no pulmão prematuro, resultando em insulto secundário através de respostas mediadas por inflamação. O aumento de citocinas pró-inflamatórias encontradas em aspirados traqueais e amostras de sangue de prematuros, incluindo fator de necrose tumoral alfa(TNFa), IL-8, IL-1β e IL-6, está relacionado com o risco aumentado de DBP [50 -52].

FISIOPATOLOGIA DA DBP • RESTRIÇÃO DE CRESCIMENTO: Bebês prematuros que são pequenos para idade gestacional (PIG) ou tem crescimento intrauterino restrito(CIUR) apresentam risco aumentado de desfecho pulmonar ruim [53, 54]. Estudos demonstram um risco duplo aumentado de DBP (28% vs. 14%) e de mortalidade neonatal (23% vs 11%) para os PIG [54 -56]. Além disso, o peso ao nascer para a idade gestacional é um importante preditor de Hipertensão pulmonar associada à DBP [57]. Embora a associação de restrição do crescimento intrauterino (RCIU) e DBP seja em parte secundária ao comprometimento do desenvolvimento pulmonar, estudos em modelos de bovinos e murinos com RCIU têm demonstrado que os riscos são mais influenciados pelos impactos na função das células endoteliais, expressão do surfactante e respostas inflamatórias[5860].

FISIOPATOLOGIA DA DBP • • • RESTRIÇÃO DE CRESCIMENTO: Os RN prematuros extremos estão em risco adicional de restrição de crescimento pós-natal secundária aos desafios de oferecer nutrição ideal. Apesar dos avanços significativos no suporte nutricional enteral e parental, 55% dos bebês nascidos com menos de 27 semanas de IG demonstram fracasso do crescimento com peso inferior ao percentil 10 às 36 semanas de Ig. PC [12, 26, 53]. A insuficiência no crescimento pós-natal influencia os riscos de desenvolver DBP com dados sugerindo que a nutrição adequada na primeira semana desempenha um papel crítico nesse desfecho [7, 53]. Principalmente a nutrição enteral adequada diminui os riscos de desenvolver DBP[8]. Estudos recentes, demonstram ainda um menor risco de DBP apesar do crescimento comprometido, com uso exclusivo do leite materno [61].

FISIOPATOLOGIA DA DBP • • • Genética: Embora o DBP resulte de exposições cumulativas aos fatores pré e pós-natais já mencionados, existe um interesse crescente pelas contribuições hereditárias para o desenvolvimento da DBP. Um total de 450 pares de gêmeos foram analisados e esta análise concluiu que 65% das variações na susceptibilidade à DBP poderiam ser explicadas por fatores genéticos e ambientais compartilhados[64]. Estudos multicêntricos subsequentes confirmaram a hereditariedade da DBP por meio de dados que identificam maior semelhança em monozigóticos em comparação aos gêmeos dizigóticos. Avanços rápidos em genômica e proteômica sugerem que os reguladores da susceptibilidade podem eventualmente ser identificados, permitindo a possibilidade de uma terapia direcionada ou individualizada para prevenir e tratar DBP.

PREVENÇÃO DA DISPLASIA BRONCOPULMONAR As estratégias de manejo tem como objetivo evitar lesões pulmonares e o desenvolvimento de DBP. Como a patogênese da doença é multifatorial, diversas abordagens foram adotadas, incluindo estratégias de ventilação e estratégias clínicas. Curiosamente, tanto os esteróides pré-natais como o surfactante reduzem as taxas de SDR e melhoram a sobrevida; no entanto, nenhum deles demonstrou reduzir a incidência de DBP [26].

ESTRATÉGIAS DA VENTILAÇÃO • • A evidência de lesão pulmonar induzida pela ventilação levou a esforços para promover a "ventilação gentil”, em parte através do uso de hipercapnia permissiva. No entanto, os dados para apoiar esta estratégia têm sido inconsistentes e os resultados do desenvolvimento neurológico a longo prazo permanecem desconhecidos [68, 69]. Não obstante, muitas Unidades adotaram essas práticas, reconhecendo dados que suportam redução significativa na necessidade de ventilação mecânica com mínima liberalização das metas de CO 2 (> 52 versus <48 mm. Hg) [70, 71]. A ventilação gentil também defendeu a ventilação volumétrica com metanálises para apoiar esta estratégia na redução das taxas de DBP e inflamação associada a ventilação [72 -74]. Ensaios clínicos randomizados demonstraram que tanto a ventilação de alta freqüência (VAF) quanto a ventilação oscilatória (VO) tem potencial para reduzir o risco de DBP [75, 76]; No entanto, uma revisão Cochrane de VAF eletiva revelou apenas uma pequena redução na incidência de doença pulmonar crônica com notável inconsistência ao longo dos 19 estudos incluídos [77]

ESTRATÉGIAS DA VENTILAÇÃO • • Foram feitos esforços significativos para se afastar o uso da ventilação invasiva ao longo das últimas duas décadas [26]. Metanálise de ensaios clínicos randomizados comparando o uso profilático ou precoce do surfactante para o suporte ventilatório inicial por CPAP identificou redução combinada no desfecho de morte e DBP, evitando a intubação [78 -80]. Estas metanálises incluíram em suas revisões, dados de estudos usando surfactante profilático seguido de rápida extubação (INSURE) e aqueles que randomizaram intubação de rotina. Apesar dos variáveis estudos incluídos, o achado comum de diminuição do risco de BPD fortalece recomendações para o uso de estratégias não-invasivas. Como resultado, muitas unidades agora estão optando por realizar um teste inicial com CPAP para gerenciar a SDR. Uso de modalidades alternativas não-invasivas, incluindo VNI, CPAP nasal de dois níveis (bi. PAP) e cânula nasal de alto fluxo (CAF) também está aumentando com algumas evidências sugerindo que esses modos também podem ser eficazes no manejo da doença respiratória neonatal [81 -83].

ESTRATÉGIAS DA VENTILAÇÃO • • • Ensaios randomizados de centro único relataram diminuição da necessidade de intubação, bem como redução da incidência de DBP com VNI em comparação com a pressão positiva contínua das vias aéreas (CPAP) [82]. Em contrapartida, uma revisão Cochrane incluindo oito ensaios que compararam VNI com CPAP identificaram menos falhas de extubação com VNI, mas nenhum benefício específico em relação ao risco de DBP [84]. A abordagem ótima, o impacto na DBP e os resultados a longo prazo com o uso da VNI permanecem indefinidos [85].

ESTRATÉGIAS DA VENTILAÇÃO Existem controvérsias adicionais que envolvem o uso da VNI não sincronizada. A sincronização pode ser alcançada e foi descrito em bebês prematuros usando uma cápsula pneumática abdominal (ou Graseby) para detectar a descida diafragmática. Esta abordagem tem a vantagem teórica de garantir a permeabilidade da glote antes do fluxo ser desencadeado. Mais recentemente, algumas unidades se moveram para o uso de ventilação não invasiva com ventilador de assistência de ajuste neuronal (NAVA) para oferecer respirações sincronizadas [87]. Embora essa abordagem em teoria possa melhorar a interação paciente-ventilador e melhorar os resultados pulmonares, os dados para apoiar esta prática ainda são necessários. Finalmente, para aqueles bebês que necessitam de intubação, um ensaio inicial de extubação é encorajado, pois pode potencialmente reduzir os riscos de lesão pulmonar induzida pelo ventilador. Estudos identificaram que uma tentativa inicial de extubação isolada pode diminuir o risco de DBP, independentemente da necessidade de reintubação ou duração de ventilação [88, 89]. Esses estudos provocativos foram ambos retrospectivos sugerindo a necessidade de ensaios prospectivos adicionais.

SATURAÇÃO ALVO Foram feitos grandes esforços para definir alvos de saturação ideais para bebês prematuros com preocupações contínuas com qualidade da evidência disponível [90]. Em uma metanálise, incluindo cinco ensaios não identificaram diferenças nos resultados de deficiência visual ou DBP, mas suscitaram preocupações com aumento do risco de mortalidade (com 18 a 22 meses) com metas de saturação mais baixas ( entre 85% -89% e alta 91% 95%), bem como taxas mais altas de enterocolite necrosante (NEC) [91, 92]. O ensaio (APOIO) realizado nos EUA encontrou taxas ligeiramente mais baixas de DBP (38% x 41, 7%) no grupo de baixa saturação sem significância estatística [93]. O Canadian Oxygen Trial (COT) de forma semelhante, identificou uma tendência semelhante com taxas de DBP de 31, 8% e 33, 1% nos grupos de baixa e alta saturação, respectivamente [94]. Finalmente, os três ensaios realizados na Nova Zelândia, Reino Unido e Austrália juntos – estudo BOOST II -Os Benefícios dos Ensaios de Saturação de Oxigênio, encontraram tendências semelhantes com taxas de 39, 5% e 44, 7%, nos grupos de baixa e alta saturação, novamente sem significância estatística [95, 96]. Uso de maiores alvos de saturação aumentaram inerentemente as taxas documentadas de DBP, uma vez que os bebês não podem ser desmamados até eles consigam manter sozinhos essas metas mais elevadas de saturação. No entanto, a metanálise incluindo os cinco estudos ainda não conseguiu identificar uma diferença significativa nas taxas de oxigênio a 36 semanas [92]. Apesar das preocupações teóricas pelo aumento do risco de lesão pulmonar oxidativa e remodelamento vascular pulmonar, muitas unidades agora usam limites de saturação maiores de 91% a 95% com base na descoberta coletiva de melhores taxas de sobrevivência nestes cinco ensaios. Alguns sugerem que metas mais elevadas de 93% a 97% devem ser consideradas com DBP estabelecida para reduzir os riscos de hipertensão pulmonar subseqüente [97].

CORTICOSTERÓIDES Os glicocorticóides pós-natais são reconhecidos para reduzir as taxas de DBP por meio da redução da inflamação assim como pela indução de mudanças na maturação pulmonar. No entanto, os benefícios potenciais dos esteróides sistêmicos são muitas vezes superado pelas preocupações com seqüelas de desenvolvimento neurológico a longo prazo, incluindo aumento do risco de paralisia cerebral [98, 99]. As taxas de uso de esteróides sistêmicos para prevenção de DBP têm reduzido marcadamente na Academia Americana de Pediatria (AAP) e na Sociedade Canadense de Pediatria desde 2002, em comparação com o uso rotineiro anterior. Preocupa-se que uma sub-população de alto risco para DBP ainda possa se beneficiar de doses mais baixas e / ou cursos mais curtos de esteróides sistêmicos e que as práticas atuais desviaram para muito longe o uso do corticóide. Na tentativa de administrar corticosteróides de forma mais confiável diretamente aos alvéolos de bebês em risco de início de lesão pulmonar, a co-administração de Budesonida com surfactante foi considerada Yeh, et al. Relataram ter observado diminuição significativa na incidência de DBP ou morte em lactentes com SDR grave que receberam budesonida endotraqueal [106]. Estudos multicêntricos, randomizados adicionais são necessários para acompanhamento dessa prática.

CAFEÍNA No recente estudo randomizado, multicêntrico Cafeína para apnéia da prematuridade (CAP), o início precoce da cafeína resultou em menor incidência de DBP, bem como um curso mais curto de suporte respiratório em comparação com controles [107]. O mecanismo específico pelo qual a cafeína protege contra lesões pulmonares ainda não está claro, e os resultados melhorados podem ter sido devido à diminuição da duração de ventilação mecânica. Os benefícios da cafeína foram validados em coortes adicionais e esses dados têm práticas influenciadas coletivamente em várias Unidades, incluindo o início precoce da cafeína em lactentes com risco de DBP [108, 109]

VITAMINA A A deficiência de vitamina A pode predispor a doença pulmonar crônica, pois desempenha um papel crítico na manutenção da integridade do epitélio do trato respiratório e é um regulador chave do crescimento normal do pulmão [110, 111]. Enquanto a metanálise sugere que a suplementação de recémnascidos prematuros com vitamina A resulta na redução do resultado combinado de morte e DBP, o uso desta terapia é altamente variável à medida que os benefícios foram observados apenas em lactentes com menos de 1000 gramas e os resultados eram marginais [112]. A administração requer injeções intramusculares associadas a desconforto significativo e potencialmente um risco aumentado de infecção [113]. Um grande estudo está atualmente em curso avaliando a eficácia da suplementação oral de vitamina A com a esperança de que uma rota de administração mais simples também possa ser efetiva [114].

ÓXIDO NÍTRICO O uso do óxido nítrico inalado (i. NO) para prevenção da displasia broncopulmonar merece menção, pois foi explorado em numerosos estudos com descobertas inconsistentes [115, 116]. Enquanto um protocolo de 24 dias, com início entre 7 e 21 dias foi associado com redução das taxas de DBP, evidência combinada de 14 ensaios clínicos randomizados em prematuros menores ou iguais a 34 semanas de gestação mostraram efeitos equívocos sobre a morbidade pulmonar, sobrevida e resultados do desenvolvimento neurológico [117, 118]. Enquanto esta metanálise incluiu uma grande variedade de protocolos com respeito em relação ao momento da iniciação e dose, os autores concluíram que o uso precoce de i. NO em recém-nascidos prematuros não afetou o risco de lesões cerebrais ou melhorou a sobrevivência sem DBP e que o uso posterior para prevenir a DBP pode ser efetivo, mas exigiu mais estudos. A subsequente metanálise de dados de pacientes individuais sugeriu que nenhum benefício específico com prematuridade e uso rotineiro declarado não poderia ser recomendado [119]. Avaliação especializada do tema resultou em opiniões de consenso tanto do NIH quanto da Academia Americana de Pediatria dissuadindo o uso rotineiro de i. NO em prematuros [120, 121]. Apesar destas declarações, o uso fora do rótulo do i. NO nos bebês extremamente prematuros permanecem em ascensão [122]. Isso pode ser devido a uso em circunstâncias graves onde os neonatologistas sentem que oferecer terapia é melhor do que não fazer nada [123]. Há também argumentos de que as subpopulações podem ser mais receptivas e apropriadas para serem consideradas para tratamento, com dados para sugerir benefícios após a ruptura prematura de membranas [122, 124]

RESULTADOS A LONGO PRAZO DA DBP Os resultados a longo prazo da DBP continuam difíceis de caracterizar, pois as populações adultas atualmente disponíveis para estudo representam sobreviventes de cuidados desatualizados. Enquanto a DBP tende a melhorar com o desenvolvimento do pulmão, dados disponíveis em estudos de acompanhamento identificam preocupações com persistência de sequelas pulmonares da doença. Notavelmente, o impacto na saúde pulmonar tardia, bem como as conseqüências de outras exposições infecciosas ou ambientais permanecem mal caracterizadas. É importante reconhecer os tremendos esforços emocionais, médicos e financeiros investidos no cuidado de bebês extremamente prematuros. O tempo médio de hospitalização para os nascidos com 1000 gramas é de aproximadamente 60 dias com altas taxas de necessidade de suporte médico adicional, incluindo reinternação após a alta [125]. Durante o primeiro ano de vida, 49% dos lactentes com DBP exigem reanimação e os riscos de mortalidade associados a complicações pulmonares da DBP são significativos. Estudos retrospectivos identificam taxas de sobrevivência de apenas 71% -81% com DBP grave exigindo ventilação doméstica [128, 129]. Estudos adicionais mostraram que a incidência da síndrome da morte súbita foi sete vezes maior em lactentes com DBP [130]. Estudos de acompanhamento de sobreviventes com DBP - crianças e adultos jovens demonstram preocupações quanto à função pulmonar comprometida e defesas, sintomas semelhantes a asma, hipertensão pulmonar e intolerância ao exercício com respostas alteradas à hipoxia.

RESULTADOS A LONGO PRAZO DAD BP • • FUNÇÃO PULMONAR COMPROMETIDA: Numerosos estudos avaliaram a função pulmonar a longo prazo após o nascimento prematuro. Uma metanálise, incluindo 59 artigos, identificou que o percentual do volume expiratório forçado previsto em 1 segundo (VEF 1) diminui em sobreviventes de nascimento prematuro, mesmo em pacientes que não tiveram história de BPD [131]. Avaliação de sobreviventes com DBP adultos ou adultos jovens especificamente observou menor VEF 1, bem como diminuição da capacidade vital forçada (CVF) e da taxa de fluxo expiratório forçado a 50% da CVF em comparação com os controles [132 -134]. Um estudo identificou ainda uma associação entre o crescimento e as melhorias do comprometimento pulmonar, destacando a importante contribuição de uma nutrição adequada em sobreviventes de DBP. Um estudo longitudinal com sobreviventes de DBD de 8 e 18 anos demonstrou deterioração da função pulmonar com idade [134]. A limitação do fluxo de ar foi atribuída a um crescimento em que as vias aéreas crescem menos rapidamente do que o parênquima pulmonar, resultando em pequenas obstrução fixa das vias respiratórias [137]. A função pulmonar comprometida pode persistir no final da idade adulta [140].

RESULTADOS A LONGO PRAZO DAD BP o • • • DEFENSAS PULMONARES COMPROMETIDAS: A exposição a insultos ambientais, incluindo infecções respiratórias, tabaco e poluição podem complicar a resolução da DBP e prolongam os riscos de morbidade pulmonar [141, 142]. Bebês prematuros têm maior suscetibilidade à infecção que persiste na infância [143]. Infecções respiratórias comuns podem resultar em morbidade grave e mortalidade potencial em sobreviventes de DBP. A inflamação associada com estes insultos pulmonares pode levar a lesões pulmonares adicionais no já vulnerável pulmão em recuperação. Tanto os dados epidemiológicos como os modelos animais demonstraram que a DBP aumenta a susceptibilidade à lesão pulmonar induzida por infecção viral com evidência de inflamação alterada como resultado de vias imunorreguladoras inatas interrompidas [144, 145]. Além dos insultos ambientais, a morbidade pulmonar em recém-nascidos pré-termo pode ser complicada por refluxo crônico e microaspiração com risco de pneumonia por aspiração e / ou inflamação crônica. Embora a evidência seja variável, a melhoria do estado respiratório foi relatada após fundoplicatura a Nissen em lactentes com doença pulmonar crônica grave[146 -148].

RESULTADOS A LONGO PRAZO DAD BP • • SINTOMAS SEMELHANTES A ASMA: Muitos sobreviventes de DBP demonstram um componente da doença reativa das vias aéreas. Acompanhamento a longo prazo dos bebês nascidos <26 semanas de gestação identificaram que 25% tinham diagnóstico de asma aos 11 anos de idade enquanto mais de duas vezes essa porcentagem (56%) apresentava evidência de espirometria anormal [149]. Eles são menos responsivos aos broncodilatadores, pois podem sofrer um estreitamento fixo da via aérea periférica [150]. os benefícios de corticosteróides inalados também são considerados menos consistentes para crianças com DBP em comparação com aqueles com asma [151]

RESULTADOS A LONGO PRAZO DAD BP • • • INTOLER NCIA AO EXERCÍCIO: Os sobreviventes de DBP podem experimentar exacerbação de morbidades pulmonares com exercício ou exposição à hipoxia. O risco significativo de broncoconstricção induzida pelo exercício foi demonstrado em crianças com DBP consistente com as preocupações com a doença reativa das vias aéreas observada no slide anterior [150]. Além do risco de broncoconstrição induzida pelo exercício, os sobreviventes de DBP apresentam comprometimento da troca de gás com atividade física. O teste de esforço identifica a transferência de gás reduzida em repouso e durante a atividade que foi atribuída a distúrbios de longo prazo na estrutura pulmonar ou residual disfunção ventricular direita que afeta o débito cardíaco [153]. Uma avaliação detalhada recente de sobreviventes de DBD de 7 a 14 anos observou limitação ventilatória com o exercício, incluindo maior uso da reserva ventilatória, menor ventilação máxima e menor volume corrente. O pico de exercício resultou em hipoxemia em 60% das crianças com DBP com um aumento concomitante na Pa. CO 2 consistente com hipoventilação alveolar [155].

RESULTADOS A LONGO PRAZO DA DBP RESPOSTAS VENTILATÓRIAS ANORMAIS: Especificamente, respostas normais de aumento da ventilação com hipoxia e a diminuição da ventilação com hiperoxia podem ser alteradas. Persistente disfunção quimiorreceptiva foi documentada em sobreviventes de DBP [156, 157]. Resposta inadequada hipoventilação e hipoxia podem representar um risco significativo de morbidade em sobreviventes de DBP que também podem sofrer comorbidades da via aérea central ou broncomalácia. A função anormal do músculo respiratório em sobreviventes de DBP pode complicar ainda mais esse risco [156].

RESULTADOS A LONGO PRAZO DAD BP • • • HIPERTENSÃO ARTERIAL PULMONAR A vasculatura pulmonar dismórfica e a angiogênese comprometida na DBP resultam em risco de pressões pulmonares elevadas ou hipertensão pulmonar associada a DBP. Pacientes com DBP e pressões pulmonares elevadas correm alto risco de crises de hipertensão pulmonar (HP) e mortalidade precoce. Aqueles que sobreviveram podem, em última instância, demonstrar uma resolução da doença com crescimento pulmonar adicional. Os resultados na idade adulta e os riscos de doença vascular pulmonar tardia com HP associada à DBP permanecem mal definidos.

CONCLUSÕES A definição, fisiopatologia e manejo da displasia broncopulmonar (DBP) tem evoluído significativamente desde a primeira descrição de Northway há quase 50 anos. Os avanços no cuidado neonatal, resultaram em taxas aumentadas de sobrevivência de bebês extremamente prematuros, levando a um novo conjunto de desafios de gestão, bem como uma população emergente de sobreviventes a longo prazo de DBP; Cuidados interdisciplinares para atender às complexas necessidades pulmonares, nutricionais e de desenvolvimento destes pacientes são críticos e podem influenciar os resultados da DBP grave [148].

CONCLUSÕES Estudos terapêuticos randomizados, além da avaliação longitudinal desses pacientes, permanecem essenciais para otimizar os cuidados e discernir os fatores de risco de morbidade. Embora esses estudos exijam recursos significativos, eles são muito necessários, pois falta evidência para o tratamento ótimo. Além do mais, pouco se sabe sobre os resultados pulmonares da DBP além da segunda década de vida. Se destacam a preocupação com o risco aumentado de disfunção ventricular direita subclínica, doença pulmonar obstrutiva, intolerância ao exercício e sintomas similares a asma em sobreviventes. À medida que as tendências demonstram a crescente sobrevivência de bebês extremamente prematuros, quase metade dos quais será diagnosticada com DBP, é imperativo que estudos futuros investiguem mecanismos e fatores de risco que influenciam a morbidade de longo prazo com um objetivo geral de reduzir o ônus da doença.


Referências-Consultem o Artigo integral! Bronchopulmonary Dysplasia: Chronic Lung Disease of Infancy and Long-Term Pulmonary Outcomes. Davidson LM, Berkelhamer SK. J Clin Med. 2017 Jan 6; 6(1). pii: E 4. doi: 10. 3390/jcm 6010004. Review. PMID: 28067830 Similar articles Artigo Livre!

Nota do Editor do site, Dr. Paulo R. Margotto Estudando Juntos! Aqui e Agora pmargotto@gmail. com

O que há de novo na Patogenia e Prevenção da Displasia Broncopulmonar (23 o Congresso Brasileiro de Perinatologia, 14 -17 de setembro de 2016, Gramado, RS) Autor(es): Eduardo Bancalari (EUA). Realizado por Paulo R. Margotto A displasia broncopulmonar (DBP), uma das sequelas mais importante dos recém-nascidos prematuros, infelizmente não tem diminuído nos últimos anos devido a maior sobrevivência dos recém-nascidos prematuros extremos. Com o uso de esteróide pré-natal, surfactante pós-natal, o uso de padrões menos agressivos de ventilação mecânica (VM) o quadro da DBP mudou muito. Do quadro de enfisema e atelectasia, metaplasia epitelial das vias aéreas, fibrose intersticial, hiperplasia da musculatura lisa das vias aéreas e dos vasos sanguíneos pulmonares, hipertrofia do ventriculo direito (velha DBP) para um quadro de mínimas lesões nas vias aéreas, edema pulmonar, não mais fibrose, e essencialmente, diminuição da septação alveolar e dminuição do desenvolvimento vascular ou seja, cessa o desenvolvimento alveolar (nova DBP). Entre os fatores que diminuem o desenvolvimento pulmonar se destacam a corioamnionite, a persistência prolongada do canal arterial hemodinamicamente significativo, altas concentrações de oxigênio, infecção, distensão pulmonar, deficiências nutricionais, restrição do crescimento intrauterino, o não uso de esteróide pré-natal e o grande vilação a ventilação mecânica prolongad, principalmente quando agressiva (24 horas a 7 dias, 2, 4 vezes mais e > 7 dias, 15 vezes mais!) O uso de CPAP nasal, INSURE (intubação-surfactante-extubação) e, como comentadoos links, o MINI INSURE (uso de surfactante de forma menos invasiva) tem resultado em menos ventilação mecânica nestes recém-nascidos. Há estratégias de ventilação que podem oferecer vantagens como a ventilação sincronizada com suporte de pressão e a ventilaçao com objetivo de volume ( volume tarjet ventilation). Na prevenção, ainda em estudo, com destaque para o uso de budesonida intra-traqueal (0, 25 mg/kg) com surfactante (100 mg/kg) , com resultados dramáticos (a incidência de DBP/morte foi de 42% versos 66% no grupo controle: RR=0, 58; IC a 95% de 0, 44 -0, 77 -P=0, 001!). Inclusive, o seguimento destes recém-nascidos não demonstrou nenhuma evidência de efeito negativo na evolução neurológica destes recém-nascidos. Também e evidência o uso de célula tronco (melhora a alveolarização inibida com altas concentrações de oxigênio, assim como a significativa redução de medidores inflamatórias nas vias aéreas). Como diz Bancalari E, é impossível eliminar a DBP, principalmente nos RN de 23 -24 -25 -26 semanas, mas com os conhecimentos já adquiridos, podemos diminuir a sua incidência. No entanto, para estes recém-nascidos com extrema prematuridade, teremos que usar novas intervenções ainda em estudo, incluindo o uso de CTGF (um fator de crescimento do tecido conjuntivo -fator profibrótico - que desacelera a alveolarização, sendo produzido em ventilação com alto volume corrente). É importante que saibamos também (nos links) que a DBP associa-e com atraso na maturação cerebral ( 3, 8 vezes mais; IC a 95% de 1, 2 – 12 P=0, 023!) Através das discussões diárias na Unidade de Neonatologia do HMIB/SES/DF, implementamos a idéia que "menos é mais", evitando sempre que possível a ventilação mecânica e quando usada, pelo menor tempo possível, dando prioridade aos métodos de ventilação não invasiva (CPAP precoce, INSURE, MINI INURE, Ventilação não invasiva e mais recentemente, o uso de cânula de alto fluxo na extubação, ainda em teste na Unidade) e a prioridade na nutrição, principalmenteral (que evita a proteólise - a DBP é uma doença inflamatória proteolítica) com maior teor proteico.

Suporte respiratório minimamente invasivo no recém-nascido de muito baixo peso. Estamos prontos para isto? (Minimally invasive respiratory support in the vlbw infant. Are we ready for it? ) Autor(es): Eduardo Bancalari (Estados Unidos)/ Mats Bennow (Su écia). Realizado por Paulo R. Margotto Em 30 minutos Eduardo Bancalari tenta convencer-nos a não usar a ventilação mecânica (VM). A intubação na sala de parto faz diferença na explicação das diferentes taxas de displasia broncopulmonar (DBP) entre os Hospitais. Os autores mostraram que com a VM >24 horas, a odds ratio ajustada (chance) para displasia broncopulmonar (DBP) foi de 2, 4 e acima de 7 dias, a odds ratio ajustada foi de 14, 9. Este é um argumento para que possamos usar o menos tempo possível a VM nestes recém-nascidos. Então, como podemos evitar esta ventilação mecânica? (How can we keep babies off mechanical ventilation? ) Já lhes digo: não inicie a VM a menos que esteja claramente justificada. Use formas alternativas: CPAP nasal, NIPPV (nasal intermittent positive pressure ventilation). Descontinue a ventilação logo que possível; desmame agressivamente para um suporte respiratório menos invasivo. Esta é a mensagem quero deixar a todos aqui em Miami. Sei que nem sempre é possível, mas devemos sempre tentar.

Prevenção da displasia broncopulmonar (IX Congresso Íberoamericano de Neonatologia, Belo Horizonte, 20 -23/6/2012). Eduardo Bancalari (EUA). Realizado por Paulo R. Margotto Devemos sim usar o CPAP. Os números mostram que há uma tendência a um melhor desfecho nos RN tratados com CPAP do que aqueles tratados com ventilação mecânica (VM); talvez seja um pouco melhor do que intubar e ventilar todos eles. No entanto, não podemos dizer que com estas estratégias vamos conseguir diminuir a incidência de DBP. Outro comentário que deve ser feito aqui é sobre o uso prolongado do CPAP com pressões e Fi. O 2 altas. Todos vocês que tratam de prematuros sabem muito bem, que, ainda queiramos mantê-los em CPAP, muito destes prematuros por causa de apnéia severa, acabam sendo colocados em VM. Uma coisa é o que desejamos e outra coisa é o que precisamos fazer pelos nossos pacientes. Outra coisa que preciso mencionar é que a necessidade de VM varia muito entre uma e outra Unidade. Isto depende muito da experiência com o uso de CPAP, dos profissionais e da mentalidade daquela Unidade. Em Columbia, eles tem maior sucesso mantendo os RN somente em CPAP em comparação com outras Unidades, porque eles tem a filosofia de que a VM seja realmente muito prejudicial. Assim, fazem todo esforço para que os RN não sejam colocados na VM. Eu digo para vocês que a nossa posição é muito mais eclética. Não acreditamos no fanatismo. Não podemos levar estes RN ao extremo no CPAP, pois podemos causar muito mais prejuízos. Obviamente se intubamos um prematuro que precisa mais do que 30% de oxigênio, usamos imediatamente o surfactante o mais precoce possível, pois quanto mais tarde usar, menos eficaz ele é. Devemos fazer um equilíbrio racional entre usar a VM e não esperar um comprometimento importante causado por insuficiência respiratória grave.

Células-tronco mesenquimais para a displasia broncopulmonar: ensaio clínico fase 1 de escalação de dose Yun Sil Chang, So Yoon Ahn, Hye Soo Yoo et al. Apresentaçao: Danilo Lima Souza, Paulo R. Margotto Transplante Intratraqueal com baixa dose (1 x 107 células/kg) ou altadose (2 x 107 células/kg) h. UCB-derived MSCs (células-tronco mesenquimais derivadas do sangue umbilical humano em prétermos) não foi associado com eventos adversos. A severidade da DBP foi significativamente menor e a retinopatia da prematuridade com necessidade de cirurgia foi menos prevalente no grupo transplantado de MSCs com grupo controle. Esses achados indicam que o transplante intratraqueal de até 2 x 10 7 células/kg de h. UCB-derived MSCs em pré-termos pode ser seguro ou saudável. Neste estudo, a concentração da IL-6, IL-8, MMP-9, TNF-alfa, e TGF-beta 1 do aspirado traqueal foi significativamente reduzido após o transplante MSC

Células-tronco para a prevenção da doença pulmonar neonatal Autor(es): Bernard Thébaud (Canadá). 30 th International Workshop on Surfactant Replacement (Stockholm, Suécia, June 4 -6, 2015). Realizado por Paulo R. Margotto Como disse o Dr. Bancalari, em 2012, em Belo Horizonte por ocasião do IX Congresso Íberoamericano de Neonatologia, O maior desafio é a DBP que ocorre nos mais prematuros extremos (23 -24 -25 semanas) e esta DBP, acredito, que não vamos conseguir diminuir com a estratégias abordadas aqui. Para o tipo atual de DBP, vamos ter que ser muito mais sofisticados, muito mais inteligentes e temos que tentar investigar quais são os mecanismos que freiam o desenvolvimento do pulmão destes prematuros extremos, como a superexpressão do CTFG, fator profibrótico que desacelera o crescimento pulmonar. Outra possibilidade está no uso de células-tronco, instilando-as na traquéia destes RN, regenerando a alveolarização e formação de vasos. Será que vamos conseguir prevenir ou nunca a DBP? Se pegarmos um RN com 23 -2425 semanas, acredito que nunca vamos conseguir fazer com que estes pulmões respirando gás tenham um desenvolvimento totalmente normal. No entanto, a ciência está avançando em grande velocidade e acredito que podemos esperar resultados muito positivos nos próximos 3 -4 anos. Segundo Thébaud, semelhante ao benefício terapêutico relatado para as células-tronco derivadas da medula, estudos utilizando células-troncos de sangue de cordão umbilical relatam efeitos comparáveis no modelo induzida por hiperoxia de lesão pulmonar neonatal - melhor estrutura alveolar / restauração do crescimento alveolar, atenuação da fibrose pulmonar, redução da inflamação pulmonar, prevenção da deficiente angiogênese pulmonar e melhorou a capacidade de exercício. Além disso, os efeitos benéficos a longo prazo da administração de células-tronco do sangue do cordão não demonstraram efeitos adversos na idade adulta. Recentemente estudo coreano mostrou que a administração de células-tronco derivadas do sangue do cordão é viável, segura e eficaz (9 pré-termos com peso e idade gestacional médios de 793 g e 25, 3 entre 5 -14 dias de vida dependentes do ventilador). A análise dás radiografias seriadas, realizadas após 84 dias de transplante, não mostraram lesões em massa em campos pulmonares. Esta Apresentação na Suécia destacou a excitante translação do laboratório para o paciente na esperança de levar em um curto futuro, melhorias nos resultados pulmonares em nossos bebês prematuros.

Displasia broncopulmonar associa -se com atraso na maturação estrutural cerebral nos recémnascidos pré-termos Vera Neubauer, Daniel Junker, Elke Griesmaier, Michael Schocke, Ursula Kiechl. Kohlendorfer. Apresentação: Laura Haydée, Tatiane Dias e Paulo R. Margotto Usando variáveis selecionadas, a análise multivariada mostrou que a DBP associa-se com 3, 8 vezes mais (IC a 95% de 1, 2 – 12 p=0, 023) com atraso na maturação estrutural cerebral (interessante que todos, menos 1, usaram hidrocortisona!). RN com atraso na maturação cerebral recebeu ventilação por um período significativamente maior do que os RN com maturação normal, razão pela qual a troca da intubação orotraqueal por CPAP nasal é realizada imediatamente ou o quanto antes após a administração do surfactante (<6 horas). Estudo em animais (babuínos prematuros saudáveis) mostrou maior redução do volume da substância branca cerebral e da densidade interneuronal quando foram ventilados por tubo orotraqueal por 5 dias antes de alterar para CPAP nasal, comparativamente aos extubados em até 24 horas. Fatores implicados na etiologia da DBP, como inflamação/infecção e suporte nutricional inadequados já foram comprovadamente relacionados ao prejuízo no crescimento cerebral e desfechos adversos em pré-termos. A relação entre DBP e atraso na maturação cerebral é mais importante devido ao fato desta condição não ser totalmente prevenível, porém pode ser uma condição modificável.

O papel da nutrição na promoção do crescimento nas crianças pré-termos com displasia broncopulmonar: estudo de coorte prospectiva de intervenção não randomizado Gianni ML, Rogerro ML, Colnaghi MR et al. Apresentação: Roberto Farias, Fabiana Márcia Alcântara de Morais Altivo. O presente estudo de Gianni et al relatou que a maior ingesta calórica na displasia broncopulmonar (DBP) associouse com maior ganho de peso (média de 14 g/dia), porém sem crescimento em comprimento e no perímetro cefálico (oferta proteica em torno de 3, 2 g/kg/dia, uma oferta considerada insuficiente para estas crianças!). O problema de administrar mais calorias, resulta em mais gordura! A DBP é uma doença inflamatória que leva a proteólise e a única forma de contrabalancear, além de outros controles, é dar a eles mais proteína para que eles aumentem a síntese proteica de maneira a contrabalançar esta perda de proteína pela via inflamatória. Dando mais calorias para estas crianças e o que ocorre: o peso aumenta, o comprimento não aumenta em nada, assim como o perímetro cefálico (é este queremos que aumenta!) Dando mais caloria que precisamos para produzir proteína, esta energia extra vai virar tecido adiposo.

O leite humano influencia no desenvolvimento da displasia broncopulmonar? Spiegler J et al (German Neonatal Network). Realizado por Paulo R. Margotto Comparando 3 grupos (alimentação com leite humano exclusivo-fortificado/ fórmula exclusiva e mista), os autores, a partir de 1433 recém-nascidos entre 22+ o semanas a 31 + 6 semanas, demonstraram que os recém-nascidos de muito baixo peso (1500 g) alimentados exclusivamente com leite humano tiveram menor incidência de displasia broncopulmonar (DBP). A alimentação exclusiva com fórmula nestes bebês foi associado com aumento do risco de DBP (OR=2, 59 com IC a 95% de 1, 33 -5, 04), assim como de enterocolite necrosante (OR=12, 86 com IC a 95% de 2, 84 -58, 29) e retinopatia da prematuridade (OR=1, 80 com IC a 95% de 1, 05 -3, 11), além de que os alimentados com leite materno alcançaram a dieta enteral plena antes dos RN alimentados com fórmula. O leite materno tem propriedades antioxidantes que podem proteger o bebês do estresse oxidativo. O estresse oxidativo pode resultar do fornecimento de oxigênio necessário para manter a saturação arterial de oxigênio nos RN de MBP com DBP. No entanto, como já inclusive demonstrado entre nós pela Dra. Anna Christina do Nascimento Granjeiro Barreto, de Natal (nos links), os RN de muito baixo peso que recebem leite materno apresentam restrição do crescimento extrauterino. Devido o deficiente crescimento constituir um fator conhecido de risco para o desenvolvimento da DBP, causou surpresa nos autores do presente estudo, a diminuição da DBP com o uso de leite humano exclusivo. Até agora, estes autores não sabem se maior ganho de peso por causa da alimentação com fórmula, em comparação com o leite materno fortificado durante o curso neonatal no hospital, é desejável ou não. Mesmo que o ganho de peso inferior esteja associado a um risco aumentado de DBP, isto não parece ser aplicável para a redução do crescimento devido a alimentação do leite materno em presente coorte. Trouxemos também o estudo de Victora, recém publicado no Lancet (30/1/2016) sobre A amamentação no século 21: epidemiologia, mecanismos e efeito ao longo da vida. Em países de baixa renda e de renda média, apenas 37% das crianças com menos de 6 meses de idade são amamentadas exclusivamente. A presente metanálise indica a proteção contra infecções em crianças e má oclusão, maior inteligência e as reduções prováveis no excesso de peso e diabetes. Em entrevista à mídia, Victora informou que a ampliação da amamentação para um nível quase universal (ricos ou pobres) poderia evitar 823 000 mortes anuais em crianças menores de 5 anos e 20 000 mortes anuais por câncer de mama, além do câncer de ovário. A economia mundial que se obteria com a amamentação seria 330 bilhões de dólares no mundo! No Brasil, o vínculo mãe e filho pode resultar numa economia de 6 milhões/ano se 90% amamentassem até 6 meses.

Intervenção precoce leva a melhora a longo prazo no desenvolvimento nas crianças muito pré-termos, especialmente naquelas com displasia broncopulmonar J W P Van Hus, et al. Apresentaçao: Brunna Cintra, Danillo Amaral, Ecimar Gonçalves, Josiane Duarte, Natália Castro, Thiago Jefferson, Paulo R. Margotto Este artigo descreve os efeitos longitudinais de intervenção do IBAIP (Avaliação Infantil Comportamental e Programa de intervenção) sobre o desenvolvimento de crianças que nasceram muito prematuras e de muito baixo peso a partir dos 6 meses até cinco anos e meio de idade; No subgrupo de crianças de intervenção com displasia broncopulmonar (DBP), o desenvolvimento, tanto cognitivo e motor foi melhorado ao longo do tempo, com grandes efeitos. RN com DBP beneficiaram da intervenção, tanto em termos de desenvolvimento cognitivo e motor. A DBP tem sido freqüentemente relatada ter uma associação negativa com os resultados do desenvolvimento

Complicaçoes placentarias e displasia broncopulmonar: Estudo de Coorte EPIPAGE-2 He loi se Torchin, Pierre-Yves Ancel, Franc ois Goffinet et al. Apresentaçao: Vinicius Lourenço de Farias, Camila Valadares Santana Recch, Sylvia Telles Chicarino, Paulo R. Margotto Gravidez mediada por complicações placentárias está associado com desenvolvimento de quadro moderado a grave de displasia broncopulmonar (DBP), independentemente da idade gestacional e do peso ao nascer. Em contraste, desordens maternas sem consequências fetais não estão associadas ao risco de se desenvolver quadros de maior gravidade na BPD. Estes resultados levantam novas questões sobre os mecanismos relacionados aos distúrbios vasculares placentários e a DBP, sugerindo a programação fetal para desenvolvimento pulmonar. O risco de moderada a severa DBP, não diferiu entre as crianças com apenas distúrbios maternos e o grupo controle, mas permaneceu significativamente maior para aqueles com apenas distúrbios fetais (OR = 4, 2; 95% CI, 2, 1 -8, 6) e ambas as doenças maternas e fetais (OR = 2, 1; IC 95%, 1, 1 -3, 9).

Asssim, foi encontrada uma associação entre complicações na gravidez mediada pela placenta e a Displasia Broncopulmonar (DBP) moderada a grave, e se tiveram consequências fetais durante a gravidez. De fato, as crianças de ambos os grupos de complicações mediadas pela placenta com prénatal com suspeita de restrição do crescimento intrauterino (RCIU) tinham um risco maior de DBP moderada a severa, enquanto as taxas de DBP em grupo com transtornos maternos só não diferiram do grupo controle.

Displasia broncopulmonar: Mitos do manejo farmacológico (Bronchopulmonary dysplasia: Myths of pharmacologic management) Donn SM. Apresentação: Ana Luiza Alves, Paulo R. Margotto A displasia broncopulmonar é uma desordem frustrante que é muitas vezes difícil de gerenciar. Dependência crônica do ventilador e um sentimento de desesperança também leva ao uso generalizado de medicamentos farmacológicos que não possuem eficácia comprovada ou segurança, e o que pode prejudicar o processo de cura e agravar a situação. Como a DBP é um processo multifatorial, estudos adequados para determinar a eficácia e a segurança são difíceis e dispendiosos de se executar. O uso de agentes farmacológicos deve ser cuidadosamente escolhido para maximizar o benefício, minimizando danos

Primeiro, defina um objetivo terapêutico razoável. Em segundo lugar, defina a duração do tratamento para ver um efeito. Uma dose pode não ser suficiente, mas uma semana de terapia sem uma resposta pode ser muito longa. Em terceiro lugar, defina toxicidade e observe de perto por isso. Em quarto lugar, de forma relacionada, determine o risco: relação benefício Quinto, interrompa o medicamento se não funcionar ou se surgirem complicações.

DBP é um distúrbio multifatorial que afeta crianças recém nascidas com insuficiência respiratória. Terapias amplamente prescritas, incluindo diuréticos, broncodilatadores, e os medicamentos anti-refluxo não possuem evidências adequadas para apoiar seu uso rotineiro. Muitos desses agentes são realmente prejudiciais. Os estudos clínicos cuidando de bebês com DBP devem fazê-los sob os princípios de medicina baseada em evidências. O papel ideal da terapia com corticosteróides ainda não está definido. Os estudos mostraram eficácia e risco. Ensaios clínicos adicionais são necessários. Compreender a história natural da hipertensão pulmonar, acompanhar a DBP grave deve ser realizada antes de tentar tratá-las com drogas de eficácia ou segurança desconhecidas. Ensaios clínicos que avaliam agentes farmacológicos para tratar a DBP ou a suas complicações devem examinar resultados a longo prazo, bem como resultados a curto prazo.

Uso de diurético na displasia broncopulmonar Paulo R. Margotto (em preparação) Os diuréticos são um dos medicamentos mais freqüentemente prescritos na Unidade Neonatal de Terapia Intensiva (UTIN). Clark et al relataram que a furosemida era o sétimo medicamente mais comumente relatados na UTIN, com mais de 8% dos pacientes na UTIN expostos a este agente. Os diuréticos são frequentemente prescritos off-label (não há indicação do FDA [Food and Drug Administration]) aos recém-nascidos (RN) prematuros, particularmente na prevenção ou tratamento da displasia broncopulmonar (DBP). No estudo de coorte retrospectivo de Laughon, envolvendo 107. 542 recém-nascidos com idade gestacional <32 semanas e peso ao nascer <1500 g em 333 UTI Neonatais na Flórida, entre 1997 -2011, 39. 357 (37%) das crianças foram expostas a pelo menos um diurético, com o principal objetivo de reduzir ou tratar a DBP. Os expostos aos diuréticos tiveram menores idades geracionais e peso ao nascer (66% <1000 g). A primeira exposição ao diurético ocorreu em média 18 dias (9 -33 dias) e a sua duração média foi de 6 dias (2 -24 dias). Houve um aumento de 10% entre 1997(29%) e 2005 (39%), mantendo-se estável a seguir (36% em 2010). O diurético mais usado tem sido a furosemide (93%), sendo também o mais frequente em números de cursos e dias de uso. Em seguida, os mais usados foram espironolactona, clorotiazida, hidrocolorotiazida, bumetanide e acetazolamina. A combinação de diuréticos ocorreu em torno de 1/3 dos pacientes (19% e 6% usaram dois e diuréticos, respectivamente), sendo mais frequente furosemide + espironolactona, seguido por furosemide+ clorotiazida e clorotiazida + espironolactona. A maioria dos RN que recebeu diuréticos não estavam em assistência ventilatória mecânica.

A administração de diurético aos RN pré-termo com displasia broncopulmonar (DBP) tem sido praticado usado há mais de 30 anos (desde 1983 com o estudo de Kao LC et al, mostrando a diminuição aguda da resistência das vias aéreas nos RN com doença pulmonar crônica). Há uma variação entre as Instituições quanto ao tempo de uso, ocorrendo em 86% em um tempo curto(≤ 5 dias)-86% e em 40% em um tempo longo ( >5 dias). A furosemide tem sido o diurético mais prescrito (85%), embora a clorotiazida tenha sido do diurético de maior tempo de uso (mediana de 21 dias) (Slaughter JL et al)

Os estudos sobre o uso de diurético na DBP tem-se concentrado e das classes de diuréticos: diurético de alça, como a furosemida e diuréticos que atuam no túbulo distal, como a tiazida ou espirolactona. Em 1983, Kao LC et al evidenciaram que a furosemida, uma hora após a sua administração. diminui a resistência das vias aéreas, especificamente a condutância das vias aéreas e aumenta a complacência pulmonar, com melhora da dinâmica pulmonar, requerendo menores parâmetros ventilatórios. Os autores aribuíram a melhora da obstrução da via aérea pela remoção do edema pulmonar intersticial. Outras ações da furosemide incluem: produção de prostaglandina levando a vasodilatação pulmonar, inibição da contração da musculatura lisa brônquica e diminuição de fatores mediadores inflamatórios (Slaughter JL) A tiazida e espironolactona, atuando no túbulo distal, causando a menor anormalidades eletrolíticos, quando usadas isoladamente (não aumentam a excreção de cálcio). A espironolactona é um esteróide sintético que atua como um antagonista competitivo do receptor de aldosterona. Ao inibir a aldosterona, a espironolactona atenua a reabsorção de sódio e pouca perda de potássio, sendo um diurético usado em combinação com a tiazida, por esta característica (Sega JL). No entanto, quando usadas juntas, associam-se com hipercalciúria (Atkinson SA et al).

Hoffman DJ et al , em 33 crianças que receberam por duas semanas tiazida com espironolatona versos apenas tiazida, não foram observadas diferenças nos eletrólitos séricos, na necessidade para a reposição de sódio e potássio, assim como diferenças na mecânica pulmonar. Os autores explicam este achado a resposta parcial do túbulo distal a aldosterona. A inefetividade da espironolactona, um antagonista da aldosterona, em preservar o potássio, pode estar relacionado ao desenvolvimento renal destes pequenos prematuros. A função renal no prematuro antes de 34 semanas é limitada durante semanas pós-natal. A hiponatremia da prematuridade pode ser devida à resposta parcial do nefron distal a aldosterona (a função da aldosterona é aumentar a reabsorção de sódio e excretar potássio). A espironolactona age somente na presença de aldosterona. Se o nefron distal não reponde a aldosterona, especula-se que este também não reponde ao antagonista da aldosterona, resultando assim, numa perda de potássio. Em 1984, Kao LC et al, , em um estudo randomizado, duplo-cego e controlado com placebo em 10 pacientes não ventilados relataram que a combinação de clorotiazida (20 mg/kg/dose) e espironolactona (1, 5 mg/kg/dose), administrados duas vezes ao dia via oral, por 7 dias, resultou em diminuição significativa da resistência das vias aéreas e na complacência dinâmica pulmonar em comparação com o placebo. Os autores relatam aumento da excreção de fósforo e potássio.

Em 1989, Engelhardt et al, randomizaram 21 crianças com DBP em respiração espontânea para receberem espironolactona+ hidroclotiazida (3 mg/kg/dia de ambas) por 6 -8 dias. Não foram relatada melhora na mecânica pulmonar ou na oxigenação. Houve aumento da diurese, questionando-se assim se o aumento da diurese por si só seja responsável pela melhora da função pulmonar. Em 1994, Kao LC et al, com 43 pacientes com DBP recebendo clorotizazida e espironolactona ou placebo até 30 dias, relatam melhora da resistência das vias aéreas (31%; P<0, 05) e na complacência dinâmica pulmonar (46%; P<0. 001). No entanto no houve redução total nos dias requerendo oxigênio e a melhora na função pulmonar associada ao uso do diurético não se manteve após a sua descontinuação. Apesar do uso generalizado de diurético na DBP há poucos dados que avaliam o valor significativo desta terapia na DBP. Todas as três revisões sistemáticas da Cochrane, avaliando os riscos e benefícios diuréticos na DBP (furosemide, tiazida + espironolactona) mostram que o uso do diurético, apresenta melhorias na oxigenação e complacência pulmonar, mas esses benefícios fisiológicos a curto prazo não se traduzem em nenhum benefício clínico significativo como mortalidade, duração da ventilação mecânica, dependência de oxigênio e internação hospitalar.

Portanto. . . Antes do uso rotineiro de diuréticos sistêmicos na DBP recomendam-se estudos que demonstram efeitos a longo prazo, como sobrevivência, duração da oxigenação, dependência do ventilador e duração da internação, além do estudo das complicações. (Brion LP, 2001) Na nossa prática clínica reservamos o diurético para casos de edema pulmonar (o furosemide diminui o edema pulmonar, diminuindo a resistência vascular pulmonar: furosemide: 1 m/kg/dia) (Margotto, PR, 2013) De todas as terapias adjuntas o prematuro com DBP, a terapia diurética é uma das mais abusadas, sem evidência de benefícios substanciais. ( Tin Win, Eiswell T). Quando há ampla variabilidade na prática clínica do uso de diurético na DBP (Slaughter et al) não existe um padrão verdadeiro e é uma declaração sobre a falta de profundidade do nosso conhecimento nessa aplicação (Donn SM, 2007)

Em resumo quanto à Displasia Broncopulmonar. . . A prevalência de displasia broncopulmonar (DBP) em crianças em ventilação mecânica está inversamente relacionada à idade gestacional e ao peso ao nascer, apoiando o fato de que o desenvolvimento incompleto dos pulmões ou lesões durante uma janela crítica do desenvolvimento pulmonar influenciam o desenvolvimento de DBP. Além da prematuridade, vários outros fatores podem contribuir para a ruptura do crescimento alveolar e para o desenvolvimento vascular pulmonar, incluindo, entre outros, ventilação mecânica, toxicidade de oxigênio, infecção pré/ pós-natal, inflamação e restrição de crescimento ou déficits nutricionais. A predisposição genética é reconhecida por modificar ainda mais o risco de doença. É importante que saibamos que a DBP ocorre quase que exclusivamente em recém-nascidos prematuros que receberam ventilação de pressão positiva sugerindo que a hiperinsuflação pulmonar e o alongamento alveolar desempenham um papel crítico na patogênese da DBP. O achado comum de diminuição do risco de BPD fortalece recomendações para o uso de estratégias nãoinvasivas. Como resultado, muitas unidades agora estão optando por realizar um teste inicial com CPAP para gerenciar a SDR. Cuidados interdisciplinares para atender às complexas necessidades pulmonares, nutricionais e de desenvolvimento destes pacientes são críticos e podem influenciar os resultados da DBP grave Paulo R. Margotto

OBRIGADA! Dra. Evely Dra. Lara Staffs e Residentes da Unidade de Neonatologia do HMIB/SES/DF
- Slides: 61