Diseo de Nuevos Medicamentos Basado en la Estructura

Diseño de Nuevos Medicamentos Basado en la Estructura de los Blancos Farmacológicos Rafael A. Zubillaga Luna Departamento de Química Universidad Autónoma Metropolitana- Iztapalapa México, D. F.
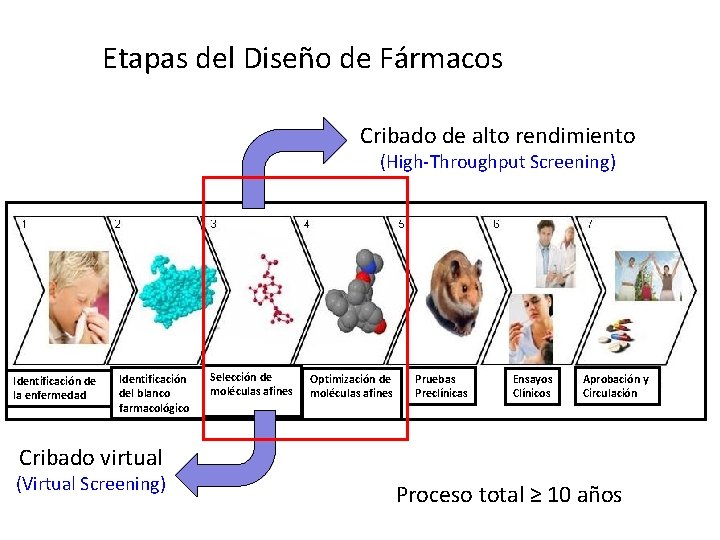
Etapas del Diseño de Fármacos Cribado de alto rendimiento (High-Throughput Screening) Identificación de la enfermedad Identificación del blanco farmacológico Selección de moléculas afines Optimización de moléculas afines Pruebas Preclínicas Ensayos Clínicos Aprobación y Circulación Cribado virtual (Virtual Screening) Proceso total ≥ 10 años

Selección de moléculas afines o identificación de “punteros” (lead identification) ____________

CRIBADO DE ALTO RENDIMIENTO (High-Throughput Screening) Método experimental de fuerza bruta en el cual miles, algunas veces millones de compuestos son ensayados robóticamente.
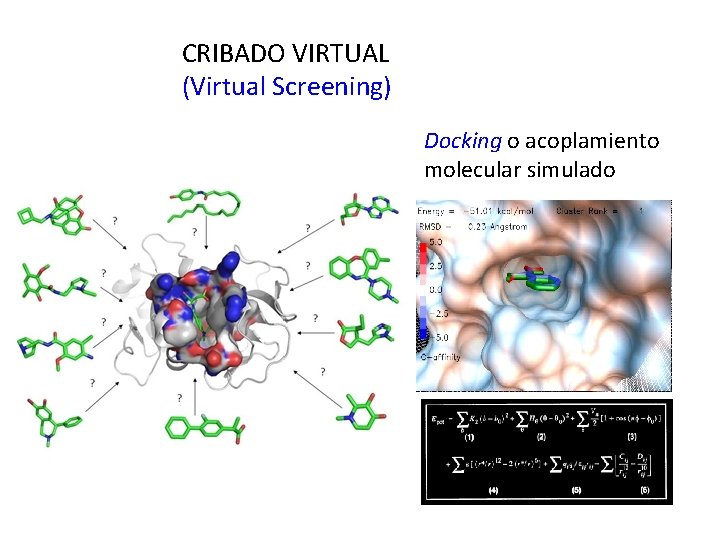
CRIBADO VIRTUAL (Virtual Screening) Docking o acoplamiento molecular simulado
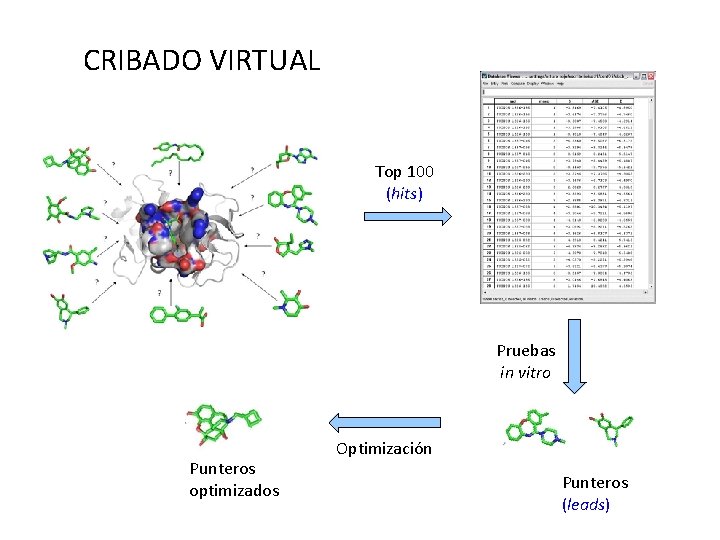
CRIBADO VIRTUAL Top 100 (hits) Pruebas in vitro Punteros optimizados Optimización Punteros (leads)

Optimización de “punteros” (Lead optimization)
![Receptor + Ku Complejo Ligando [Complejo] ___________ = [Receptor] [Ligando] Gu = -RT ln Receptor + Ku Complejo Ligando [Complejo] ___________ = [Receptor] [Ligando] Gu = -RT ln](http://slidetodoc.com/presentation_image_h/26f23745065c5a2a68950bfbb9bffff9/image-9.jpg)
Receptor + Ku Complejo Ligando [Complejo] ___________ = [Receptor] [Ligando] Gu = -RT ln Ku G u = Hu - T S u
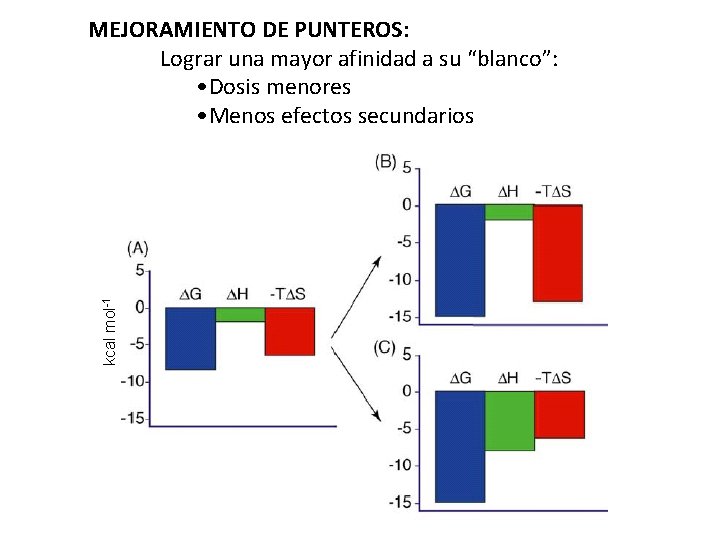
kcal mol-1 MEJORAMIENTO DE PUNTEROS: Lograr una mayor afinidad a su “blanco”: • Dosis menores • Menos efectos secundarios
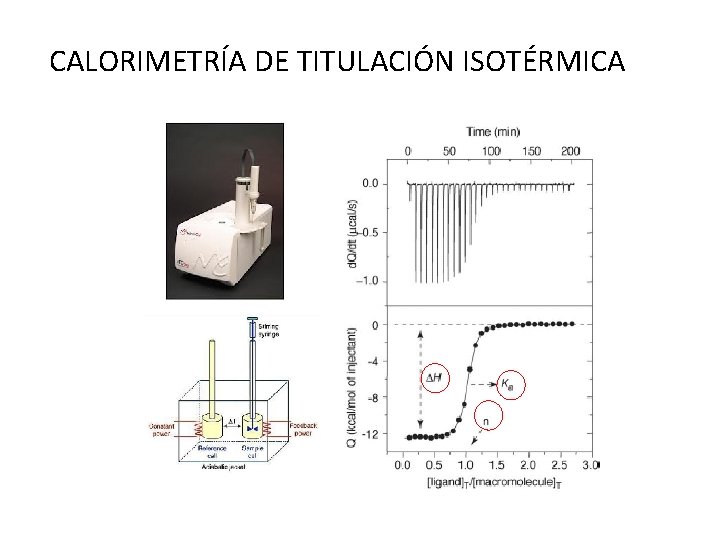
CALORIMETRÍA DE TITULACIÓN ISOTÉRMICA
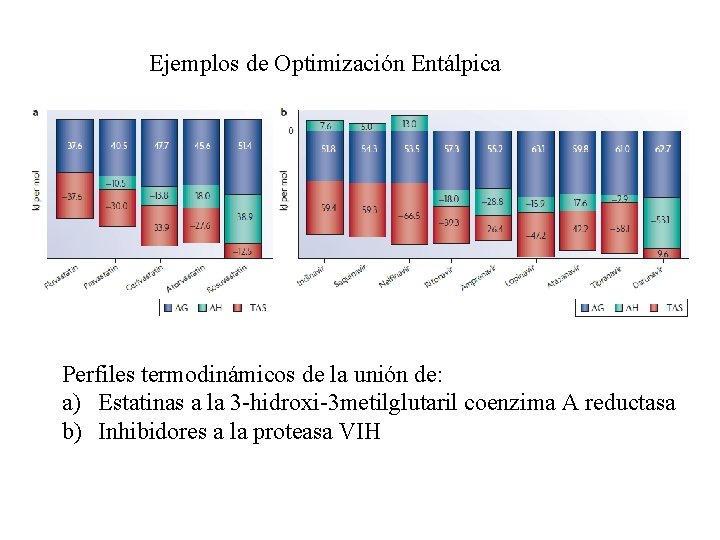
Ejemplos de Optimización Entálpica Perfiles termodinámicos de la unión de: a) Estatinas a la 3 -hidroxi-3 metilglutaril coenzima A reductasa b) Inhibidores a la proteasa VIH

Mejoramiento Entálpico: Más y/o mejores puentes de hidrógeno Mayor selectividad Mejoramiento Entrópico: Disminución de grados de libertad del fármaco libre. Aumento de superficie hidrofóbica de contacto (menor solubilidad).
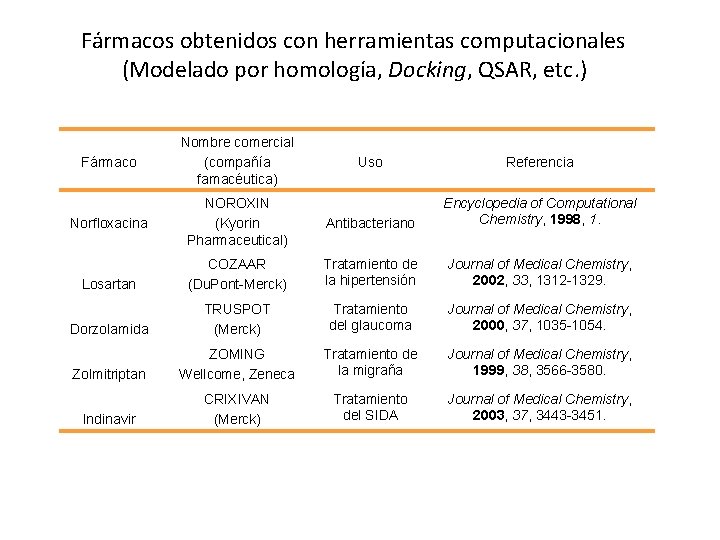
Fármacos obtenidos con herramientas computacionales (Modelado por homología, Docking, QSAR, etc. ) Fármaco Nombre comercial (compañía famacéutica) Norfloxacina Uso Referencia NOROXIN (Kyorin Pharmaceutical) Antibacteriano Encyclopedia of Computational Chemistry, 1998, 1. Losartan COZAAR (Du. Pont-Merck) Tratamiento de la hipertensión Journal of Medical Chemistry, 2002, 33, 1312 -1329. Dorzolamida TRUSPOT (Merck) Tratamiento del glaucoma Journal of Medical Chemistry, 2000, 37, 1035 -1054. Zolmitriptan ZOMING Wellcome, Zeneca Tratamiento de la migraña Journal of Medical Chemistry, 1999, 38, 3566 -3580. Indinavir CRIXIVAN (Merck) Tratamiento del SIDA Journal of Medical Chemistry, 2003, 37, 3443 -3451.

PRIMER BLANCO FARMACOLÓGICO: SUPERÓXIDO DISMUTASA de Taenia solium _________________
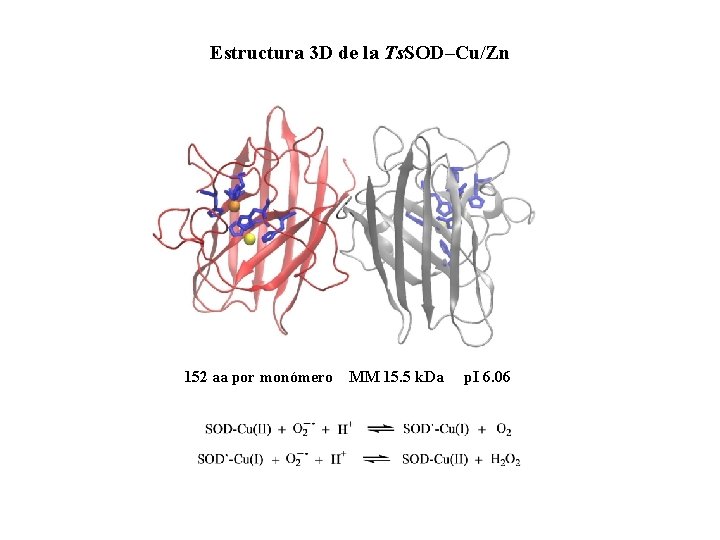
Estructura 3 D de la Ts. SOD–Cu/Zn 152 aa por monómero MM 15. 5 k. Da p. I 6. 06

Docking de la biblioteca Lead. Quest® sobre la estructura 3 D de la Ts. SOD–Cu/Zn Quimioteca Lead. Quest (~50 mil compuestos, 2 D) Hidrógenos/cargas (MMFF 24 x) Depuración de la biblioteca: Reglas de Lipinski. Eliminación de moléculas de agua, solvente y de grupos reactivos Búsqueda de confórmeros estructurales, 3 D ~2 millones de confórmeros, Econf≤ 3. 0 kcal/mol Preparación de la estructura de rayos X de Ts. SOD–Cu/Zn: asignación de cargas (CHARMM 27)/hidrógenos. Búsqueda de sitios potenciales de unión. Simulación del acoplamiento molecular P-L en sitios de potenciales de unión (15 mil orientaciones). Mejores diez complejos P-L (puntajes) de cada confórmero acoplado. (~20 millones de complejos P-L modelados) Segunda simulación de acoplamiento P-L Pero sólo de los compuestos que dieron más altos puntajes Sitios 1 y 2 500 compuestos con mejores puntajes P-L Minimización de la energía Selección de los mejores compuestos: Eint, puentes H, log. P, MM. 50 mejores compuestos Lead. Quest® para ensayos de inhibición
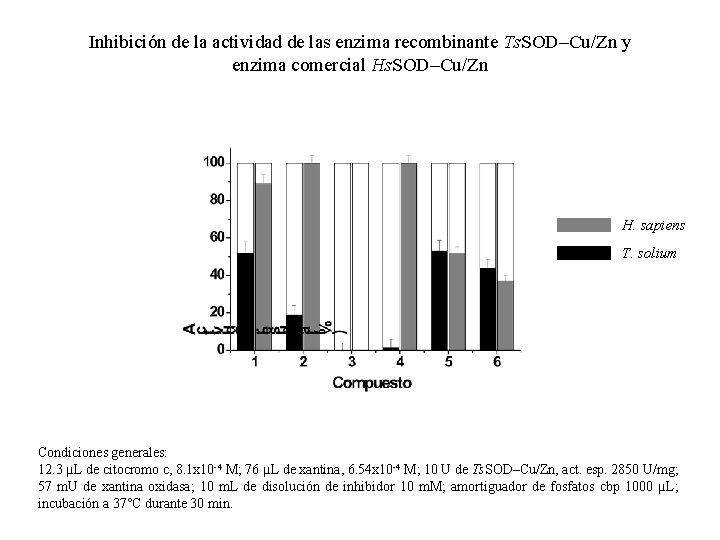
Inhibición de la actividad de las enzima recombinante Ts. SOD–Cu/Zn y enzima comercial Hs. SOD–Cu/Zn H. sapiens T. solium Condiciones generales: 12. 3 µL de citocromo c, 8. 1 x 10 -4 M; 76 µL de xantina, 6. 54 x 10 -4 M; 10 U de Ts. SOD–Cu/Zn, act. esp. 2850 U/mg; 57 m. U de xantina oxidasa; 10 m. L de disolución de inhibidor 10 m. M; amortiguador de fosfatos cbp 1000 µL; incubación a 37°C durante 30 min.

¿Qué sigue? • Comprar o sintetizar los compuestos 2 y 4. • Posibilidad de sintetizar compuestos similares con andamiajes moleculares diferentes acordes a la experiencia de síntesis chez nous. • Caracterizar por ITC la termodinámica de unión de 2 y 4 con Ts-SOD. • Realizar modificaciones in silico a las estructuras de 2 y 4 que propicien interacciones más favorables. • Evaluar in silico el cambio de afinidad (en términos de ΔGunión) provocado con las modificaciones anteriores. • Sintetizar las moléculas optimizadas y evaluar sus efectos inhibitorios.

SEGUNDO BLANCO FARMACOLÓGICO: Esc. N de Escherichia coli enteropatógena ___________________
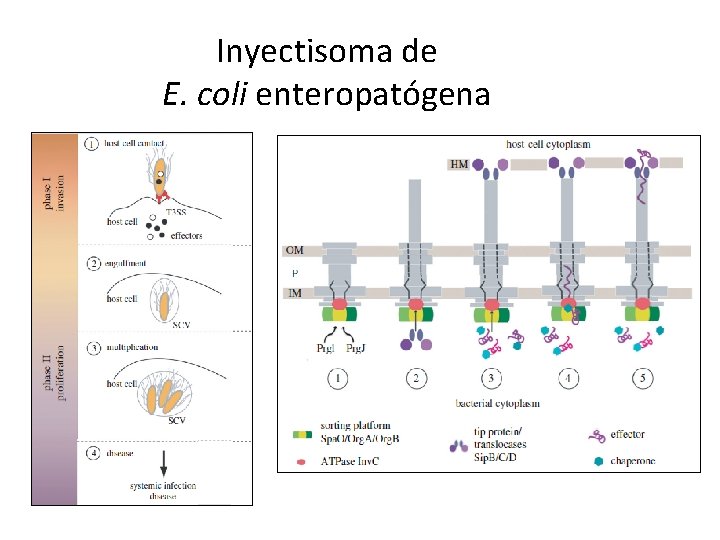
Inyectisoma de E. coli enteropatógena
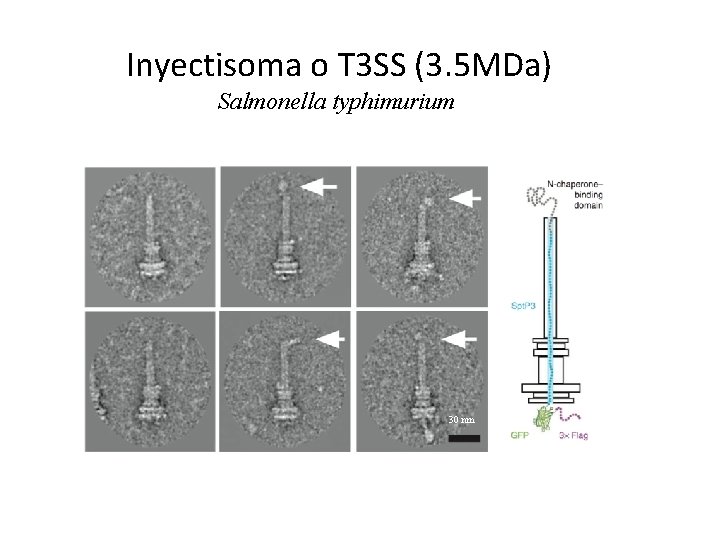
Inyectisoma o T 3 SS (3. 5 MDa) Salmonella typhimurium 30 nm
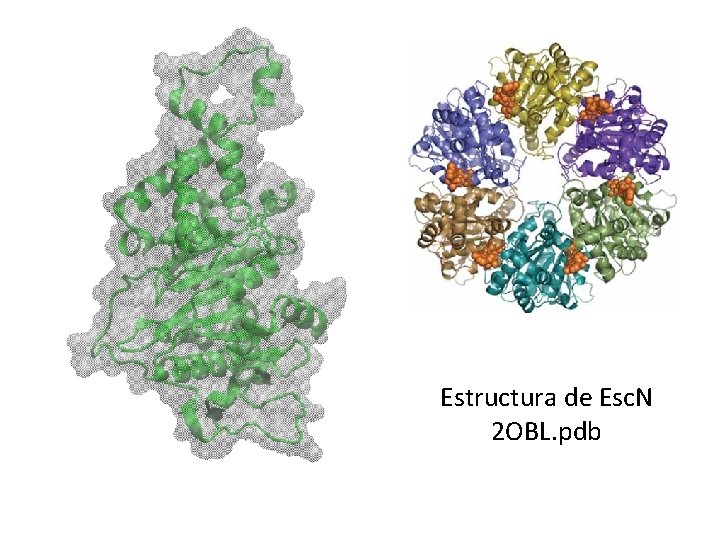
Estructura de Esc. N 2 OBL. pdb
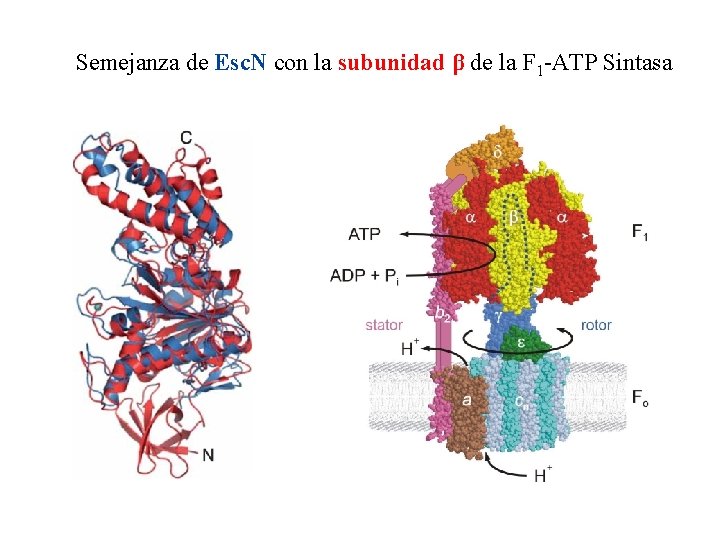
Semejanza de Esc. N con la subunidad β de la F 1 -ATP Sintasa

OBJETIVOS DE COLABORACIÓN: Poner a punto metodologías que permitan estimar diferencias en la energía libre de unión de al menos 2. 0 k. J/mol, al cambiar, suprimir o adicionar un grupo funcional al protofármaco. Sintetizar los compuestos punteros encontrados y sus formas optimizadas.
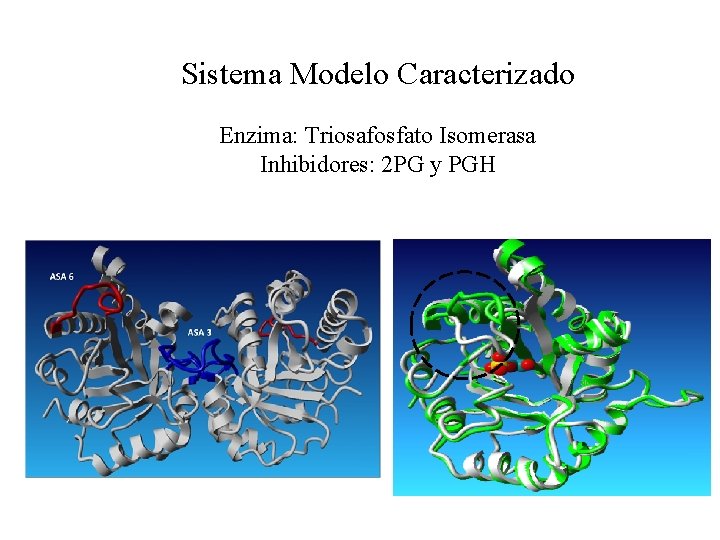
Sistema Modelo Caracterizado Enzima: Triosafosfato Isomerasa Inhibidores: 2 PG y PGH 27
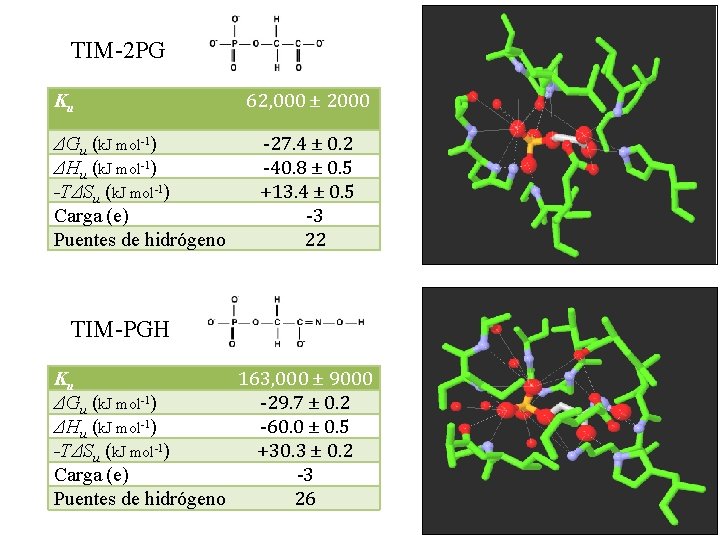
TIM-2 PG Ku ΔGu (k. J mol-1) ΔHu (k. J mol-1) -TΔSu (k. J mol-1) Carga (e) Puentes de hidrógeno 62, 000 ± 2000 -27. 4 ± 0. 2 -40. 8 ± 0. 5 +13. 4 ± 0. 5 -3 22 TIM-PGH Ku 163, 000 ± 9000 ΔGu (k. J mol-1) -29. 7 ± 0. 2 ΔHu (k. J mol-1) -60. 0 ± 0. 5 -TΔSu (k. J mol-1) +30. 3 ± 0. 2 Carga (e) -3 Puentes de hidrógeno 26 28







- Slides: 35