Disciplina Qumica Professor Rubens Barreto III Unidade Ligaes

Disciplina: Química Professor: Rubens Barreto III Unidade

Ligações Químicas
Tipos de Ligações iônicas Ligações covalentes Ligações metálicas
Os gases nobres e a regra do octeto Todas as substâncias químicas são formadas por átomos dos elementos químicos. A maioria das substâncias conhecidas é formada por átomos combinados, unidos.
. . . dos milhões de substâncias conhecidas, sabe-se de apenas seis nas quais existem átomos não-combinados. Os gases nobres Hélio (He), neônio (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe) e radônio (Rn). Já que os gases nobres não tendem a se combinar, tudo indica que possuir uma eletrosfera semelhante à de um gás nobre permite o átomo estabilizar-se.
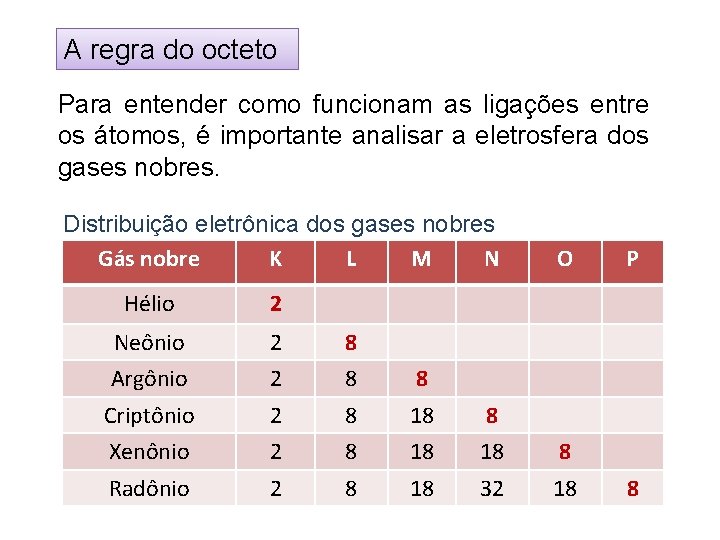
A regra do octeto Para entender como funcionam as ligações entre os átomos, é importante analisar a eletrosfera dos gases nobres. Distribuição eletrônica dos gases nobres Gás nobre K L M N O Hélio 2 Neônio Argônio 2 2 8 8 8 Criptônio Xenônio 2 2 8 8 18 18 8 Radônio 2 8 18 32 18 P 8

William Kossel e Gilbert Newton Lewis (1916) – Propuseram uma regra para interpretar a ligação entre átomos, que ficou conhecida como regra do octeto de elétrons. Um átomo estará estável quando sua última camada possuir 8 elétrons (ou 2, caso se trate da camada K). . os átmos não-estáveis se unem uns aos outros a fim de adquirir essa configuração de estabilidade.

Ligação iônica, eletrovalente ou heteropolar Vamos considerar a reação entre o sódio e o cloro, produzindo-se cloreto de sódio: Na + Cl → Na. Cl Nesse exemplo, o átomo de sódio cede definitivamente 1 elétron ao átomo de cloro.
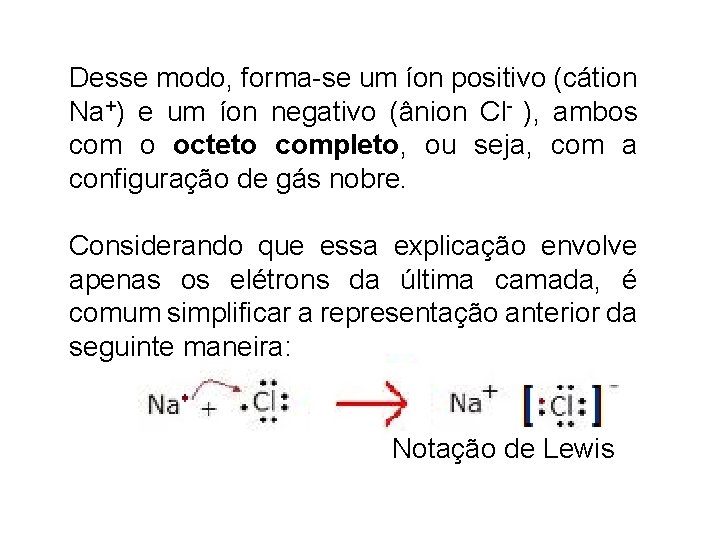
Desse modo, forma-se um íon positivo (cátion Na+) e um íon negativo (ânion Cl- ), ambos com o octeto completo, ou seja, com a configuração de gás nobre. Considerando que essa explicação envolve apenas os elétrons da última camada, é comum simplificar a representação anterior da seguinte maneira: Notação de Lewis
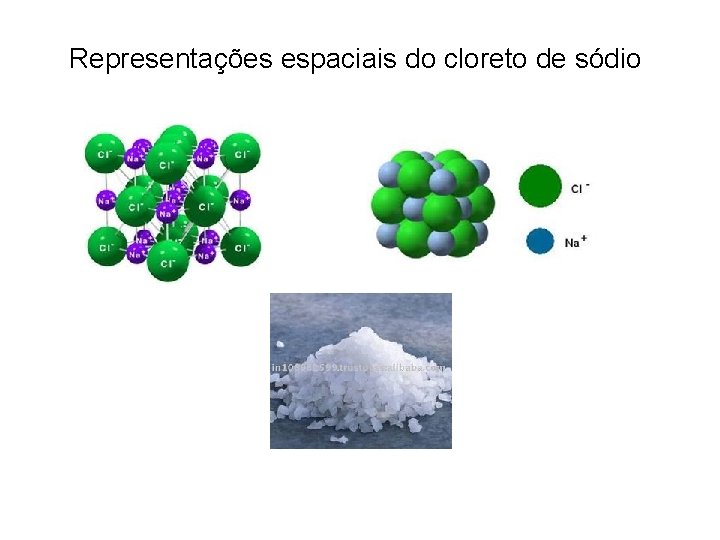
Representações espaciais do cloreto de sódio

Agora é a sua vez: 1. Faça a representação da ligação do magnésio com o cloro, formando o cloreto de magnésio. 2. Faça a representação da ligação do alumínio com o fluor, formando o fluoreto de alumínio. 3. Faça a representação da ligação do alumínio com o oxigênio, formando o óxido de alumínio.

Ligação iônica é a força que mantêm os íons unidos, depois que um átomo cede definitivamente um, dois ou mais elétrons para outro átomo. A ligação iônica é geralmente, bastante forte e mantêm os íons firmemente “presos” no retículo. Por isso, os compostos iônicos são sólidos e, em geral, tem ponto de fusão e de ebulição elevados.

A ligação iônica ocorre, em geral entre átomos de metais com átomos de nãometais, pois: Ø os átomos dos metais possuem 1, 2 ou 3 elétrons na última camada e têm forte tendência a perdê-los, Ø os átomos dos não-metais possuem 5, 6, ou 7 elétrons na última camada e têm acentuada tendência a receber mais 3, 2 ou 1 elétron e, assim completar seu octetos eletrônicos.
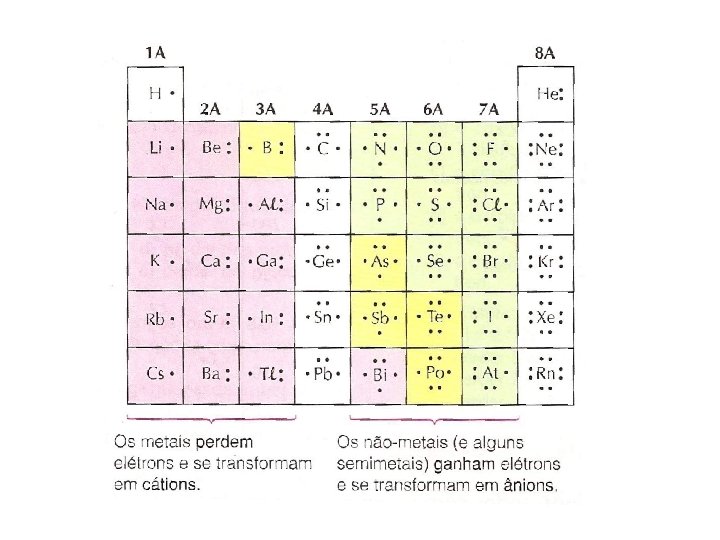
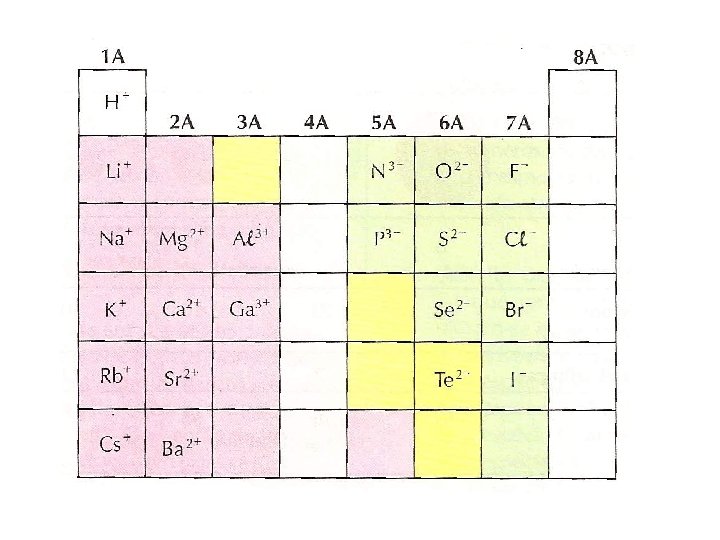

A ligação iônica e a Tabela Periódica
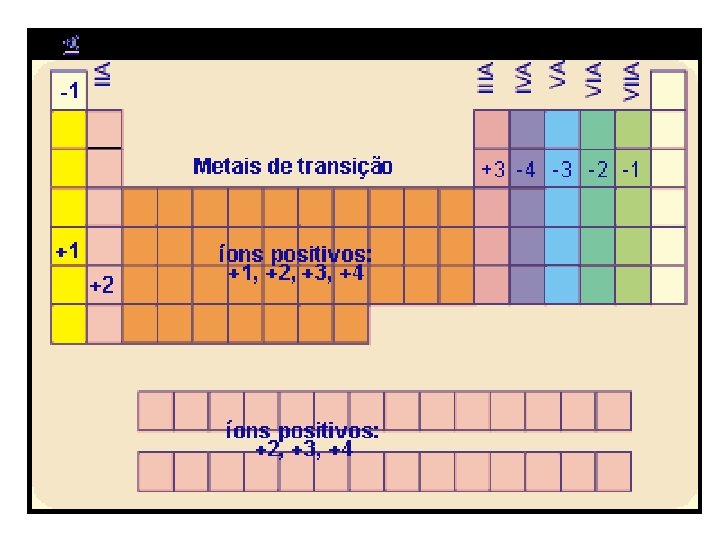

O tamanho do íon Quando um átomo perde elétrons, o núcleo passa a atrair mais intensamente os elétrons restantes; desse modo, o diâmetro ou raio do cátion é sempre menor que o diâmetro ou raio do átomo original.
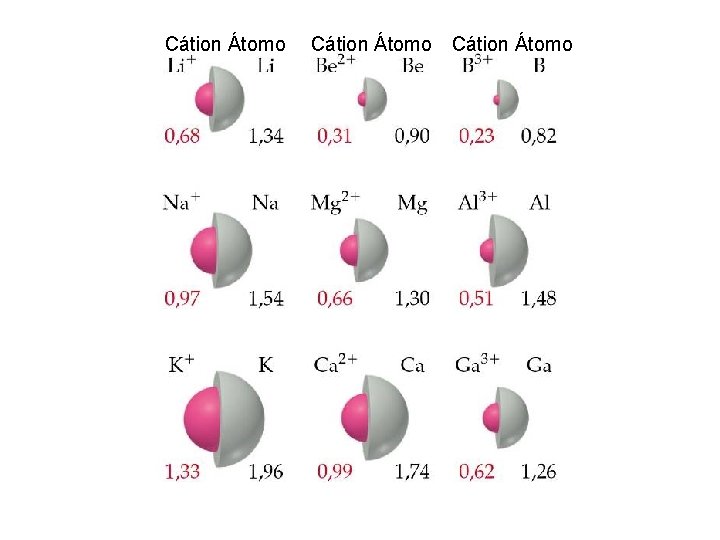
Cátion Átomo

Ao contrário, quando um átomo recebe elétrons, a carga total da eletrosfera (negativa), torna-se maior do que a carga do núcleo (positiva); desse modo, a atração do núcleo sobre o conjunto dos elétrons é menor e, consequentemente, o raio do ânion é sempre maior que raio do átomo original.
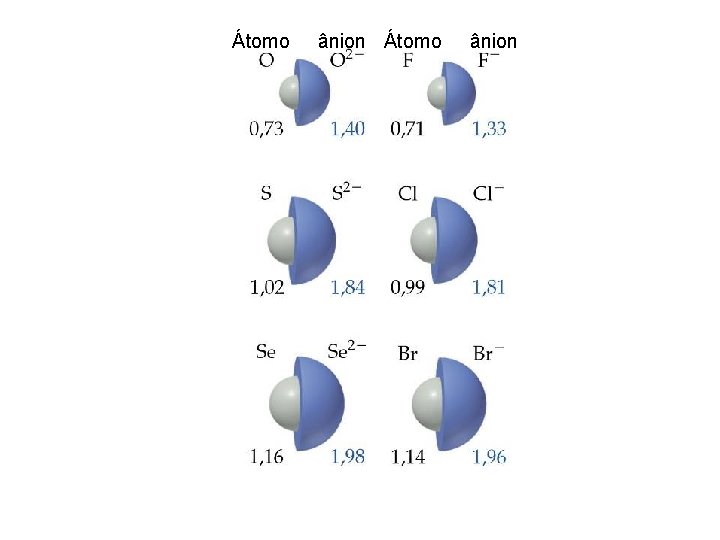
Átomo ânion

Ligação covalente Consideremos, como primeiro exemplo, a união entre dois átomos do elemento hidrogênio (H) para formar a molécula da substância simples hidrogênio (H 2): H + H → H 2
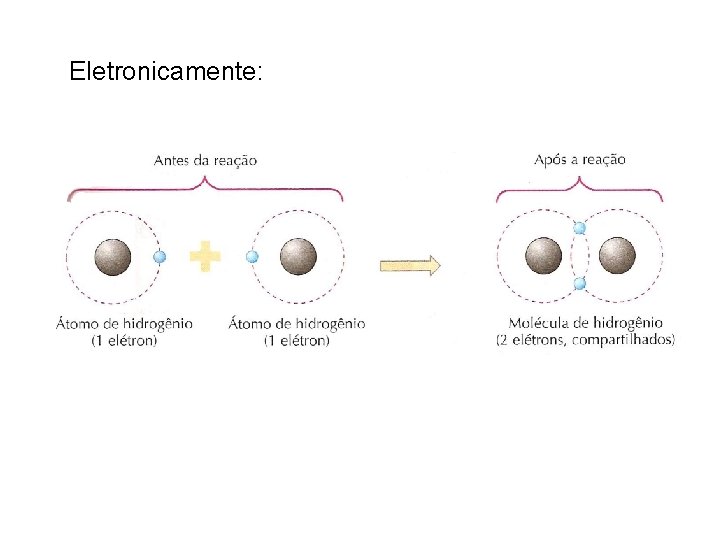
Eletronicamente:
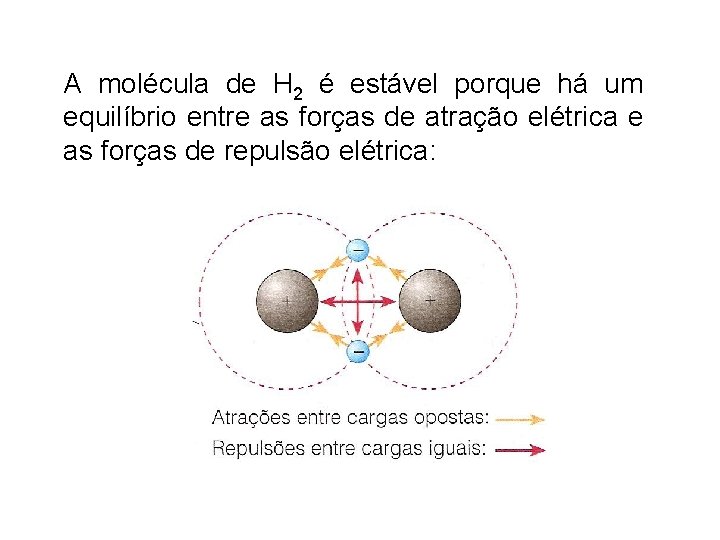
A molécula de H 2 é estável porque há um equilíbrio entre as forças de atração elétrica e as forças de repulsão elétrica:
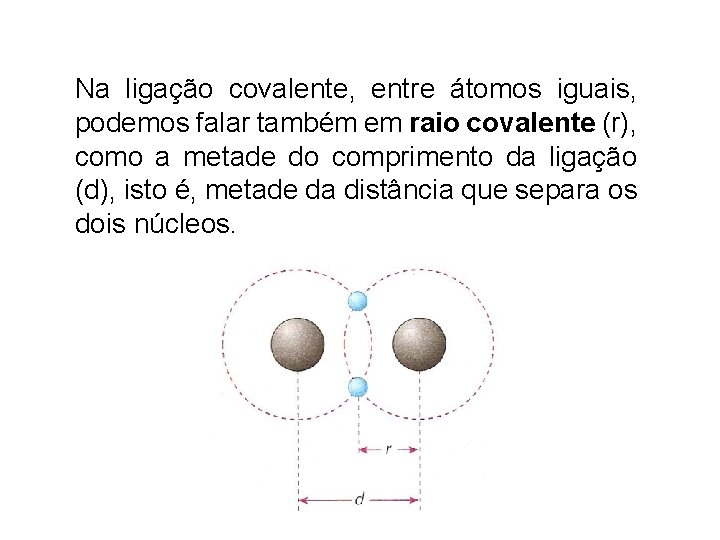
Na ligação covalente, entre átomos iguais, podemos falar também em raio covalente (r), como a metade do comprimento da ligação (d), isto é, metade da distância que separa os dois núcleos.

Por fim, observe que cada átomo de hidrogênio dispõe de dois elétrons, fazendo com que o hidrogênio adquira a configuração do gás nobre hélio. Exemplos de ligações covalentes: Cl 2 ; F 2 ; I 2 O 2 N 2

Ligação covalente ou covalência é a união entre átomos estabelecida pelo compartilhamento de pares de elétrons. Podemos dizer que a ligação é covalente quando os átomos apresentam a tendência de ganhar elétrons.

Fórmulas das substâncias moleculares: representações de Lewis e fórmulas estruturais. H 2 HCl H 2 O CO 2 NH 3 N 2 148

Ela ocorre quando dois átomos têm 4, 5, 6 ou 7 elétrons na última camada eletrônica (e mais o hidrogênio). Em outras palavras a ligação covalente ocorre entre dois átomos de não metais, ou ainda, entre esses elementos e o hidrogênio.
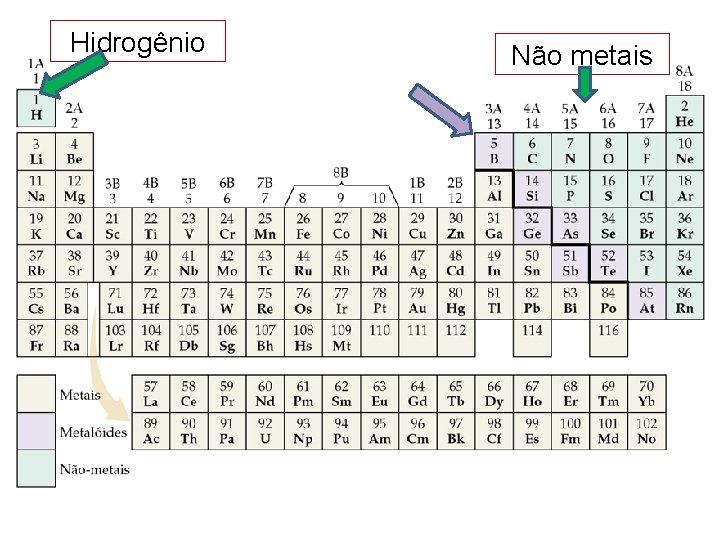
Hidrogênio Não metais

Caso particular de ligação covalente Essa ligação é semelhante à covalente comum, e ocorre entre um átomo que já atingiu a estabilidade eletrônica e outro ou outros que necessitem de dois elétrons para completar sua camada de valência.

O exemplo clássico dessa ligação é o dióxido de enxofre (SO 2). Nesse caso, o enxofre estabelece uma dupla ligação com um dos oxigênios, atingindo a estabilidade eletrônica (oito elétrons na camada de valência). A seguir, o enxofre compartilha um par de seus elétrons com o outro oxigênio, através de uma ligação covalente dativa ou coordenada.

Sua vez. . . Outra situação semelhante acontece com o anidrido sulfúrico (SO 3). Faça a representação dessa ligação.
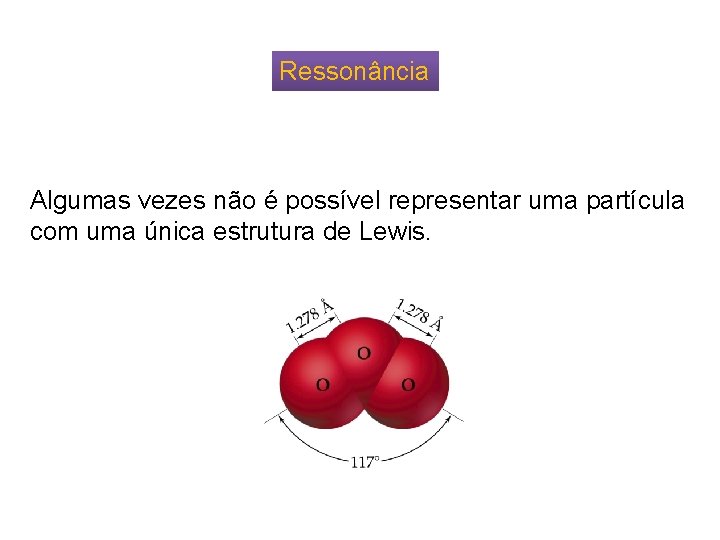
Ressonância Algumas vezes não é possível representar uma partícula com uma única estrutura de Lewis.
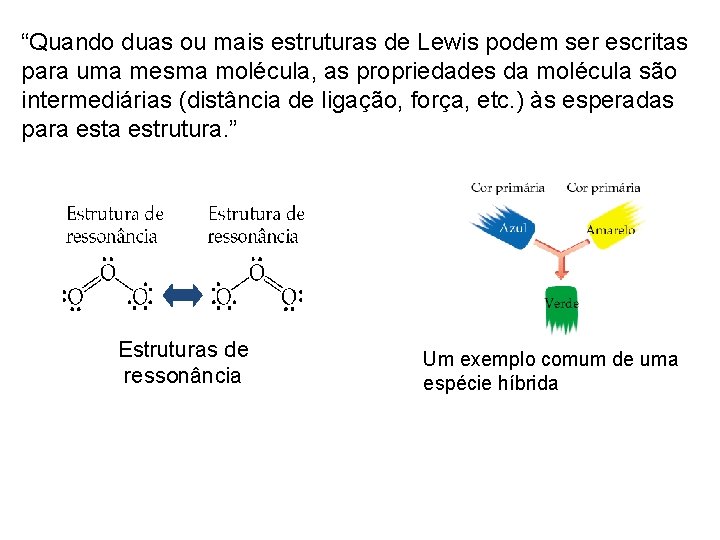
“Quando duas ou mais estruturas de Lewis podem ser escritas para uma mesma molécula, as propriedades da molécula são intermediárias (distância de ligação, força, etc. ) às esperadas para estrutura. ” Estruturas de ressonância Um exemplo comum de uma espécie híbrida

Eletronegatividade A atração exercida por um átomo sobre o par de elétrons na sua camada de valência depende da carga nuclear efetiva e da distância entre os núcleos e a camada de valência. “A eletronegatividade é a tendência relativa mostrada por um átomo ligado em atrair o par de elétrons da ligação. ”
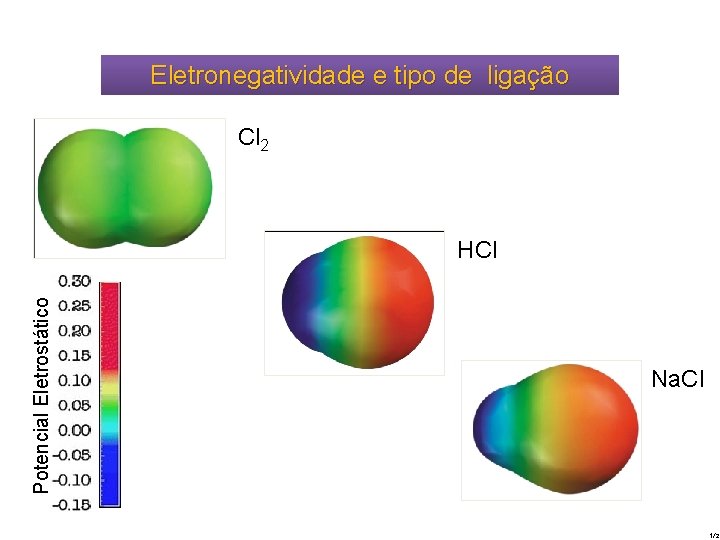
Eletronegatividade e tipo de ligação Cl 2 Potencial Eletrostático HCl Na. Cl 1/2
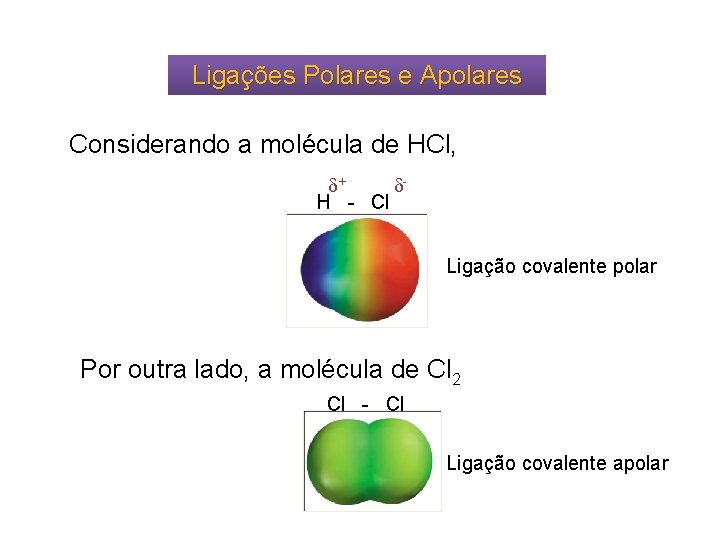
Ligações Polares e Apolares Considerando a molécula de HCl, + H - Cl Ligação covalente polar Por outra lado, a molécula de Cl 2 Cl - Cl Ligação covalente apolar

• Uma ligação covalente será polar sempre que os átomos que estabelecem esse ligação possuírem diferentes eletronegatividades. • Quando os átomos envolvidos na ligação possuirem a mesma eletronegatividade, a ligação é dita apolar.
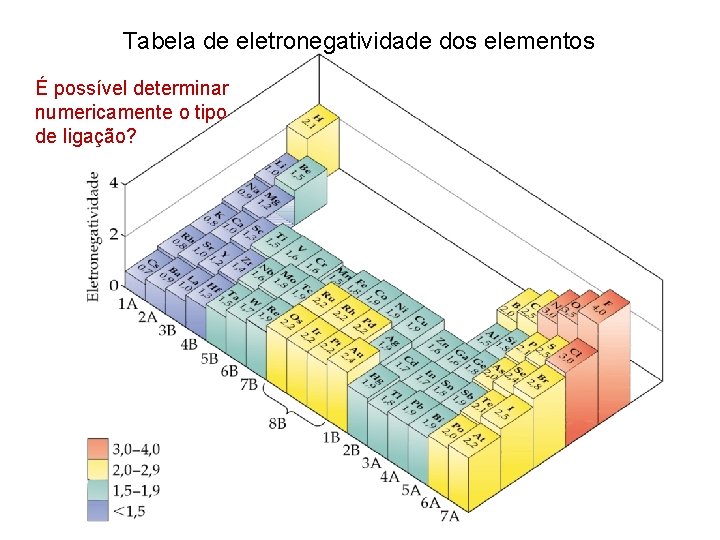
Tabela de eletronegatividade dos elementos É possível determinar numericamente o tipo de ligação?

A medida que a diferença de eletronegatividade aumenta, os elétrons passam a ser cada vez mais predominantemente atraídos por um dos átomos. A ligação iônica pode ser considerada como um caso extremo da ligação covalente polar, onde a diferença de eletronegatividade é tão grande que o elétron é transferido de um átomo para o outro em vez de ser compartilhado por ambos. Em geral, quando a diferença de eletronegatividade é maior que 1, 7 a ligação é considerada iônica. Valores abaixo de 1, 7 indicam que a ligação é predominantemente covalente.
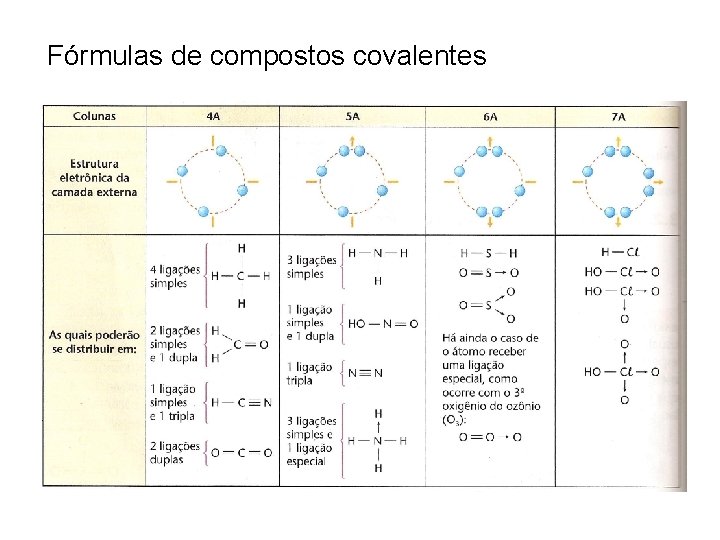
Fórmulas de compostos covalentes

Compostos moleculares e compostos iônicos Um composto é considerado composto molecular quando apresenta exclusivamente ligações covalentes. ex. : H 2 O, CO 2 e SO 3 Caso contrário, ele será considerado um composto iônico. ex. : Na. Cl, Na. NO 3 e Na 2 SO 4

Exceções a regra do octeto ü Moléculas com octeto incompleto (ex. : BF 3) üMoléculas com átomos com mais de 8 elétrons na camada de valência (ex. : H 3 PO 4). üCompostos com átomos com a camada de valência com número impar de elétrons (ex. : NO 2). ü Compostos dos gases nobres (Xe. F 2).

A ligação metálica Propriedades dos metais ü Brilho metálico üMaleabilidade üDuctibilidade üResistência a tração üAlta condutibilidade elétrica e térmica

O modelo do mar de elétrons ü Os átomos metálicos estão arranjados em retículo compacto. Cada átomo perde um ou mais elétrons. Os íons metálicos resultantes são chamados “troncos” dos átomos; ü Os elétrons se movem livremente dentro dos limites do cristal metálico; ü Os elétrons estão retidos dentro do cristal pela atração coulômbica dos troncos de átomos. Os troncos de átomos são mantidos juntos por atração eletrostática mútua dos elétrons.
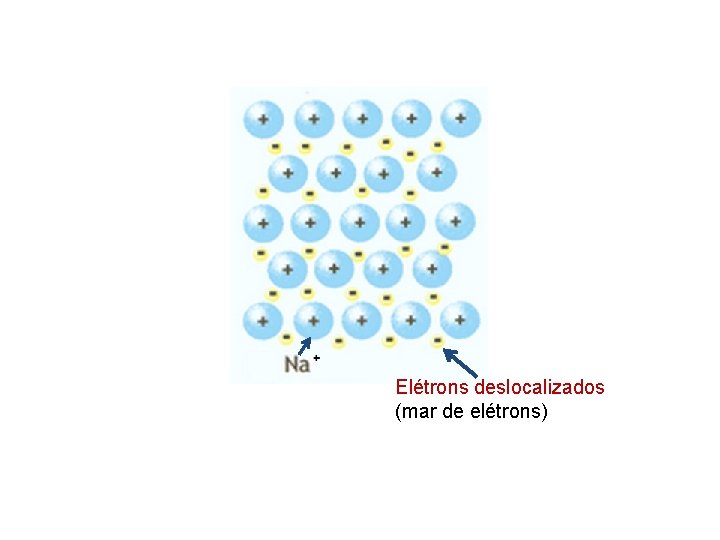
Elétrons deslocalizados (mar de elétrons)

Ligas Metálicas Misturas sólidas de dois ou mais elementos, sendo que a totalidade (ou pelo menos a maior parte) dos átomos presentes é de elementos metálicos. Ex. : -“Ouro 18 quilates” (ouro + cobre) - Bronze (cobre + estanho) - Latão (cobre e zinco) - Aço (ferro + carbono) 152 moedas

Composição e aplicação de algumas ligas metálicas
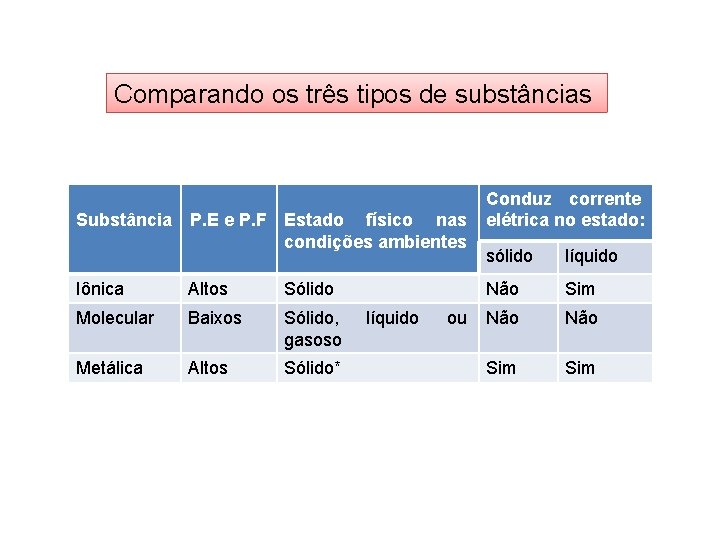
Comparando os três tipos de substâncias Substância P. E e P. F Estado físico nas condições ambientes Iônica Altos Sólido Molecular Baixos Sólido, gasoso Metálica Altos Sólido* líquido ou Conduz corrente elétrica no estado: sólido líquido Não Sim

Materiais Semicondutores - Germânio, silício, carbono* - Tipos de semicondutores - Funcionamento - Algumas aplicações: (Diodos, LED, CI, placas solares.

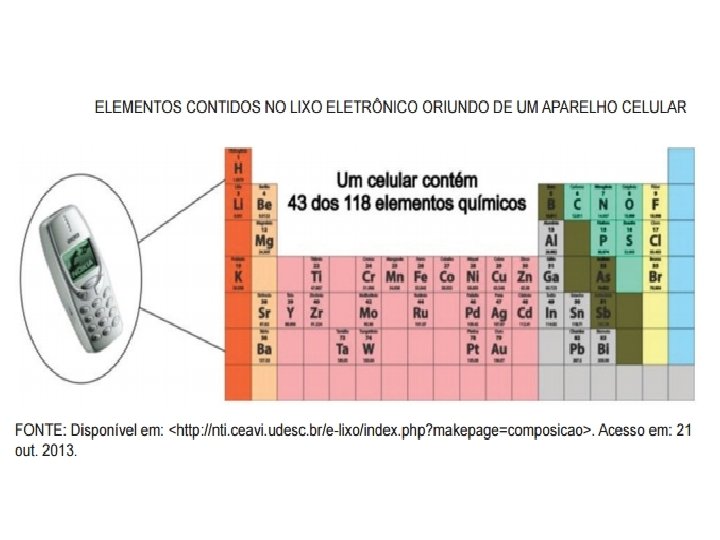
Lixo eletrônico
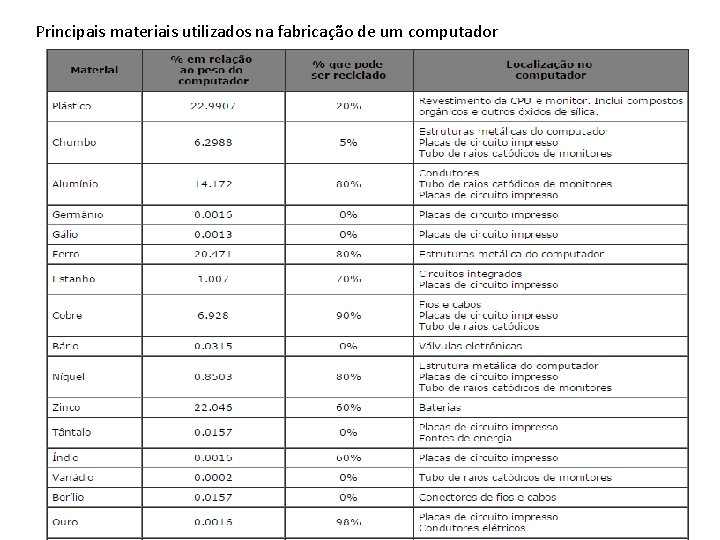
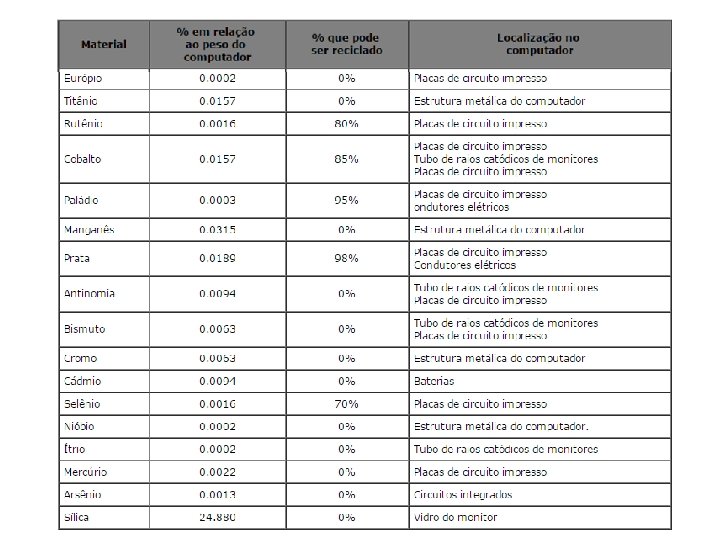
Principais materiais utilizados na fabricação de um computador
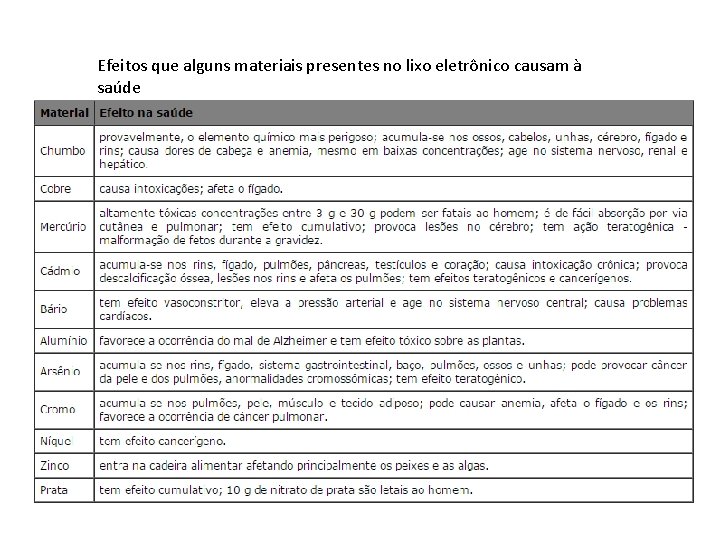
Efeitos que alguns materiais presentes no lixo eletrônico causam à saúde
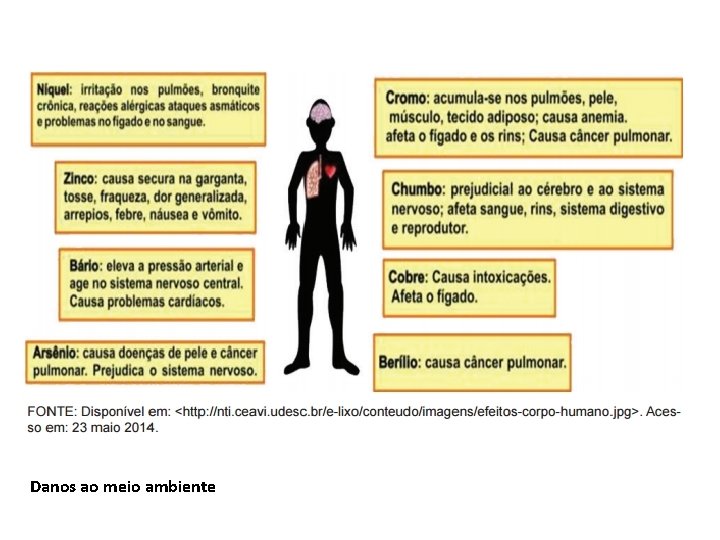
Danos ao meio ambiente
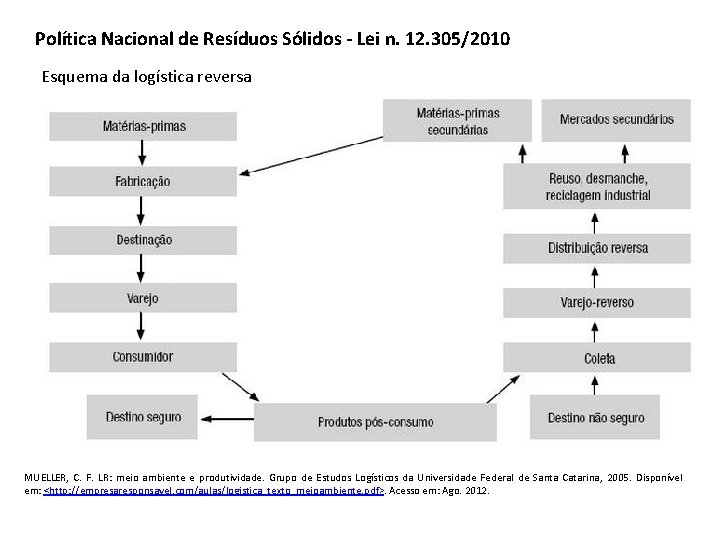
Política Nacional de Resíduos Sólidos - Lei n. 12. 305/2010 Esquema da logística reversa MUELLER, C. F. LR: meio ambiente e produtividade. Grupo de Estudos Logísticos da Universidade Federal de Santa Catarina, 2005. Disponível em: <http: //empresaresponsavel. com/aulas/logistica_texto_meioambiente. pdf>. Acesso em: Ago. 2012.
- Slides: 58