Direktorat Registrasi Obat Tradisional Suplemen Kesehatan dan Kosmetik

Direktorat Registrasi Obat Tradisional, Suplemen Kesehatan dan Kosmetik

OUTLINE Sistem Registrasi OT & SK Regulasi di Bidang Registrasi OT & SK Clustering & Registrasi OT & SK Simplifikasi Roadmap Penerapan TTE & 2 D Barcode

Sistem Registrasi OT & SK 3
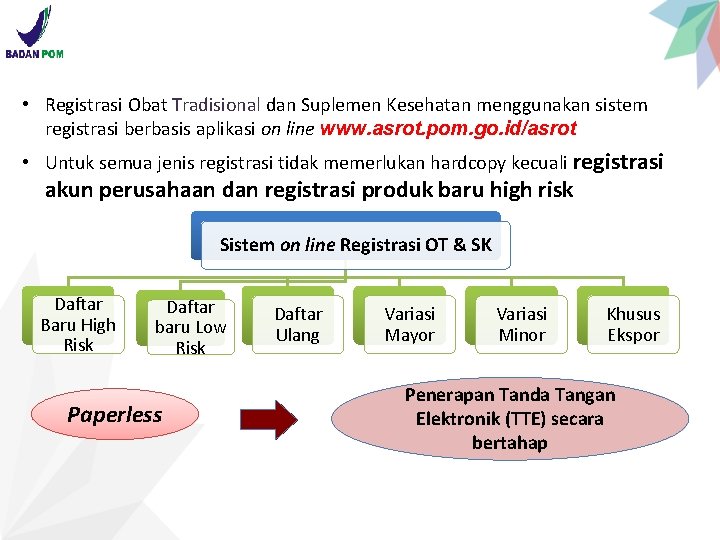
• Registrasi Obat Tradisional dan Suplemen Kesehatan menggunakan sistem registrasi berbasis aplikasi on line www. asrot. pom. go. id/asrot • Untuk semua jenis registrasi tidak memerlukan hardcopy kecuali registrasi akun perusahaan dan registrasi produk baru high risk Sistem on line Registrasi OT & SK Daftar Baru High Risk Daftar baru Low Risk Paperless Daftar Ulang Variasi Mayor Variasi Minor Khusus Ekspor Penerapan Tanda Tangan Elektronik (TTE) secara bertahap

Jenis Unggah/ upload Hardcopy Lokal DOKUMEN PENDAFTARAN AKUN PERUSAHAAN Impor • Izin usaha (jika sudah ada) • Sertifikat Cara Pembuatan yg Baik jika ada / Sertifikat CPOTB Bertahap • NPWP/ NIB (Nomor Induk Berusaha) • Surat Kuasa Bermaterai sebagai Penanggung Jawab Akun • SIUP (jika sudah ada) • NPWP/ NIB (Nomor Induk Berusaha)/ API • Surat Kuasa Bermaterai sebagai Penanggung Jawab Akun • Fotokopi Izin usaha (jika sudah ada) • SIUP (jika sudah ada) • Sertifikat Cara Pembuatan yg Baik jika ada / Sertifikat CPOTB Bertahap • Berita Acara Hasil Pemeriksaan untuk importir baru • Berita Acara Hasil Pemeriksaan (untuk industri pangan yg akan mendaftar suplemen kesehatan) • NPWP/ NIB (Nomor Induk Berusaha)/API (fotokopi) • NPWP/ NIB (Nomor Induk Berusaha) (fotokopi) • Surat Kuasa Bermaterai sebagai Penanggung Jawab Akun • Akta Notaris Pendirian Perusahaan • Surat Persetujuan Fasber Obat dan SK (untuk industri farmasi) 5

• Pada pendaftaran akun perusahaan selain Izin Usaha/ Industri di bidang obat tradisional juga melampirkan NIB (Nomor Induk Berusaha). NIB adalah identitas Pelaku Usaha yang diterbitkan oleh Lembaga Online Single Submission setelah Pelaku Usaha melakukan Pendaftaran. • Izin Komersial atau Operasional adalah izin yang diterbitkan oleh Lembaga OSS sesuai ketentuan peraturan perundang-undangan, setelah Pelaku Usaha mendapatkan Izin Usaha dan untuk melakukan kegiatan komersial atau operasional dengan memenuhi persyaratan dan/atau Komitmen. • Komitmen adalah pernyataan Pelaku Usaha untuk memenuhi persyaratan Izin Komersial atau Operasional.

Peraturan BPOM No. 26 tahun 2018 tentang Pelayanan Perizinan Berusaha Terintegrasi secara Elektronik sektor Obat dan Makanan Pasal 7 ayat (2) huruf a: Selain harus memenuhi persyaratan sebagaimana dimaksud pada ayat (1), untuk memperoleh Izin Edar Obat Tradisional dalam negeri, Pelaku Usaha sebagaimana dimaksud dalam Pasal 6 juga harus memenuhi persyaratan dokumen administratif sebagai berikut: sertifikat CPOTB atau sertifikat CPOTB Bertahap bagi UKOT dan/atau UMOT; Ø Pendaftaran Akun Perusahaan (UKOT dan UMOT Baru) harus sudah memiliki sertifikat CPOTB Bertahap Ø UKOT yang telah memiliki akun perusahaan melampirkan Surat komitmen bermaterai yang menyatakan bahwa akan melakukan pengurusan sertifikat CPOTB bertahap sesuai dengan bentuk sediaan yang diproduksi dan bukti pengurusan di Balai Setempat
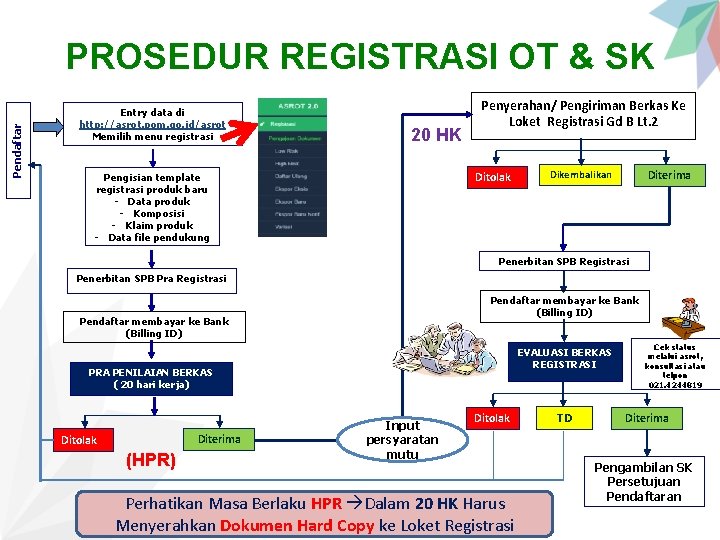
Pendaftar PROSEDUR REGISTRASI OT & SK Entry data di http: //asrot. pom. go. id/asrot Memilih menu registrasi 20 HK Penyerahan/ Pengiriman Berkas Ke Loket Registrasi Gd B Lt. 2 Ditolak Pengisian template registrasi produk baru - Data produk - Komposisi - Klaim produk - Data file pendukung Diterima Dikembalikan Penerbitan SPB Registrasi Penerbitan SPB Pra Registrasi Pendaftar membayar ke Bank (Billing ID) EVALUASI BERKAS REGISTRASI PRA PENILAIAN BERKAS ( 20 hari kerja) Diterima Ditolak (HPR) Input persyaratan mutu Ditolak Perhatikan Masa Berlaku HPR Dalam 20 HK Harus Menyerahkan Dokumen Hard Copy ke Loket Registrasi TD Cek status melalui asrot, konsultasi atau telpon 021. 4244819 Diterima Pengambilan SK Persetujuan Pendaftaran

Regulasi di Bidang Registrasi OT & SK 9

REGULASI DI BIDANG REGISTRASI OT jdih. pom. go. id UU No. 36 tahun 2009 Kesehatan PERMENKES No. 007 tahun 2012 Registrasi Obat Tradisional Keputusan Kepala Badan Pengawas Obat dan Makanan RI No. HK. 00. 05. 41. 1384 tahun 2005 Kriteria dan Tata Laksana Pendaftaran Obat Tradisional, Obat Herbal Terstandar, Proses Revisi dan Fitofarmaka Keputusan Kepala Badan Pengawas Obat dan Makanan RI No. HK. 00. 05. 4. 2411 tahun 2004 Ketentuan Pokok Pengelompokan Dan Penandaan Obat Bahan Alam Indonesia Peraturan Kepala Badan POM No. 12 tahun 2014 Persyaratan Mutu Obat Tradisional Peraturan Presiden No. 32 Tahun 2017 Jenis dan Tarif Atas Jenis Penerimaan Negara Bukan Pajak Peraturan BPOM No. 26 tahun 2018 Pelayanan Perizinan Berusaha Terintegrasi Secara Elektronik sektor Obat dan Makanan Peraturan BPOM No. 27 tahun 2018 Standar Pelayanan Publik di Lingkungan BPOM Proses Revisi

REGULASI DI BIDANG REGISTRASI SK jdih. pom. go. id Undang-undang No. 9 Tahun 1999 Perlindungan Konsumen Peraturan Pemerintah 72/ 1998 Pengamanan Sediaan Farmasi dan Alat Kesehatan Peraturan Kepala Badan Pengawas Obat Kriteria dan Tata Laksana Pendaftaran dan Makanan RI Nomor Suplemen Makanan Proses Revisi HK. 00. 05. 41. 1381 Tahun 2005 Peraturan Presiden No. 32 Tahun 2017 Jenis dan Tarif Atas Jenis Penerimaan Negara Bukan Pajak Peraturan Kepala BPOM No. 26 tahun 2018 Pelayanan Perizinan Berusaha Terintegrasi Secara Elektronik sektor Obat dan Makanan Peraturan BPOM No. 27 tahun 2018 Standar Pelayanan Publik di Lingkungan BPOM Peraturan BPOM No. 16 Tahun 2019 Pokok Pengawasan Suplemen Kesehatan Peraturan BPOM No. 17 Tahun 2019 Persyaratan Mutu Suplemen Kesehatan 11

Persyaratan Mutu OT & SK Parameter Uji SUPLEMEN KESEHATAN Peraturan BPOM No. 17 Tahun 2019 OBAT TRADISIONAL Perka BPOM No. 12 Tahun 2014 & Surat Edaran Batas Residu Pelarut Lampiran II Surat Edaran No. HK. 04. 02. 421. 12. 17. 1673 tanggal 11 Desember 2017 tentang Pelarut yang Diizinkan Digunakan dalam Proses Ekstraksi/ Fraksinasi Tumbuhan dalam Produk Obat Bahan Alam dan Suplemen Kesehatan beserta Batasan Residunya. Bahan Penggunaan Bahan Tambahan Lampiran III 1. 2. 3. Surat Edaran No. HK. 04. 01. 421. 12. 17. 1666 tanggal 11 Desember 2017 tentang Batas Maksimum Penggunaan Pemanis Buatan yang Diizinkan dalam OT dan SK Surat Edaran No. HK. 04. 01. 421. 12. 17. 1672 tanggal 11 Desember 2017 tentang Jenis Pengawet dan Batas Maksimal Penggunaannya dalam Obat Bahan Alam dan Suplemen Kesehatan Perka BPOM No. 12 Tahun 2014 (Pewarna) Penggunaan Bahan Tambahan harus sesuai ketentuan: a. Produk dengan proses rekonstitusi (contoh: produk efervesen), penggunaan bahan tambahan dihitung terhadap produk siap konsumsi, kecuali bahan pengawet. b. Penggunaan kombinasi bahan tambahan mengikuti ketentuan rasio penggunaan kurang dari atau sama dengan 1 (satu).
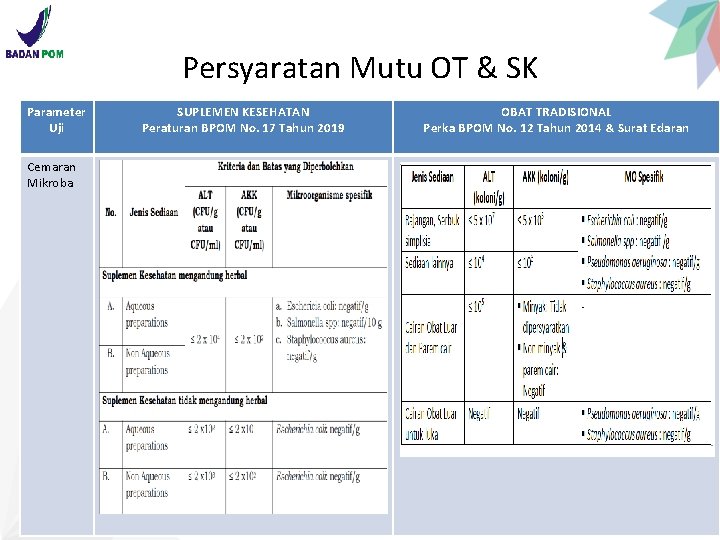
Persyaratan Mutu OT & SK Parameter Uji Cemaran Mikroba SUPLEMEN KESEHATAN Peraturan BPOM No. 17 Tahun 2019 OBAT TRADISIONAL Perka BPOM No. 12 Tahun 2014 & Surat Edaran

KETENTUAN PERALIHAN Peraturan BPOM No. 17 Tahun 2019 • Pelaku Usaha di bidang Suplemen Kesehatan yang telah mendapatkan izin edar sebelum berlakunya Peraturan Badan ini wajib menyesuaikan dengan ketentuan dalam Peraturan Badan ini paling lama 2 (dua) tahun terhitung sejak Peraturan Badan ini diundangkan. Max. 29 Juli 2021

§ Clustering Registrasi OTSK § Simplifikasi (Notifikasi) Reg OTSK Komposisi Tunggal Tertentu 15
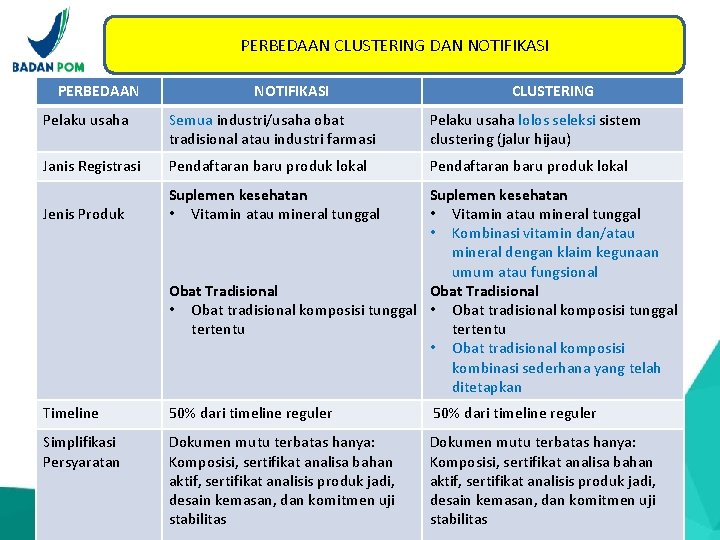
PERBEDAAN CLUSTERING DAN NOTIFIKASI PERBEDAAN NOTIFIKASI CLUSTERING Pelaku usaha Semua industri/usaha obat tradisional atau industri farmasi Pelaku usaha lolos seleksi sistem clustering (jalur hijau) Janis Registrasi Pendaftaran baru produk lokal Jenis Produk Suplemen kesehatan • Vitamin atau mineral tunggal Timeline 50% dari timeline reguler Simplifikasi Persyaratan Dokumen mutu terbatas hanya: Komposisi, sertifikat analisa bahan aktif, sertifikat analisis produk jadi, desain kemasan, dan komitmen uji stabilitas Suplemen kesehatan • Vitamin atau mineral tunggal • Kombinasi vitamin dan/atau mineral dengan klaim kegunaan umum atau fungsional Obat Tradisional • Obat tradisional komposisi tunggal tertentu • Obat tradisional komposisi kombinasi sederhana yang telah ditetapkan
LATAR BELAKANG & TUJUAN Latar Belakang 1. Keberpihakan negara pada pelaku usaha untuk menggerakan perekonomian 2. Perbaikan pelayanan publik dibidang registrasi OT, SK dan Kosmetik 3. Keterbatasan SDM di unit layanan publik Tujuan v Umum: Meningkatkan perdagangan/ komersialisasi produk v Khusus: • Mempermudah pelaku usaha dalam memperoleh izin edar. • Simplifikasi proses
KONSEP DASAR Clustering pelaku usaha berdasarkan compliance terhadap persyaratan evaluasi pre market dan pengawasan post market Pemberian insentif untuk perusahaan yang mempunyai track record yang baik dari sisi pre dan post market JALUR HIJAU BENEFIT KONSEKUENSI
KONSEP DASAR • Simplifikasi persyaratan registrasi • Percepatan timeline evaluasi (4 kategori*) • Untuk registrasi baru produk dalam negeri BENEFIT KONSEKUENSI • Memberikan komitmen untuk memenuhi ketentuan • Menjadi prioritas sampling/ audit/ inpeksi oleh Ditwas • Status Jalur Hijau diberikan dalam jangka waktu 1 tahun • Bila terjadi pelanggaran maka status Jalur Hijau akan dicabut dan dikembalikan ke Jalur Reguler.
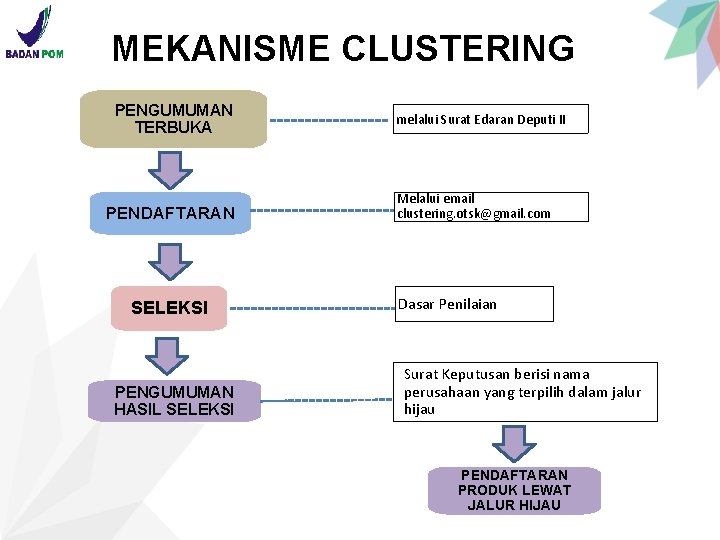
MEKANISME CLUSTERING PENGUMUMAN TERBUKA PENDAFTARAN SELEKSI PENGUMUMAN HASIL SELEKSI melalui Surat Edaran Deputi II Melalui email clustering. otsk@gmail. com Dasar Penilaian Surat Keputusan berisi nama perusahaan yang terpilih dalam jalur hijau PENDAFTARAN PRODUK LEWAT JALUR HIJAU
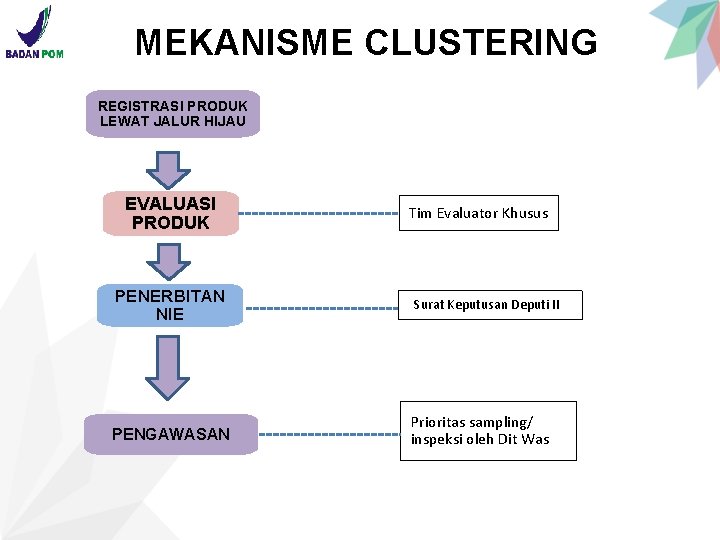
MEKANISME CLUSTERING REGISTRASI PRODUK LEWAT JALUR HIJAU EVALUASI PRODUK Tim Evaluator Khusus PENERBITAN NIE Surat Keputusan Deputi II PENGAWASAN Prioritas sampling/ inspeksi oleh Dit Was

DASAR PENILAIAN JALUR HIJAU REGISTRASI OTSK Persyaratan Tidak pernah terlibat dalam tindak pidana di bidang obat dan makanan umum Tertib dokumen administrasi (tidak melakukan pemalsuan dokumen, telah melakukan pembaharuan izin produksi) Mempunyai sertifikat CPOB/ CPOTB/CPOTB minimal tahap 2&3 sesuai sediaan yang didaftarkan Memiliki apoteker atau tenaga teknis kefarmasian sebagai penanggung jawab regitrasi Tidak menggunakan biro jasa dalam pengurusan izin edar

DASAR PENILAIAN JALUR HIJAU REGISTRASI OTSK Persyaratan Tidak melakukan pelanggaran di bidang OTSK (BKO, OT ilegal, masuk public warning) Khusus Tidak pernah masuk dalam public warning dalam 2 tahun terakhir Tidak Pernah mendapatkan peringatan keras Di utamakan bagi perusahaan yang telah memiliki sistem pelaporan efek samping Diberlakukan untuk OTSK produksi dalam negeri (lokal)

PENDAFTARAN CLUSTERING Pendaftaran perusahaan dapat dilakukan melalui email clustering_otsk@gmail. com dengan melampirkan : • Surat Izin Industri/ Sertifikat Produksi yang masih berlaku • Sertifikat CPOB/CPOTB/CPOTB bertahap minimal tahap 2 yang masih berlaku. • Surat Penunjukan Apoteker atau Tenaga Teknis Kefarmasian sebagai penanggung jawab registrasi dari pimpinan perusahaan. • Surat penyataan bermaterai bahwa tidak pernah terlibat dalam tindak pidana di bidang obat dan makanan. • Surat pernyataan bermaterai tentanggung jawab pendaftar dan kebenaran & keabsahan dokumen registrasi. • Surat pernyataan bermaterai tidak menggunakan biro jasa dalam pengurusan izin edar.

PERBANDINGAN JALUR REGULER DAN JALUR HIJAU KETERANGAN JALUR REGULER JALUR HIJAU Timeline Sesuai Perka BPOM 50% dari timeline sesuai Perka BPOM Jenis pendaftaran Semua jenis pendaftaran Pendaftaran produk baru Kategori produk Semua jenis produk a. Obat tradisional : Komposisi sederhana, non OHT & FF b. Suplemen Kesehatan: Vitamin atau mineral tunggal, Kombinasi vitamin dan/atau mineral dengan klaim general atau fungsional Simplifikasi persyaratan Dokumen lengkap: adminitrasi, mutu, keamanan & kemanfaatan Dokumen mutu terbatas hanya: Komposisi, sertifikat analisa bahan aktif, sertifikat analisis produk jadi, desain kemasan, dan komitmen uji stabilitas
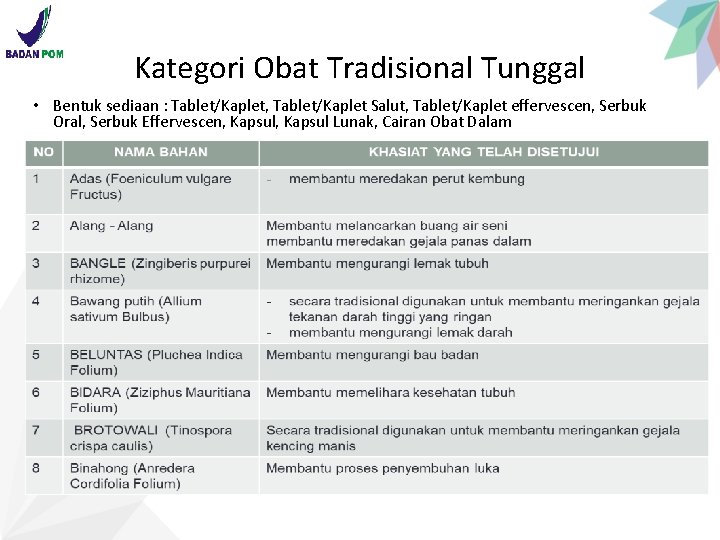
Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam
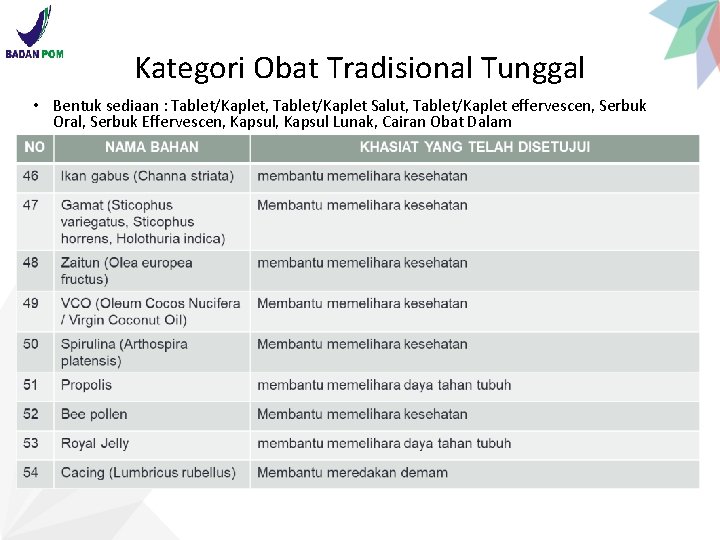
Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam
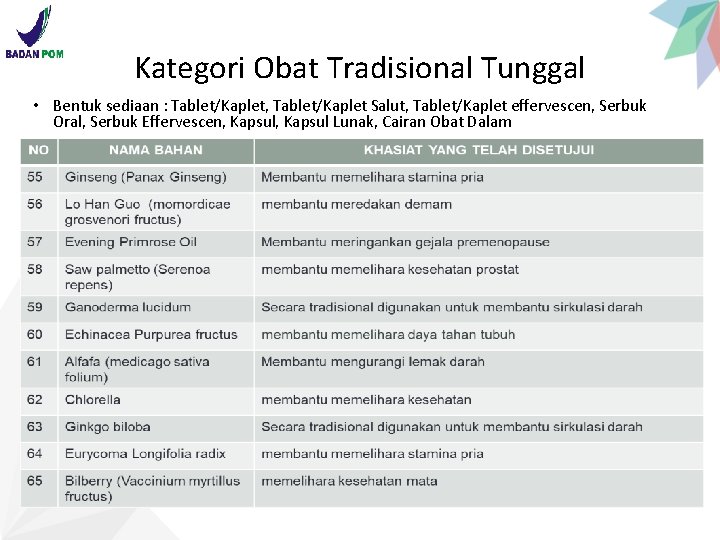
Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam
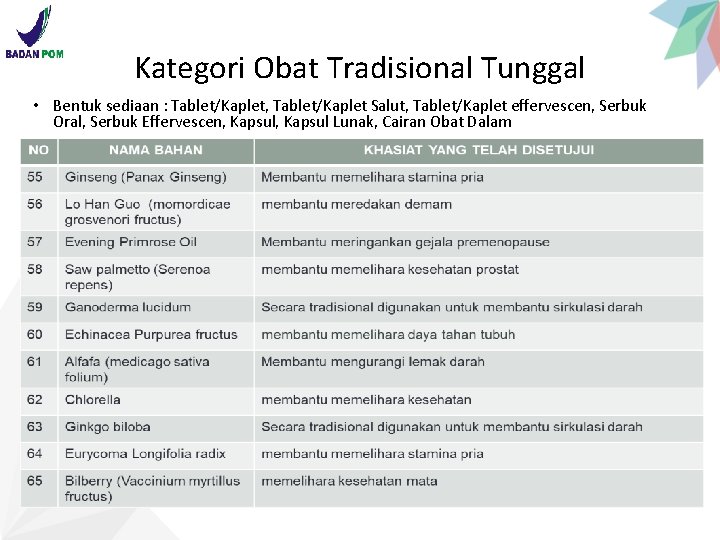
Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Tunggal • Bentuk sediaan : Tablet/Kaplet, Tablet/Kaplet Salut, Tablet/Kaplet effervescen, Serbuk Oral, Serbuk Effervescen, Kapsul Lunak, Cairan Obat Dalam

Kategori Obat Tradisional Komposisi Sederhana • Dapat dilihat pada file ini
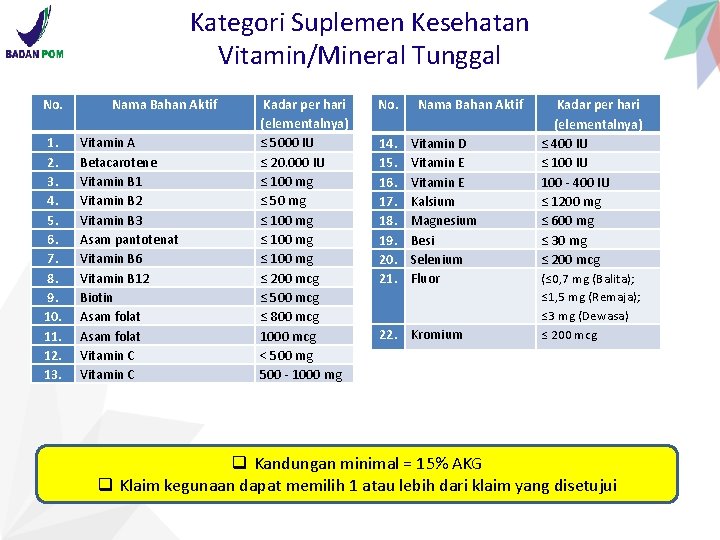
Kategori Suplemen Kesehatan Vitamin/Mineral Tunggal No. 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. Nama Bahan Aktif Vitamin A Betacarotene Vitamin B 1 Vitamin B 2 Vitamin B 3 Asam pantotenat Vitamin B 6 Vitamin B 12 Biotin Asam folat Vitamin C Kadar per hari (elementalnya) ≤ 5000 IU ≤ 20. 000 IU ≤ 100 mg ≤ 50 mg ≤ 100 mg ≤ 200 mcg ≤ 500 mcg ≤ 800 mcg 1000 mcg < 500 mg 500 - 1000 mg No. 14. 15. 16. 17. 18. 19. 20. 21. Nama Bahan Aktif Vitamin D Vitamin E Kalsium Magnesium Besi Selenium Fluor 22. Kromium Kadar per hari (elementalnya) ≤ 400 IU ≤ 100 IU 100 - 400 IU ≤ 1200 mg ≤ 600 mg ≤ 30 mg ≤ 200 mcg (≤ 0, 7 mg (Balita); ≤ 1, 5 mg (Remaja); ≤ 3 mg (Dewasa) ≤ 200 mcg q Kandungan minimal = 15% AKG q Klaim kegunaan dapat memilih 1 atau lebih dari klaim yang disetujui

Kategori Suplemen Kesehatan Kombinasi Vitamin dan/atau Mineral • Kombinasi yang diizinkan: 1. Kombinasi Multivitamin 2. Kombinasi Multimineral 3. Kombinasi Multivitamin Mineral • Kadar masing-masing bahan memenuhi ketentuan batas maksimal yang diizinkan • Klaim kegunaan yang disetujui berdasarkan hasil evaluasi terhadap formula dan klaim yang diajukan

Hal-hal yang harus diperhatikan pada dokumen mutu FORMULA Bahan yang ditimbang (sesuai Co. A Bahan Baku)a Jumlah (satuan metriks)b Overage (Jika ada) Label Klaimc Jumlah Perhitungane (satuan metriks)d Fungsi bahanf Catatan : • a : Jenis bahan baku sesuai Co. A bahan baku yang ditimbang (Misal : Thiamine HCl) • b : Jumlah bahan baku sesuai Co. A bahan baku yang ditimbang (Misal : 50 mg) • c : Jenis bahan aktif yang diklaim pada desain kemasan (Misal : Vitamin B 1) • d : Jumlah bahan aktif yang diklaim pada desain kemasan (Misal : Vitamin B 1 44, 60 mg) • e : Perhitungan kesetaraan vitamin atau elemental mineral (Misal : Perhitungan dari Thiamine HCl 50 mg mengandung Vitamin B 1 44, 60 mg) • f : Fungsi dari masing-masing bahan baku sebagai bahan aktif atau bahan tambahan
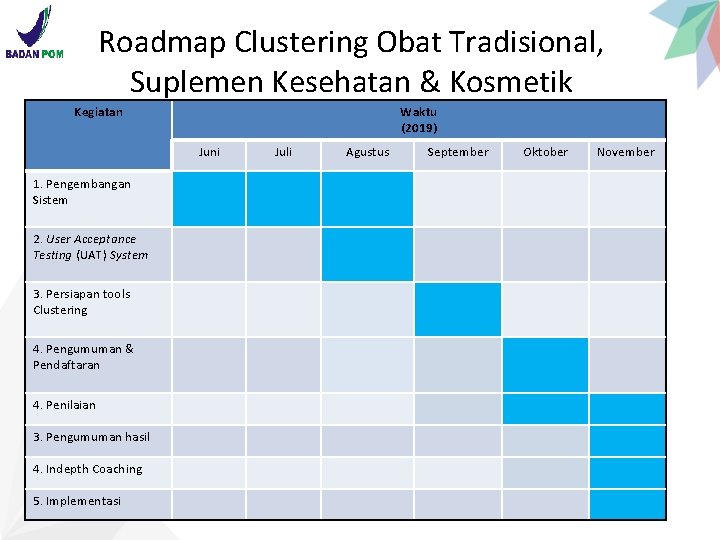
Roadmap Clustering Obat Tradisional, Suplemen Kesehatan & Kosmetik Kegiatan Waktu (2019) Juni 1. Pengembangan Sistem 2. User Acceptance Testing (UAT) System 3. Persiapan tools Clustering 4. Pengumuman & Pendaftaran 4. Penilaian 3. Pengumuman hasil 4. Indepth Coaching 5. Implementasi Juli Agustus September Oktober November

Roadmap Penerapan TTE & 2 D Barcode 41

• Dit. Registrasi OTSK sedang mengembangkan sistem registrasi baru obat tradisional, suplemen kesehatan dan obat kuasi. • Sistem registrasi baru yang dimaksud adalah paperless dan dengan TTE & 2 D barcode. • Jenis Registrasi yang dikembangkan: 1. 2. 3. 4. 5. 6. 7. 8. 9. Suplemen kesehatan vitamin atau mineral tunggal * Suplemen kesehatan komposisi sederhana (kombinasi vitamin dan/atau mineral) * Obat Tradisional komposisi tunggal * Obat tradisonal komposisi sederhana * Daftar baru highrisk OT, SK & Obat kuasi Daftar variasi mayor OT, SK & Obat kuasi Daftar variasi minor OT, SK & Obat kuasi Daftar ulang OT, SK & Obat kuasi Khusus ekspor eksis OT, SK & Obat kuasi *) kategori ini hanya bagi pendaftaran produk lokal
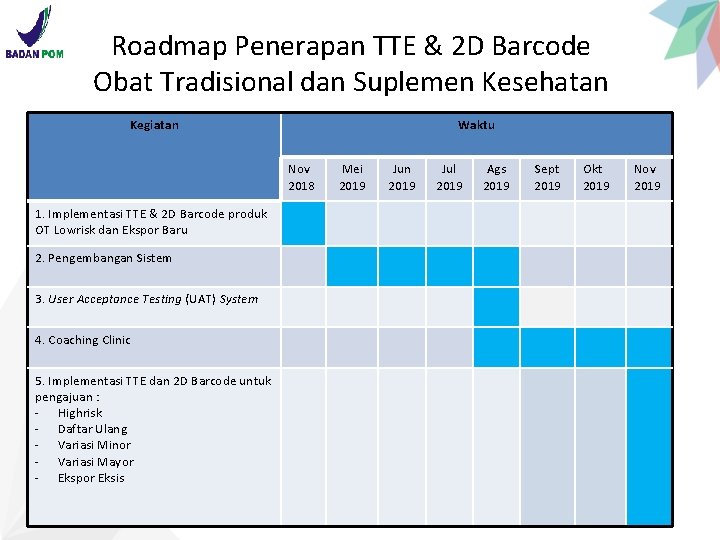
Roadmap Penerapan TTE & 2 D Barcode Obat Tradisional dan Suplemen Kesehatan Kegiatan Waktu Nov 2018 1. Implementasi TTE & 2 D Barcode produk OT Lowrisk dan Ekspor Baru 2. Pengembangan Sistem 3. User Acceptance Testing (UAT) System 4. Coaching Clinic 5. Implementasi TTE dan 2 D Barcode untuk pengajuan : - Highrisk - Daftar Ulang - Variasi Minor - Variasi Mayor - Ekspor Eksis Mei 2019 Jun 2019 Jul 2019 Ags 2019 Sept 2019 Okt 2019 Nov 2019

TERIMA KASIH SATU TINDAKAN UNTUK MASA DEPAN, BACA LABEL SEBELUM MEMBELI halobpom@pom. go. id www. pom. go. id @bpom_ri Bpom RI bpom_ri 44
- Slides: 44