Direction des Sciences du Vivant Institut de Biologie
Direction des Sciences du Vivant Institut de Biologie et de Technologies de Saclay Service de Bioénergétique, Biologie Structurale et Mécanismes CEA Saclay URA 2096 Protéines Membranaires Transductrices d’Energie

ATP synthase année 2006 -2007

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
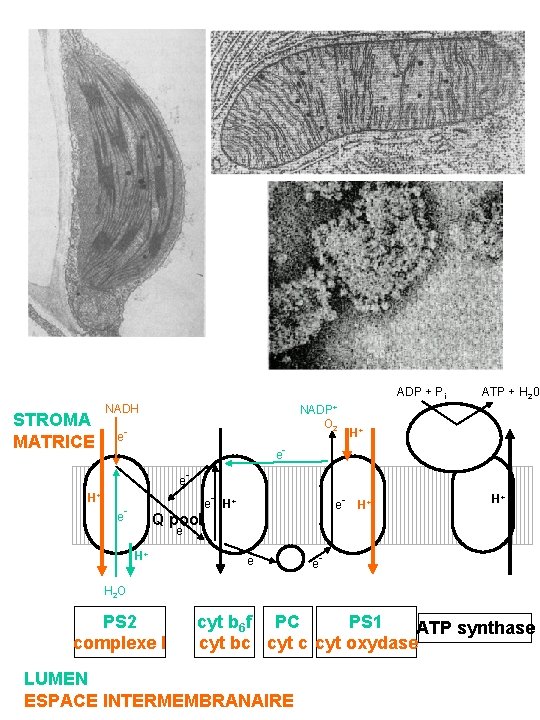
ADP + Pi STROMA MATRICE NADH NADP+ O 2 e- ATP + H 20 H+ ee- H+ e- Q pool - e- H+ H+ e- e- H 2 O PS 2 complexe I cyt b 6 f PC PS 1 ATP synthase cyt bc cyt oxydase LUMEN ESPACE INTERMEMBRANAIRE

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
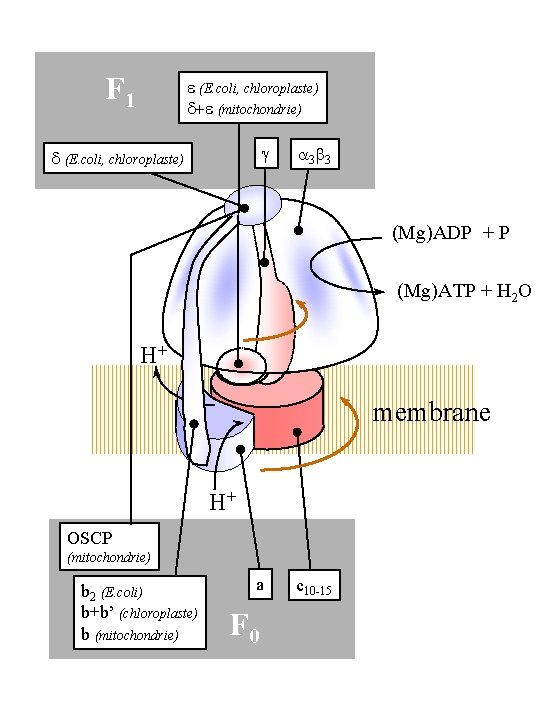
F 1 e (E. coli, chloroplaste) d+e (mitochondrie) d (E. coli, chloroplaste) 3 3 (Mg)ADP + P (Mg)ATP + H 2 O H+ membrane H+ OSCP (mitochondrie) b 2 (E. coli) b+b’ (chloroplaste) b (mitochondrie) a F 0 c 10 -15

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
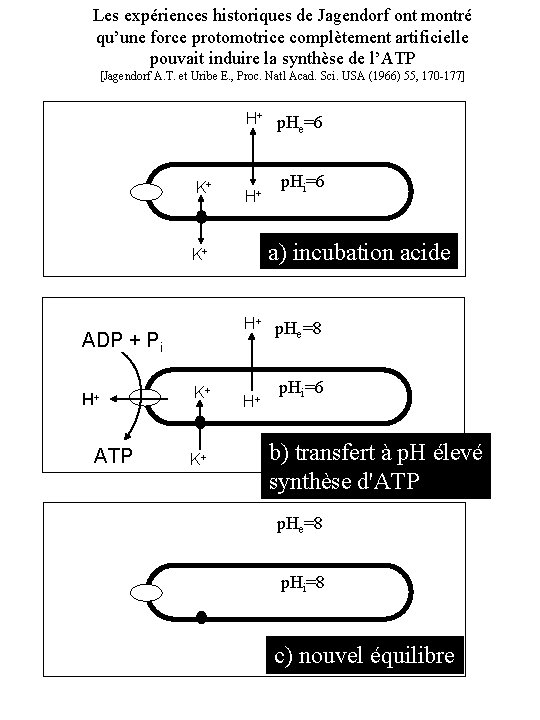
Les expériences historiques de Jagendorf ont montré qu’une force protomotrice complètement artificielle pouvait induire la synthèse de l’ATP [Jagendorf A. T. et Uribe E. , Proc. Natl Acad. Sci. USA (1966) 55, 170 -177] H+ p. H =6 e K+ H+ a) incubation acide K+ H+ p. H =8 e ADP + Pi H+ ATP p. Hi=6 K+ K+ H+ p. Hi=6 b) transfert à p. H élevé synthèse d'ATP p. He=8 p. Hi=8 c) nouvel équilibre
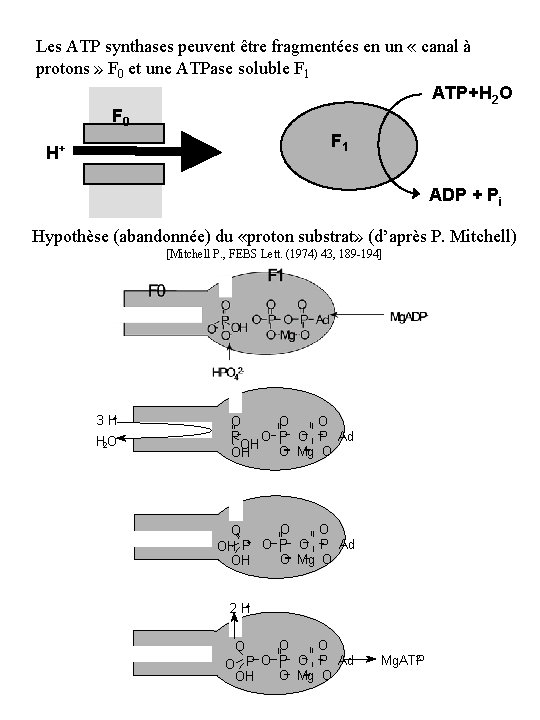
Les ATP synthases peuvent être fragmentées en un « canal à protons » F 0 et une ATPase soluble F 1 ATP+H 2 O F 0 F 1 H+ ADP + Pi Hypothèse (abandonnée) du «proton substrat» (d’après P. Mitchell) [Mitchell P. , FEBS Lett. (1974) 43, 189 -194] 3 H+ H 2 O O + O P Ad P OH O Mg O OH O O O + O- P O P Ad OH P O Mg O OH 2 H+ O O OO- P O P Ad O Mg O OH 2 Mg. ATP
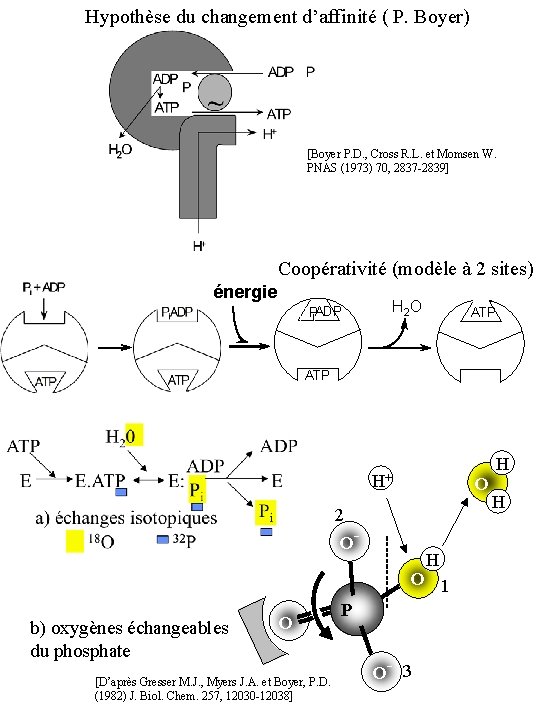
Hypothèse du changement d’affinité ( P. Boyer) [Boyer P. D. , Cross R. L. et Momsen W. PNAS (1973) 70, 2837 -2839] Coopérativité (modèle à 2 sites) énergie Pi ADP H 2 O ATP H+ O 2 O- H O 1 b) oxygènes échangeables du phosphate O [D’après Gresser M. J. , Myers J. A. et Boyer, P. D. (1982) J. Biol. Chem. 257, 12030 -12038] P O- 3 H H

MF 1 D’après Boekema E. J. , Berden J. A. et Heel M. G. , Biochim. Biophys. Acta (1986) 851, 353 -360 9 nm 2 nm 11 nm D’après Gogol E. P. , Lucken U. et Capaldi R. A. , FEBS Lett. (1987) 219, 274 -278 4. 5 nm EF 0 F 1 D’après Wilkens S. et Capaldi R. A. , Nature (1998) 393, 29
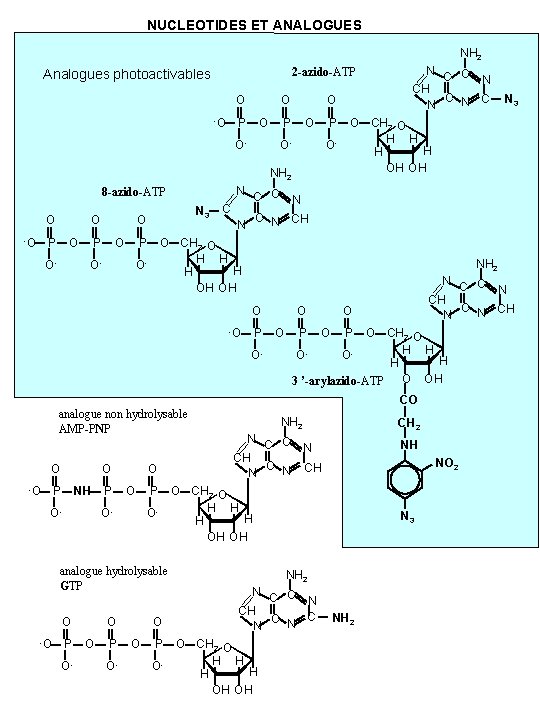
NUCLEOTIDES ET ANALOGUES NH 2 2 -azido-ATP Analogues photoactivables O -O O P O- O- NH 2 8 -azido-ATP O -O O P O O- N 3 O P O- C N C C N N CH N NH 2 O P -O O O P N C C N CH N O O CH 2 O H H OOH H 3 ’-arylazido-ATP O OH O- O P CO analogue non hydrolysable AMP-PNP O -O O P NH O- P O O O- P O- analogue hydrolysable GTP O -O P O- O O P O- N 3 O CH 2 O H H H H OH OH O- C C NH 2 N C C CH C N N CH 2 NH N NO 2 CH O CH 2 O H H OH OH N 3 NH 2 N C C N CH C N O CH 2 O H H OH OH NH 2

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
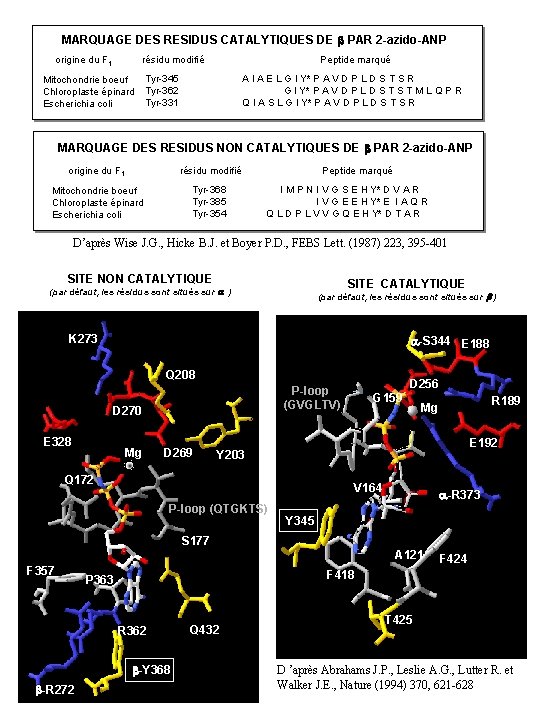
MARQUAGE DES RESIDUS CATALYTIQUES DE b PAR 2 -azido-ANP origine du F 1 résidu modifié Peptide marqué Tyr-345 Mitochondrie boeuf Chloroplaste épinard Tyr-362 Tyr-331 Escherichia coli A I A E L G I Y* P A V D P L D S T S R G I Y* P A V D P L D S T M L Q P R Q I A S L G I Y* P A V D P L D S T S R MARQUAGE DES RESIDUS NON CATALYTIQUES DE b PAR 2 -azido-ANP origine du F 1 résidu modifié Mitochondrie boeuf Chloroplaste épinard Escherichia coli Tyr-368 Tyr-385 Tyr-354 Peptide marqué I M P N I V G S E H Y* D V A R I V G E E H Y* E I A Q R Q L D P L V V G Q E H Y* D T A R D’après Wise J. G. , Hicke B. J. et Boyer P. D. , FEBS Lett. (1987) 223, 395 -401 SITE NON CATALYTIQUE SITE CATALYTIQUE (par défaut, les résidus sont situés sur a ) (par défaut, les résidus sont situés sur b ) K 273 a-S 344 E 188 Q 208 D 270 E 328 Mg D 256 P-loop (GVGLTV) D 269 G 159 R 189 Mg E 192 Y 203 Q 172 V 164 P-loop (QTGKTS) a-R 373 Y 345 S 177 A 121 F 357 F 418 P 363 R 362 b-Y 368 b-R 272 F 424 Q 432 T 425 D ’après Abrahams J. P. , Leslie A. G. , Lutter R. et Walker J. E. , Nature (1994) 370, 621 -628
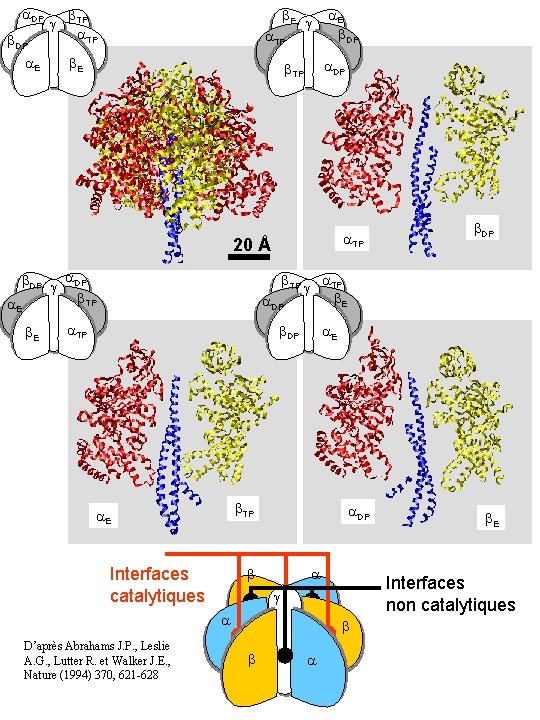
DP DP E TP TP E E DP DP TP 20 Å DP TP E E TP DP TP E DP E TP E Interfaces catalytiques DP E Interfaces non catalytiques D’après Abrahams J. P. , Leslie A. G. , Lutter R. et Walker J. E. , Nature (1994) 370, 621 -628 DP

TP E g b Double mutation en cystéine g b Pontage INACTIVATI ON Le pontage de sous-unités proches permet de savoir si elles bougent l’une par rapport à l’autre durant le cycle catalytique. (Aggeler R. , Haughton M. A. & Capaldi R. A. (1995) J. Biol Chem. 270, 9185 -9191) Quand la topologie n’est pas connue avec certitude, il permet aussi d’établir des proximités (étude du secteur membranaire F 0).
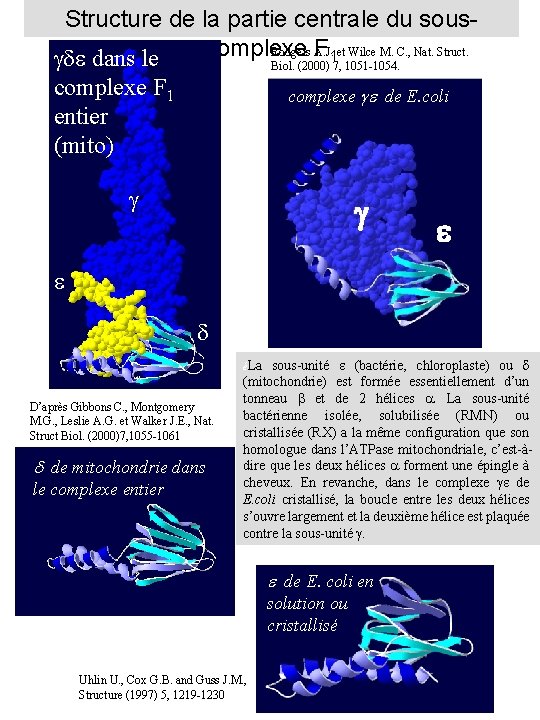
Structure de la partie centrale du sous. Rodgers A. J. complexe F 1 et Wilce M. C. , Nat. Struct. de dans le Biol. (2000) 7, 1051 -1054. complexe F 1 entier (mito) complexe ge de E. coli g e e d sous-unité e (bactérie, chloroplaste) ou d (mitochondrie) est formée essentiellement d’un tonneau et de 2 hélices . La sous-unité bactérienne isolée, solubilisée (RMN) ou cristallisée (RX) a la même configuration que son homologue dans l’ATPase mitochondriale, c’est-àdire que les deux hélices forment une épingle à cheveux. En revanche, dans le complexe e de E. coli cristallisé, la boucle entre les deux hélices s’ouvre largement et la deuxième hélice est plaquée contre la sous-unité . éLa D’après Gibbons C. , Montgomery M. G. , Leslie A. G. et Walker J. E. , Nat. Struct Biol. (2000)7, 1055 -1061 d de mitochondrie dans le complexe entier e de E. coli en solution ou cristallisé Uhlin U. , Cox G. B. and Guss J. M. , Structure (1997) 5, 1219 -1230
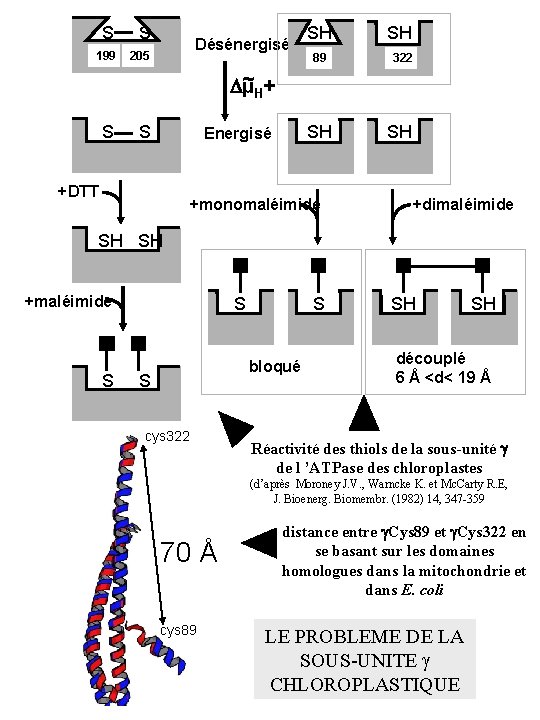
S S 199 205 Désénergisé SH 89 SH 322 ~ + Dµ H S S SH Energisé +DTT +monomaléimide SH +dimaléimide SH SH +maléimide S S S bloqué S cys 322 SH SH découplé 6 Å <d< 19 Å Réactivité des thiols de la sous-unité g de l ’ATPase des chloroplastes (d’après Moroney J. V. , Warncke K. et Mc. Carty R. E, J. Bioenerg. Biomembr. (1982) 14, 347 -359 70 Å cys 89 distance entre g. Cys 89 et g. Cys 322 en se basant sur les domaines homologues dans la mitochondrie et dans E. coli LE PROBLEME DE LA SOUS-UNITE CHLOROPLASTIQUE

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
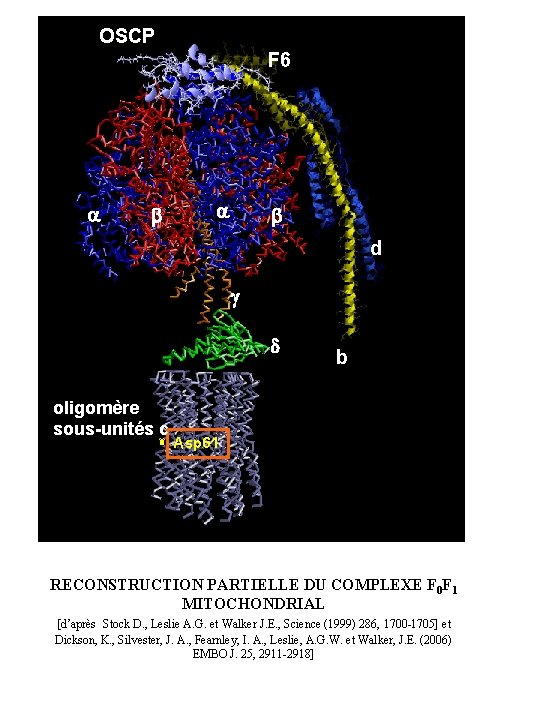
OSCP F 6 a b d g d oligomère sous-unités c b Asp 61 RECONSTRUCTION PARTIELLE DU COMPLEXE F 0 F 1 MITOCHONDRIAL [d’après Stock D. , Leslie A. G. et Walker J. E. , Science (1999) 286, 1700 -1705] et Dickson, K. , Silvester, J. A. , Fearnley, I. A. , Leslie, A. G. W. et Walker, J. E. (2006) EMBO J. 25, 2911 -2918]
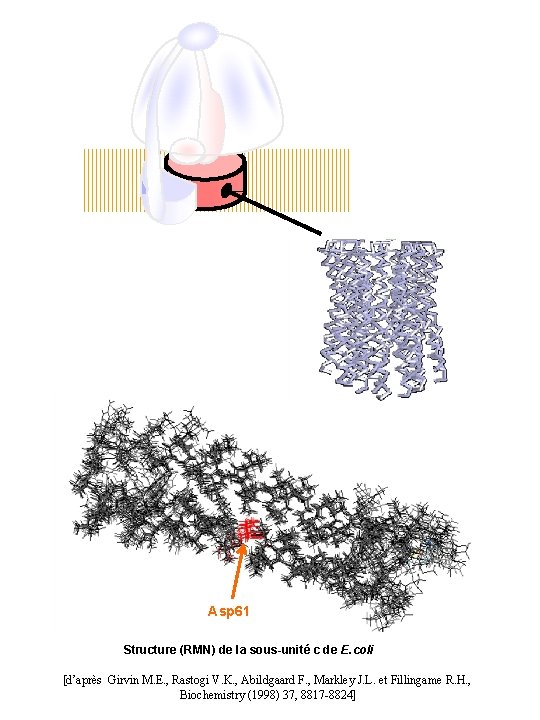
Asp 61 Structure (RMN) de la sous-unité c de E. coli [d’après Girvin M. E. , Rastogi V. K. , Abildgaard F. , Markley J. L. et Fillingame R. H. , Biochemistry (1998) 37, 8817 -8824]
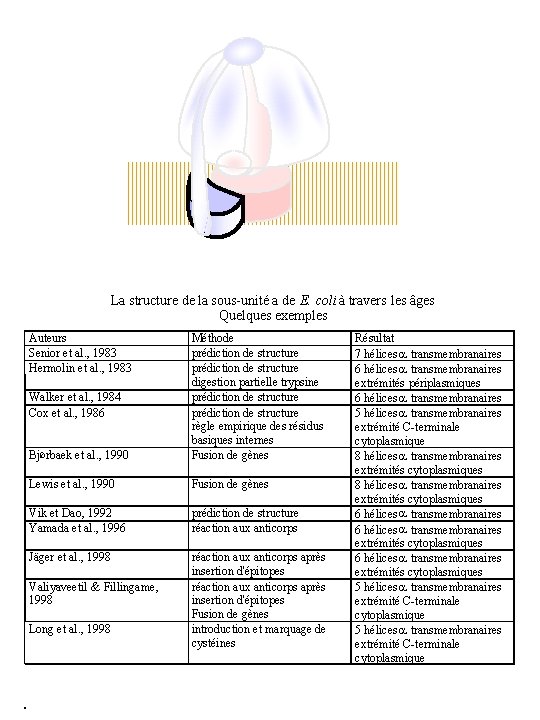
La structure de la sous-unité a de E. coli à travers les âges Quelques exemples Auteurs Senior et al. , 1983 Hermolin et al. , 1983 BjØrbaek et al. , 1990 Méthode prédiction de structure digestion partielle trypsine prédiction de structure règle empirique des résidus basiques internes Fusion de gènes Lewis et al. , 1990 Fusion de gènes Vik et Dao, 1992 Yamada et al. , 1996 prédiction de structure réaction aux anticorps Jäger et al. , 1998 réaction aux anticorps après insertion d'épitopes Fusion de gènes introduction et marquage de cystéines Walker et al. , 1984 Cox et al. , 1986 Valiyaveetil & Fillingame, 1998 Long et al. , 1998 Résultat 7 hélices transmembranaires 6 hélices transmembranaires extrémités périplasmiques 6 hélices transmembranaires 5 hélices transmembranaires extrémité C-terminale cytoplasmique 8 hélices transmembranaires extrémités cytoplasmiques 6 hélices transmembranaires extrémités cytoplasmiques 5 hélices transmembranaires extrémité C-terminale cytoplasmique
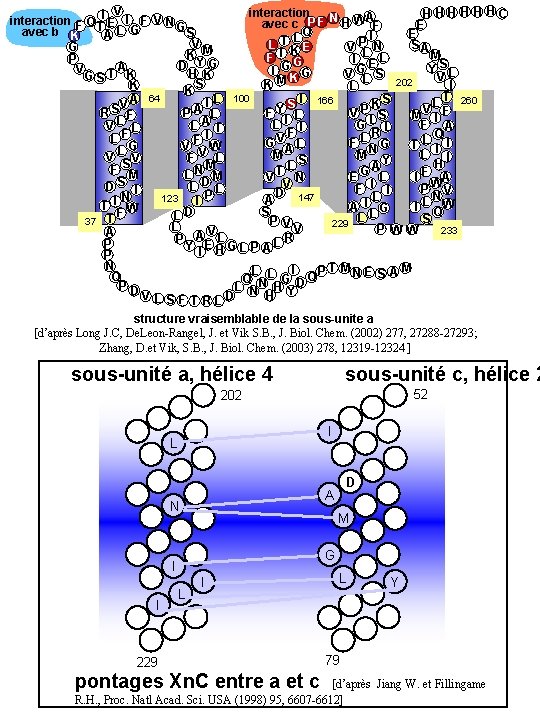
V interaction H HH HH HC interaction F Q TI E I F V N G P F N H W AF avec c E avec b K Q S E AL G I L V L TKE SA G V PL N M T K M F L P I G YG E D G A Y SL V I G H K V GL S GST K V K 202 S I KM K L K T 64 100 A L I S 166 260 L I S K V V F RS F PA L FY L VP S M I F A L I I GL L VL L LA T F R Q F F IW LL G G VA L F LN G TL I I V L I M S M Y VL V FV L S H M L A T N G L F A FF M LN M I V E V L DS I PWV F I I D P N N L 147 123 A I T I W A I G I L QW S D F L LL S P V 37 T 229 L V P WW 233 V A R P A L L P Y IE HGL P A P N I L P T MN E S A M Q Q NL G D Q PD L H V L SF T RLD N H Y structure vraisemblable de la sous-unite a [d’après Long J. C, De. Leon-Rangel, J. et Vik S. B. , J. Biol. Chem. (2002) 277, 27288 -27293; Zhang, D. et Vik, S. B. , J. Biol. Chem. (2003) 278, 12319 -12324 ] sous-unité a, hélice 4 sous-unité c, hélice 2 52 202 I L A N M G I I D L I 229 pontages Xn. C entre a et c L Y 79 [d’après Jiang W. et Fillingame R. H. , Proc. Natl Acad. Sci. USA (1998) 95, 6607 -6612]
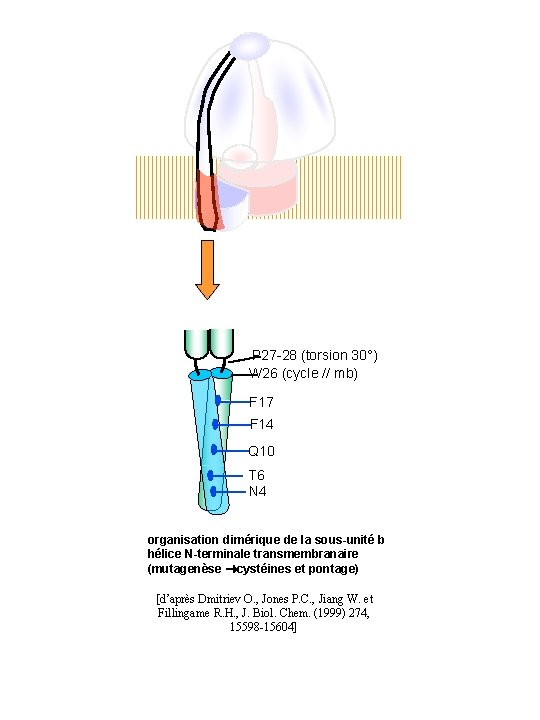
P 27 -28 (torsion 30°) W 26 (cycle // mb) F 17 F 14 Q 10 T 6 N 4 organisation dimérique de la sous-unité b hélice N-terminale transmembranaire (mutagenèse cystéines et pontage) [d’après Dmitriev O. , Jones P. C. , Jiang W. et Fillingame R. H. , J. Biol. Chem. (1999) 274, 15598 -15604]
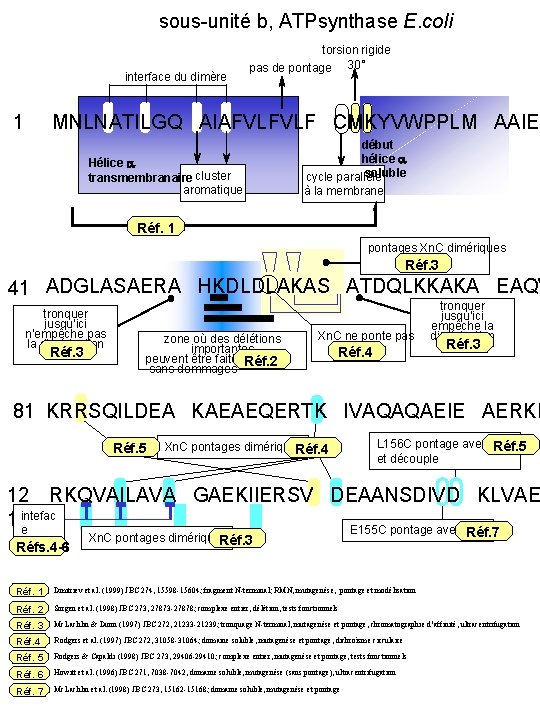
sous-unité b, ATPsynthase E. coli interface du dimère 1 torsion rigide pas de pontage 30° MNLNATILGQ AIAFVLFVLF CMKYVWPPLM AAIEK Hélice a transmembranaire cluster aromatique début hélice a soluble cycle parallèle à la membrane Réf. 1 pontages Xn. C dimériques Réf. 3 41 ADGLASAERA HKDLDLAKAS ATDQLKKAKA EAQV tronquer jusqu’ici n’empêche pas la dimérisation Réf. 3 zone où des délétions importantes peuvent être faites. Réf. 2 sans dommages Xn. C ne ponte pas Réf. 4 tronquer jusqu’ici empêche la dimérisation Réf. 3 81 KRRSQILDEA KAEAEQERTK IVAQAQAEIE AERKR Réf. 5 Xn. C pontages dimériques Réf. 4 L 156 C pontage avec Réf. 5 et découple 12 RKQVAILAVA GAEKIIERSV DEAANSDIVD KLVAE 1 intefac e E 155 C pontage avec d dimère Réfs. 4 -6 Xn. C pontages dimériques Réf. 3 Réf. 7 Réf. 1 Dmitriev et al. (1999) JBC 274, 15598 -15604; fragment N-terminal; RMN, mutagenèse, pontage et modélisation Réf. 2 Sorgen et al. (1998) JBC 273, 27873 -27878; complexe entier, délétion, tests fonctionnels Réf. 3 Mc. Lachlin & Dunn (1997) JBC 272, 21233 -21239; tronquage N-terminal, mutagenèse et pontage, chromatographie d’affinité, ultracentrifugation Réf. 4 Rodgers et al. (1997) JBC 272, 31058 -31064; domaine soluble, mutagenèse et pontage, dichroïsme circulaire Réf. 5 Rodgers & Capaldi (1998) JBC 273, 29406 -29410; complexe entier, mutagenèse et pontage, tests fonctionnels Réf. 6 Howitt et al. (1996) JBC 271, 7038 -7042, domaine soluble, mutagenèse (sans pontage), ultracentrifugation Réf. 7 Mc. Lachlin et al. (1998) JBC 273, 15162 -15168; domaine soluble, mutagenèse et pontage
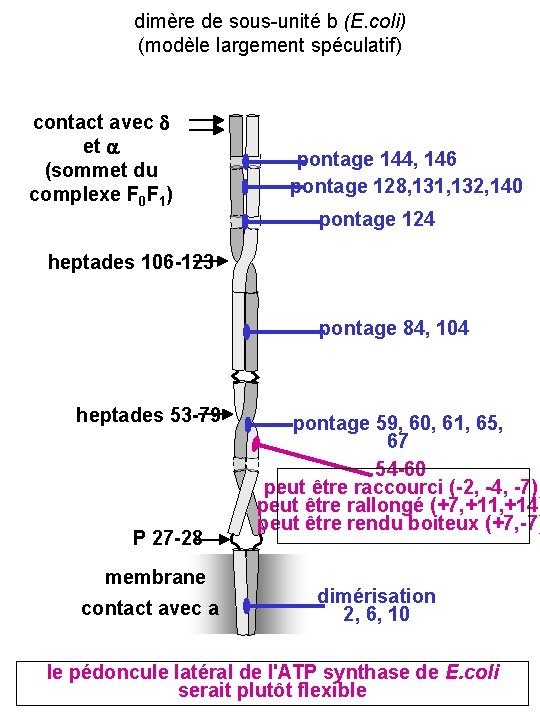
dimère de sous-unité b (E. coli) (modèle largement spéculatif) contact avec d et a (sommet du complexe F 0 F 1) pontage 144, 146 pontage 128, 131, 132, 140 pontage 124 heptades 106 -123 pontage 84, 104 heptades 53 -79 P 27 -28 membrane contact avec a pontage 59, 60, 61, 65, 67 54 -60 peut être raccourci (-2, -4, -7) peut être rallongé (+7, +11, +14) peut être rendu boiteux (+7, -7) dimérisation 2, 6, 10 le pédoncule latéral de l'ATP synthase de E. coli serait plutôt flexible
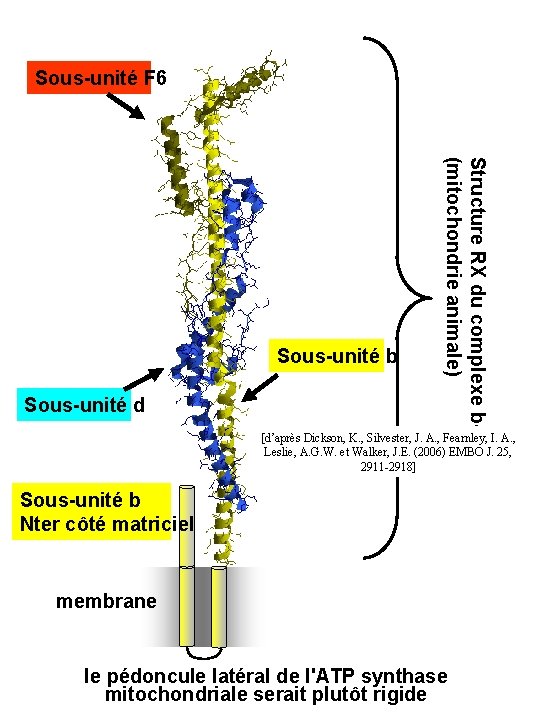
Sous-unité F 6 Sous-unité d Structure RX du complexe b-d-F 6 (mitochondrie animale) Sous-unité b [d’après Dickson, K. , Silvester, J. A. , Fearnley, I. A. , Leslie, A. G. W. et Walker, J. E. (2006) EMBO J. 25, 2911 -2918] Sous-unité b Nter côté matriciel membrane le pédoncule latéral de l'ATP synthase mitochondriale serait plutôt rigide

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
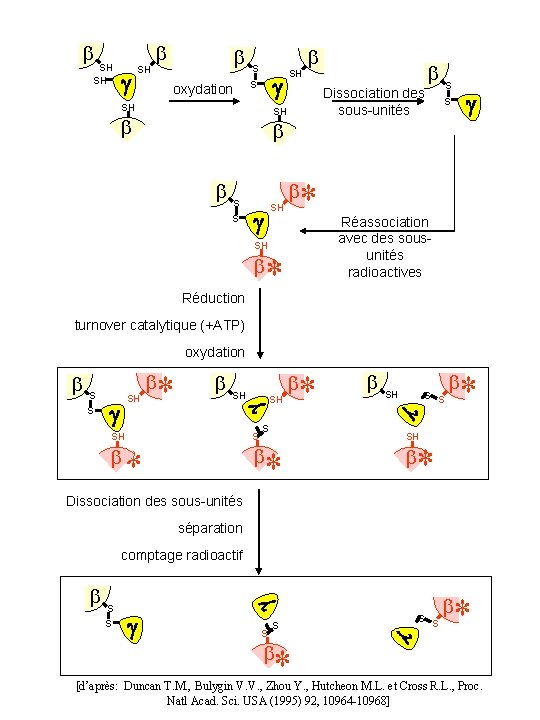
SH SH g SH S g S oxydation SH SH Dissociation des sous-unités SH S g S S S SH g * SH Réduction * Réassociation avec des sousunités radioactives turnover catalytique (+ATP) oxydation SH g * SH S SH * S SH S S * g S S g SH * * Dissociation des sous-unités séparation S S g comptage radioactif S S g g S S * * [d’après: Duncan T. M. , Bulygin V. V. , Zhou Y. , Hutcheon M. L. et Cross R. L. , Proc. Natl Acad. Sci. USA (1995) 92, 10964 -10968]
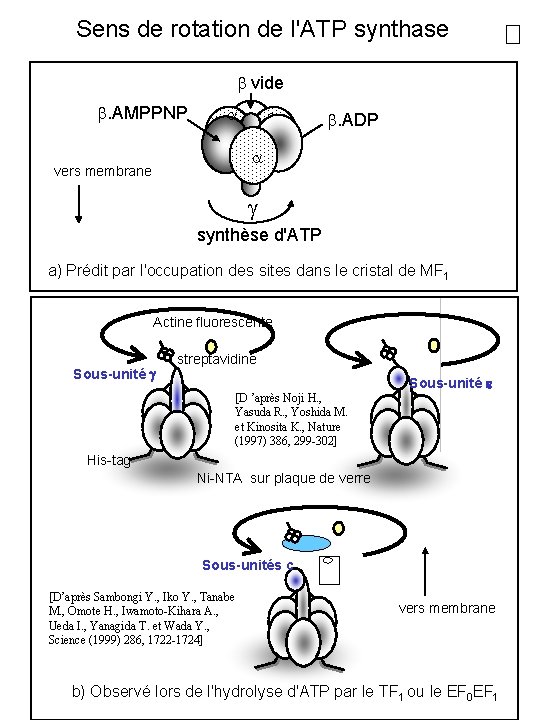
Sens de rotation de l'ATP synthase vide . AMPPNP . ADP vers membrane synthèse d'ATP a) Prédit par l'occupation des sites dans le cristal de MF 1 Actine fluorescente Sous-unité g streptavidine Sous-unité e [D ’après Noji H. , Yasuda R. , Yoshida M. et Kinosita K. , Nature (1997) 386, 299 -302] His-tag Ni-NTA sur plaque de verre Sous-unités c [D’après Sambongi Y. , Iko Y. , Tanabe M. , Omote H. , Iwamoto-Kihara A. , Ueda I. , Yanagida T. et Wada Y. , Science (1999) 286, 1722 -1724] vers membrane b) Observé lors de l'hydrolyse d'ATP par le TF 1 ou le EF 0 EF 1
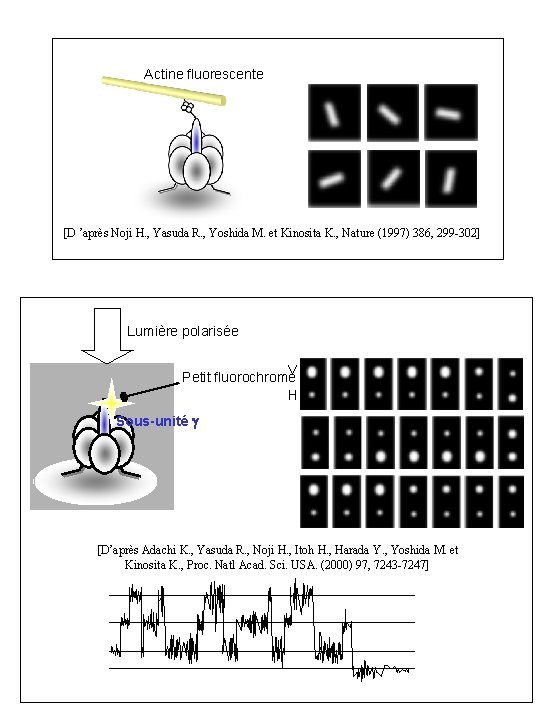
Actine fluorescente [D ’après Noji H. , Yasuda R. , Yoshida M. et Kinosita K. , Nature (1997) 386, 299 -302] Lumière polarisée V Petit fluorochrome H Sous-unité g [D’après Adachi K. , Yasuda R. , Noji H. , Itoh H. , Harada Y. , Yoshida M. et Kinosita K. , Proc. Natl Acad. Sci. USA. (2000) 97, 7243 -7247]
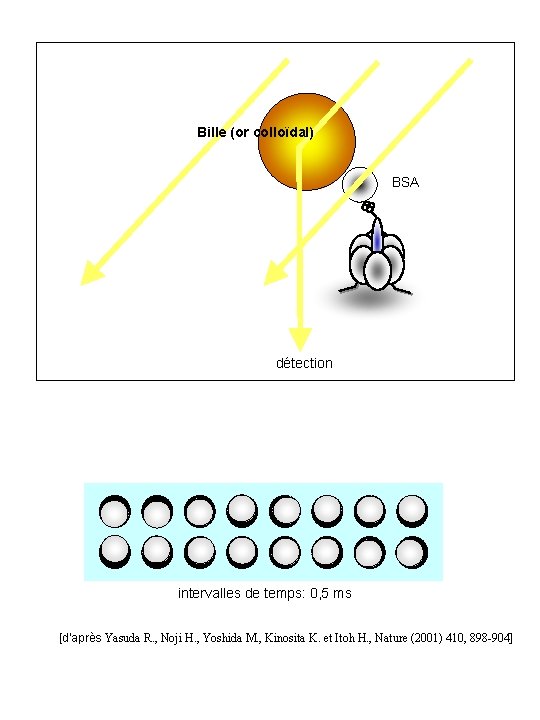
Bille (or colloïdal) BSA détection intervalles de temps: 0, 5 ms [d’après Yasuda R. , Noji H. , Yoshida M. , Kinosita K. et Itoh H. , Nature (2001) 410, 898 -904]
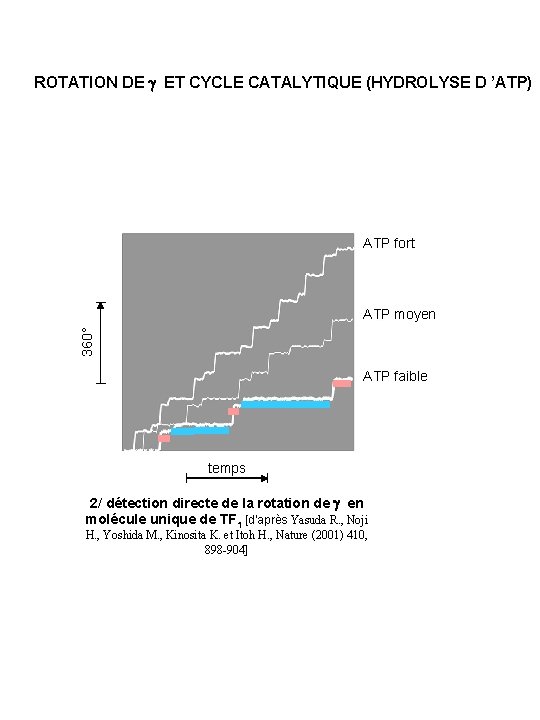
ROTATION DE g ET CYCLE CATALYTIQUE (HYDROLYSE D ’ATP) ATP fort 360° ATP moyen ATP faible temps 2/ détection directe de la rotation de g en molécule unique de TF 1 [d’après Yasuda R. , Noji H. , Yoshida M. , Kinosita K. et Itoh H. , Nature (2001) 410, 898 -904]
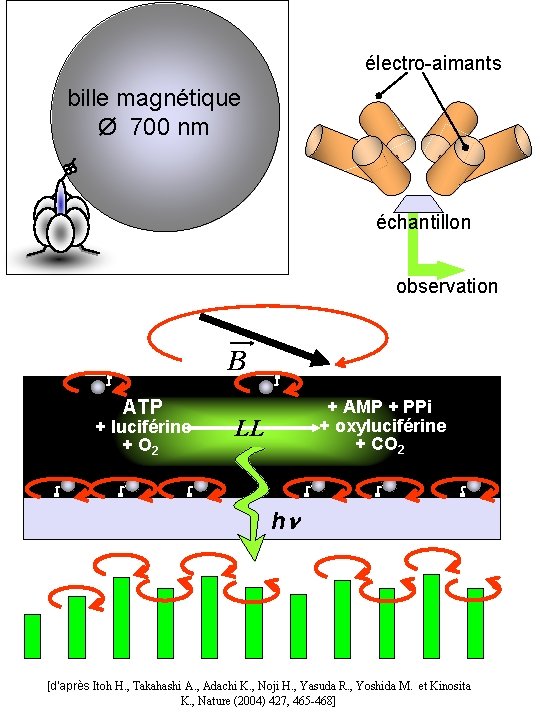
électro-aimants bille magnétique Ø 700 nm échantillon observation B ATP + luciférine + O 2 + AMP + PPi + oxyluciférine + CO 2 LL hn [d’après Itoh H. , Takahashi A. , Adachi K. , Noji H. , Yasuda R. , Yoshida M. et Kinosita K. , Nature (2004) 427, 465 -468]
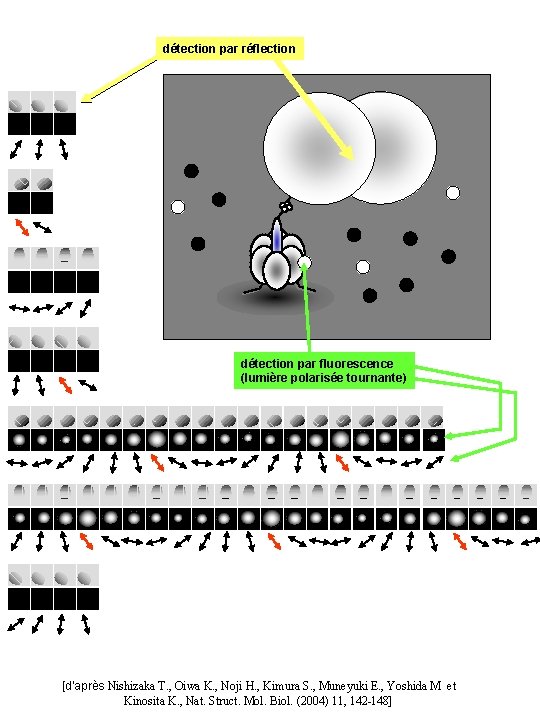
détection par réflection détection par fluorescence (lumière polarisée tournante) [d’après Nishizaka T. , Oiwa K. , Noji H. , Kimura S. , Muneyuki E. , Yoshida M et Kinosita K. , Nat. Struct. Mol. Biol. (2004) 11, 142 -148]
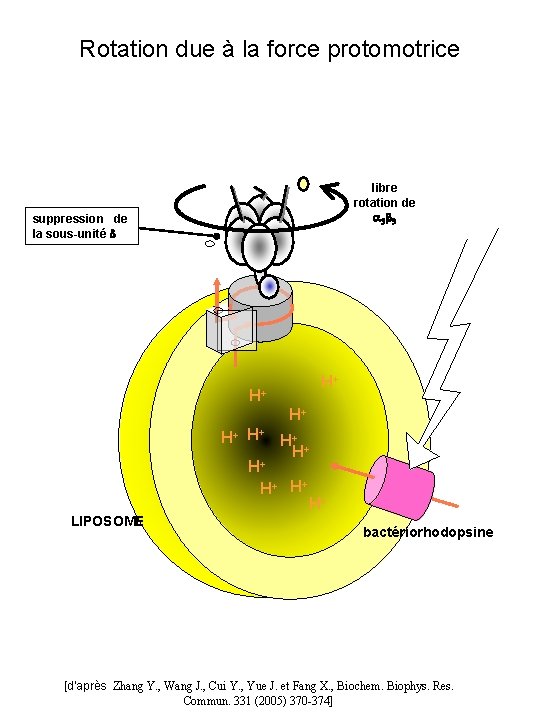
Rotation due à la force protomotrice libre rotation de a 3 b 3 suppression de la sous-unité d H+ H+ + H H+ H+ H+ LIPOSOME bactériorhodopsine [d’après Zhang Y. , Wang J. , Cui Y. , Yue J. et Fang X. , Biochem. Biophys. Res. Commun. 331 (2005) 370 -374]
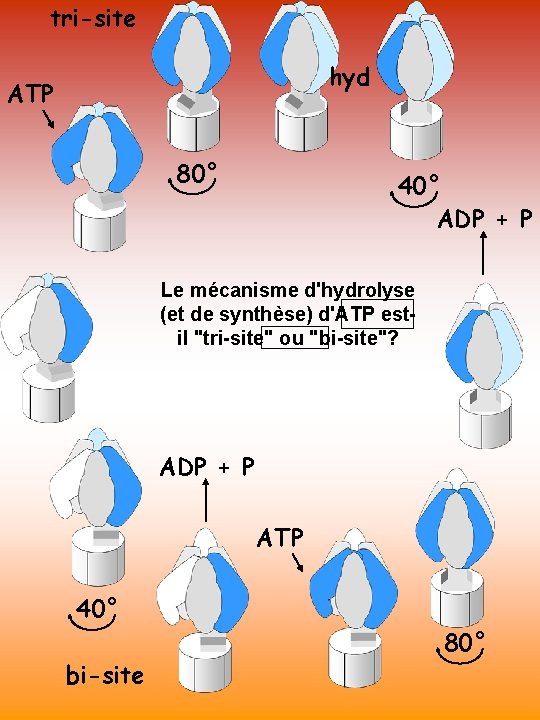
tri-site hyd ATP 80° 40° ADP + P Le mécanisme d'hydrolyse (et de synthèse) d'ATP estil "tri-site" ou "bi-site"? ADP + P ATP 40° bi-site 80°
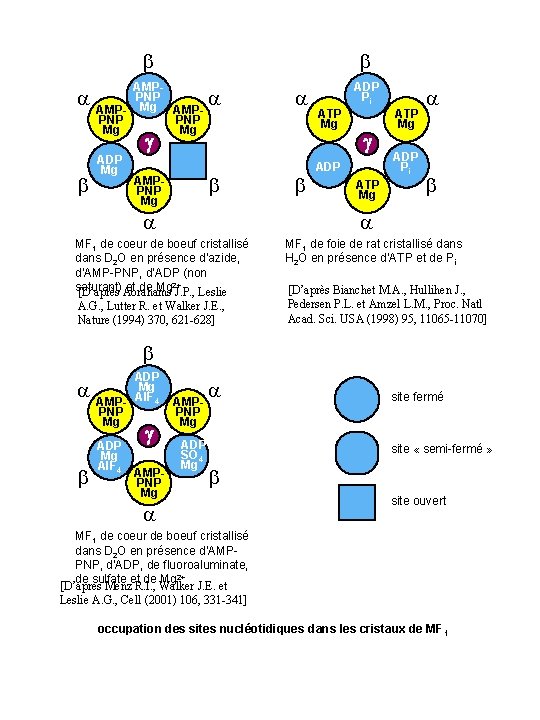
AMPPNP AMP- Mg AMPPNP Mg Mg ADP Pi g ADP Mg AMPPNP Mg ATP Mg g ADP ATP Mg ADP Pi MF 1 de coeur de boeuf cristallisé dans D 2 O en présence d’azide, d’AMP-PNP, d’ADP (non saturant) et de Mg 2+ [D’après Abrahams J. P. , Leslie A. G. , Lutter R. et Walker J. E. , Nature (1994) 370, 621 -628] MF 1 de foie de rat cristallisé dans H 2 O en présence d’ATP et de Pi [D’après Bianchet M. A. , Hullihen J. , Pedersen P. L. et Amzel L. M. , Proc. Natl Acad. Sci. USA (1998) 95, 11065 -11070] ADP Mg Al. F 4 AMPPNP Mg ADP Mg Al. F 4 g AMPPNP Mg ADP SO 4 Mg site fermé site « semi-fermé » site ouvert MF 1 de coeur de boeuf cristallisé dans D 2 O en présence d’AMPPNP, d’ADP, de fluoroaluminate, de sulfate et de Mg 2+ [D’après Menz R. I. , Walker J. E. et Leslie A. G. , Cell (2001) 106, 331 -341] occupation des sites nucléotidiques dans les cristaux de MF 1
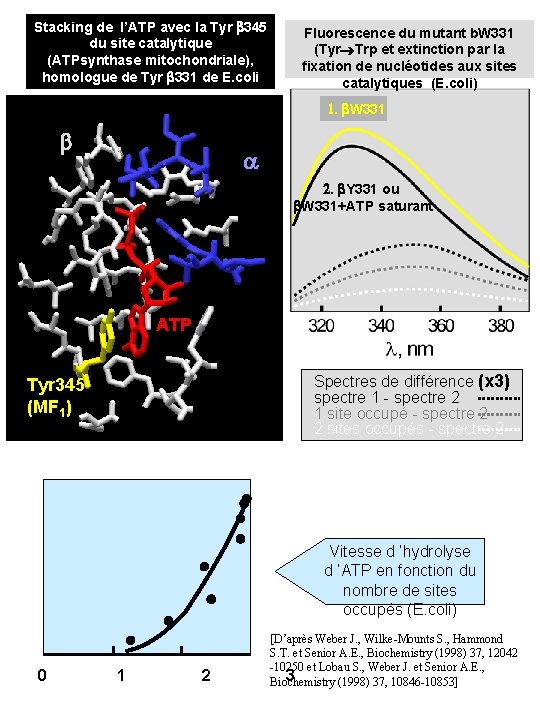
Stacking de l’ATP avec la Tyr b 345 du site catalytique (ATPsynthase mitochondriale), homologue de Tyr b 331 de E. coli Fluorescence du mutant b. W 331 (Tyr Trp et extinction par la fixation de nucléotides aux sites catalytiques (E. coli) 1. b. W 331 b a 2. b. Y 331 ou b. W 331+ATP saturant ATP Spectres de différence (x 3) spectre 1 - spectre 2 1 site occupé - spectre 2 2 sites occupés - spectre 2 Tyr 345 (MF 1) Vitesse d ’hydrolyse d ’ATP en fonction du nombre de sites occupés (E. coli) 0 1 2 [D’après Weber J. , Wilke-Mounts S. , Hammond S. T. et Senior A. E. , Biochemistry (1998) 37, 12042 -10250 et Lobau S. , Weber J. et Senior A. E. , 3 Biochemistry (1998) 37, 10846 -10853]
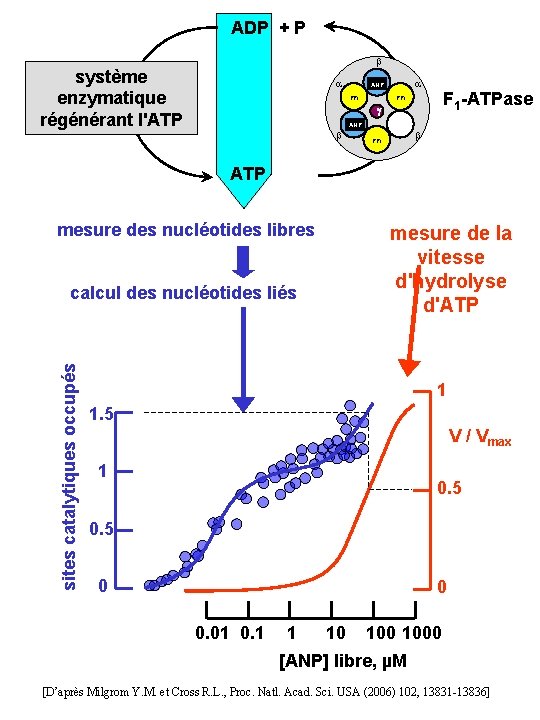
ADP + P système enzymatique régénérant l'ATP ANP PPi F 1 -ATPase PPi g ANP PPi ATP mesure des nucléotides libres mesure de la vitesse d'hydrolyse d'ATP sites catalytiques occupés calcul des nucléotides liés 1 1. 5 V / Vmax 1 0. 5 0 0 0. 01 0. 1 1 10 1000 [ANP] libre, µM [D’après Milgrom Y. M. et Cross R. L. , Proc. Natl. Acad. Sci. USA (2006) 102, 13831 -13836]
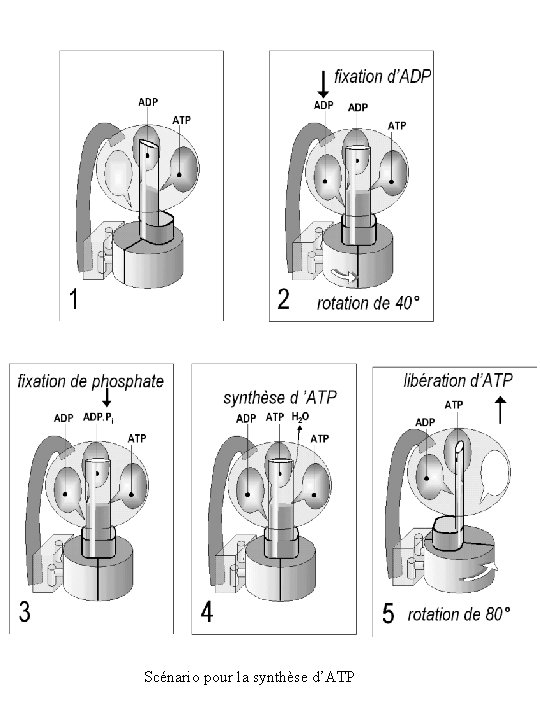
Scénario pour la synthèse d’ATP

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
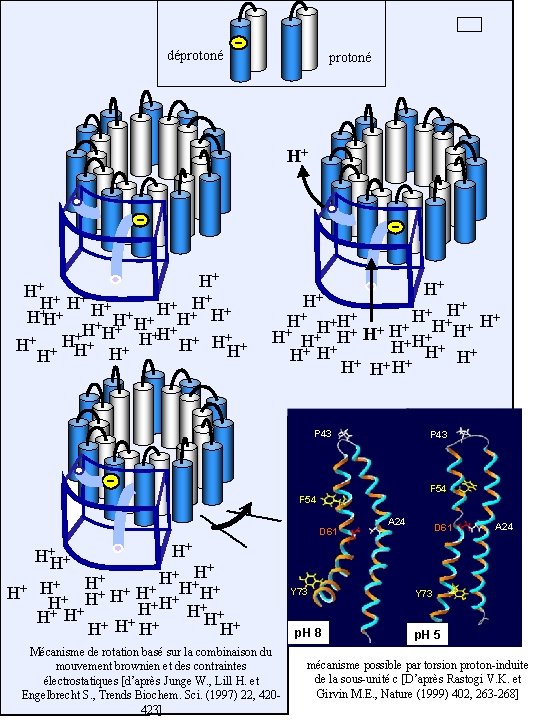
déprotoné H+ H+ + + H+ H + H H + + H+ H+ H+H+ + H H H + H+ H H+H+ + H H H+ H+ H+ + + H H H+ H + + H+ H+ H H + H+ H+ + + H+ H+ H H H P 43 F 54 D 61 H+H+ A 24 D 61 A 24 H+ + + H H + H+ H+ H + H +H H+H+ H+ H+ + + H H H H+ H+ H+ Mécanisme de rotation basé sur la combinaison du mouvement brownien et des contraintes électrostatiques [d’après Junge W. , Lill H. et Engelbrecht S. , Trends Biochem. Sci. (1997) 22, 420423] Y 73 p. H 8 Y 73 p. H 5 mécanisme possible par torsion proton-induite de la sous-unité c [D’après Rastogi V. K. et Girvin M. E. , Nature (1999) 402, 263 -268]
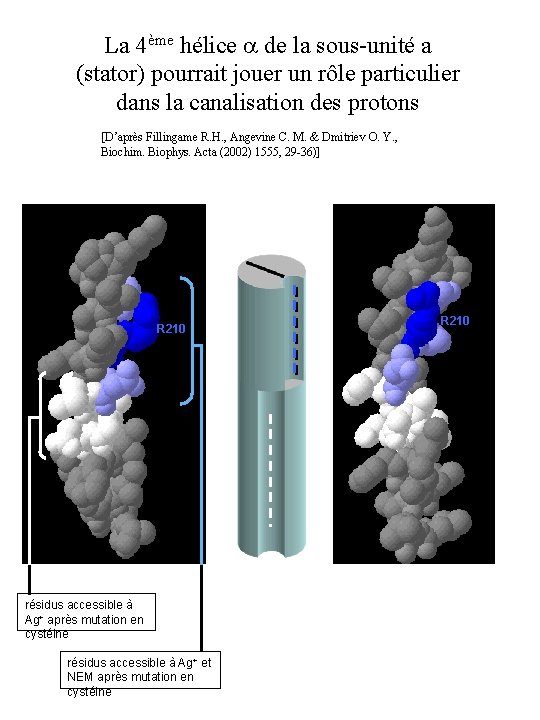
La 4ème hélice de la sous-unité a (stator) pourrait jouer un rôle particulier dans la canalisation des protons [D’après Fillingame R. H. , Angevine C. M. & Dmitriev O. Y. , Biochim. Biophys. Acta (2002) 1555, 29 -36)] R 210 résidus accessible à Ag+ après mutation en cystéine résidus accessible à Ag+ et NEM après mutation en cystéine R 210
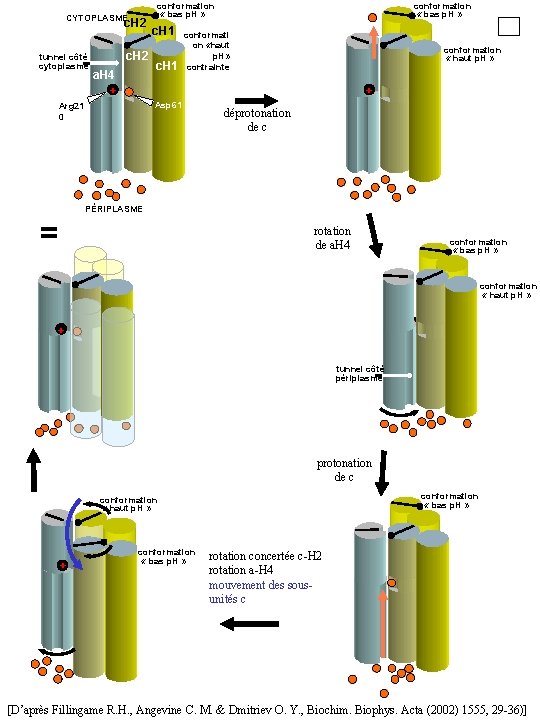
CYTOPLASME c. H 2 tunnel côté cytoplasme c. H 2 a. H 4 + conformation « bas p. H » c. H 1 conformation « bas p. H » conformati on «haut p. H» contrainte conformation « haut p. H » + Asp 61 Arg 21 0 déprotonation de c PÉRIPLASME = rotation de a. H 4 conformation « bas p. H » conformation « haut p. H » + + tunnel côté périplasme protonation de c conformation « bas p. H » conformation « haut p. H » + conformation « bas p. H » rotation concertée c-H 2 rotation a-H 4 mouvement des sousunités c [D’après Fillingame R. H. , Angevine C. M. & Dmitriev O. Y. , Biochim. Biophys. Acta (2002) 1555, 29 -36)]

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
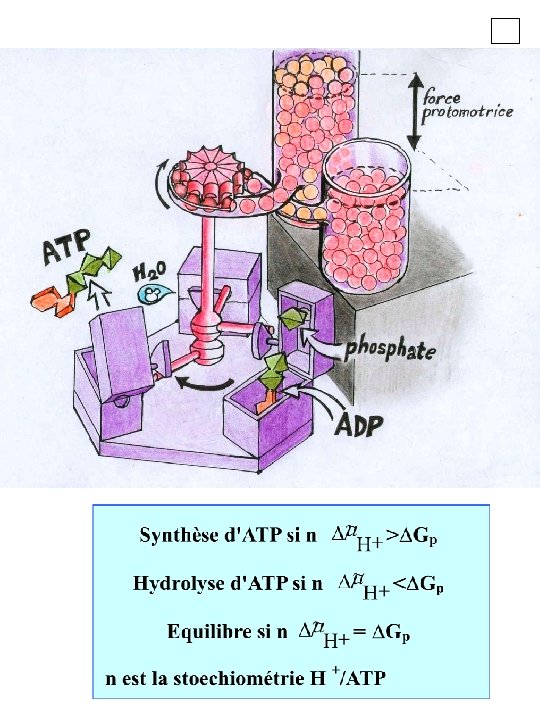
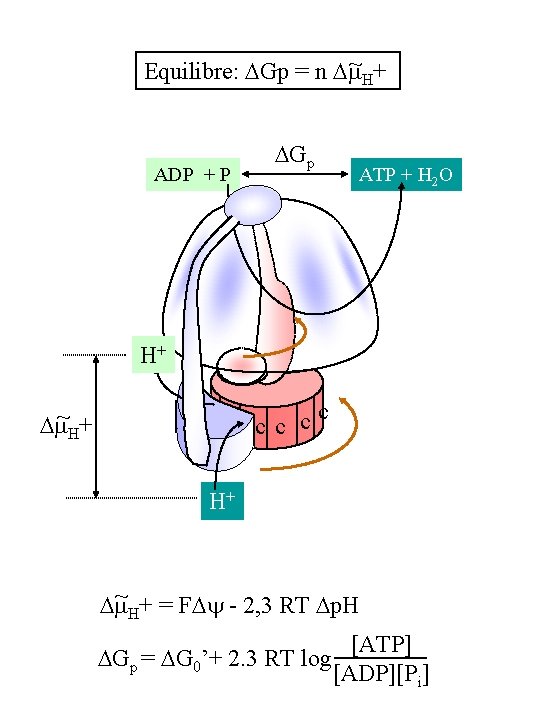
~ + Equilibre: Gp = n H ADP + P Gp ATP + H 2 O H+ c c ~H+ H+ ~ + = F - 2, 3 RT p. H H Gp = G 0’+ 2. 3 RT log [ATP] [ADP][Pi]
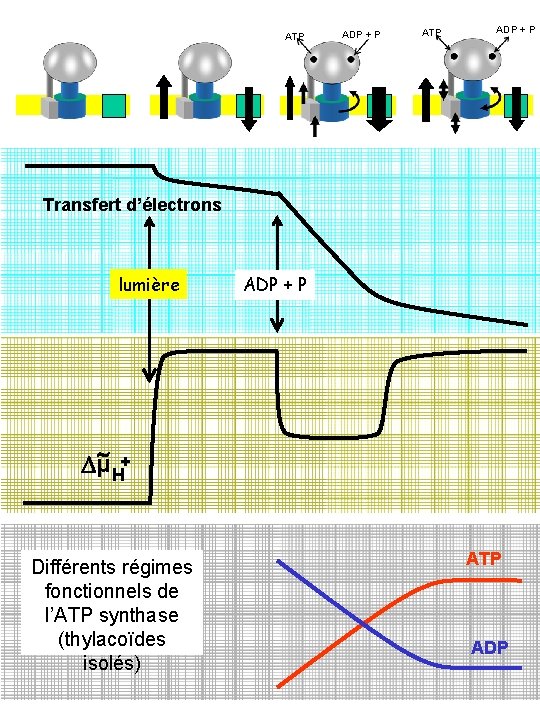
ATP ADP + P Transfert d’électrons lumière ADP + P + Dµ H Différents régimes fonctionnels de l’ATP synthase (thylacoïdes isolés) ATP ADP



Nombre de sous-unités c 1 10 9 2 Structure 3 D de MF 0 MF 1 de levure [d’après Stock D. , Leslie 8 A. G. et Walker J. E. , Science (1999) 286, 1700 -1705] 3 7 4 5 n=10 6 3 1 2 14 13 4 n=14 12 5 Cristal 2 D de sous-unités c de CF 0 CF 1. Microscopie de force atomique [d’après Seelert H. , Poetsch A. , Dencher N. A. , Engel A. , Stahlberg H. et Müller, D. J. , Nature (2000) 405, 418 -419] 11 6 7 10 8 9 Cristal 2 D de sous-unités c de Ilyobacter Tartaricus. Microscopie électronique par transmission [d’après Stahlberg H. , Müller D. J. , Suda K. , Fotiadis D. , Engel A. , Meier T. , Matthey U. et Dimroth P. , EMBO Rep. (2001)2, 229 -233] n=11
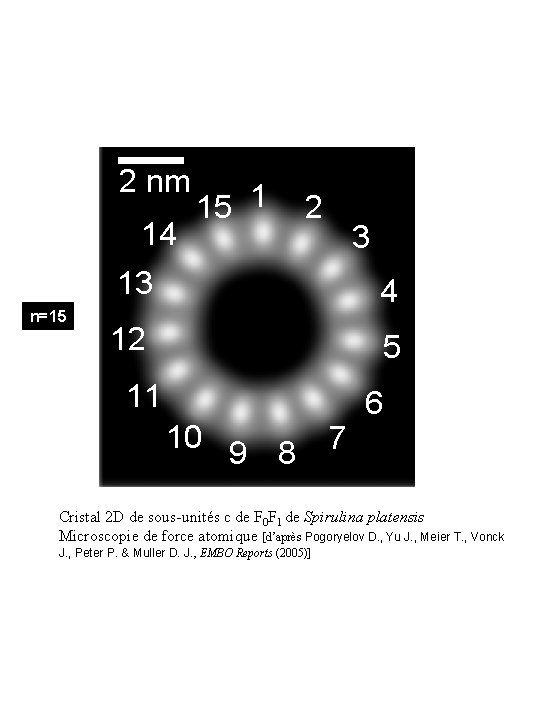
2 nm 14 n=15 15 1 2 3 13 4 12 5 11 10 9 8 7 6 Cristal 2 D de sous-unités c de F 0 F 1 de Spirulina platensis Microscopie de force atomique [d’après Pogoryelov D. , Yu J. , Meier T. , Vonck J. , Peter P. & Muller D. J. , EMBO Reports (2005)]
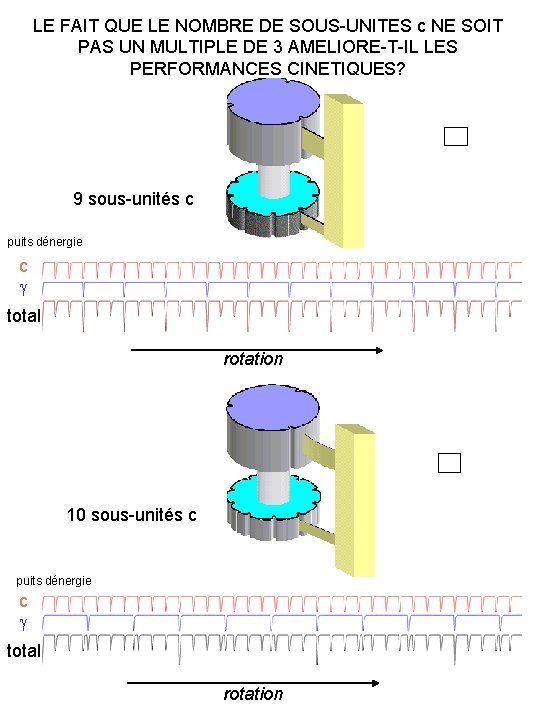
LE FAIT QUE LE NOMBRE DE SOUS-UNITES c NE SOIT PAS UN MULTIPLE DE 3 AMELIORE-T-IL LES PERFORMANCES CINETIQUES? 9 sous-unités c puits dénergie c total rotation 10 sous-unités c puits dénergie c total rotation
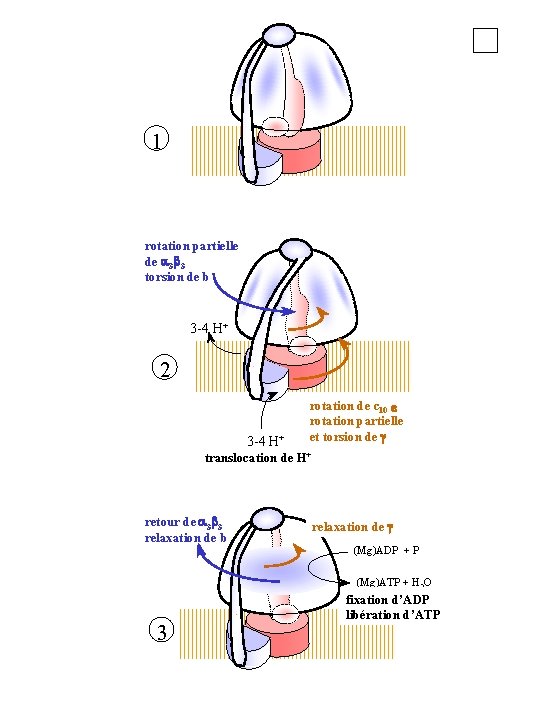
1 rotation partielle de a 3 b 3 torsion de b 3 -4 H + 2 3 -4 H+ rotation de c 10 e rotation partielle et torsion de g translocation de H+ retour de a 3 b 3 relaxation de b relaxation de g (Mg)ADP + P (Mg)ATP + H 2 O 3 fixation d’ADP libération d’ATP

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
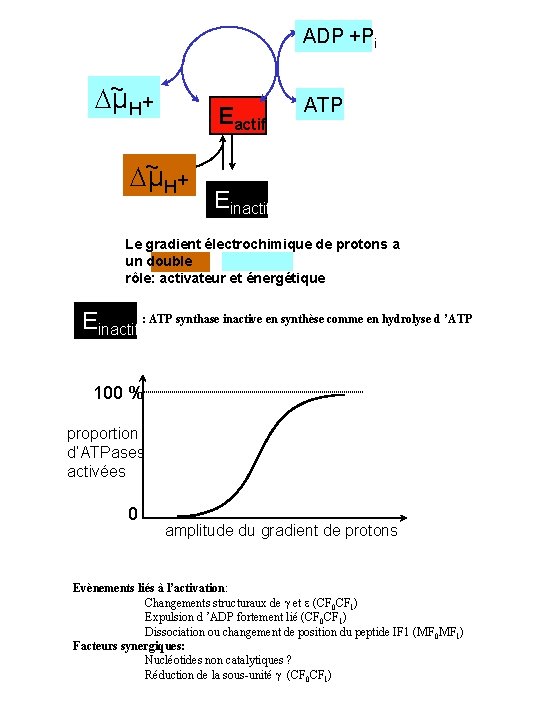
ADP +Pi ~ + µ H Eactif ~ + µ H ATP Einactif Le gradient électrochimique de protons a un double rôle: activateur et énergétique Einactif : ATP synthase inactive en synthèse comme en hydrolyse d ’ATP 100 % proportion d’ATPases activées 0 amplitude du gradient de protons Evènements liés à l’activation: Changements structuraux de et e (CF 0 CF 1) Expulsion d ’ADP fortement lié (CF 0 CF 1) Dissociation ou changement de position du peptide IF 1 (MF 0 MF 1) Facteurs synergiques: Nucléotides non catalytiques ? Réduction de la sous-unité (CF 0 CF 1)
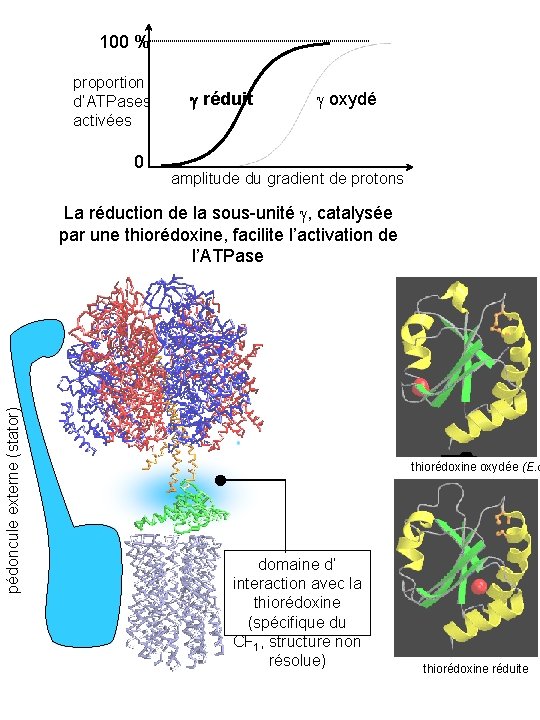
100 % proportion d’ATPases activées 0 g réduit oxydé amplitude du gradient de protons pédoncule externe (stator) La réduction de la sous-unité , catalysée par une thiorédoxine, facilite l’activation de l’ATPase thiorédoxine oxydée (E. c domaine d’ interaction avec la thiorédoxine (spécifique du CF 1, structure non résolue) thiorédoxine réduite
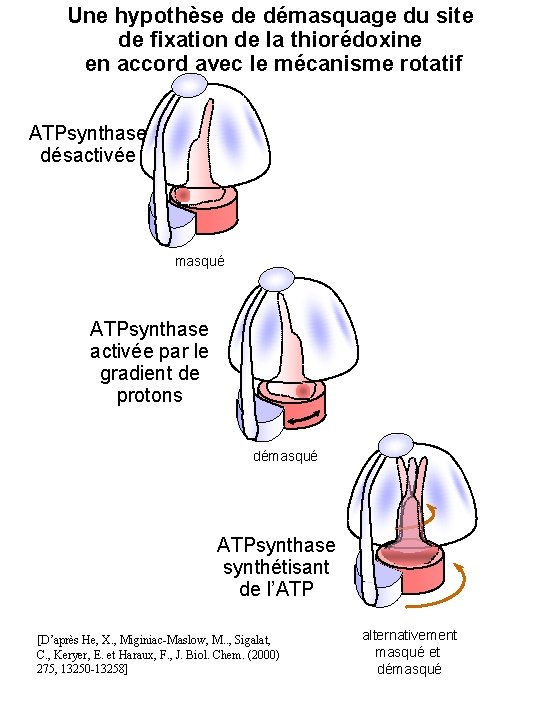
Une hypothèse de démasquage du site de fixation de la thiorédoxine en accord avec le mécanisme rotatif ATPsynthase désactivée masqué ATPsynthase activée par le gradient de protons démasqué ATPsynthase synthétisant de l’ATP [D’après He, X. , Miginiac-Maslow, M. . , Sigalat, C. , Keryer, E. et Haraux, F. , J. Biol. Chem. (2000) 275, 13250 -13258] alternativement masqué et démasqué
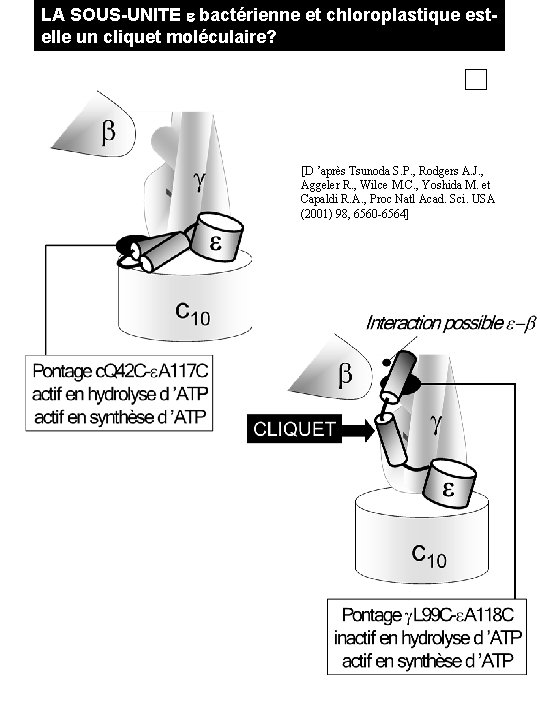
LA SOUS-UNITE e bactérienne et chloroplastique estelle un cliquet moléculaire? [D ’après Tsunoda S. P. , Rodgers A. J. , Aggeler R. , Wilce M. C. , Yoshida M. et Capaldi R. A. , Proc Natl Acad. Sci. USA (2001) 98, 6560 -6564]
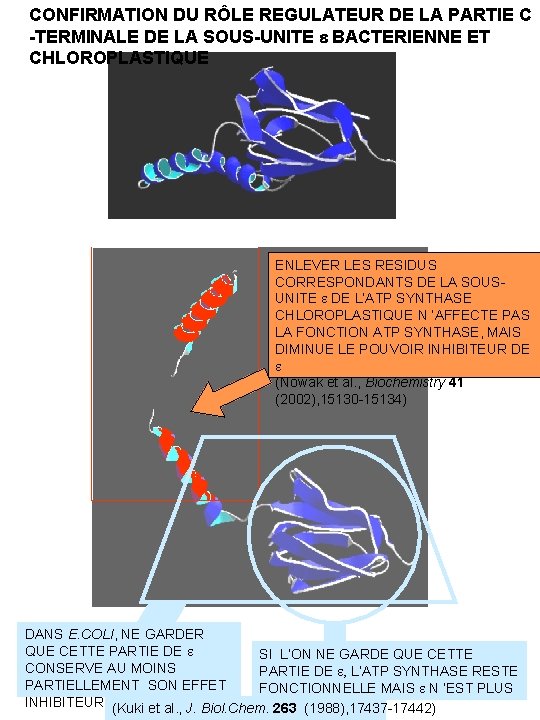
CONFIRMATION DU RÔLE REGULATEUR DE LA PARTIE C -TERMINALE DE LA SOUS-UNITE e BACTERIENNE ET CHLOROPLASTIQUE ENLEVER LES RESIDUS CORRESPONDANTS DE LA SOUSUNITE e DE L’ATP SYNTHASE CHLOROPLASTIQUE N ’AFFECTE PAS LA FONCTION ATP SYNTHASE, MAIS DIMINUE LE POUVOIR INHIBITEUR DE e (Nowak et al. , Biochemistry 41 (2002), 15130 -15134) DANS E. COLI, NE GARDER QUE CETTE PARTIE DE e SI L’ON NE GARDE QUE CETTE CONSERVE AU MOINS PARTIE DE e, L’ATP SYNTHASE RESTE PARTIELLEMENT SON EFFET FONCTIONNELLE MAIS e N ’EST PLUS INHIBITEUR (Kuki et al. , J. Biol. Chem. INHIBITEUR 263 (1988), 17437 -17442)

REGULATION DES ATP SYNTHASES DE E. COLI ET DE CHLOR Dans E. coli, la régulation fait intervenir la sous-unité e, qui peut exister au moins sous deux conformations différentes, haute et basse, de sa partie Cterminale. En conformation haute, l’hydrolyse d’ATP est inhibée, mais pas sa synthèse. L’ADP et le gradient de protons favoriseraient la position haute. L’ATP favoriserait la position basse. Un détecteur d ’ATP pourrait être présent sur la sous-unité e. La fonction de cette régulation pourrait être d’adapter l’ATP synthase aux besoins de la cellule, en lui faisant, selon les conditions, synthétiser de l’ATP ou maintenir le gradient de protons à travers la membrane cytoplasmique si celui-ci tend à diminuer. Mais par ailleurs, la disparition totale du gradient de protons conduit à l’inactivation de l’ATPase en présence d’ADP, ce qui est paradoxal. Dans l’ATPase chloroplastique, la sous-unité e inhibe l’hydrolyse d’ATP, également par sa partie C-terminale. Le gradient de protons favorise l’activation de l’enzyme, à la fois pour la synthèse et l’hydrolyse d’ATP. L’hydrolyse d ’ATP est totalement inhibée en absence de gradient de protons. L’ADP, ajouté directement ou provenant de l ’hydrolyse d ’ATP, est inhibiteur. La régulation fait également intervenir la sous-unité . La réduction du pont disulfure de favorise l’activation de l’enzyme. Dans les membranes, cette activation (ou levée d’inhibition) porterait à la fois sur la synthèse et l’hydrolyse de l’ATP. La réduction de a probablement deux effets activateurs différents: un effet direct dû à un changement de conformation de , et un effet indirect de sur fonction la sous-unité e diminuant son pourrait pouvoir inhibiteur. Il n’yl’hydrolyse a pas encore La de cette régulation être d’éviter de d’interprétation structurale de cesdurant effets. les périodes où la chaîne de l’ATP en inactivant l’enzyme transfert d’électrons ne génère pas de force protomotrice, par exemple la nuit. Toutefois, le rôle de la forme oxydée et de la forme réduite n’est pas clair. In vivo, la forme réduite pourrait être constamment active. Conclusion: malgré la parenté structurale et fonctionnelle évidente entre les sous-unités e bactérienne et chloroplastique, les modalités de la régulation de l’activité ATPasique peuvent différer notablement. De plus, cette régulation n’a peut-être pas le même rôle physiologique dans ces deux

INHIBITION DES F 1 -ATPases MITOCHONDRIALES e d c 10 Dans le cas de l'ATPase mitochondriale, seule existe la configuration où les deux hélices de la sous-unité d sont plaquées sur la couronne des sous-unités c. Cette configuration est non inhibitrice. Même si les hélices avaient envie de basculer vers le haut, la présence de la sous-unité e additionnelle les en empêche. IF 1 e d Dans ce cas, le rôle inhibiteur est rempli par une sous-unité dissociable, IF 1 c 10 La force protomotrice (ou la rotation de l’enzyme dans le sens de la synthèse d ’ATP? ) favorise la dissociation de IF 1, ou éventuellement sa fixation sur un site non inhibiteur. La dissipation de la force protomotrice (ou plutôt la rotation dans le sens de l ’hydrolyse? ) entraîne l’inhibition.
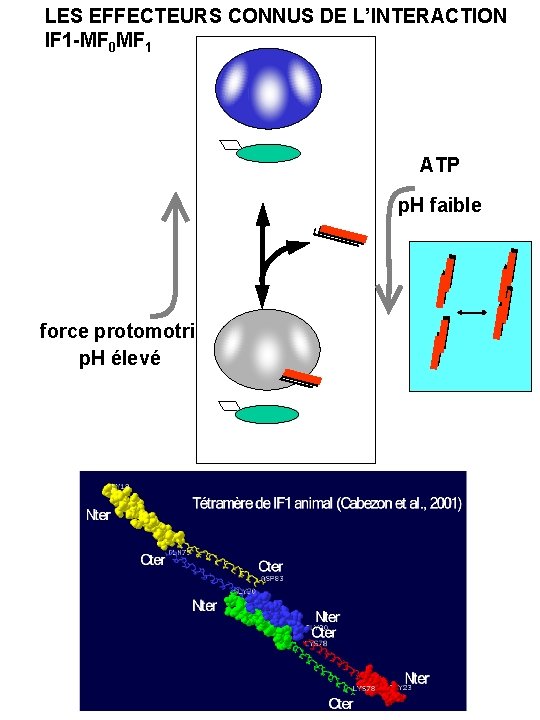
LES EFFECTEURS CONNUS DE L’INTERACTION IF 1 -MF 0 MF 1 ATP p. H faible force protomotrice p. H élevé
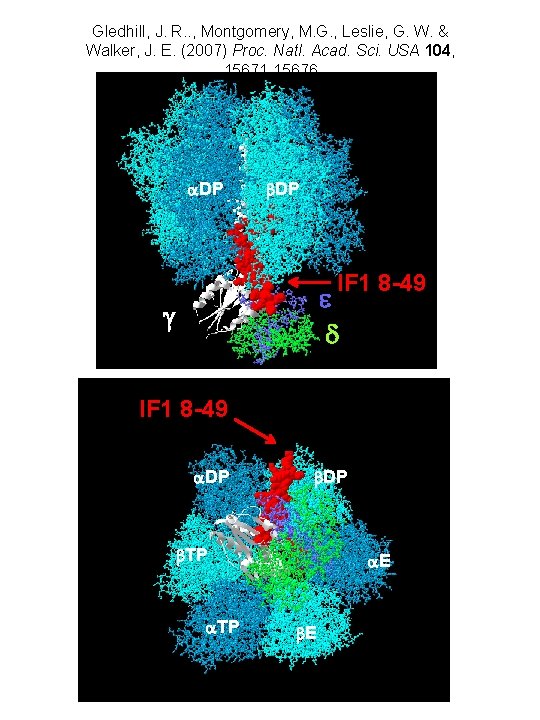
Gledhill, J. R. . , Montgomery, M. G. , Leslie, G. W. & Walker, J. E. (2007) Proc. Natl. Acad. Sci. USA 104, 15671 -15676 a. DP b. DP IF 1 8 -49 e d g IF 1 8 -49 a. DP b. TP a. E b. E

REGULATION DES ATP SYNTHASES MITOCHONDRIALE Dans les mitochondries, l’hydrolyse d ’ATP est inhibée par un peptide inhibiteur appelé IF 1 inhibe l’ATPase de façon stoechiométrique. L’inhibiteur IF 1 (de boeuf) se fixe sur l ’ATPase à l ’interface et interagit aussi avec , quoique plus faiblement. La composante électrique du gradient de protons ( ) favorise la dissociation de IF 1. Un p. H élevé favorise la dissociation de IF 1. L’ATPase ne peut fixer IF 1 que si elle est en train d’hydrolyser de l ’ATP. Il a été proposé que IF 1 pourrait rester fixé sur l’ATP synthase en n’inhibant que l’hydrolyse de l’ATP, mais pas sa synthèse. Propriétés spécifiques au modèle bovin Le peptide IF 1 de boeuf existe sous forme dimérique et tétramérique. Le tétramère serait inactif. Un p. H élevé favorise la tétramérisation du IF 1. In vitro (sous-complexe MF 1 purifié), la fixation de IF 1 favorise la formation de dimères d’ATPase. Cette propriété n ’est pas nécessairement extrapolable au complexe lié à la membrane. Propriétés spécifiques au modèle levure Saccharomyces cerevisiae possède deux peptides inhibiteurs de l’ATPase mitochondriale, IF 1 et STF 1. Leurs séquences sont très proches. Les propriétés d’oligomérisation de ces deux peptides sont différentes de celles du IF 1 de boeuf. La seule différence fonctionnelle claire entre IF 1 et STF 1 est que l’affinité de STF 1 pour l’ATP synthase est nettement plus faible que celle de IF 1. A l’heure actuelle, personne ne sait à quoi sert STF 1, ni même s’il sert à quelque chose. Le rôle physiologique de l’inhibition de l’hydrolyse d’ATP par IF 1 pourrait être d’éviter l’hydrolyse d’ATP lors d’arrêts de la chaîne respiratoire. Cependant, d’autres phénomènes limitent déjà sévèrement l’hydrolyse de l’ATP dans les mitochondries. IF 1 pourrait devenir réellement nécessaire si la membrane mitochondriale devenait in vivo très perméable aux protons (ouverture du «MPT» , situations pré-apoptotiques, etc). On pourrait imaginer que IF 1, en empêchant la génération d’un gradient de protons lors d’arrêts de la chaîne respiratoire, limite l’apparition de radicaux libres.

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
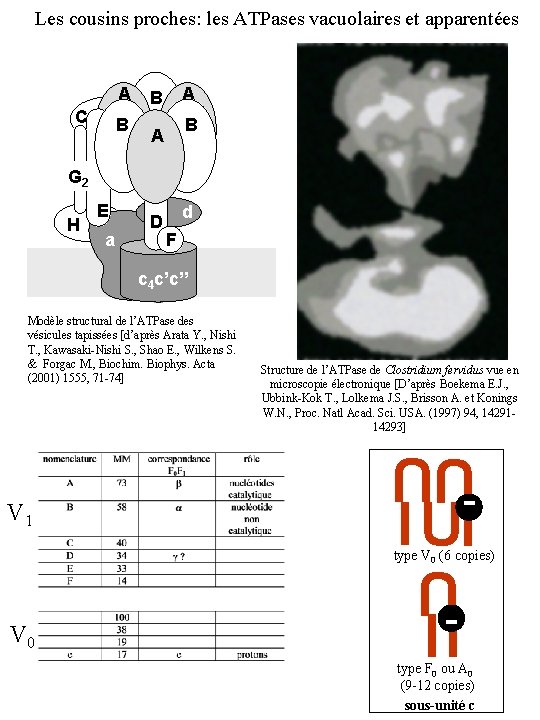
Les cousins proches: les ATPases vacuolaires et apparentées A C B A B B A G 2 H E a D d F c 4 c’c’’ V 1 Structure de l’ATPase de Clostridium fervidus vue en microscopie électronique [D’après Boekema E. J. , Ubbink-Kok T. , Lolkema J. S. , Brisson A. et Konings W. N. , Proc. Natl Acad. Sci. USA. (1997) 94, 1429114293] U I I UU Modèle structural de l’ATPase des vésicules tapissées [d’après Arata Y. , Nishi T. , Kawasaki-Nishi S. , Shao E. , Wilkens S. & Forgac M. , Biochim. Biophys. Acta (2001) 1555, 71 -74] - U type V 0 (6 copies) V 0 - II type F 0 ou A 0 (9 -12 copies) sous-unité c
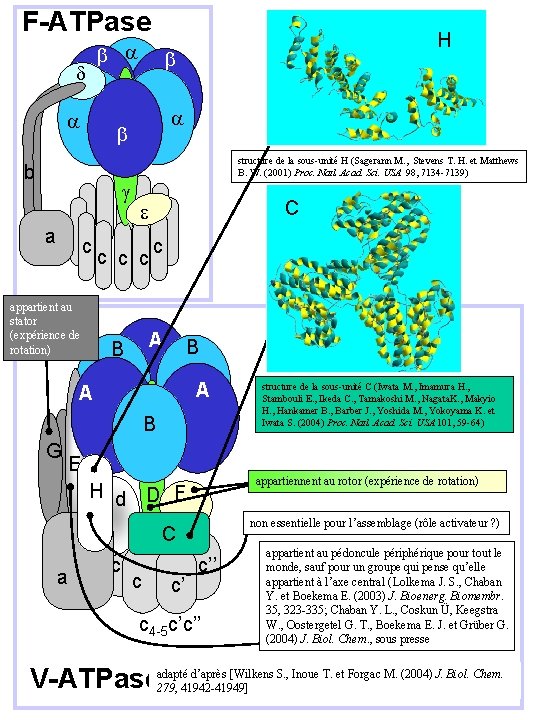
F-ATPase d H structure de la sous-unité H (Sagerann M. , Stevens T. H. et Matthews B. W. (2001) Proc. Natl. Acad. Sci. USA 98, 7134 -7139) b a c appartient au stator (expérience de rotation) C e c c A B B A A B G E H d a c appartiennent au rotor (expérience de rotation) D F c c C c c’ structure de la sous-unité C (Iwata M. , Imamura H. , Stambouli E. , Ikeda C. , Tamakoshi M. , Nagata. K. , Makyio H. , Hankamer B. , Barber J. , Yoshida M. , Yokoyama K. et Iwata S. (2004) Proc. Natl. Acad. Sci. USA 101, 59 -64) non essentielle pour l’assemblage (rôle activateur ? ) c’’ c 4 -5 c’c’’ appartient au pédoncule périphérique pour tout le monde, sauf pour un groupe qui pense qu’elle appartient à l’axe central (Lolkema J. S. , Chaban Y. et Boekema E. (2003) J. Bioenerg. Biomembr. 35, 323 -335; Chaban Y. L. , Coskun Ü, Keegstra W. , Oostergetel G. T. , Boekema E. J. et Grüber G. (2004) J. Biol. Chem. , sous presse d’après [Wilkens S. , Inoue T. et Forgac M. (2004) J. Biol. Chem. V-ATPaseadapté 279, 41942 -41949]
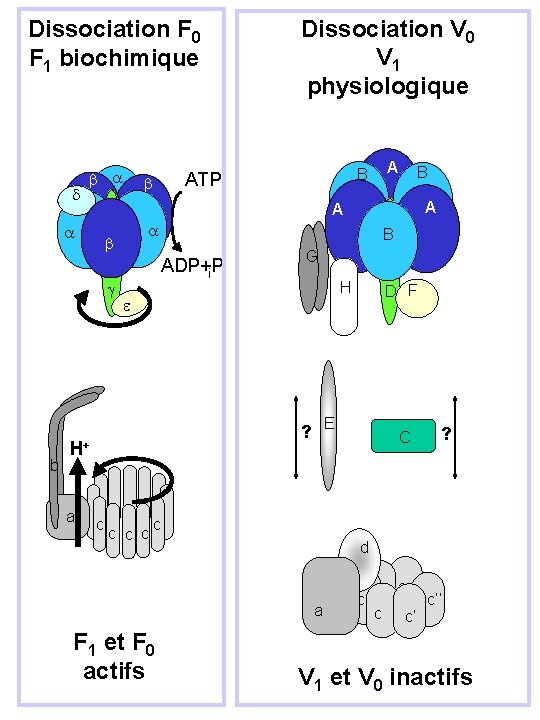
Dissociation F 0 F 1 biochimique d B A d e B ADP+P i A B B H D F A A B G e c c H+ c c c E H d a c G b a A B ATP A b Dissociation V 0 V 1 physiologique E ? a D F C ? C c c c’’ c c c’ c d a F 1 et F 0 actifs c c’’ c c’ V 1 et V 0 inactifs
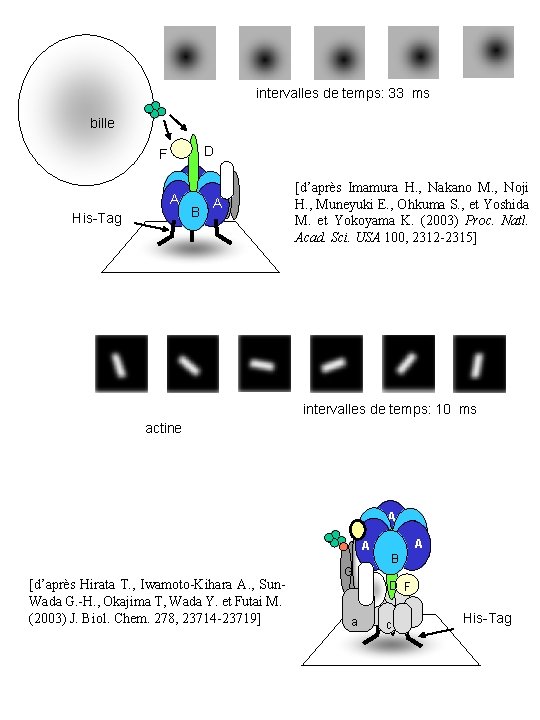
intervalles de temps: 33 ms bille D F A His-Tag B A [d’après Imamura H. , Nakano M. , Noji H. , Muneyuki E. , Ohkuma S. , et Yoshida M. et Yokoyama K. (2003) Proc. Natl. Acad. Sci. USA 100, 2312 -2315] intervalles de temps: 10 ms actine B A A [d’après Hirata T. , Iwamoto-Kihara A. , Sun. Wada G. -H. , Okajima T, Wada Y. et Futai M. (2003) J. Biol. Chem. 278, 23714 -23719] GE B D F a c c c His-Tag
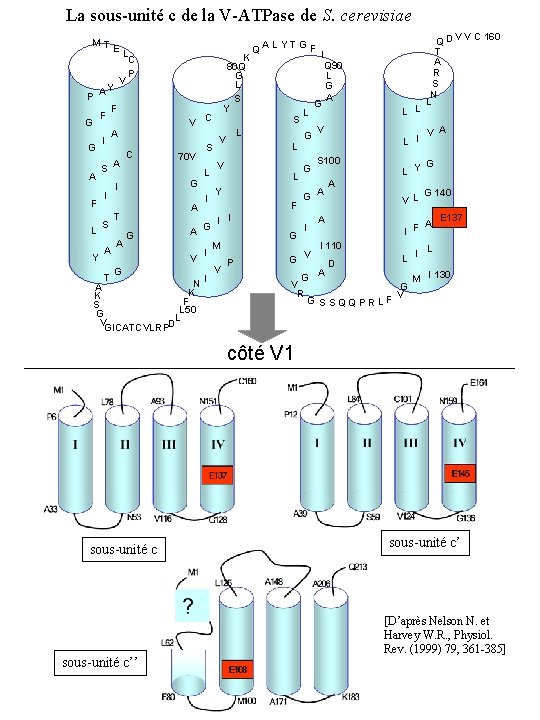
La sous-unité c de la V-ATPase de S. cerevisiae MT E Y P A F F G A I G A F L Y L C P V S A I S A T V C C 70 V G I A T A K 80 Q G L S Y G A V G A K S G V GICATCVLRPD S L I G I NI K F L 50 L Q ALYTGF S L V L Y F I I G M V P L G G I G Q 90 L G A V I G V L I S 100 G A L L V A G 140 A I F I 110 D V V C 160 G L Y A A QD T A R S N L L E 137 I L G A M I 130 V G R V G S S Q Q P R LF côté V 1 sous-unité c’’ sous-unité c’ [D’après Nelson N. et Harvey W. R. , Physiol. Rev. (1999) 79, 361 -385]

Quelques fonctions des ATPases de type V 1. Dans la membrane cytoplasmique de certaines cellules. è Energisation de la membrane apicale de l’épithélium de l’intestin moyen chez les Lépidoptères. Excrétion de potassium par un échangeur électrophorétique + + H /K è Energisation de la membrane apicale de l’épiderme de grenouille. + + + Absorption de Na par un antiport H /Na , et du Cl par un échangeur électrophorétique Cl /HCO 3 è Excrétion d’ions H+ de plusieurs types de cellules : cellules rénales, macrophages, ostéoclastes. 2. Dans les différents compartiments cellulaires è Acidification des phagosomes (activation des protéases et des lipases). è Acidification des vésicules chromaffines et des vésicules synaptiques conduisant à l’accumulation de neurotransmetteurs. è Energisation de la membrane des vacuoles de plantes pour effectuer des transports secondaires (Na+, Ca 2+, métabolites). è Acidification des endosomes (dissociation p H-dépendante des ligands de leurs récepteurs). è Acidification des lysosomes (activation des réactions de dégradation). Quelques modes de régulation des ATPases de type V è Régulation rédox : pontage de deux cystéines situées dans les sous-unités catalytiques. La forme oxydée (pontée) est inactive. è Dissociation réversible de la partie V 0 et de la partie V 1, produisant deux sous-complexes inactifs. è Interaction avec des effecteurs spécifiques.

Déconnexion de V 0 et V 1 dans l’épithélium de l’intestin moyen d’une chenille durant la mue [d’après Sumner J. P. , Dow J. A. , Earley F. G. , Klein U. , Jager D. et Wieczorek H. , J. Biol. Chem. (1995) 270, 5649 -5653] (La chenille photographiée n’est pas de la même espèce que celle de l’expérience; elle provient d’un site WEB: http: //www. univ-lille 1. fr/orchid/frichorc/orinjava. htm#. . /premices/prem_p 11. htm) H+ lumen ADP + PATP i 2 H+ K+ cellule épithéliale
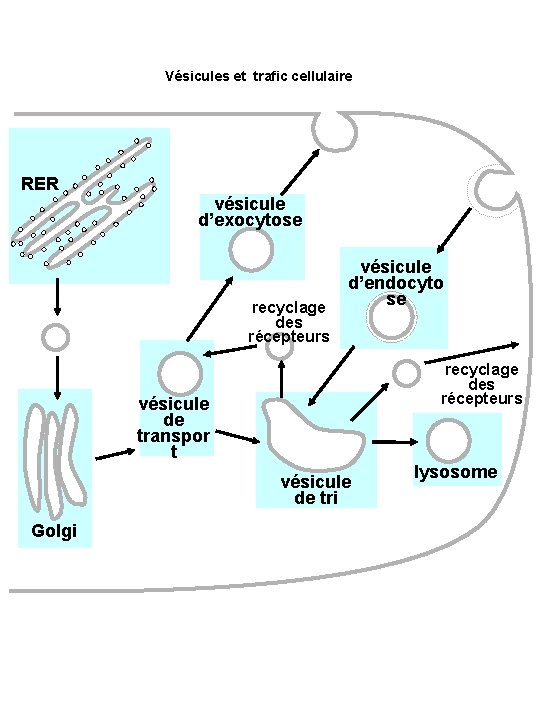
Vésicules et trafic cellulaire RER vésicule d’exocytose recyclage des récepteurs vésicule d’endocyto se recyclage des récepteurs vésicule de transpor t vésicule de tri Golgi lysosome
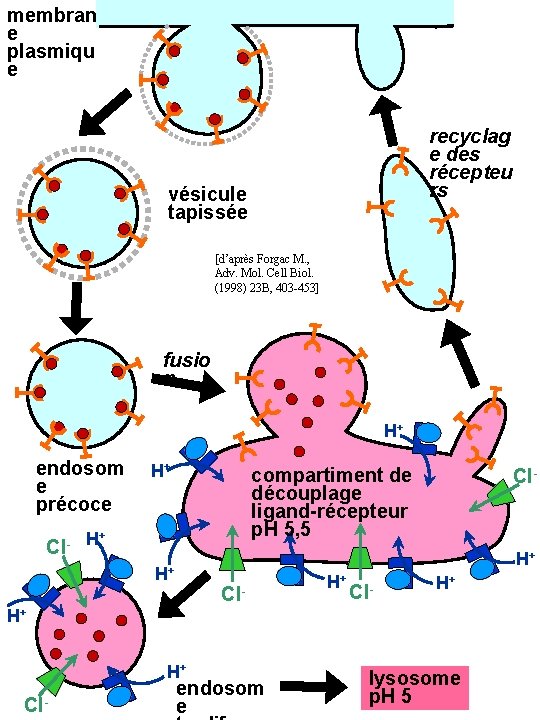
membran e plasmiqu e recyclag e des récepteu rs vésicule tapissée [d’après Forgac M. , Adv. Mol. Cell Biol. (1998) 23 B, 403 -453] fusio n H+ endosom e précoce H+ compartiment de découplage ligand-récepteur p. H 5, 5 + Cl- H+ H+ H+ Cl- endosom e lysosome p. H 5
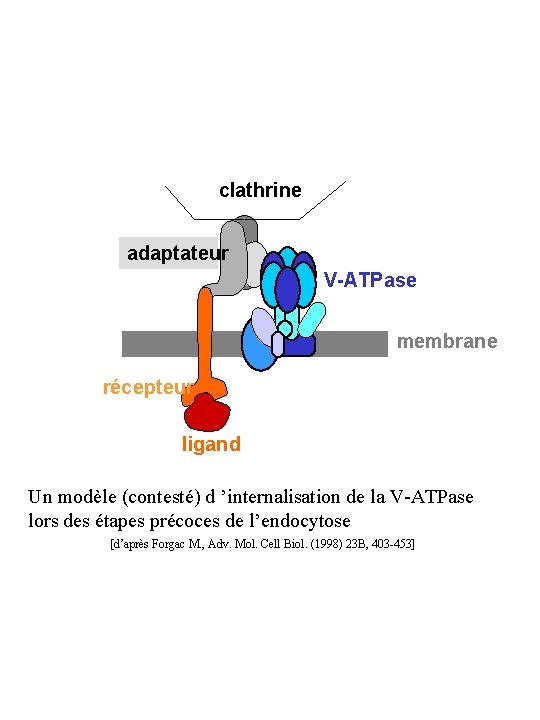
clathrine adaptateur V-ATPase membrane récepteur ligand Un modèle (contesté) d ’internalisation de la V-ATPase lors des étapes précoces de l’endocytose [d’après Forgac M. , Adv. Mol. Cell Biol. (1998) 23 B, 403 -453]
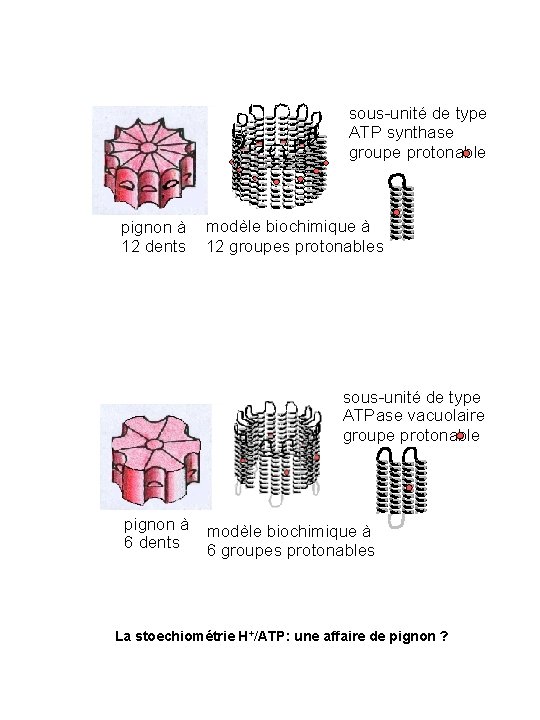
sous-unité de type ATP synthase groupe protonable pignon à 12 dents modèle biochimique à 12 groupes protonables sous-unité de type ATPase vacuolaire groupe protonable pignon à 6 dents modèle biochimique à 6 groupes protonables La stoechiométrie H+/ATP: une affaire de pignon ?
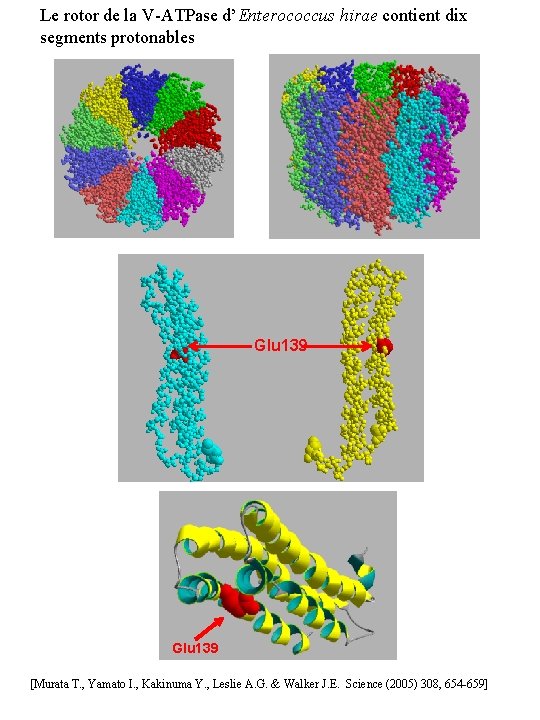
Le rotor de la V-ATPase d’Enterococcus hirae contient dix segments protonables Glu 139 [Murata T. , Yamato I. , Kakinuma Y. , Leslie A. G. & Walker J. E. Science (2005) 308, 654 -659]

Localisation et fonction des ATP synthases Structure générale des ATP synthases et aperçu du mécanisme Les hypothèses fondatrices sur le mécanisme L’hypothèse du proton substrat Le mécanisme de changement d’affinité Structure détaillée de la partie F 1 Les sites nucléotidiques L’axe central Structure de la partie F 0 Architecture du complexe F 0 F 1 Structure de la sous-unité c Structure de la sous-unité a Structure de la sous-unité b Mécanisme de la partie F 1 Evidence biochimique de la rotation Visualisation de la rotation Etats catalytiques, occupation des sites et étapes du mouvement rotatif Mécanisme de la partie F 0 Couplage entre F 0 et F 1 Stoechiométrie H+/ATP nombre de sous-unités c Elasticité et problèmes connexes Régulation de l’activité des ATP synthases Le cas des chloroplastes Le cas de E. coli Existe-t-il des cliquets moléculaires? Comparaison E. coli-chloroplaste Le cas des mitochondries Le peptide inhibiteur IF 1 Les V-ATPases Structure générale des V-ATPases Les sous-unités c des V-ATPases Fonctions des V-ATPases Stoechiométrie H+/ATP: une affaire de pignon Les hélicases hexamériques
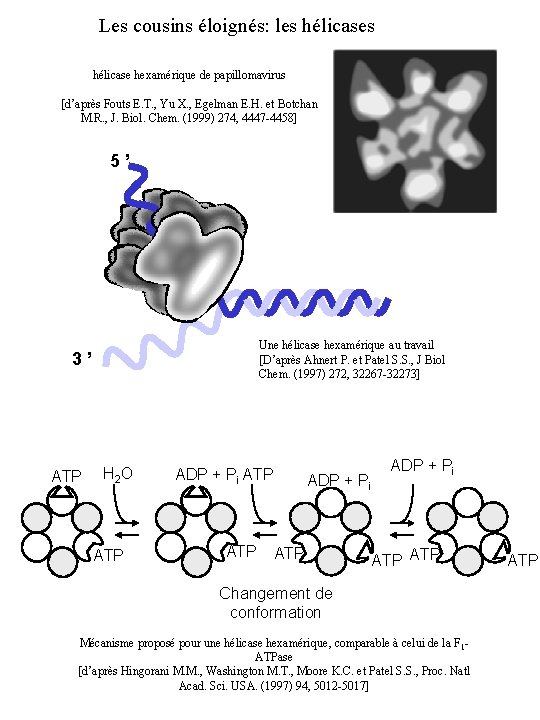
Les cousins éloignés: les hélicase hexamérique de papillomavirus [d’après Fouts E. T. , Yu X. , Egelman E. H. et Botchan M. R. , J. Biol. Chem. (1999) 274, 4447 -4458] 5’ Une hélicase hexamérique au travail [D’après Ahnert P. et Patel S. S. , J Biol Chem. (1997) 272, 32267 -32273] 3’ ATP H 2 O ATP ADP + Pi ATP Changement de conformation Mécanisme proposé pour une hélicase hexamérique, comparable à celui de la F 1 ATPase [d’après Hingorani M. M. , Washington M. T. , Moore K. C. et Patel S. S. , Proc. Natl Acad. Sci. USA. (1997) 94, 5012 -5017] ATP
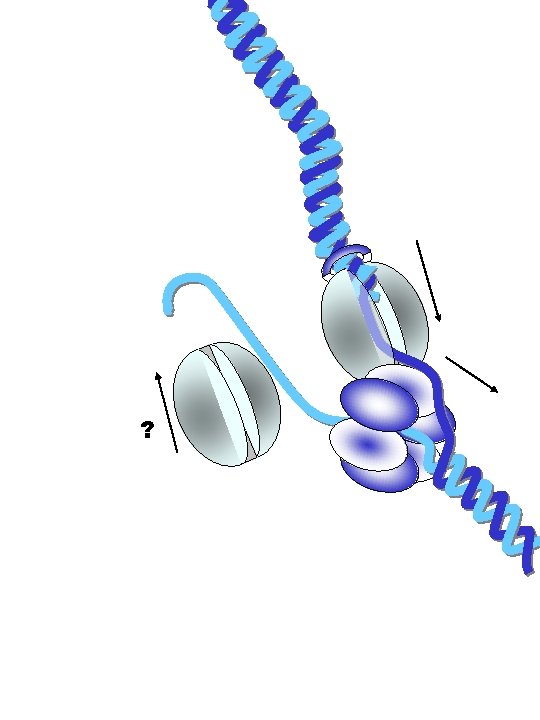
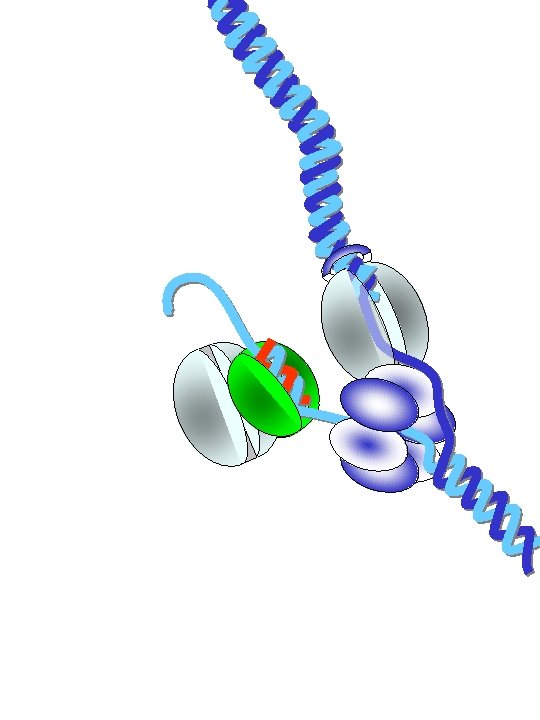
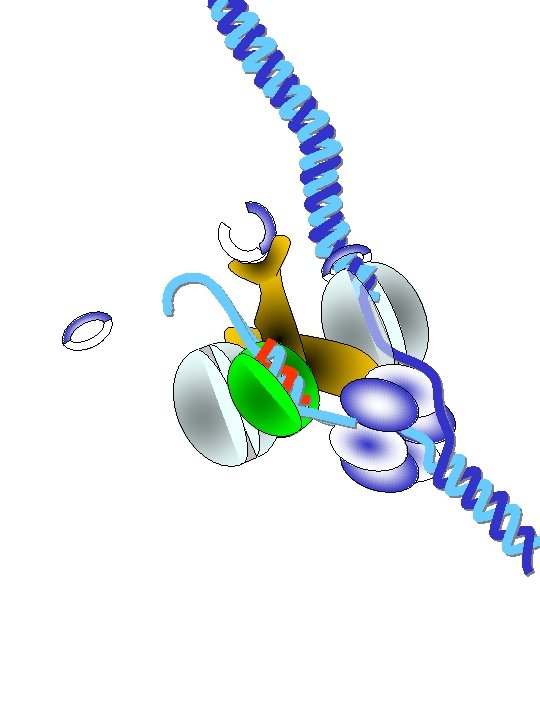


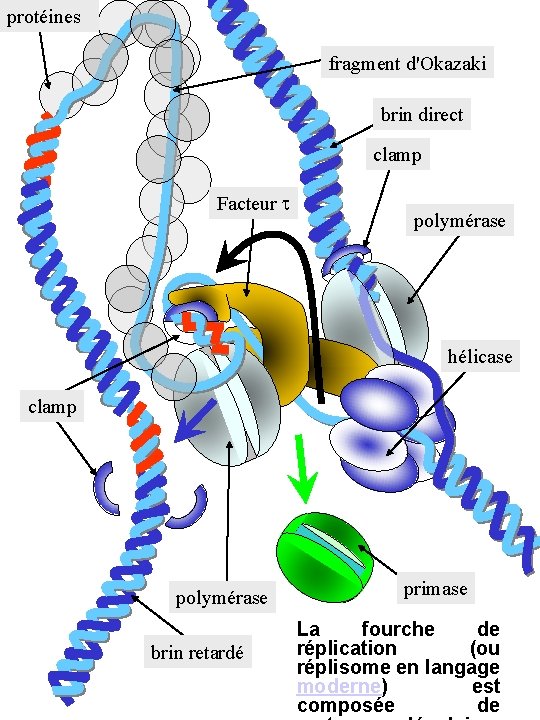
protéines fragment d'Okazaki brin direct clamp Facteur t polymérase hélicase clamp polymérase brin retardé primase La fourche de réplication (ou réplisome en langage moderne) est composée de

Léonard de Vinci (1452 -1519) Etude des vertèbres cervicales de la base du crâne (Royal Collection, Londres) Etude des vertèbres cervicales; analogie avec un mât de navire (Royal Collection, Londres)
- Slides: 90