DIOXIDO DE CARBONO ESTADO ACIDO BASE LA PANTALLA

DIOXIDO DE CARBONO ESTADO ACIDO - BASE

LA PANTALLA SIGUIENTE PERMITE EL ACCESO AL MENÚ EN LA FORMA SECUENCIAL PROGRAMADA. Otra forma es colocar la señal del ratón sobre cada texto marcado para dirigirse a un tema de su elección; debe marcar obligatoriamente el botón REGRESAR para volver a esta pantalla. Alteraciones mixtas Apnea Concentración Consumo de O 2 (VO 2) Curva amortiguadora Diagrama de Davenport p. H Hidrogeniones Bicarbonato normal aumentado disminuido Isobara normal PCO 2 aumentada PCO 2 disminuida Curva amortiguadora normal PCO 2 aumentada PCO 2 disminuida Diagrama de Cohen Diagrama de Sigaard-Andersen Diferencia arterio-venosa de O 2 Diferencia veno-arterial de CO 2 DIÓXIDO DE CARBONO (CO 2) Presión parcial (Pp). . . Alveolar (PA). . . Arterial (Pa). . . Capilar (Pc). . . Venosa (Pv) Disuelto Combinado Bicarbonato Acido carbónico Carbamino Hidrogenión Ecuación Henderson-Hasselbach Eliminación de CO 2 (VCO 2) Fracción de gas Gas seco Gas húmedo Masa Ley de Dalton Saturación (SO 2) p. H ácido p. H alcalino Porcentaje de gas Presión parcial Principio de Fick Procesos agudos acidosis respiratoria alcalosis respiratoria acidosis metabólica alcalosis metabólica Procesos crónicos acidosis respiratoria alcalosis respiratoria acidosis metabólica alcalosis metabólica Receptores cardiopulmonares Receptores pulmonares J Volumen minuto cardiaco

SISTEMA CARDIOPULMONAR Volumen minuto cardíaco Receptores cardiopulmonares Cambios químicos DIOXIDO DE CARBONO MENU GENERAL

REGRESAR S I S T E M A C A R D I O P U L M O N A R La forma tal vez mas simple y mas comúnmente usada para explicar el sistema cardiopulmonar o la relación funcional entre el sistema ventilatorio y el sistema cardiovascular, es a través del principio de Fick. Se usa en fisiología para diferentes órganos o sistemas. Este principio permite analizar y cuantificar la relación entre v masa ( M, gr o l ) v volumen ( V, l ) v M V concentración ( c, gr / l, l / l ) c clic M=c*V V=M/c c=M/V De estas ecuaciones se puede concluir que conociendo dos de las variables se puede calcular la tercera, en una relación funcional múltiple ya que el resultado es diferente según cual sea la variable independiente del fenómeno que se analiza. Ello es así por las complejas interrelaciones que ocurren en los fenómenos biológicos. 1 de 9 MENU

REGRESAR C A R D I O P U L M O N A R En el caso del sistema ventilatorio, éste produce el ingreso del oxígeno en una cantidad que se puede medir en la unidad de tiempo y se conoce como. consumo de oxígeno ( VO 2, cc / min ). Es la masa ( M ) de sustancia incorporada al sistema que se analiza. clic . VO 2 Cv Ca . Q M===M V cc/**V M. . . VCa =(Ca */ Q Q O 2 O 2 (Q – O 2 Cv )Cv =O 2 V = O 2 –O 2–Cv ) O 2 *) V O 2 . S I S T E M A En este mismo sistema, la concentración ( c ) estará dada por la diferencia entre la concentración de oxígeno en arteria menos su concentración en sangre venosa ( Ca. O 2 - Cv. O 2 ), y representa la cantidad de oxígeno por unidad de volumen incorporada a nivel pulmonar. Conocidas estas dos variables se conocerá el volumen ( V ) de líquido en el que se incorporó la sustancia, en este caso el O 2; el cálculo permitirá conocer el. valor del volumen minuto cardíaco (Q) a partir del consumo de O 2 2 de 9 MENU A

S I S T E M A C A R D I O P U L M O N A R REGRESAR Durante la realización de diferentes actividades, la. . . demanda. de O 2 aumenta y el VO 2 puede incrementarse por aumento de la ventilación o de la circulación. En condiciones normales es un efecto combinado de ambos sistemas. En patología uno de ellos puede ser el limitante principal y no es fácil determinarlo con certeza en diferentes pruebas que se realizan. Se puede representar el comportamiento. VO 2 del sistema de una manera mas simplificada pero sumamente útil y también de uso común. Es mas simple si la concentración ( c ) igual a Ca. O 2 – Cv. O 2 Cv Dav Ca se llama diferencia arterio venosa. ( Dav. O 2 ). clic Q La ecuación a usar se simplifica. . VO 2 = Dav. O 2 * Q. clien c El valor de Q no puede ser aumentado mas de 4 o 5 veces sobre su valor reposo. Pero la ventilación puede ser aumentada mas de 15 veces sobre su valor de reposo, por lo que no se considera un factor limitante durante la realización de esfuerzo en el individuo normal. No es este el caso en presencia de patología. 3 de 9 MENU A
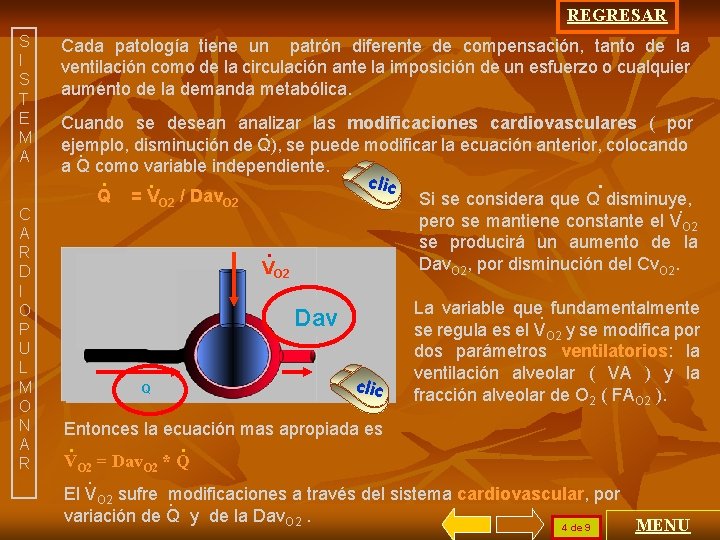
REGRESAR S I S T E M A C A R D I O P U L M O N A R Cada patología tiene un patrón diferente de compensación, tanto de la ventilación como de la circulación ante la imposición de un esfuerzo o cualquier aumento de la demanda metabólica. Cuando se desean analizar las modificaciones cardiovasculares ( por. ejemplo, disminución de Q), se puede modificar la ecuación anterior, colocando. a Q como variable independiente. . clic. . Q = VO 2 / Dav. O 2 Si se considera que Q disminuye, . pero se mantiene constante el VO 2 se producirá un aumento de la. Dav. O 2, por disminución del Cv. O 2. VO 2 Dav clic Q Q La variable que. fundamentalmente se regula es el VO 2 y se modifica por dos parámetros ventilatorios: la ventilación alveolar ( VA ) y la fracción alveolar de O 2 ( FAO 2 ). Entonces la ecuación mas apropiada es . . VO 2 = Dav. O 2 * Q . El VO 2 sufre modificaciones a través del sistema cardiovascular, por. variación de Q y de la Dav. O 2. 4 de 9 MENU

S I S T E M A C A R D I O P U L M O N A R Si se analiza el fenómeno hipoxemiante que se genera por el ingreso al pulmón normal de sangre venosa con muy bajos contenidos de O 2 se estará frente a hipoxemias de origen cardiovascular y no específicamente generadas por un problema ventilatorio. (ver el programa Hematosis, sangre venosa mixta) Los gases en sangre son factores moduladores del sistema cardiovascular fundamentalmente a través de los quimiorreceptores periféricos y de la acción directa sobre los diferentes vasos sanguíneos. Como el organismo a través de complejos mecanismos mantiene la homeostasis por la modificación de diferentes variables, es fundamental el análisis de la ecuación descrita y sus variables, para explicar algunas de las modificaciones que se producen en la realización de esfuerzo o aumento de demandas metabólicas. 5 de 9 MENU

REGRESAR S I S T E M A C A R D I O P U L M O N A R En el caso del sistema ventilatorio el ingreso del oxígeno es una cantidad que se puede. medir en la unidad de tiempo y se conoce como consumo de oxígeno ( VO 2, cc/min. ). (ver el programa HEMATOSIS). Suele calcularse el consumo de O 2 ( VO 2 ) para cuantificar el comportamiento del sistema cardiopulmonar. clic Habitualmente el principio de Fick se analiza para el intercambio de O 2, pero su análisis es también válido para el dióxido de carbono ( CO 2 ). M=c*V V=M/c. VV O 2 Cv Q Ca c=M/V clic Como factor fundamental de control de la ventilación se puede analizar la cantidad de sustancia eliminada del sistema, la que es la masa ( M ) de dióxido de carbono expresada en términos fisiológicos como eliminación de. CO 2 ( VCO 2 ). 6 de 9 MENU

REGRESAR S I S T E M A C A R D I O P U L M O N A R A La concentración (c) estará dada por el contenido de dióxido de carbono en la sangre venosa que ingresa por la arteria pulmonar ( Cv. CO 2), al que se le debe restar el contenido de la sangre arterial que egresa del pulmón con cierta concentración de CO 2 ( Ca. CO 2 ). Conocidas estas dos variables, masa y concentración, se conocerá el volumen ( V ) de líquido del que el CO 2 fue eliminado o excretado; en este caso corresponderá también al volumen minuto cardíaco (Q). M=c*V . . VCO 2 = (Cv. CO 2 – Ca. CO 2 ) * Q clic . VCO 2 Cv. CO 2 Ca. CO 2 . Q (Ver Concentración en el programa Disociacion de Electrolitos) Producto de la actividad metabólica normal, hay una cantidad de CO 2 que es eliminada alcanzando un estado estacionario que mantiene los valores normales de las presiones parciales de CO 2 intracelular ( Pic. CO 2 ) y arterial ( Pa. CO 2 ). Esta regulación se cumple en toda actividad que no llega a producir metabolismo anaerobio. Se altera también por la producción aumentada de diferentes ácidos. ( ver mas adelante ). 7 de 9 MENU

REGRESAR S I S T E M A C A R D I O P U L M O N A R Cuando. se desean analizar las modificaciones cardiovasculares se puede colocar Q como variable independiente, tal como se analizó para el O 2. . . VCO 2 = Dva. CO 2 * Q . . Q = VCO 2 / Dva. CO 2. Si Q disminuye y se mantienen constantes la ventilación y el VO 2 se producirá un aumento de la diferencia entre el Cv. CO 2 y el Ca. CO 2, llamada diferencia venoarterial de CO 2 ( Dva. CO 2 ). El comportamiento normal es un clic ajuste. de la ventilación ante cambios. VCO 2 de Q. La naturaleza exacta de este mecanismo de regulación no está totalmente definida. Dva Cv. CO 2 Ca CO 2 . Se ha postulado la existencia de quimiorreceptores a nivel de sangre. . Q Q venosa mixta (arteria pulmonar) que. no han sido identificados. Este fenómeno se ha explorado, sin llegar a conclusiones precisas modificando el ingreso pulmonar de CO 2 q por el gas alveolar ( ventilación ) q por la sangre venosa mixta ( circulación ) 8 de 9 MENU A
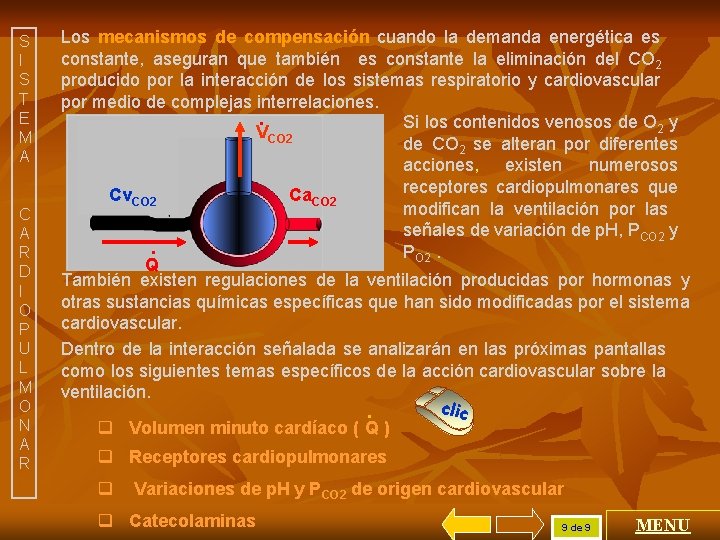
S I S T E M A C A R D I O P U L M O N A R Los mecanismos de compensación cuando la demanda energética es constante, aseguran que también es constante la eliminación del CO 2 producido por la interacción de los sistemas respiratorio y cardiovascular por medio de complejas interrelaciones. . Si los contenidos venosos de O 2 y VCO 2 de CO 2 se alteran por diferentes acciones, existen numerosos receptores cardiopulmonares que Cv. CO 2 Ca. CO 2 modifican la ventilación por las señales de variación de p. H, PCO 2 y. PO 2. Q También existen regulaciones de la ventilación producidas por hormonas y otras sustancias químicas específicas que han sido modificadas por el sistema cardiovascular. Dentro de la interacción señalada se analizarán en las próximas pantallas como los siguientes temas específicos de la acción cardiovascular sobre la ventilación. clic. q Volumen minuto cardíaco ( Q ) q Receptores cardiopulmonares q Variaciones de p. H y PCO 2 de origen cardiovascular q Catecolaminas 9 de 9 MENU

S I S T E M A C A R D I O P U L M O N A R V O L U M E N M I N U T O C A R D I A C O Hay. una incidencia de la ventilación sobre el volumen minuto cardíaco ( Q ), en forma directa o a través de modificaciones de la presión arterial ( Pa ) que se producen por cambios de la frecuencia cardiaca ( Fc ) o del. volumen latido del ventrículo izquierdo ( VL ). También hay acción de Q sobre la ventilación Ventilación > La forma mas directa de producir un aumento. de Q sería por un marcapaso o estimulador 3 segundos eléctrico, que aumentara la frecuencia Quimiorreceptores cardíaca (Fc) sin modificaciones de otro parámetro. clic. Después de aproximadamente 20 segundos Fc > Q > de producido el cambio, se observa un aumento de la ventilación que compensa parte 15 segundos de las modificaciones producidas y se acompaña de un aumento simultáneo del consumo de O 2, de la eliminación de CO 2 y un aumento de la PAO 2. Si se tratara solamente de la acción de los quimiorreceptores ante los cambios de Pa. O 2 y de Pa. CO 2 producidos, su respuesta tardaría c lic entre 3 y 5 segundos. Hay en esta respuesta entonces, un retardo de 15 a 17 segundos, por lo que la aparición del aumento de ventilación está determinado por el tiempo circulatorio y el de. . . transmisión de las señales. 1 de 1 MENU
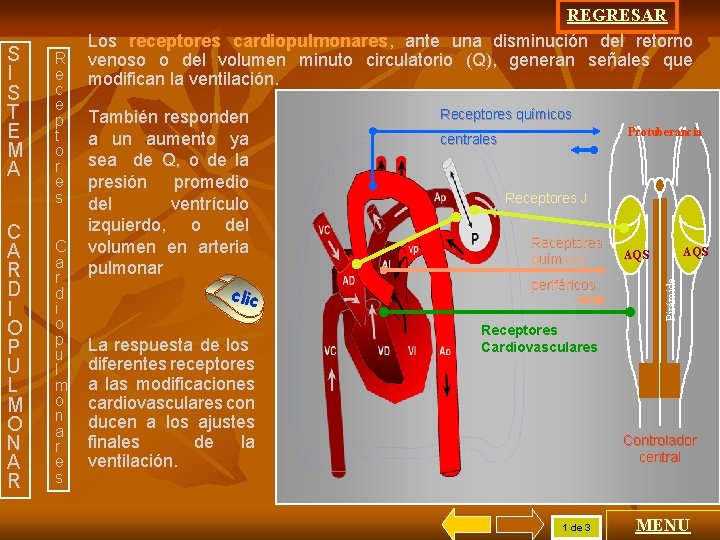
C A R D I O P U L M O N A R R e c e p t o r e s C a r d i o p u l m o n a r e s También responden a un aumento ya sea de Q, o de la presión promedio del ventrículo izquierdo, o del volumen en arteria pulmonar clic La respuesta de los diferentes receptores a las modificaciones cardiovasculares con ducen a los ajustes finales de la ventilación. Receptores químicos Protuberancia centrales Receptores J Receptores químicos periféricos AQS Pirámide S I S T E M A REGRESAR Los receptores cardiopulmonares, ante una disminución del retorno venoso o del volumen minuto circulatorio (Q), generan señales que modifican la ventilación. Receptores Cardiovasculares Controlador central 1 de 3 MENU
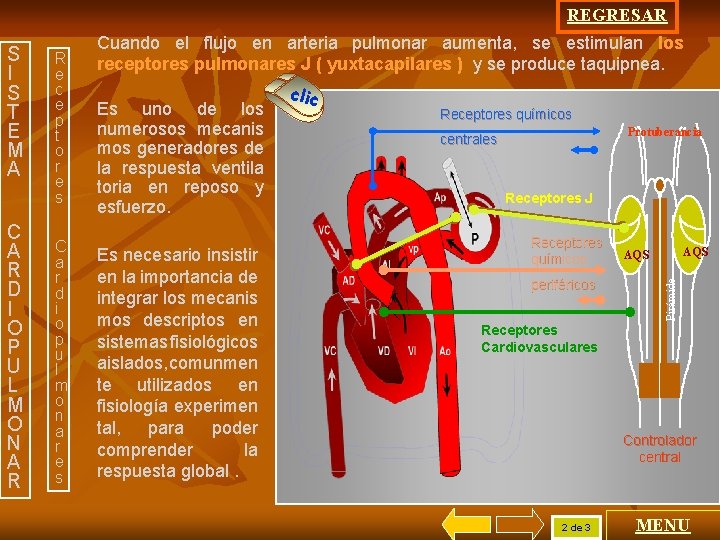
REGRESAR C A R D I O P U L M O N A R R e c e p t o r e s C a r d i o p u l m o n a r e s Cuando el flujo en arteria pulmonar aumenta, se estimulan los receptores pulmonares J ( yuxtacapilares ) y se produce taquipnea. Es uno de los numerosos mecanis mos generadores de la respuesta ventila toria en reposo y esfuerzo. Es necesario insistir en la importancia de integrar los mecanis mos descriptos en sistemas fisiológicos aislados, comunmen te utilizados en fisiología experimen tal, para poder comprender la respuesta global. clic Receptores químicos Protuberancia centrales Receptores J Receptores químicos periféricos AQS Pirámide S I S T E M A Receptores Cardiovasculares Controlador central 2 de 3 MENU
C A R D I O P U L M O N A R R e c e p t o r e s C a r d i o p u l m o n a r e s Protuberancia Solamente se han encarado en este programa algunos de los aspectos más conocidos o más importantes para interpretar la respuesta global producida en varias situaciones. AQS Receptores Cardiovasculares Pirámide S I S T E M A Es muy difícil separar y analizar los efectos cardiovasculares sobre la ventilación de una manera clara, ya que se trata de una red de interconexión con múltiples entradas y salidas. Es por ello que en este tema se desarrollará la integración a nivel de sistema nervioso central y luego la acción de Q sobre la ventilación. Controlador central 3 de 3 MENU
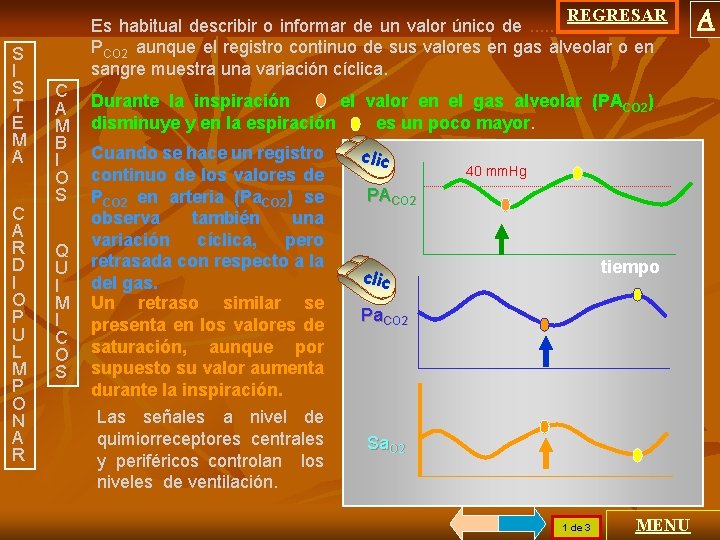
S I S T E M A C A R D I O P U L M P O N A R REGRESAR Es habitual describir o informar de un valor único de. . . PCO 2 aunque el registro continuo de sus valores en gas alveolar o en sangre muestra una variación cíclica. C A M B I O S Q U I M I C O S Durante la inspiración el valor en el gas alveolar (PACO 2) disminuye y en la espiración es un poco mayor. Cuando se hace un registro continuo de los valores de PCO 2 en arteria (Pa. CO 2) se observa también una variación cíclica, pero retrasada con respecto a la del gas. Un retraso similar se presenta en los valores de saturación, aunque por supuesto su valor aumenta durante la inspiración. Las señales a nivel de quimiorreceptores centrales y periféricos controlan los niveles de ventilación. clic 40 mm. Hg PACO 2 tiempo clic Pa. CO 2 Sa. O 2 1 de 3 MENU A
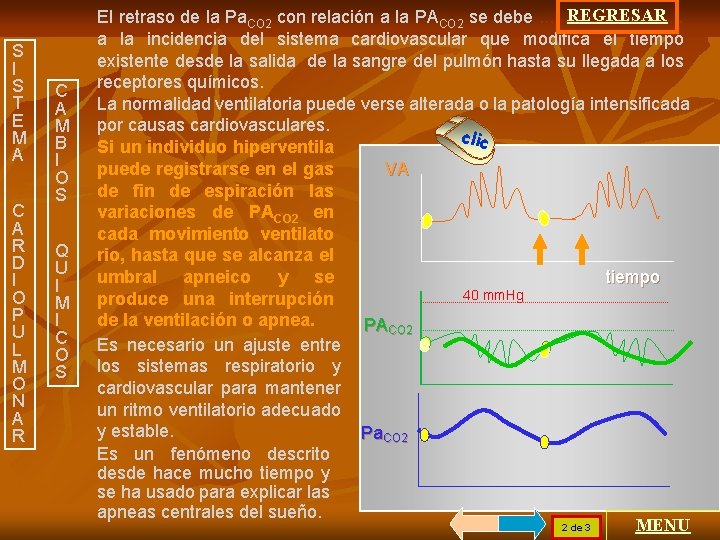
S I S T E M A C A R D I O P U L M O N A R C A M B I O S Q U I M I C O S REGRESAR El retraso de la Pa. CO 2 con relación a la PACO 2 se debe. . . . a la incidencia del sistema cardiovascular que modifica el tiempo existente desde la salida de la sangre del pulmón hasta su llegada a los receptores químicos. La normalidad ventilatoria puede verse alterada o la patología intensificada por causas cardiovasculares. clic Si un individuo hiperventila VA puede registrarse en el gas de fin de espiración las variaciones de PACO 2 en cada movimiento ventilato rio, hasta que se alcanza el umbral apneico y se tiempo 40 mm. Hg produce una interrupción de la ventilación o apnea. PACO 2 Es necesario un ajuste entre los sistemas respiratorio y cardiovascular para mantener un ritmo ventilatorio adecuado y estable. Pa. CO 2 Es un fenómeno descrito desde hace mucho tiempo y se ha usado para explicar las apneas centrales del sueño. 2 de 3 MENU

REGRESAR VA S I. S T E M A C A R D I O P U L M O N A R C A M B I O S Q U I M I C O S VA tiempo clic En este caso especial, es necesario comprender que el tratamiento de la alteración respiratoria ( a presión positiva o CPAP, administra ción de O 2 o CO 2 ) es fundamental para impedir el agravamiento de la patología cardiovascular preexistente ( liberación de catecolaminas, péptido natriurético atrial y otros). A Obviamente cuando el tiempo circulatorio aumenta, por ejemplo en enfermedad cardiaca severa, las señales están muy retrasadas. La hiperventilación continua por más tiempo por retraso en la llegada de la señal y también la apnea que ésta desencadena. No es fácil aceptar que una terapia ventilatoria sea de elección para reducir la incidencia de trastornos cardiovasculares como la hipertensión. También presenta dificultades la aceptación de la incidencia del sistema cardiovascular sobre la ventilación, aunque llega a producir alteraciones graves. 3 de 3 MENU

DIOXIDO DE CARBONO DISUELTO COMBINADO ESTADO ACIDO-BASE MENU GENERAL

DIOXIDO DE CARBONO PRESION PARCIAL DISUELTO Acido carbónico COMBINADO Bicarbonato Carbamino MENU GENERAL

REGRESAR P R E S I O N P A R C I A L Por la ley de Dalton, la presión total de una mezcla gaseosa es igual a la suma de la presión ejercida por cada fracción de gas que la constituye, manteniendo las propiedades como si ocupara el volumen total. Esta ley es fundamental para la comprensión del concepto de presión parcial y para realizar los cálculos correspondientes. La presión barométrica (Pb) es la fuerza ejercida por las capas de aire sobre los objetos y por ello varía con la altura. A nivel del mar es de 760 mm. Hg y a nivel de Caracas, 1000 metros sobre el nivel del mar, es de 690 mm. Hg. La presión total o Pb , al actuar sobre una mezcla como el aire, es ejercida parcialmente por cada componente, dependiendo de la cantidad de cada uno presente en la mezcla. clic Presión PN 2 Total Pb = PO 2 + PN 2 + Potros Pb PO 2 Conociendo la composición de la mezcla y la Pb se pueden calcular las presiones parciales de cada gas. 1 de 3 MENU A
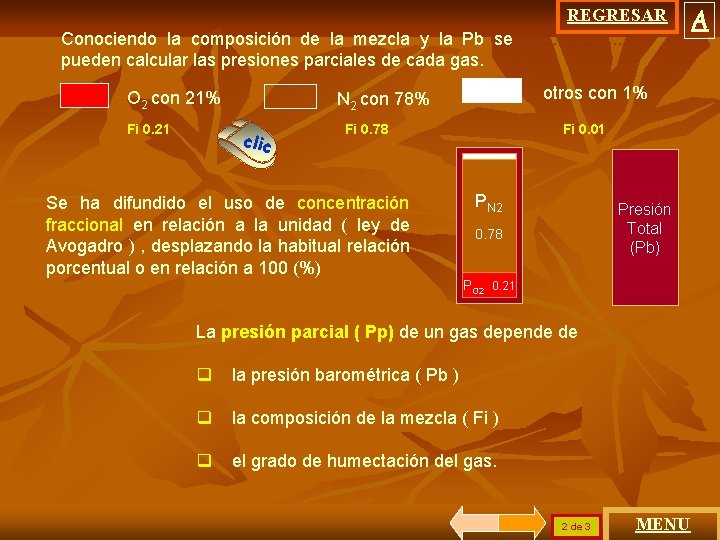
REGRESAR Conociendo la composición de la mezcla y la Pb se. . . pueden calcular las presiones parciales de cada gas. O 2 con 21% Fi 0. 21 otros con 1% N 2 con 78% clic Fi 0. 78 Se ha difundido el uso de concentración fraccional en relación a la unidad ( ley de Avogadro ) , desplazando la habitual relación porcentual o en relación a 100 (%) Fi 0. 01 PN 2 Presión Total (Pb) 0. 78 PO 2 0. 21 La presión parcial ( Pp) de un gas depende de q la presión barométrica ( Pb ) q la composición de la mezcla ( Fi ) q el grado de humectación del gas. 2 de 3 MENU A

REGRESAR P R E S I O N El aire seco inspirado está constituido por Oxígeno, Ntrógeno. y otros gases dentro de los que normalmente no existe CO 2. Pva PN 2 Pb = PO 2+ PN 2 + Potros PO 2 P A R C I A L El aire ambiente saturado con vapor de agua está constituido por Oxígeno, Nitrógeno, otros gases y vapor de agua (va) Pb = PO 2 + PN 2 + Potros + Pva = 47 mm. Hg a 37 o. C clic La presión parcial ( Pp ) de un gas depende de la presión barométrica ( Pb ) , de la composición de la mezcla ( Fi ) y del grado de humectación del gas. Pp gas seco = Pb * Fi Pp gas húmedo = (Pb - Pva ) * Fi 3 de 3 MENU A

REGRESAR Normalmente el gas inspirado no contiene CO 2. salvo durante la realización de pruebas como q la reinhalación para estudiar la respuesta del centro respiratorio CO 2 D I S U E L T O q el agregado de CO 2 en pruebas de peritaje para producir la ventilación máxima involuntaria del paciente q la administración por alcalosis respiratoria extrema y contractura muscular masiva Pv. CO 2 Pa. CO 2 (Ver Gradientes en el programa O 2 Hematosis) El CO 2 aparece en alveolo en su tránsito normal de tejido (Pv. CO 2) a pulmón, pasando por el capilar pulmonar (Pc. CO 2) para su eliminación al exterior. La PCO 2 alveolar ( PACO 2 ) es tan difícil de determinar con exactitud como la PAO 2 , debido a la estructura no homogénea del pulmón. 1 de 5 MENU A

REGRESAR A Se reconoce un equivalente a la PACO 2 cuando se mide la composición del gas eliminado en la fracción de fin de espiración ( end tidal en inglés ). CO 2 D I S U E L T O También suele ser aceptada la PACO 2 como un valor igual al hallado en sangre arterial ( Pa. CO 2 ) debido a la gran difusibilidad y al bajo gradiente arterio-alveolar para este gas en condiciones normales. En patología esto no es válido. clic PCO 2 El CO 2 disuelto depende del coeficiente de solubilidad y de la PCO 2. El coeficiente de solubilidad del CO 2 en plasma ( a ) a 37 grados centígrados es de 0. 03 cc de CO 2 por cada 100 cc de plasma y por mm. Hg de presión parcial de CO 2 disuelto = PCO 2 * a CO 2 disuelto = 40 mm. Hg * 0. 03 cc / 100 cc * mm. Hg (Ver Ley de Henry en el programa Hematosis) CO 2 disuelto = 1. 2 cc / 100 cc 2 de 5 MENU
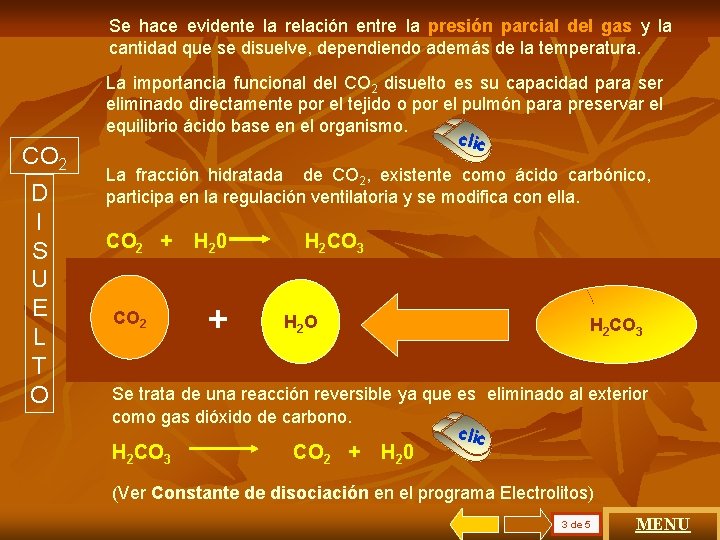
Se hace evidente la relación entre la presión parcial del gas y la cantidad que se disuelve, dependiendo además de la temperatura. CO 2 D I S U E L T O La importancia funcional del CO 2 disuelto es su capacidad para ser eliminado directamente por el tejido o por el pulmón para preservar el equilibrio ácido base en el organismo. clic La fracción hidratada de CO 2, existente como ácido carbónico, participa en la regulación ventilatoria y se modifica con ella. CO 2 + CO 2 H 20 + H 2 CO 3 H 2 O H 2 CO 3 Se trata de una reacción reversible ya que es eliminado al exterior como gas dióxido de carbono. clic H 2 CO 3 CO 2 + H 20 (Ver Constante de disociación en el programa Electrolitos) 3 de 5 MENU
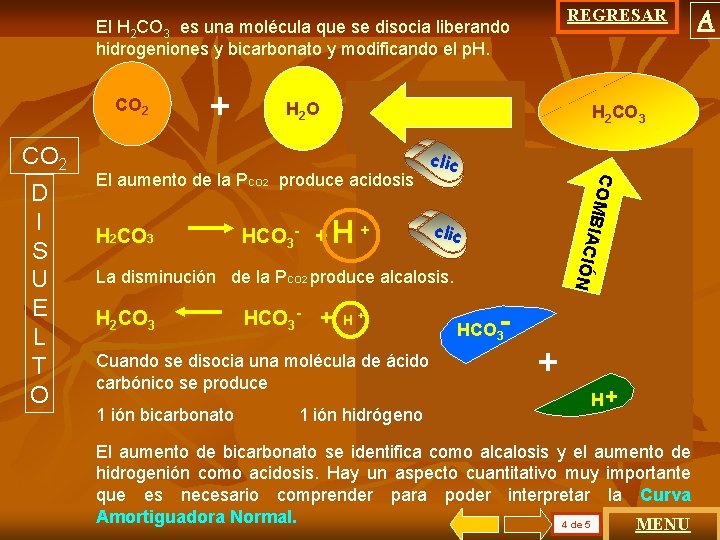
REGRESAR El H 2 CO 3 es una molécula que se disocia liberando. . . . . hidrogeniones y bicarbonato y modificando el p. H. H 2 CO 3 HCO 3 - + H+ IÓN C El aumento de la PCO 2 produce acidosis clic O MB I AC clic IÓN D I S U E L T O H 2 O CI A C CO 2 + DI S O CO 2 La disminución de la PCO 2 produce alcalosis. H 2 CO 3 HCO 3 - + H+ Cuando se disocia una molécula de ácido carbónico se produce 1 ión bicarbonato 1 ión hidrógeno - HCO 3 3 + + H H+ + El aumento de bicarbonato se identifica como alcalosis y el aumento de hidrogenión como acidosis. Hay un aspecto cuantitativo muy importante que es necesario comprender para poder interpretar la Curva Amortiguadora Normal. 4 de 5 MENU A
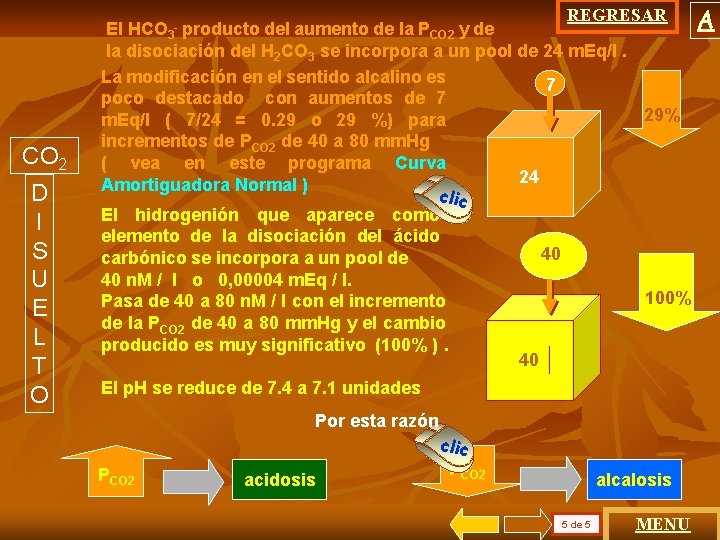
CO 2 D I S U E L T O REGRESAR El HCO 3 - producto del aumento de la PCO 2 y de. . . . la disociación del H 2 CO 3 se incorpora a un pool de 24 m. Eq/l. La modificación en el sentido alcalino es 7 poco destacado con aumentos de 7 29% m. Eq/l ( 7/24 = 0. 29 o 29 %) para incrementos de PCO 2 de 40 a 80 mm. Hg ( vea en este programa Curva 24 Amortiguadora Normal ) clic El hidrogenión que aparece como elemento de la disociación del ácido 40 carbónico se incorpora a un pool de 40 n. M / l o 0, 00004 m. Eq / l. 100% Pasa de 40 a 80 n. M / l con el incremento de la PCO 2 de 40 a 80 mm. Hg y el cambio producido es muy significativo (100% ). 40 El p. H se reduce de 7. 4 a 7. 1 unidades Por esta razón PCO 2 acidosis clic PCO 2 alcalosis 5 de 5 MENU A

REGRESAR El dióxido de carbono se transporta en los fluidos corporales como: q gas disuelto (CO 2 ) q hidratado como ácido carbónico ( H 2 CO 3 ) CO 2 C O M B I N A D O q bicarbonato (HCO 3 -) de sodio y otros iones q compuesto carbamino unido a la hemoglobina (CO 2 Hb ) y proteínas CO 2 total = CO 2 + H 2 CO 3 + HCO 3 - + CO 2 Hb CO 2 disuelto clic CO 2 total clic El CO 2 total en su mayoría está compues to por bicarbo nato. a * PCO 2 El CO 2 disuelto tiene un crecimiento lineal tal como se deduce de la ecuación con que se calcula. PCO 2 La fracción unida a las proteínas ( CO 2 Hb ) es de baja concentración llegando a 10% del total. MENU 1 de 2

REGRESAR Desde el punto de vista de su control y de su regulación hay dos fracciones que componen el bicarbonato plasmático (HCO 3 -) CO 2 C O M B I N A D O q El proveniente de la disociación del ácido carbónico y por lo tanto de las variaciones de PCO 2 a través de la ventilación. clic q El modificado por la excreción y reabsorción a través del riñón. Por supuesto hay posibilidades que se incorpore bicarbonato directamente al organismo a través de la ingesta o por administración endovenosa. También puede modificarse por diálisis renal o peritoneal. (Ver Líquidos del organismo en el programa Distribución Iónica) 2 de 2 MENU

ESTADO ACIDO - BASE DIAGRAMA DE DAVENPORT COMPENSACION DIFERENTES DIAGRAMAS MENU GENERAL

REGRESAR Para comenzar un análisis muy simple de las patologías. . . . ácido-base conviene recordar algunos aspectos de la ecuación de Henderson – Hasselbach. 7. 7 PCO 2 p. H = p. K + log HCO 3 - / a* PCO 2 HCO 37. 4 El valor de p. K para plasma a 37 grados centígrados es de 7. 0 6. 1: es la constante que establece la proporcionalidad entre el p. H y el logaritmo del cociente entre el clic bicarbonato y la presión parcial de CO 2. Analizando la relación entre HCO 3 - y PCO 2 pueden entenderse los cambios que se producen en el p. H. Pero ello no es suficiente para entender los procesos clínicos ya que es necesario conocer la historia del paciente y la evolución de la patología. El análisis de las tres variables no es realmente un proceso complicado, pero sí lo es el poder hacer un diagnóstico diferencial de su relación. La condición de normalidad se describe por los valores clic 7. 4 = 6. 1 + log 24 / a * 40 Debe enfatizarse que en forma aislada ni un p. H de 7. 4, ni un HCO 3 - de 24 m. Eq/l, ni una PCO 2 de 40 mm. Hg son indicadores de normalidad en el estado ácido-base. MENU 1 de 3
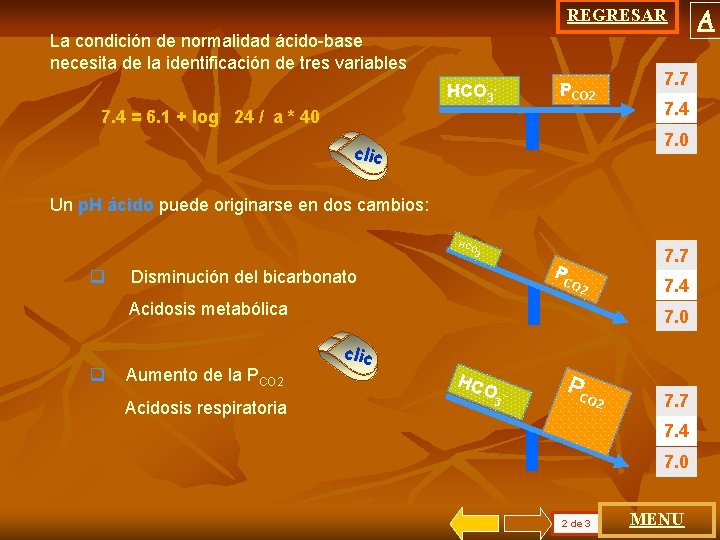
REGRESAR La condición de normalidad ácido-base necesita de la identificación de tres variables PCO 2 HCO 37. 4 = 6. 1 + log 24 / a * 40 7. 7 7. 4 7. 0 clic Un p. H ácido puede originarse en dos cambios: HC O q 7. 7 3 PC Disminución del bicarbonato 7. 4 O 2 Acidosis metabólica q Aumento de la PCO 2 Acidosis respiratoria 7. 0 clic HC O 3 - PC O 2 7. 7 7. 4 7. 0 2 de 3 MENU A
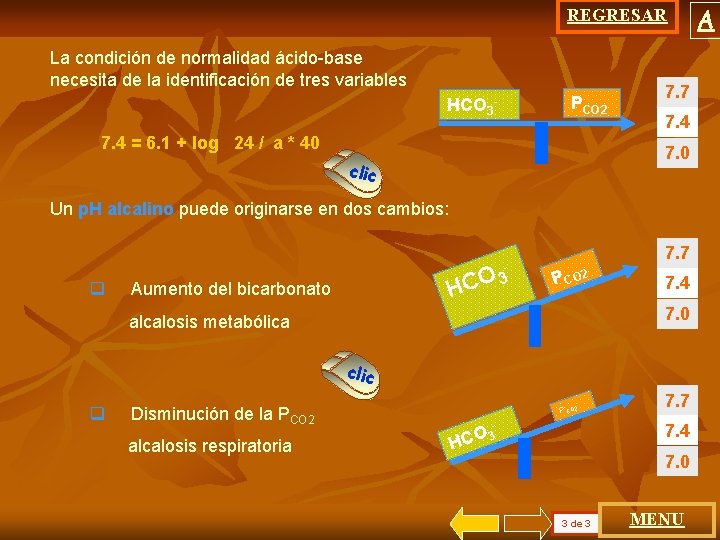
REGRESAR La condición de normalidad ácido-base necesita de la identificación de tres variables PCO 2 HCO 37. 4 = 6. 1 + log 24 / a * 40 7. 7 7. 4 7. 0 clic Un p. H alcalino puede originarse en dos cambios: - q 3 HCO Aumento del bicarbonato 7. 7 P CO 2 7. 4 7. 0 alcalosis metabólica clic q Disminución de la PCO 2 alcalosis respiratoria P CO 2 - 7. 7 7. 4 3 HCO 7. 0 3 de 3 MENU A

Los cambios mencionados en las pantallas anteriores pueden ser complejos : q Agudos o de escaso tiempo de evolución q Crónicos o de largos períodos de evolución q Primarios o causa originaria de la modificación ácido-base q Compensatorios o que responden a mecanismos de regulación ácido-base normales 4 de 3 MENU

DIAGRAMA DE DAVENPORT BICARBONATO ISOBARAS DE PCO 2 CURVA AMORTIGUADORA NORMAL ALTERACIONES MIXTAS MENU GENERAL

REGRESAR Existen tres variables que definen la relación descrita por Henderson y Hasselbach, con una ecuación que generalmente se usa para presentar las alteraciones ácido-base de una manera cuantitativa. 44 40 36 32 28 24 20 BICARBONATO (m. Eq/l) 16 12 8 p. H (Unidades) 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. El diagrama realizado por Horace Davenport es el que se utilizará inicialmente, por sus cualidades didácticas. Se mostrarán otros gráficos de uso clínico. En ordenadas se presenta la concentración del bicarbonato en plasma, de 0 a 44 m. Eq/l. En abcisas se presenta el p. H en sangre, desde 7, 0 hasta 7, 8 unidades. 1 de 5 MENU
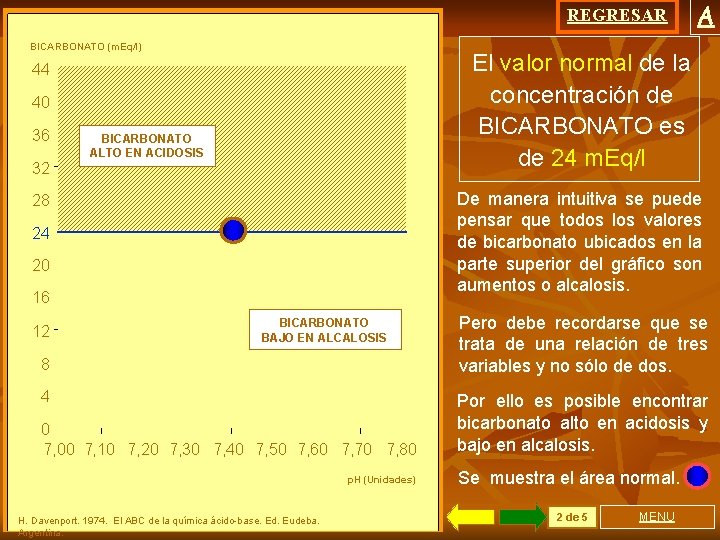
REGRESAR BICARBONATO (m. Eq/l) El valor normal de la concentración de BICARBONATO es de 24 m. Eq/l 44 40 36 32 BICARBONATO ALTO EN ACIDOSIS De manera intuitiva se puede pensar que todos los valores de bicarbonato ubicados en la parte superior del gráfico son aumentos o alcalosis. 28 24 20 16 12 A BICARBONATO BAJO EN ALCALOSIS 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. Pero debe recordarse que se trata de una relación de tres variables y no sólo de dos. Por ello es posible encontrar bicarbonato alto en acidosis y bajo en alcalosis. Se muestra el área normal. 2 de 5 MENU
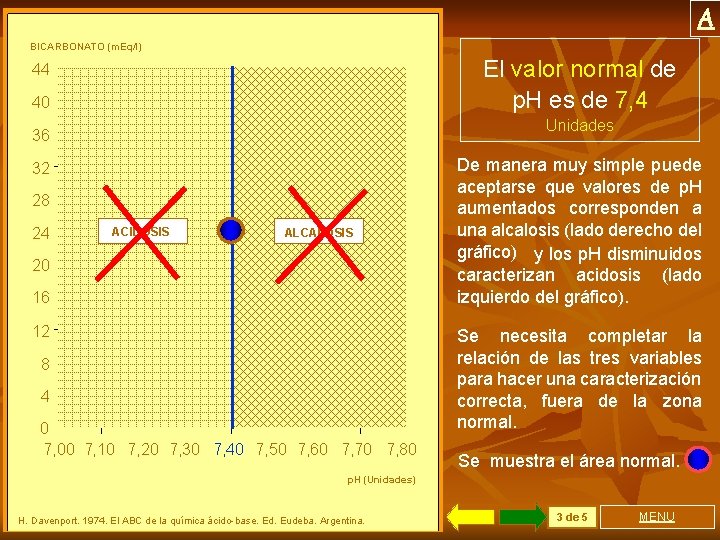
A BICARBONATO (m. Eq/l) El valor normal de p. H es de 7, 4 44 40 Unidades 36 32 28 24 ACIDOSIS ALCALOSIS 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 De manera muy simple puede aceptarse que valores de p. H aumentados corresponden a una alcalosis (lado derecho del gráfico) y los p. H disminuidos caracterizan acidosis (lado izquierdo del gráfico). Se necesita completar la relación de las tres variables para hacer una caracterización correcta, fuera de la zona normal. Se muestra el área normal. p. H (Unidades) H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. 3 de 5 MENU

REGRESAR El p. H es el logaritmo del valor inverso de la concentración de hidrogeniones ( [H+] ). A p. H = log (H+) -1 = log 1/ (H+) Su origen se debe a Sorensen, que desarrolló el potenciómetro con electrodos sensibles a la diferencia de concentración de hidrogeniones entre dos paredes de vidrio. La diferencia de potencial generada en el sistema se expresó en números enteros y por supuesto, dada su definición, en relación logarítmica con la concentración de H+. Si el p. H se representa en una escala lineal, como en el ejemplo actual, la concentración de hidrogeniones tiene una escala logarítmica. clic EN ESTE PROGRAMA SE CONTINUARA USANDO p. H 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 p. H (Unidades) 7, 60 7, 70 7, 80 Ello determina una diferencia de: § 20 n. Moles de [H ] entre p. H de 7, 0 y 7, 1 § 10 n. Moles de [H ] entre p. H de 7, 2 y 7, 3 § 5 n. Moles de [H ] entre p. H de 7, 6 y 7, 7 + + + 100 80 60 50 40 30 25 20 15 + [H ] (n. M/l) (ver Disociación del agua en el programa Electrolitos) Es cómodo utilizar valores enteros de p. H, pero es difícil comparar estos valores concentraciones reales, como es de uso habitual en electrolitos tales como Na+, K+, Ca 2+, entre otros. 4 de 5 MENU
![[H+] (n. M/l) 100 44 80 60 50 40 30 25 20 15 40 [H+] (n. M/l) 100 44 80 60 50 40 30 25 20 15 40](http://slidetodoc.com/presentation_image/eb38554720e20f6cde740a88703c0b39/image-42.jpg)
[H+] (n. M/l) 100 44 80 60 50 40 30 25 20 15 40 36 BICARBONATO (m. Eq/l) 32 28 UNA MISMA VARIACION DE p. H CORRESPONDE A CONCENTRACIONES DIFERENTES EN NANO MOLES p. H [H+] (n. M/l) 7, 00 100 7, 10 80 7, 20 60 7, 30 50 24 (PCO 2) 7, 40 40 [HCO 3 -] 7, 50 30 7, 60 25 7, 70 20 7, 80 15 24 20 16 p. H = 6, 1 + log 10 [HCO 3 -] a (PCO 2) 12 8 4 [H+] = Es necesario incorporar. . el concepto de la concentra ción de H+ en nanomoles por litro, pues su uso se hace cada vez mas común. Se tiene una equivalencia entre ellas a través de la ecuación que define el estado ácido-base: 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) (ver Unidades en el programa Electrolitos) H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. 5 de 5 MENU

BICARBONATO y p. H BICARBONATO DISMINUIDO ACIDOSIS METABOLICA BICARBONATO AUMENTADO ALCALOSIS METABOLICA MENU GENERAL
![REGRESAR 44 p. H = p. K + log ( [HCO 3 -] / REGRESAR 44 p. H = p. K + log ( [HCO 3 -] /](http://slidetodoc.com/presentation_image/eb38554720e20f6cde740a88703c0b39/image-44.jpg)
REGRESAR 44 p. H = p. K + log ( [HCO 3 -] / a PCO 2 ) 40 36 H+ = 24 PCO 2 / [HCO 3 -] BICARBONATO (m. Eq/l) 32 PCO 2: 40 mm. Hg NORMALIDAD RESPIRATORIA 28 24 20 clic 16 Es obvio por la ecuación. . . que define el estado ácido-base, que existe una relación de tres variables: La concentración de bicarbonato ([HCO 3 -]), el p. H y la presión parcial de CO 2 (PCO 2). Se ha descrito la relación bicarbonato – p. H: si el primero vale 24 m Eq/l y el segundo 7, 40 Unidades, necesariamente la tercera variable, la PCO 2, es de 40 mm. Hg. Para una condición de PCO 2 de 40 mm. Hg (NORMALIDAD RESPIRATORIA): 12 [HCO 3 -] m. Eq/l 8 10 p. H 7, 02 4 12 7, 10 16 7, 22 20 7, 32 24 7, 40 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) A 1 de 2 MENU
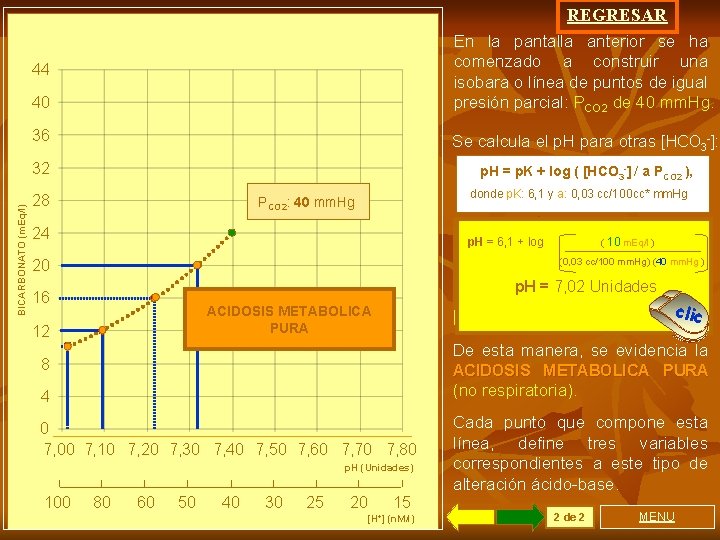
REGRESAR En la pantalla anterior se ha comenzado a construir una isobara o línea de puntos de igual presión parcial: PCO 2 de 40 mm. Hg. 44 BICARBONATO (m. Eq/l) 40 36 Se calcula el p. H para otras [HCO 3 -]: 32 p. H = p. K + log ( [HCO 3 -] / a PCO 2 ), 28 donde p. K: 6, 1 y a: 0, 03 cc/100 cc* mm. Hg PCO 2: 40 mm. Hg 24 De igual se ((identifican los +++forma, log ))) ) log (10 m. Eq/l p. H == 6, 1 U+ log (20 12 m. Eq/l p. H log 16 m. Eq/l demás puntos(0, 03 que configuran una (0, 03 cc/100 mm. Hg)(40 (40 mm. Hg (0, 03 cc/100 mm. Hg) (40 mm. Hg cc/100 mm. Hg) ))) condición de la PCO 2 normal y p. H =p. H 7, 027, 10 Unidades 7, 32 U U disminuido p. H por== 7, 22 descenso de la cclliicc [HCO 3 -] 20 16 ACIDOSIS METABOLICA PURA 12 De esta manera, se evidencia la 8 ACIDOSIS METABOLICA PURA 4 (no respiratoria). 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 Cada punto que compone esta línea, define tres variables correspondientes a este tipo de alteración ácido-base. p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 2 de 2 MENU
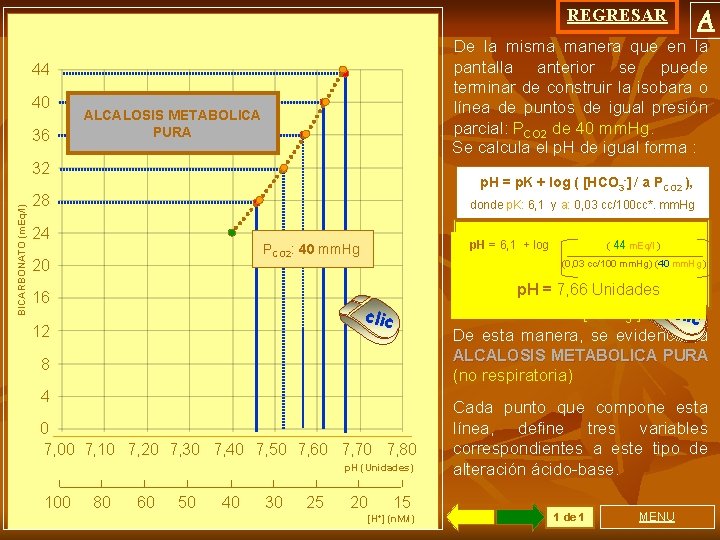
REGRESAR De la misma manera que en la pantalla anterior se puede terminar de construir la isobara o línea de puntos de igual presión parcial: PCO 2 de 40 mm. Hg. Se calcula el p. H de igual forma : 44 40 36 ALCALOSIS METABOLICA PURA BICARBONATO (m. Eq/l) 32 p. H = p. K + log ( [HCO 3 -] / a PCO 2 ), 28 donde p. K: 6, 1 y a: 0, 03 cc/100 cc*. mm. Hg 24 p. H==6, 1 ++log 16 clic 12 (((36 40 32 44 m. Eq/l))) p. H = 6, 1 + log ( 28 m. Eq/l ) Se identifican los demás puntos, (0, 03 cc/100 mm. Hg)(40 (40 mm. Hg))) que configuran una condición de 7, 62 7, 58 p. H===y 7, 47 7, 53 7, 66 Unidades por p. H PCO 2 normal p. H Unidades aumentado incremento en la [HCO 3 -] cclliic De esta manera, se evidencia la PCO 2: 40 mm. Hg 20 ALCALOSIS METABOLICA PURA 8 (no respiratoria) 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 A 80 60 50 40 30 25 20 15 [H+] (n. M/l) Cada punto que compone esta línea, define tres variables correspondientes a este tipo de alteración ácido-base. 1 de 1 MENU

ISOBARA de PCO 2 NORMAL PCO 2 AUMENTADA PCO 2 DISMINUIDA Acidosis respiratoria Alcalosis respiratoria MENU GENERAL
![Toda disminución de. la. concentración de [HCO 3 -] producido con una PCO 2 Toda disminución de. la. concentración de [HCO 3 -] producido con una PCO 2](http://slidetodoc.com/presentation_image/eb38554720e20f6cde740a88703c0b39/image-48.jpg)
Toda disminución de. la. concentración de [HCO 3 -] producido con una PCO 2 constante, conduce a una disminución del p. H. 44 40 36 Para una condición de PCO 2 de 40 mm. Hg (NORMALIDAD RESPIRATORIA): BICARBONATO (m. Eq/l) 32 [HCO 3 -] m. Eq/l p. H 24 24 7, 40 20 20 7, 32 16 16 7, 22 12 12 7, 10 10 7, 02 28 PCO 2: 40 mm. Hg clic 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 A 80 60 50 40 30 25 20 15 [H+] (n. M/l) Con la isobara de PCO 2 de 40 mm. Hg (NORMALIDAD RESPIRATORIA), construida anteriormente, se divide el gráfico y se pueden diferenciar patologías ventilato rias. 1 de 2 MENU
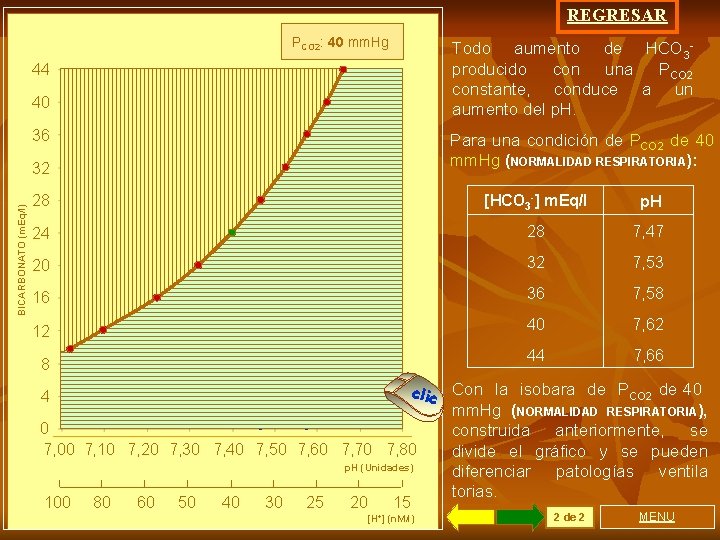
REGRESAR PCO 2: 40 mm. Hg Todo aumento de HCO 3 producido con una PCO 2 constante, conduce a un aumento del p. H. 44 40 36 Para una condición de PCO 2 de 40 mm. Hg (NORMALIDAD RESPIRATORIA): BICARBONATO (m. Eq/l) 32 28 [HCO 3 -] m. Eq/l p. H 24 28 7, 47 20 32 7, 53 16 36 7, 58 12 40 7, 62 44 7, 66 8 clic Con la isobara de PCO 2 de 40 mm. Hg (NORMALIDAD RESPIRATORIA), 0 construida anteriormente, se 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 divide el gráfico y se pueden p. H (Unidades) diferenciar patologías ventila torias. 4 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 2 de 2 MENU
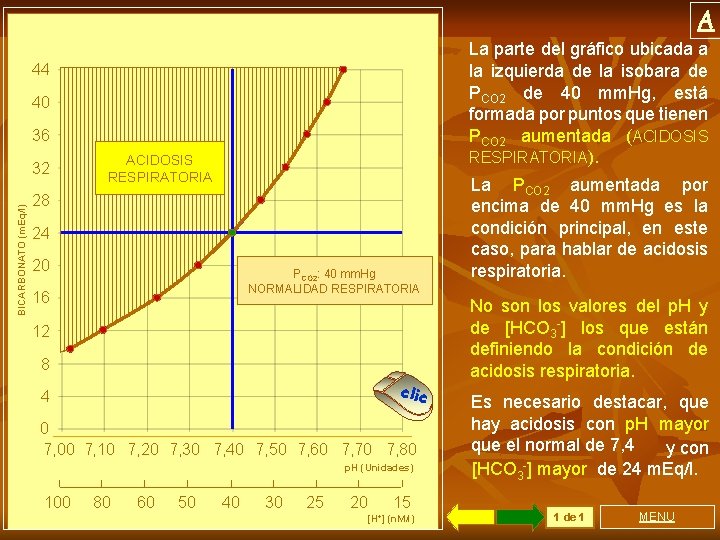
A La parte del gráfico ubicada a la izquierda de la isobara de PCO 2 de 40 mm. Hg, está formada por puntos que tienen PCO 2 aumentada (ACIDOSIS RESPIRATORIA). 44 40 PCO 2 36 BICARBONATO (m. Eq/l) 32 ACIDOSIS PCO 2 RESPIRATORIA 28 24 PCO 2 20 PCO 2: 40 mm. Hg NORMALIDAD RESPIRATORIA 16 12 8 clic 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) La PCO 2 aumentada por encima de 40 mm. Hg es la condición principal, en este caso, para hablar de acidosis respiratoria. No son los valores del p. H y de [HCO 3 -] los que están definiendo la condición de acidosis respiratoria. Es necesario destacar, que hay acidosis con p. H mayor que el normal de 7, 4 y con [HCO 3 -] mayor de 24 m. Eq/l. 1 de 1 MENU
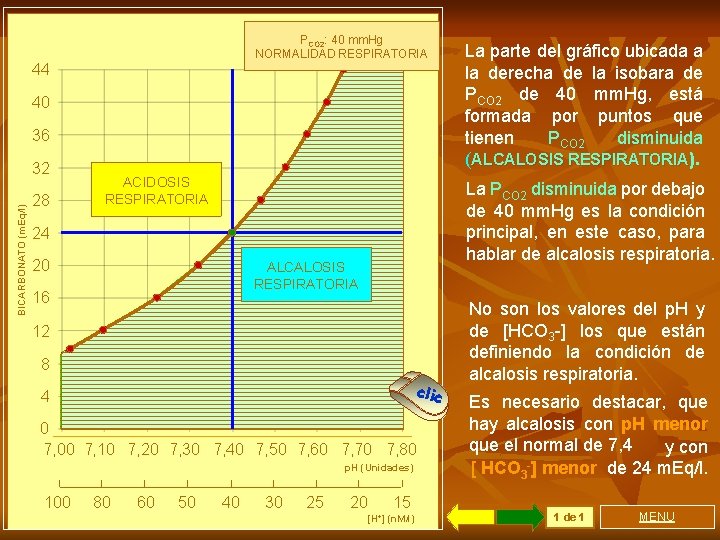
PCO 2: 40 mm. Hg NORMALIDAD RESPIRATORIA 44 40 PCO 2 36 BICARBONATO (m. Eq/l) 32 28 ACIDOSIS RESPIRATORIA La PCO 2 disminuida por debajo de 40 mm. Hg es la condición principal, en este caso, para hablar de alcalosis respiratoria. PCO 2 24 PCO 2 ALCALOSIS RESPIRATORIA 20 16 PCO 2 12 PCO 2 8 PCO 2 4 clic PCO 2 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 La parte del gráfico ubicada a la derecha de la isobara de PCO 2 de 40 mm. Hg, está formada por puntos que tienen PCO 2 disminuida (ALCALOSIS RESPIRATORIA). 15 [H+] (n. M/l) No son los valores del p. H y de [HCO 3 -] los que están definiendo la condición de alcalosis respiratoria. Es necesario destacar, que hay alcalosis con p. H menor que el normal de 7, 4 y con [ HCO 3 -] menor de 24 m. Eq/l. 1 de 1 MENU
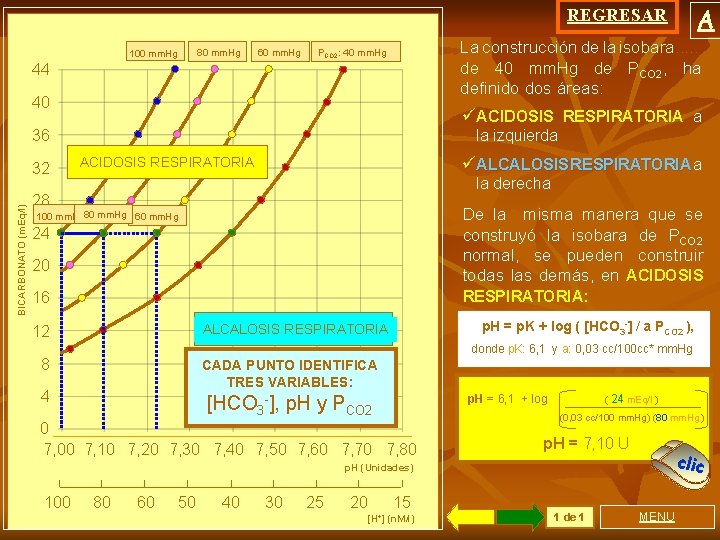
A REGRESAR 80 mm. Hg 100 mm. Hg 60 mm. Hg La construcción de la isobara. . . de 40 mm. Hg de PCO 2, ha definido dos áreas: PCO 2: 40 mm. Hg 44 40 üACIDOSIS RESPIRATORIA a 36 BICARBONATO (m. Eq/l) 32 la izquierda üALCALOSIS RESPIRATORIA a ACIDOSIS RESPIRATORIA la derecha 28 De la misma manera que se construyó la isobara de PCO 2 normal, se pueden construir todas las demás, en ACIDOSIS RESPIRATORIA: 100 mm. Hg 80 mm. Hg 60 mm. Hg 24 20 16 p. H = p. K + log ( [HCO 3 -] / a PCO 2 ), ALCALOSIS RESPIRATORIA 12 donde p. K: 6, 1 y a: 0, 03 cc/100 cc* mm. Hg 8 CADA PUNTO IDENTIFICA TRES VARIABLES: 4 [HCO 3 -], p. H y PCO 2 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 Se calculan las isobaras con p. H = 6, 1 + log ( 24 m. Eq/l ) todos los valores de [HCO 3 ], ) (0, 03 (80 mm. Hg (0, 03 cc/100 mm. Hg)(100 (60 para las PCO 2 seleccionadas p. H =p. H 7, 00 Unidades 7, 10 = 7, 22 U p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 1 de 1 MENU cclliicc
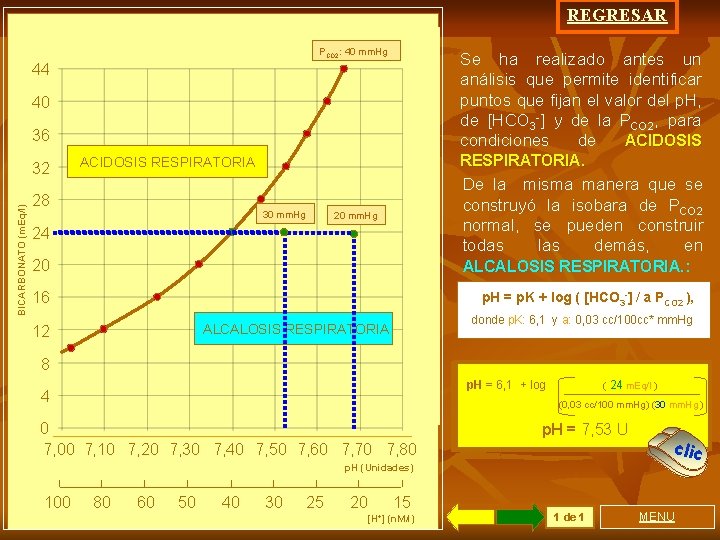
REGRESAR 40 mm. Hg 30 mm. Hg PCO 2 P : 40 CO 2: mm. Hg 44 40 36 BICARBONATO (m. Eq/l) 32 ACIDOSIS RESPIRATORIA 28 20 mm. Hg 30 mm. Hg 24 15 mm. Hg 20 16 Se ha realizado antes un análisis que permite identificar puntos que fijan el valor del p. H, de [HCO 3 -] y de la PCO 2, para condiciones de ACIDOSIS RESPIRATORIA. De la misma manera que se construyó la isobara de PCO 2 normal, se pueden construir todas las demás, en ALCALOSIS RESPIRATORIA. : p. H = p. K + log ( [HCO 3 -] / a PCO 2 ), donde p. K: 6, 1 y a: 0, 03 cc/100 cc* mm. Hg ALCALOSIS RESPIRATORIA 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H==6, 1 + log ( 24 m. Eq/l ) Se calculan las isobaras con p. H - )) (0, 03 cc/100 mm. Hg) (30 mm. Hg (0, 03 (20 todos los valores de [HCO 3 ], para las CO 2 =seleccionadas 7, 53 U p. H P=p. H 7, 70 Unidades cclliicc p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 1 de 1 MENU

CURVA AMORTIGUADORA NORMAL PCO 2 AUMENTADA PCO 2 DISMINUIDA MENU GENERAL
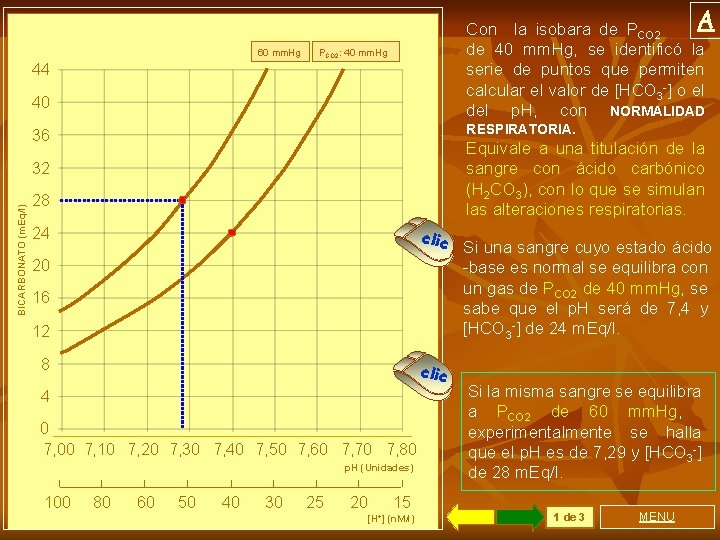
60 mm. Hg Con la isobara de PCO 2. . . A de 40 mm. Hg, se identificó la serie de puntos que permiten calcular el valor de [HCO 3 -] o el del p. H, con NORMALIDAD PCO 2: 40 mm. Hg 44 40 RESPIRATORIA. 36 Equivale a una titulación de la sangre con ácido carbónico (H 2 CO 3), con lo que se simulan las alteraciones respiratorias. BICARBONATO (m. Eq/l) 32 28 clic 24 20 16 12 8 clic 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) Si una sangre cuyo estado ácido -base es normal se equilibra con un gas de PCO 2 de 40 mm. Hg, se sabe que el p. H será de 7, 4 y [HCO 3 -] de 24 m. Eq/l. Si la misma sangre se equilibra a PCO 2 de 60 mm. Hg, experimentalmente se halla que el p. H es de 7, 29 y [HCO 3 -] de 28 m. Eq/l. 1 de 3 MENU
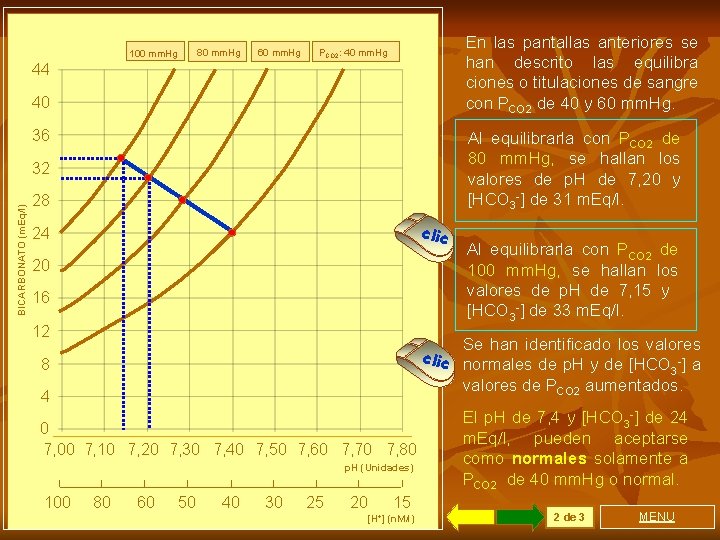
80 mm. Hg 100 mm. Hg 60 mm. Hg En las pantallas anteriores se han descrito las equilibra ciones o titulaciones de sangre con PCO 2 de 40 y 60 mm. Hg. PCO 2: 40 mm. Hg 44 40 36 Al equilibrarla con PCO 2 de 80 mm. Hg, se hallan los valores de p. H de 7, 20 y [HCO 3 -] de 31 m. Eq/l. BICARBONATO (m. Eq/l) 32 28 clic 24 20 16 12 Se han identificado los valores clic normales de p. H y de [HCO -] a 3 valores de PCO 2 aumentados. 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 Al equilibrarla con PCO 2 de 100 mm. Hg, se hallan los valores de p. H de 7, 15 y [HCO 3 -] de 33 m. Eq/l. 80 60 50 40 30 25 20 15 [H+] (n. M/l) El p. H de 7, 4 y [HCO 3 -] de 24 m. Eq/l, pueden aceptarse como normales solamente a PCO 2 de 40 mm. Hg o normal. 2 de 3 MENU
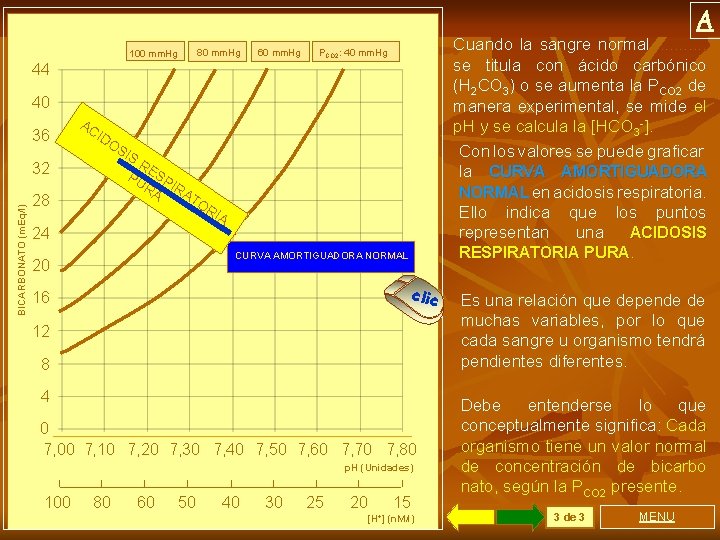
A 80 mm. Hg 100 mm. Hg 60 mm. Hg Cuando la sangre normal. . . se titula con ácido carbónico (H 2 CO 3) o se aumenta la PCO 2 de manera experimental, se mide el p. H y se calcula la [HCO 3 -]. Con los valores se puede graficar la CURVA AMORTIGUADORA NORMAL en acidosis respiratoria. Ello indica que los puntos representan una ACIDOSIS PCO 2: 40 mm. Hg 44 40 36 AC ID OS IS BICARBONATO (m. Eq/l) 32 28 R PU ESP RA IRA T OR IA 24 RESPIRATORIA PURA. CURVA AMORTIGUADORA NORMAL 20 clic 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) Es una relación que depende de muchas variables, por lo que cada sangre u organismo tendrá pendientes diferentes. Debe entenderse lo que conceptualmente significa: Cada organismo tiene un valor normal de concentración de bicarbo nato, según la PCO 2 presente. 3 de 3 MENU
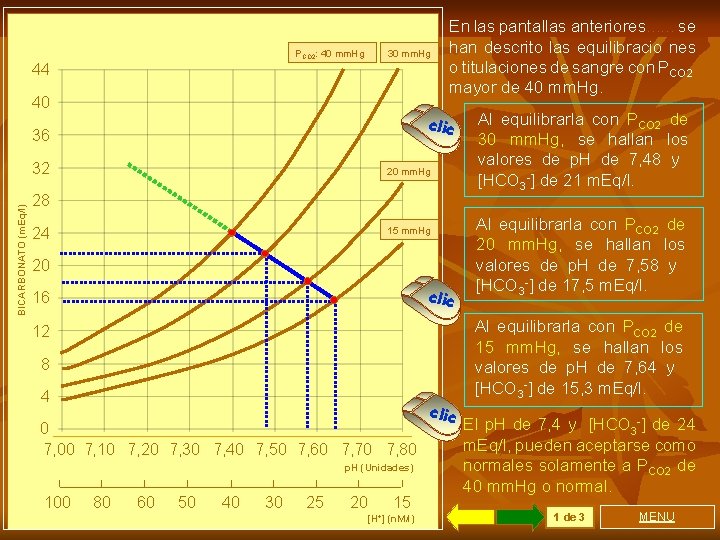
30 mm. Hg PCO 2: 40 mm. Hg 44 40 clic 36 32 BICARBONATO (m. Eq/l) En las pantallas anteriores. . . se han descrito las equilibracio nes o titulaciones de sangre con PCO 2 mayor de 40 mm. Hg. 20 mm. Hg 28 24 15 mm. Hg 20 clic 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) clic Al equilibrarla con PCO 2 de 30 mm. Hg, se hallan los valores de p. H de 7, 48 y [HCO 3 -] de 21 m. Eq/l. Al equilibrarla con PCO 2 de 20 mm. Hg, se hallan los valores de p. H de 7, 58 y [HCO 3 -] de 17, 5 m. Eq/l. Al equilibrarla con PCO 2 de 15 mm. Hg, se hallan los valores de p. H de 7, 64 y [HCO 3 -] de 15, 3 m. Eq/l. El p. H de 7, 4 y [HCO 3 -] de 24 m. Eq/l, pueden aceptarse como normales solamente a PCO 2 de 40 mm. Hg o normal. 1 de 3 MENU
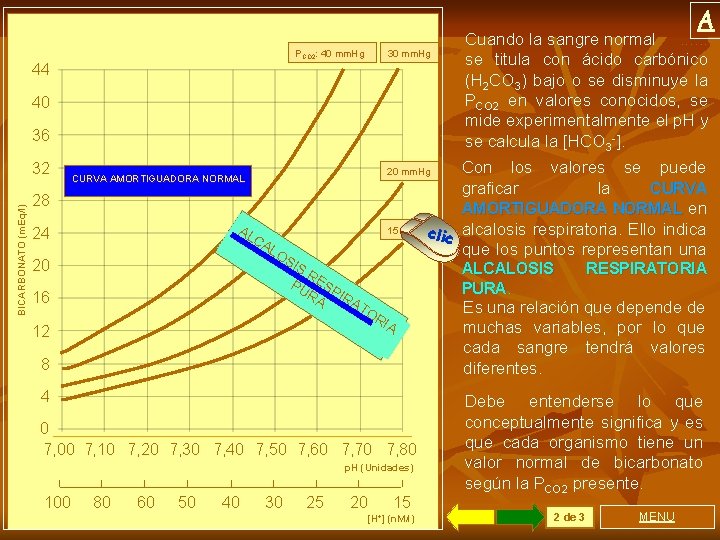
A PCO 2: 40 mm. Hg 44 30 mm. Hg 40 36 BICARBONATO (m. Eq/l) 32 valores se puede la CURVA AMORTIGUADORA NORMAL en 15 mm. Hgc lic alcalosis respiratoria. Ello indica que los puntos representan una 20 mm. Hg CURVA AMORTIGUADORA NORMAL 28 AL 24 CA 20 LO SI S R PU ESP RA IR A 16 IA 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 Con los graficar ALCALOSIS PURA. TO R 12 Cuando la sangre normal. . . se titula con ácido carbónico (H 2 CO 3) bajo o se disminuye la PCO 2 en valores conocidos, se mide experimentalmente el p. H y se calcula la [HCO 3 -]. 20 15 [H+] (n. M/l) RESPIRATORIA Es una relación que depende de muchas variables, por lo que cada sangre tendrá valores diferentes. Debe entenderse lo que conceptualmente significa y es que cada organismo tiene un valor normal de bicarbonato según la PCO 2 presente. 2 de 3 MENU
![REGRESAR La CURVA AMORTIGUA DORA NORMAL contiene los valores normales de [HCO 3 -] REGRESAR La CURVA AMORTIGUA DORA NORMAL contiene los valores normales de [HCO 3 -]](http://slidetodoc.com/presentation_image/eb38554720e20f6cde740a88703c0b39/image-60.jpg)
REGRESAR La CURVA AMORTIGUA DORA NORMAL contiene los valores normales de [HCO 3 -] con aumento o disminución de la PCO 2. Se observa: 44 40 36 ALCALOSIS METABOLICA BICARBONATO (m. Eq/l) 32 ü Un área superior que contiene 28 valores de [HCO 3 -] mayores al normal para cada PCO 2. 24 üEllo se caracteriza como ALCALOSIS METABOLICA, METABOLICA de manera independiente del valor de [HCO 3 -]. clicü Un área inferior que contiene valores de [HCO 3 -] menores al valor normal para cada PCO 2. 20 16 12 ACIDOSIS METABOLICA 8 4 üEllo 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 A 80 60 50 40 30 25 20 15 [H+] (n. M/l) se caracteriza como ACIDOSIS METABOLICA, de manera independiente del valor de [HCO 3 -], de p. H o de [ H+ ] que presente. 3 de 3 MENU
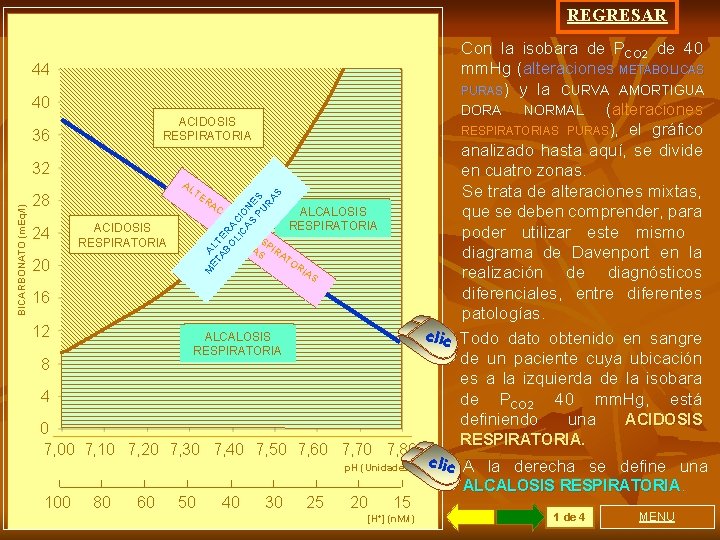
REGRESAR 44 40 ACIDOSIS RESPIRATORIA 36 28 24 ET AL AB TE O RA LI CI CA O S NE PU S RA S AL TE RA CI ACIDOSIS RESPIRATORIA ON ES PU RES RA PI S R ALCALOSIS RESPIRATORIA AT 20 M BICARBONATO (m. Eq/l) 32 OR IA S 16 12 ALCALOSIS RESPIRATORIA 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) Con la isobara de PCO 2 de 40 mm. Hg (alteraciones METABOLICAS PURAS) y la CURVA AMORTIGUA DORA NORMAL (alteraciones RESPIRATORIAS PURAS), el gráfico analizado hasta aquí, se divide en cuatro zonas. Se trata de alteraciones mixtas, que se deben comprender, para poder utilizar este mismo diagrama de Davenport en la realización de diagnósticos diferenciales, entre diferentes patologías. clic Todo dato obtenido en sangre de un paciente cuya ubicación es a la izquierda de la isobara de PCO 2 40 mm. Hg, está definiendo una ACIDOSIS RESPIRATORIA. clic A la derecha se define una ALCALOSIS RESPIRATORIA. 1 de 4 MENU
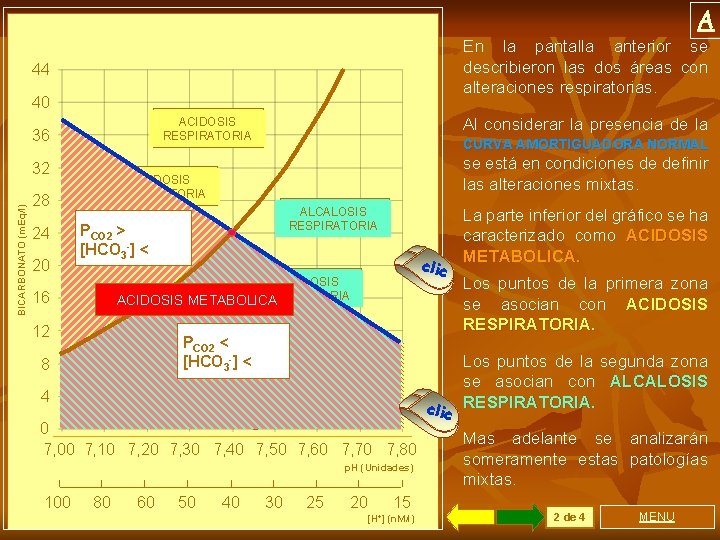
A En la pantalla anterior se describieron las dos áreas con alteraciones respiratorias. 44 40 36 BICARBONATO (m. Eq/l) 32 20 CURVA AMORTIGUADORA NORMAL se está en condiciones de definir las alteraciones mixtas. ACIDOSIS RESPIRATORIA 28 24 Al considerar la presencia de la ACIDOSIS RESPIRATORIA ALCALOSIS RESPIRATORIA ACIDOSIS PCO 2 > RESPIRATORIA [HCO 3 -] < clic ALCALOSIS RESPIRATORIA ACIDOSIS METABOLICA 16 12 ALCALOSIS PRESPIRATORIA CURVA CO 2 < AMORTIGUADORA [HCO 3 ] < NORMAL 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) clic La parte inferior del gráfico se ha caracterizado como ACIDOSIS METABOLICA. Los puntos de la primera zona se asocian con ACIDOSIS RESPIRATORIA. Los puntos de la segunda zona se asocian con ALCALOSIS RESPIRATORIA. Mas adelante se analizarán someramente estas patologías mixtas. 2 de 4 MENU
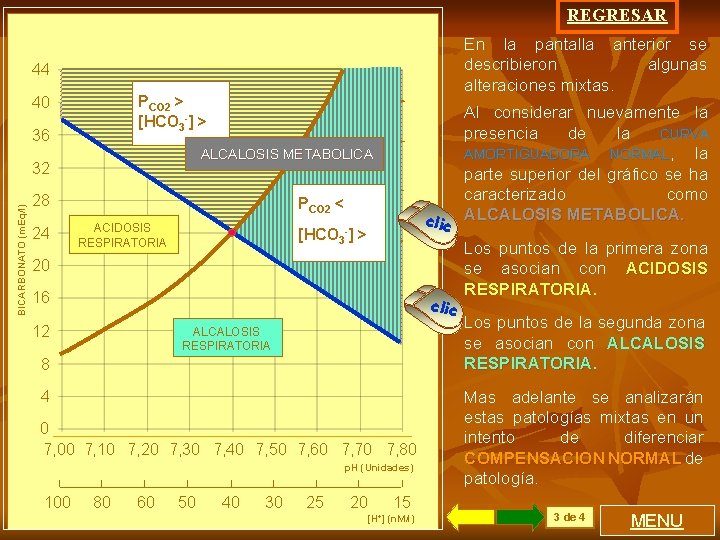
REGRESAR En la pantalla anterior se describieron algunas alteraciones mixtas. 44 PCO 2 > [HCOACIDOSIS 3] > 40 36 RESPIRATORIA ALCALOSIS METABOLICA BICARBONATO (m. Eq/l) 32 28 24 P CO 2 < ALCALOSIS clic RESPIRATORIA - ACIDOSIS RESPIRATORIA [HCO 3 ] > 20 16 clic Al considerar nuevamente la presencia de la CURVA AMORTIGUADORA NORMAL, la parte superior del gráfico se ha caracterizado como ALCALOSIS METABOLICA. Los puntos de la primera zona se asocian con ACIDOSIS RESPIRATORIA. ALCALOSIS RESPIRATORIA Los puntos de la segunda zona se asocian con ALCALOSIS RESPIRATORIA. 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 Mas adelante se analizarán estas patologías mixtas en un intento de diferenciar COMPENSACION NORMAL de patología. 12 8 4 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 3 de 4 MENU

Para realizar un análisis muy simple de las patologías mixtas conviene. . . . recordar algunos aspectos de la ecuación de Henderson – Hasselbach: p. H = p. K + log ( [HCO 3 -] / a *PCO 2 ) p. K, p. K es la constante que establece la proporcionalidad entre el p. H y el logaritmo en base a 10, del cociente entre la concentración del bicarbonato y la presión parcial del CO 2. El valor de p. K para el plasma, a 37 °C, es de 6, 1. clic Analizando la relación entre la [HCO 3 -] y la PCO 2, pueden entenderse los cambios que se producen en el p. H. Pero ello no es suficiente para entender los procesos clínicos, ya que es necesario conocer la historia del paciente y la evolución de la patología. El análisis de las tres variables no es realmente un proceso complicado, pero sí lo es el poder hacer un diagnóstico diferencial de su relación. La condición de normalidad se ha presentado numerosas veces, con anterioridad: 7, 4 = 6, 1 + log ( 24 / 0, 03 *40 ) DEBE ENFATIZARSE QUE EN FORMA AISLADA, NI p. H DE 7, 4, NI [HCO 3 -] DE 24 m. Eq/l, NI PCO 2 DE 40 mm. Hg, SON INDICADORES DE NORMALIDAD EN EL ESTADO ACIDO-BASE 4 de 4 MENU A
DIAGRAMA DE COMPENSACION PROCESOS Agudos Compensados MENU GENERAL

PROCESOS AGUDOS ACIDOSIS RESPIRATORIA ALCALOSIS RESPIRATORIA ACIDOSIS METABOLICA ALCALOSIS METABOLICA MENU GENERAL
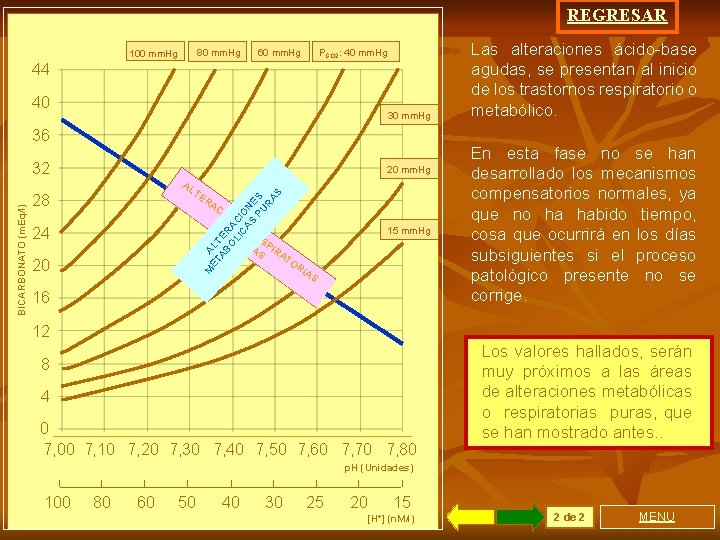
REGRESAR 80 mm. Hg 100 mm. Hg 60 mm. Hg PCO 2: 40 mm. Hg 44 40 30 mm. Hg 36 20 mm. Hg AL TE ET AL AB TE O RA LI CI CA O S NE PU S RA S 28 RA CI 24 20 ON ES PU RES RA PI S RA M BICARBONATO (m. Eq/l) 32 15 mm. Hg TO RI AS 16 Las alteraciones ácido-base agudas, se presentan al inicio de los trastornos respiratorio o metabólico. En esta fase no se han desarrollado los mecanismos compensatorios normales, ya que no ha habido tiempo, cosa que ocurrirá en los días subsiguientes si el proceso patológico presente no se corrige. 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 Los valores hallados, serán muy próximos a las áreas de alteraciones metabólicas o respiratorias puras, que se han mostrado antes. . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) 2 de 2 MENU
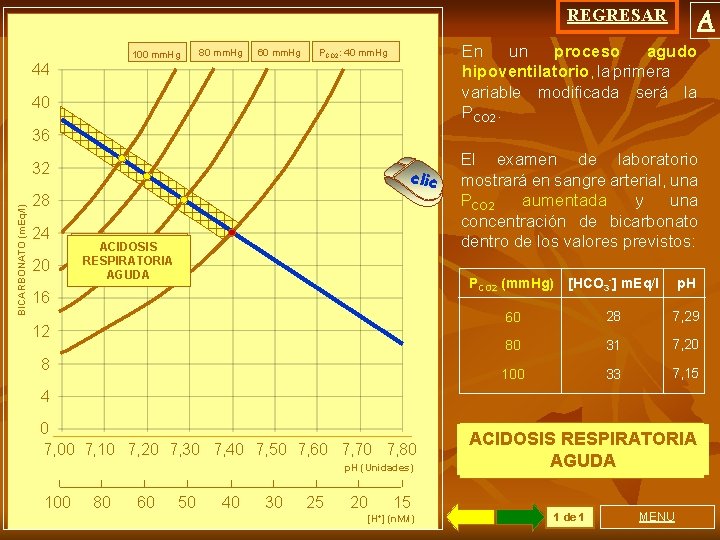
A REGRESAR 100 mm. Hg 80 mm. Hg 60 mm. Hg En un proceso agudo hipoventilatorio, la primera variable modificada será la PCO 2: 40 mm. Hg 44 40 36 BICARBONATO (m. Eq/l) 32 clic 28 24 20 ACIDOSIS RESPIRATORIA AGUDA 16 12 8 El examen de laboratorio mostrará en sangre arterial, una PCO 2 aumentada y una concentración de bicarbonato dentro de los valores previstos: PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 60 28 7, 29 80 31 7, 20 100 33 7, 15 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) ACIDOSIS RESPIRATORIA AGUDA 1 de 1 MENU
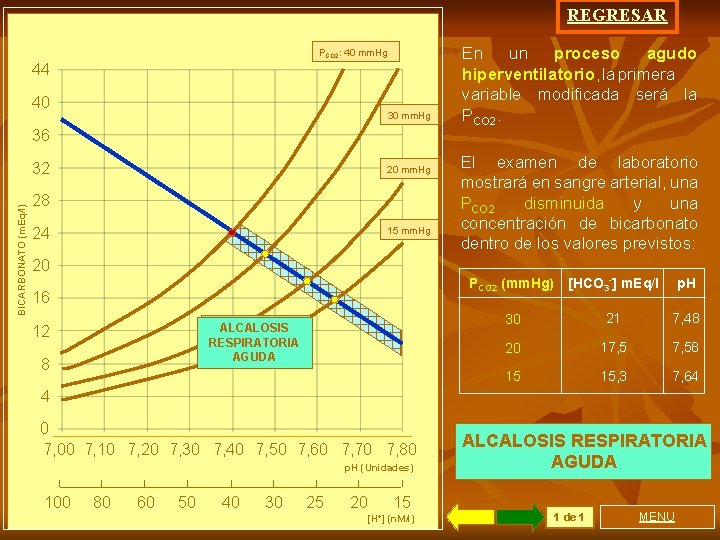
REGRESAR PCO 2: 40 mm. Hg 44 40 30 mm. Hg 36 BICARBONATO (m. Eq/l) 32 20 mm. Hg 28 24 15 mm. Hg En un proceso agudo hiperventilatorio, la primera variable modificada será la PCO 2. El examen de laboratorio mostrará en sangre arterial, una PCO 2 disminuida y una concentración de bicarbonato dentro de los valores previstos: 20 16 ALCALOSIS RESPIRATORIA AGUDA 12 8 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 30 21 7, 48 20 17, 58 15 15, 3 7, 64 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) ALCALOSIS RESPIRATORIA AGUDA 1 de 1 MENU
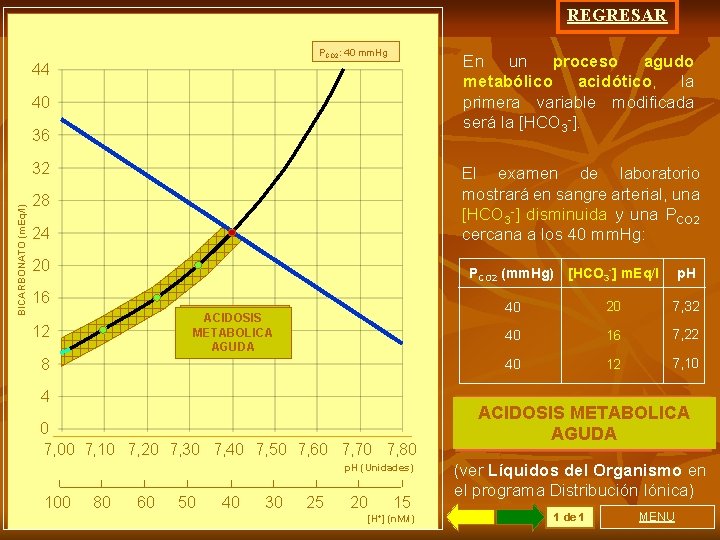
REGRESAR PCO 2: 40 mm. Hg En un proceso agudo metabólico acidótico, la primera variable modificada será la [HCO 3 -]. 44 40 36 BICARBONATO (m. Eq/l) 32 El examen de laboratorio mostrará en sangre arterial, una [HCO 3 -] disminuida y una PCO 2 cercana a los 40 mm. Hg: 28 24 20 16 ACIDOSIS METABOLICA AGUDA 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 40 20 7, 32 40 16 7, 22 40 12 7, 10 ACIDOSIS METABOLICA AGUDA (ver Líquidos del Organismo en el programa Distribución Iónica) 1 de 1 MENU
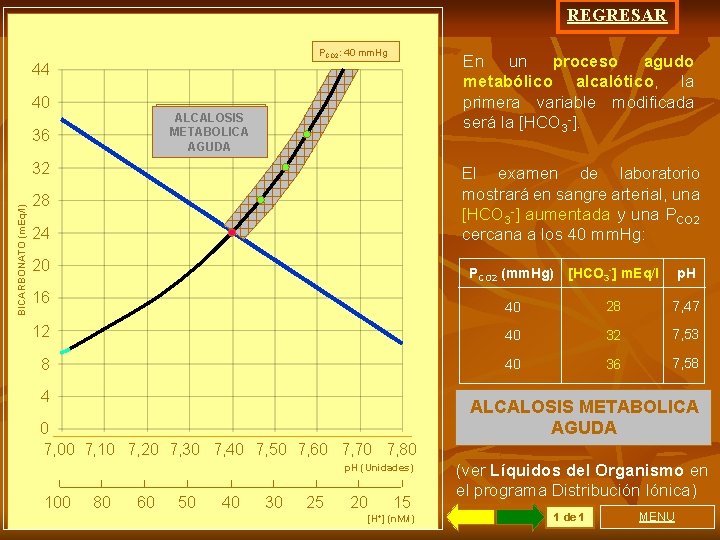
REGRESAR PCO 2: 40 mm. Hg En un proceso agudo metabólico alcalótico, la primera variable modificada será la [HCO 3 -]. 44 40 ALCALOSIS METABOLICA AGUDA 36 BICARBONATO (m. Eq/l) 32 El examen de laboratorio mostrará en sangre arterial, una [HCO 3 -] aumentada y una PCO 2 cercana a los 40 mm. Hg: 28 24 20 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 40 28 7, 47 12 40 32 7, 53 8 40 36 7, 58 16 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) ALCALOSIS METABOLICA AGUDA (ver Líquidos del Organismo en el programa Distribución Iónica) 1 de 1 MENU

PROCESOS CRONICOS ACIDOSIS RESPIRATORIA ALCALOSIS RESPIRATORIA ACIDOSIS METABOLICA ALCALOSIS METABOLICA MENU GENERAL
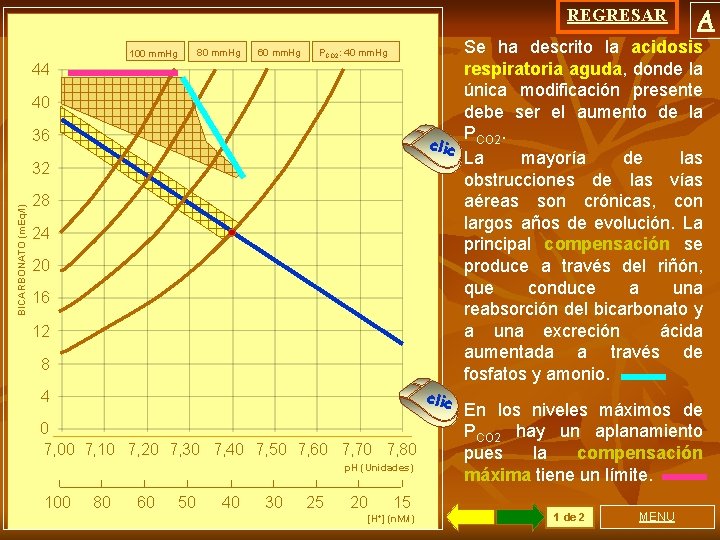
REGRESAR 80 mm. Hg 100 mm. Hg 60 mm. Hg Se ha descrito la acidosis respiratoria aguda, donde la única modificación presente debe ser el aumento de la P. clic CO 2 La mayoría de las obstrucciones de las vías aéreas son crónicas, con largos años de evolución. La principal compensación se produce a través del riñón, que conduce a una reabsorción del bicarbonato y a una excreción ácida aumentada a través de fosfatos y amonio. PCO 2: 40 mm. Hg 44 40 36 BICARBONATO (m. Eq/l) 32 28 24 20 16 12 8 clic 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 A 15 [H+] (n. M/l) En los niveles máximos de PCO 2 hay un aplanamiento pues la compensación máxima tiene un límite. 1 de 2 MENU
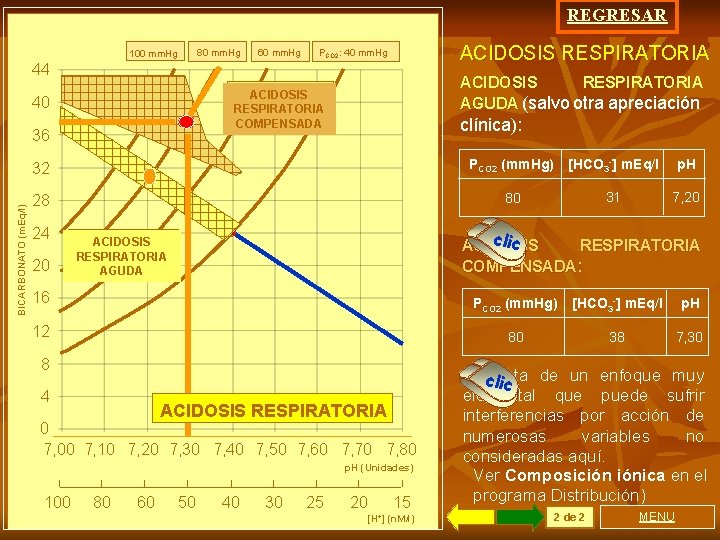
REGRESAR 80 mm. Hg 100 mm. Hg 60 mm. Hg ACIDOSIS RESPIRATORIA PCO 2: 40 mm. Hg 44 40 36 BICARBONATO (m. Eq/l) ACIDOSIS RESPIRATORIA AGUDA (salvo otra apreciación ACIDOSIS RESPIRATORIA COMPENSADA clínica): 32 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 28 80 31 7, 20 24 20 clic ACIDOSIS RESPIRATORIA COMPENSADA: ACIDOSIS RESPIRATORIA AGUDA 16 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 12 80 38 7, 30 8 4 ACIDOSIS RESPIRATORIA 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) Se cltrata de un enfoque muy ic elemental que puede sufrir interferencias por acción de numerosas variables no consideradas aquí. Ver Composición iónica en el programa Distribución) 2 de 2 MENU
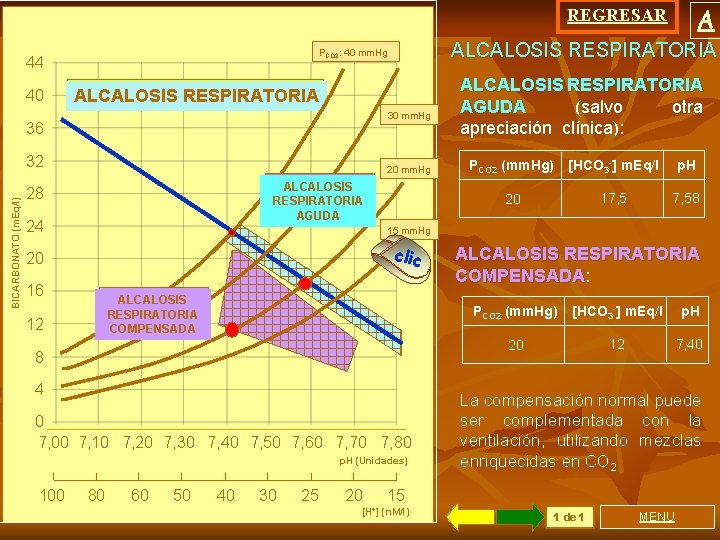
A REGRESAR 40 ALCALOSIS RESPIRATORIA 30 mm. Hg 36 32 BICARBONATO (m. Eq/l) ALCALOSIS RESPIRATORIA PCO 2: 40 mm. Hg 44 20 mm. Hg ALCALOSIS RESPIRATORIA AGUDA 28 24 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 20 17, 58 15 mm. Hg clic 20 16 ALCALOSIS RESPIRATORIA COMPENSADA 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 ALCALOSIS RESPIRATORIA AGUDA (salvo otra apreciación clínica): 80 60 50 40 30 25 20 ALCALOSIS RESPIRATORIA COMPENSADA: COMPENSADA PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 20 12 7, 40 La compensación normal puede ser complementada con la ventilación, utilizando mezclas enriquecidas en CO 2. 15 [H+] (n. M/l) 1 de 1 MENU
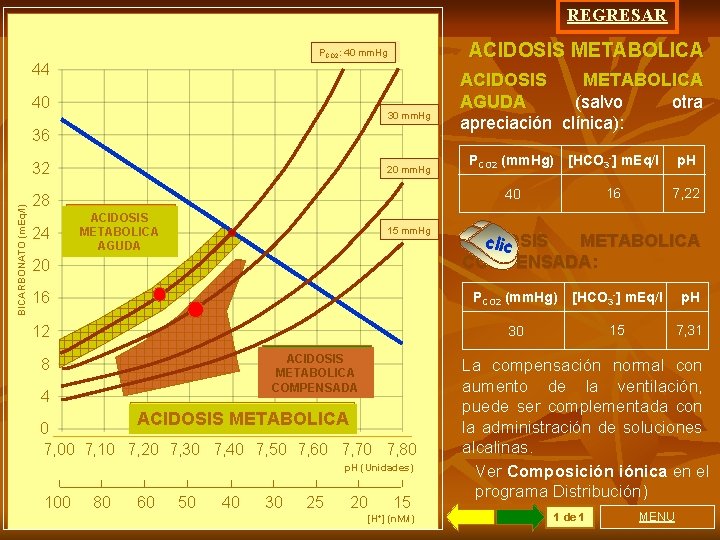
REGRESAR ACIDOSIS METABOLICA PCO 2: 40 mm. Hg 44 40 30 mm. Hg 36 BICARBONATO (m. Eq/l) 32 20 mm. Hg 28 24 ACIDOSIS METABOLICA AGUDA 15 mm. Hg 20 ACIDOSIS METABOLICA AGUDA (salvo otra apreciación clínica): PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 40 16 7, 22 clic ACIDOSIS METABOLICA COMPENSADA: COMPENSADA 16 PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 12 30 15 7, 31 ACIDOSIS METABOLICA COMPENSADA 8 4 ACIDOSIS METABOLICA 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) La compensación normal con aumento de la ventilación, puede ser complementada con la administración de soluciones alcalinas. Ver Composición iónica en el programa Distribución) 1 de 1 MENU
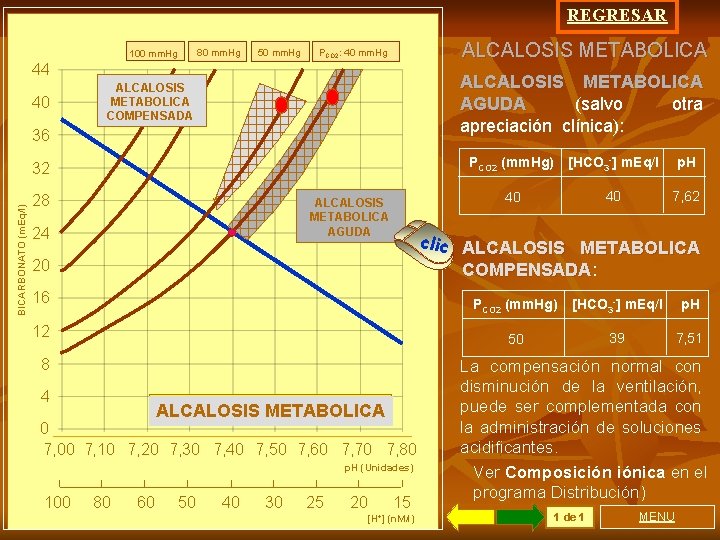
REGRESAR 80 mm. Hg 100 mm. Hg 50 mm. Hg ALCALOSIS METABOLICA PCO 2: 40 mm. Hg 44 40 ALCALOSIS METABOLICA AGUDA (salvo otra apreciación clínica): ALCALOSIS METABOLICA COMPENSADA 36 BICARBONATO (m. Eq/l) 32 28 ALCALOSIS METABOLICA AGUDA 24 16 12 8 ALCALOSIS METABOLICA 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 [HCO 3 -] m. Eq/l p. H 40 40 7, 62 clic ALCALOSIS METABOLICA COMPENSADA: COMPENSADA 20 4 PCO 2 (mm. Hg) 15 [H+] (n. M/l) PCO 2 (mm. Hg) [HCO 3 -] m. Eq/l p. H 50 39 7, 51 La compensación normal con disminución de la ventilación, puede ser complementada con la administración de soluciones acidificantes. Ver Composición iónica en el programa Distribución) 1 de 1 MENU

Diagrama H. Davenport Como se ha apreciado en desarrollos anteriores la interpretación de los datos ob tenidos en el estudio del estado ácido-base es sumamente complejo, lo que ha llevado a la elaboración de diferentes gráficos que ayudan a la interpretación fisiopatológica y a realizar diagnósticos diferenciales en forma rápida. Por su gran ventaja didáctica los autores se han apoyado en el gráfico elaborado por Horace Davenport. Se presenta un resumen de las patologías puras y mixtas y las compensaciones que se pueden hallar. 1 de 3 MENU
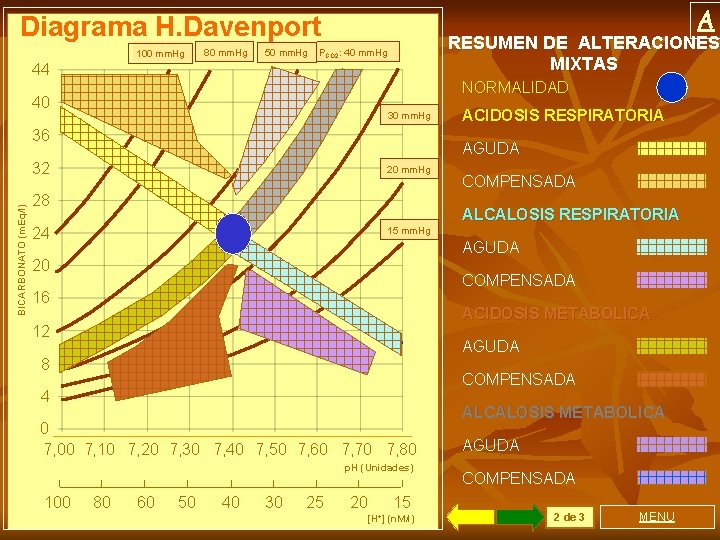
A Diagrama H. Davenport 100 mm. Hg 80 mm. Hg 50 mm. Hg RESUMEN DE ALTERACIONES MIXTAS PCO 2: 40 mm. Hg 44 NORMALIDAD 40 30 mm. Hg 36 AGUDA BICARBONATO (m. Eq/l) 32 20 mm. Hg 28 COMPENSADA ALCALOSIS RESPIRATORIA 24 15 mm. Hg AGUDA 20 COMPENSADA 16 ACIDOSIS METABOLICA 12 AGUDA 8 COMPENSADA 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 ACIDOSIS RESPIRATORIA 80 60 50 40 30 25 20 15 [H+] (n. M/l) ALCALOSIS METABOLICA AGUDA COMPENSADA 2 de 3 MENU

Existen una gran variedad Henderson Hasselbach. de formas de graficación de la ecuación de Por otra parte la variable metabólica descrita, que es el bicarbonato, se ha mostrado que tiene numerosas variaciones, producidas tanto por procesos metabólicos como ventilatorios. Por ello es que se han elaborado variables complejas que no entramos a describir. BUFFER BASE EXCESO DE BASE DEFICIT DE BASE BICARBONATO ESTANDARD Todos lo gráficos representan los mismos valores, pero los autores han considerado cada forma de presentación mas útil o fácil de entender. Diagrama J. J. Cohen Diagrama O. Siggaard Andersen 3 de 3 MENU
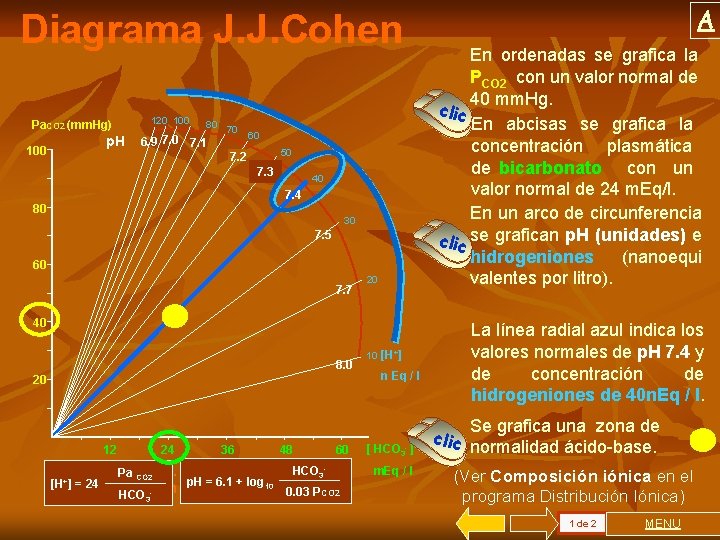
Diagrama J. J. Cohen Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 60 50 7. 2 7. 3 40 7. 4 80 30 7. 5 60 7. 7 20 A En ordenadas se grafica la PCO 2 con un valor normal de 40 mm. Hg. clic En abcisas se grafica la concentración plasmática de bicarbonato con un valor normal de 24 m. Eq/l. En un arco de circunferencia clic se grafican p. H (unidades) e hidrogeniones (nanoequi valentes por litro). 40 8. 0 20 12 24 36 48 60 HCO 3 J. J. Cohen y col. Acid-base. Pa CO 2 p. H = 6. 1 + log 10 [H+]Ed. = 24 Little, Brown Co. 1982 0. 03 PCO 2 HCO 3 - 10 La línea radial azul indica los valores normales de p. H 7. 4 y de concentración de hidrogeniones de 40 n. Eq / l. [H+] n Eq / l [ HCO 3 - ] m. Eq / l clic Se grafica una zona de normalidad ácido-base. (Ver Composición iónica en el programa Distribución Iónica) 1 de 2 MENU
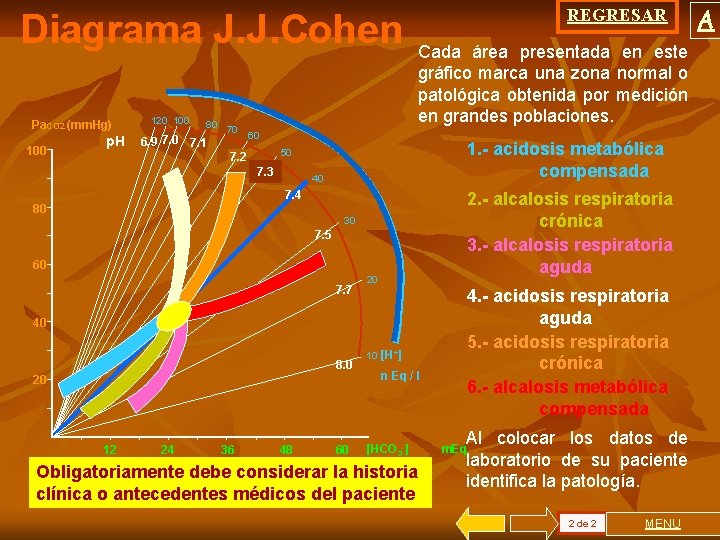
Diagrama J. J. Cohen Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 REGRESAR Cada área presentada en este gráfico marca una zona normal o patológica obtenida por medición en grandes poblaciones. 60 1. - acidosis metabólica compensada 50 7. 2 7. 3 40 7. 4 80 2. - alcalosis respiratoria crónica 3. - alcalosis respiratoria aguda 30 7. 5 60 7. 7 20 40 8. 0 20 12 24 36 48 60 10 [H+] n Eq / l [HCO 3 -] /l HCO 3 - la historia J. J. Cohen y col. Acid-base. Pa CO 2 Obligatoriamente debe considerar + p. H = 6. 1 + log 10 [H Ed. ] = 24 Little, Brown Co. 1982 0. 03 del PCO 2 paciente HCO clínica o antecedentes médicos 3 4. - acidosis respiratoria aguda 5. - acidosis respiratoria crónica 6. - alcalosis metabólica compensada Al colocar los datos de laboratorio de su paciente identifica la patología. m. Eq 2 de 2 MENU A
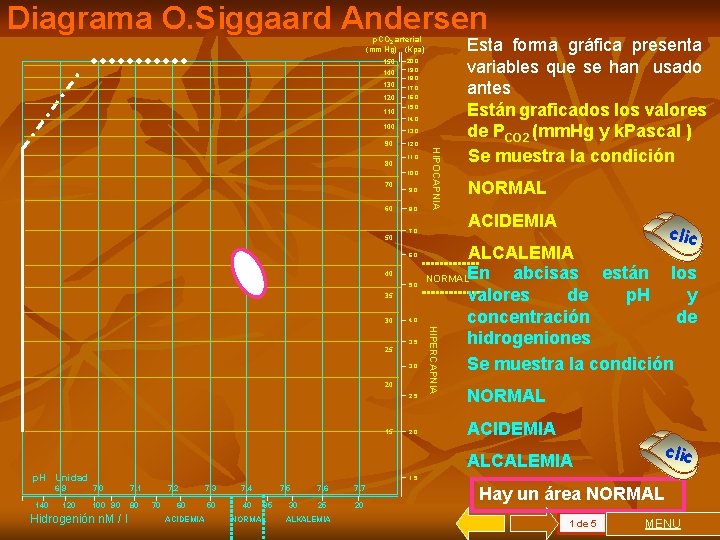
Diagrama O. Siggaard Andersen p. CO 2 arterial (mm Hg) (Kpa) 150 140 130 120 110 100 80 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 70 60 50 9. 0 8. 0 40 5. 0 35 4. 0 3. 0 20 2. 5 15 2. 0 NORMAL clic ALCALEMIA abcisas están los NORMALEn valores de p. H y concentración de hidrogeniones Se muestra la condición HIPERCAPNIA 3. 5 25 Esta forma gráfica presenta variables que se han usado antes Están graficados los valores de PCO 2 (mm. Hg y k. Pascal ) Se muestra la condición ACIDEMIA 7. 0 6. 0 30 HIPOCAPNIA 90 20. 0 19. 0 18. 0 NORMAL ACIDEMIA ALCALEMIA p. H Unidad 6. 9 140 120 clic 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 ACIDEMIA 7. 3 7. 4 50 40 7. 5 35 NORMAL 30 7. 6 7. 7 25 20 ALKALEMIA Hay un área NORMAL 1 de 5 MENU
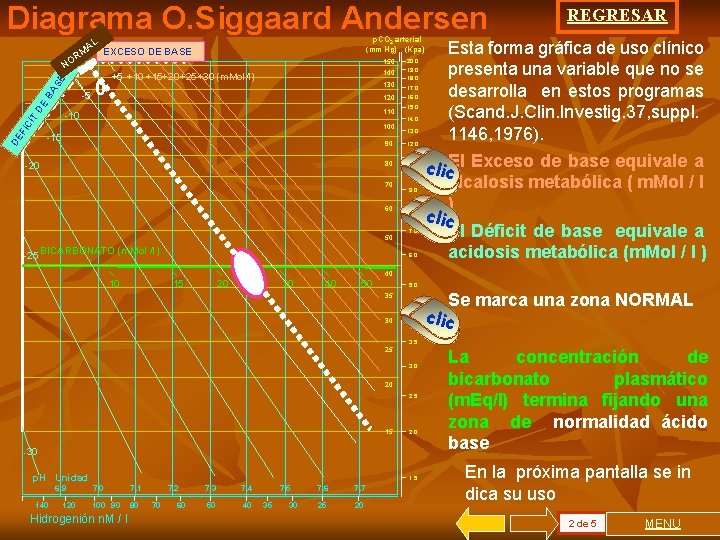
Diagrama O. Siggaard Andersen p. CO 2 arterial (mm Hg) (Kpa) AL EXCESO DE BASE RM DE BA SE NO 0 140 +5 +10 +15+20 +25 +30 (m. Mol/l) 130 120 110 -10 CI T FI -5 150 100 DE -15 90 80 -20 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 70 60 50 -25 20. 0 19. 0 18. 0 BICARBONATO (m. Mol /l) 9. 0 8. 0 7. 0 6. 0 REGRESAR Esta forma gráfica de uso clínico presenta una variable que no se desarrolla en estos programas (Scand. J. Clin. Investig. 37, suppl. 1146, 1976). clic. El Exceso de base equivale a alcalosis metabólica ( m. Mol / l ) clic El Déficit de base equivale a acidosis metabólica (m. Mol / l ) 40 10 15 20 30 40 50 5. 0 35 30 4. 0 Se marca una zona NORMAL clic 3. 5 25 3. 0 20 2. 5 15 2. 0 -30 p. H Unidad 6. 9 140 120 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 La concentración de bicarbonato plasmático (m. Eq/l) termina fijando una zona de normalidad ácido base En la próxima pantalla se in dica su uso 2 de 5 MENU
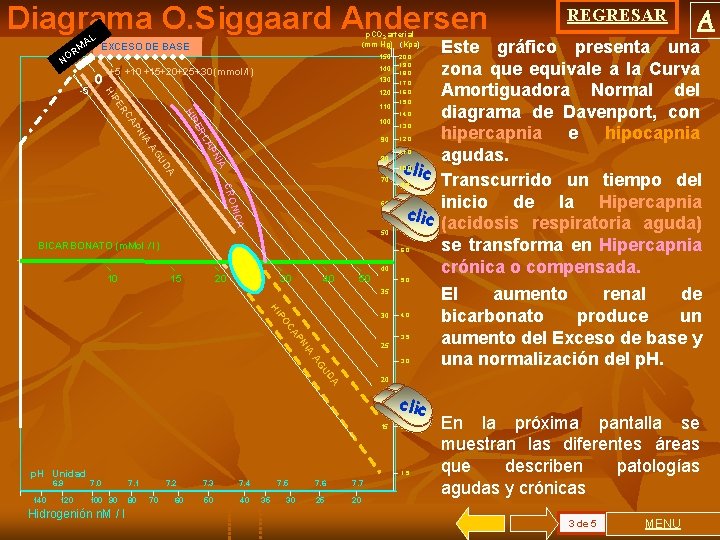
Diagrama O. Siggaard Andersen AL M R NO p. CO 2 arterial (mm Hg) (Kpa) EXCESO DE BASE 150 0 140 +5 +10 +15+20 +25 +30 (mmol/l) 130 120 110 100 90 80 A UD NI AG AP IA RC PN CA PE HI ER P HI -5 A Este gráfico presenta una zona que equivale a la Curva Amortiguadora Normal del diagrama de Davenport, con hipercapnia e hipocapnia agudas. clic Transcurrido un tiempo del inicio de la Hipercapnia clic (acidosis respiratoria aguda) se transforma en Hipercapnia crónica o compensada. 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 A 10. 0 70 CRO A NIC 60 50 BICARBONATO (m. Mol / l) 9. 0 8. 0 7. 0 6. 0 40 10 REGRESAR 15 20 30 40 50 5. 0 35 P HI 30 4. 0 N AP OC 3. 5 IA 25 DA U AG 3. 0 El aumento renal de bicarbonato produce un aumento del Exceso de base y una normalización del p. H. 20 2. 5 clic 15 p. H Unidad 6. 9 140 120 2. 0 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 En la próxima pantalla se muestran las diferentes áreas que describen patologías agudas y crónicas 3 de 5 MENU
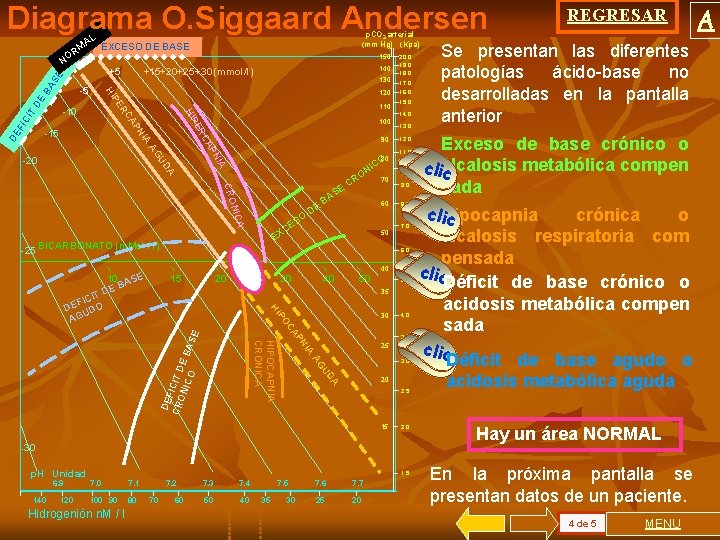
Diagrama O. Siggaard Andersen AL M EXCESO DE BASE 150 BA DE CI T 100 90 A NIC CRO O ES C X A -25 80 CO NI A UD NI AG AP IA -20 110 RC PN CA -10 PE HI ER FI 120 -15 DE 130 P HI -5 140 +15+20 +25 +30 (mmol/l) +5 SE R NO p. CO 2 arterial (mm Hg) (Kpa) DE B E AS O CR 60 50 E BICARBONATO (m. Mol / l) 70 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 9. 0 8. 0 7. 0 6. 0 40 10 ASE B DE 15 20 30 40 50 5. 0 35 P HI IT FIC DE DO U AG 30 4. 0 IA 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE N AP OC HIPOCAPNIA CRONICA 3. 5 25 20 2. 5 15 2. 0 -30 p. H Unidad 6. 9 140 120 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 REGRESAR Se presentan las diferentes patologías ácido-base no desarrolladas en la pantalla anterior Exceso de base crónico o metabólica compen clialcalosis c sada cli. Hipocapnia crónica o c alcalosis respiratoria com pensada clic Déficit de base crónico o acidosis metabólica compen sada clic Déficit de base agudo o acidosis metabólica aguda Hay un área NORMAL En la próxima pantalla se presentan datos de un paciente. 4 de 5 MENU A
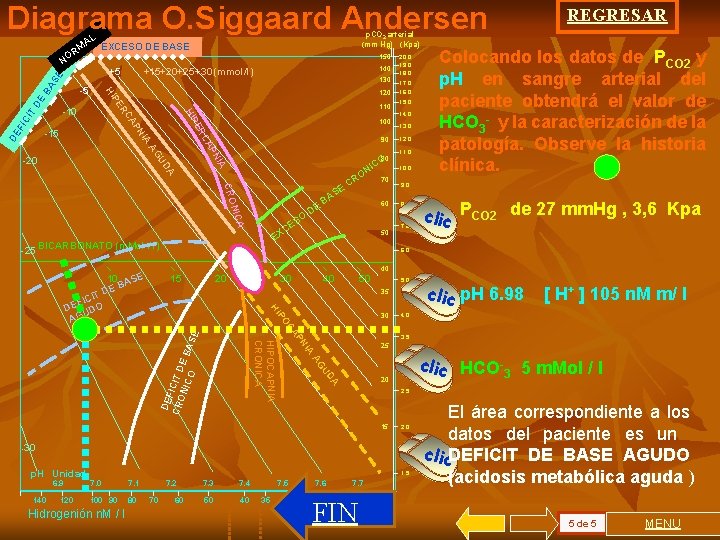
Diagrama O. Siggaard Andersen p. CO 2 arterial (mm Hg) (Kpa) AL EXCESO DE BASE RM 150 BA DE CI T 100 90 A NIC CRO SO CE A -25 80 CO NI A UD NI AG AP IA -20 110 RC PN CA -10 PE HI ER FI 120 -15 DE 130 P HI -5 140 +15+20 +25 +30 (mmol/l) +5 SE NO DE B E AS O CR 60 EX BICARBONATO (m. Mol / l) 70 50 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 9. 0 8. 0 7. 0 15 20 30 40 50 5. 0 35 P HI 30 IA 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE N AP OC HIPOCAPNIA CRONICA 3. 5 20 7. 1 100 90 80 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 clic HCO-3 5 m. Mol / l 2. 5 2. 0 1. 5 7. 0 Hidrogenión n. M / l [ H+ ] 105 n. M m/ l 4. 0 -30 120 clic p. H 6. 98 25 15 140 clic PCO 2 de 27 mm. Hg , 3, 6 Kpa 6. 0 IT FIC DE DO U AG 6. 9 Colocando los datos de PCO 2 y p. H en sangre arterial del paciente obtendrá el valor de HCO 3 - y la caracterización de la patología. Observe la historia clínica. 40 10 ASE B DE p. H Unidad REGRESAR 30 7. 6 7. 7 25 20 FIN El área correspondiente a los datos del paciente es un clic. DEFICIT DE BASE AGUDO (acidosis metabólica aguda ) 5 de 5 MENU

AUTOEVALUACION CO 2 ACIDO-BASE

Se acepta que Q (volumen) es igual a la diferencia arterio-venosa de CO 2 (concentración ) multiplicada por la eliminación de CO 2 (masa) Porque Como principio físico general se ha establecido que la masa (M) de una sustancia es igual al cociente entre la concentración (c) y el volumen en que está contenida VV VF FF FV VOLVER

M=c*V VCO 2 = (Cv. CO 2 – Ca. CO 2 ) * Q Se acepta que Q (volumen) es igual a la diferencia arterio-venosa de CO 2 (concentración ) multiplicada por la eliminación de CO 2 (masa) Porque Como principio físico general se ha establecido que la masa (M) de una sustancia es igual al cociente entre la concentración (c) y el volumen en que está contenida FF VOLVER

Se acepta en fisiología como diferencia arterio-venosa de O 2 ( Dav. O 2 ) a la diferencia entre la saturación de O 2 de la sangre arterial y venosa Porque Es una medida del volumen de oxígeno que ha sido transferida al tejido por cada unidad de volumen sanguíneo que lo perfunde ( cc. O 2 / cc sangre, cc. O 2 / 100 cc sangre, cc. O 2 / litro sangre) VV VF FF FV VOLVER

La diferencia arterio-venosa de O 2 ( Dav. O 2 ) se acepta en fisiología como la diferencia entre la saturación de O 2 de la sangre arterial y venosa Porque Es una medida del volumen de oxígeno que ha sido transferida al tejido por cada unidad de volumen sanguíneo que lo perfunde ( cc. O 2 / cc sangre, cc. O 2 / 100 cc sangre, cc. O 2 / litro sangre) FV VOLVER

Elija la ecuación adecuada para cuantificar el intercambio de CO 2 con el principio de Fick 1. 2. 3. 4. 5. - . . VCO 2 = (Ca. CO 2 – Cv. CO 2 ) * Q. . Q = VCO 2 * (Cv. CO 2 - Ca. CO 2). . Dva. CO 2 = VCO 2 / Q. . VCO 2 = (Ca. CO 2 – Cv. CO 2 ) + Q. . Q = VCO 2 * (Ca. CO 2 -Cv. CO 2) VOLVER

. VCO 2 Cv . . VCO 2 = (Cv. CO 2 – Ca. CO 2 ) * Q. . . = Dva. CO 2 * Q VCO 2 Dva Ca . Q Elija la ecuación adecuada para cuantificar el intercambio de CO 2 con el principio de Fick. . 1. - VCO 2 = (Ca. CO 2 – Ca. CO 2 ) * Q. . 2. - Q = VCO 2 * (Cv. CO 2 -Ca. CO 2) . . 3. - Dva. CO 2 = VCO 2 / Q. . 4. - VCO 2 = (Ca. CO 2 – Cv. CO 2 ) + Q. . 5. - Q = VCO 2 * (Ca. CO 2 -Cv. CO 2) VOLVER
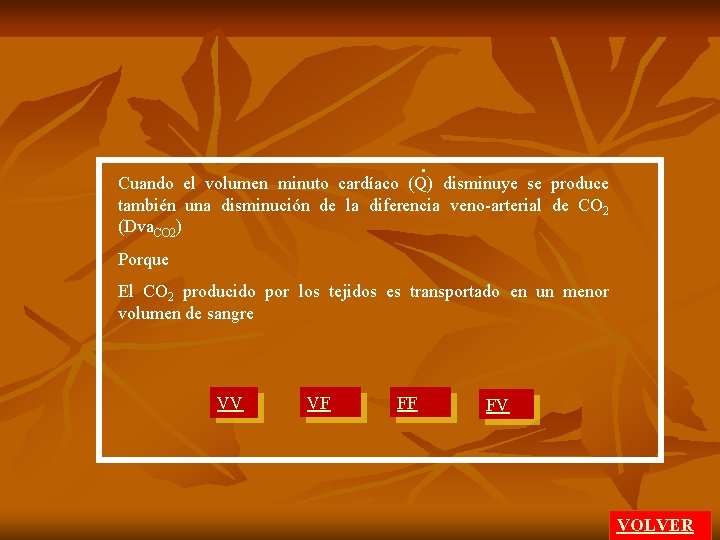
. Cuando el volumen minuto cardíaco (Q) disminuye se produce también una disminución de la diferencia veno-arterial de CO 2 (Dva. CO 2) Porque El CO 2 producido por los tejidos es transportado en un menor volumen de sangre VV VF FF FV VOLVER

. Cuando el volumen minuto cardíaco (Q) disminuye se produce también una disminución de la diferencia veno-arterial de CO 2 (Dva. CO 2) Porque El CO 2 producido por los tejidos es transportado en un menor volumen de sangre FV VOLVER

La adecuada relación entre la presión alveolar y arterial de CO 2 ( PACO 2, Pa. CO 2 ) depende de la interrelación entre los sistemas ventilatorio y cardiovascular Porque Si bien se maneja como dato de laboratorio un valor único de PCO 2 en gas o en sangre, en realidad se trata de un valor que oscila en el tiempo VV VF FF FV VOLVER

La adecuada relación entre la presión alveolar y arterial de CO 2 ( PACO 2, Pa. CO 2 ) depende de la interrelación entre los sistemas ventilatorio y cardiovascular Porque Si bien se maneja como dato de laboratorio un valor único de PCO 2 en gas o en sangre, en realidad se trata de un valor que oscila en el tiempo VV VOLVER

VA VA tiempo En el dibujo superior derecho se representan dos gráficas y hay tres características ventilatorias que debe señalar 1. - Una apnea posterior a una hiperventilación 2. - Una hipoventilación con posterior apnea 3. - Un aumento del período de hiperventilación 4. - Una hipoventilación sostenida 5. - Incremento del período de apnea por aumento del tiempo circulatorio VOLVER

VA tiempo En el dibujo superior derecho se representan dos gráficas y hay tres características ventilatorias que debe señalar 1. - Una apnea posterior a una hiperventilación 2. - Una hipoventilación con posterior apnea 3. - Un aumento del período de hiperventilación 4. - Una hipoventilación sostenida 5. - Incremento del período de apnea por aumento del tiempo circulatorio. VOLVER

VA tiempo En el dibujo superior derecho se representan dos gráficas y hay tres características ventilatorias que debe señalar 1. - Una apnea posterior a una hiperventilación 2. - Una hipoventilación con posterior apnea 3. - Un aumento del período de hiperventilación 4. - Una hipoventilación sostenida 5. - Incremento del período de apnea por aumento del tiempo circulatorio. VOLVER

VA tiempo En el dibujo superior derecho se representan dos gráficas y hay tres características ventilatorias que debe señalar 1. - Una apnea posterior a una hiperventilación 2. - Una hipoventilación con posterior apnea 3. - Un aumento del período de hiperventilación 4. - Una hipoventilación sostenida 5. - Incremento del período de apnea por aumento de la hiperventilación Incremento del período de apnea por aumento tiempo circulatorio del . VOLVER

La presión total ejercida por una mezcla gaseosa es igual a la suma de la presión ejercida de manera parcial por cada gas Porque Los gases de la mezcla contribuyen en igual proporción a la generación de la presión total VV VF FF FV VOLVER

N 2 con 78% O 2 con 21% F 0. 78 F 0. 21 otros con 1% F 0, 01 La presión total ejercida por una mezcla gaseosa es igual a la suma de la presión ejercida de manera parcial por cada gas Porque Los gases de la mezcla contribuyen en igual proporción a la generación de la presión total VF VOLVER

Cuando un gas se satura con vapor de agua las presiones parciales de los gases de la mezcla aumentan Porque La presión total ejercida sobre el gas será igual a lo presión barométrica ( Pb ) mas la presión parcial ejercida por el agua ( PH 2 O = Pva ) VV VF FF FV VOLVER

Pva 47 mm. Hg Gas seco húmedo Cuando un gas se satura con vapor de agua las presiones parciales de los gases de la mezcla aumentan Porque La presión total ejercida sobre el gas será igual a lo presión barométrica ( Pb ) mas la presión parcial ejercida por el agua ( PH 2 O = Pva ) FF VOLVER
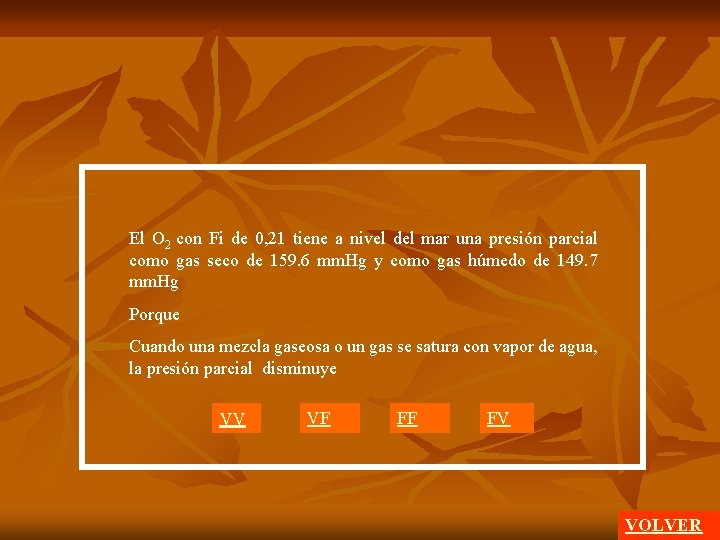
El O 2 con Fi de 0, 21 tiene a nivel del mar una presión parcial como gas seco de 159. 6 mm. Hg y como gas húmedo de 149. 7 mm. Hg Porque Cuando una mezcla gaseosa o un gas se satura con vapor de agua, la presión parcial disminuye VV VF FF FV VOLVER

Pva 47 mm. Hg PO 2 Gas seco Gas húmedo El O 2 con Fi de 0, 21 tiene a nivel del mar una presión parcial como gas seco de 159. 6 mm. Hg y como gas húmedo de 149. 7 mm. Hg Porque Cuando se satura con vapor de agua la presión parcial de una mezcla gaseosa o de un gas disminuye VV VOLVER

Cuando una mezcla gaseosa se pone en contacto con un líquido se produce su disolución en función de las presiones parciales de cada gas Porque La disolución de un gas en un líquido depende exclusivamente de su presión parcial. VV VF FF FV VOLVER

CO 2 disuelto =( Pb * FCO 2 ) * coeficiente de solubilidad = PCO 2 * a Cuando una mezcla gaseosa se pone en contacto con un líquido se produce su disolución en función de las presiones parciales de cada gas Porque La disolución de un gas en un líquido depende exclusivamente de su presión parcial. VF VOLVER

Señale dos variaciones que se producen en plasma cuando el CO 2 se disuelve 1. - aumenta el carbonato 2. - aumenta el ácido carbónico 3. - se produce una alcalosis 4. - aumenta el número de hidrogeniones libres 5. - disminuye la concentración de bicarbonato VOLVER

Señale dos variaciones que se producen en plasma cuando el CO 2 se disuelve 1. - aumenta el carbonato 2. - aumenta el ácido carbónico 3. - se produce una alcalosis 4. - aumenta el número de hidrogeniones libres 5. - disminuye la concentración de bicarbonato VOLVER

Señale dos variaciones que se producen en plasma cuando el CO 2 se disuelve 1. - aumenta el carbonato 2. - aumenta el ácido carbónico 3. - se produce una alcalosis 4. - aumentan los hidrogeniones libres 5. - disminuye la concentración de bicarbonato VOLVER

Cuando se disuelve el CO 2 en plasma se hidrata a ácido carbónico que al disociarse produce una acidosis Porque 1 m. Eq de bicarbonato incorporado a 24 m. Eq/l produce un aumento mucho menor que 1 m. Eq de hidrogenión incorporado a 0, 00004 m. Eq/l VV VF FF FV VOLVER

1 1 24 m. Eq 0. 00004 m. Eq Cuando se disuelve el CO 2 en plasma se hidrata a ácido carbónico que al disociarse produce una acidosis Porque 1 m. Eq de bicarbonato incorporado a 24 m. Eq/l produce un aumento proporcional mente mucho menor que 1 m. Eq de hidrogenión incorporado a 0, 00004/l m. Eq, lo que se traduce en acidosis. VV VOLVER

HCO 3 - PCO 2 7. 7 7. 4 7. 0 HC O 3 - PC 7. 7 O 2 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria VOLVER

HCO 3 - PCO 2 7. 7 7. 4 7. 0 HC O 3 - PC 7. 7 O 2 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar : 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria. VOLVER

HCO 3 - PCO 2 7. 7 7. 4 7. 0 HC O 3 - PC 7. 7 O 2 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar : 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria. VOLVER

HCO 3 - PCO 2 7. 7 7. 4 7. 0 P CO 2 - H CO 3 7. 7 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria VOLVER

HCO 3 - PCO 2 7. 7 7. 4 P CO 2 - H CO 3 7. 0 7. 7 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria. VOLVER

HCO 3 - PCO 2 7. 7 7. 4 P CO 2 - H CO 3 7. 0 7. 7 7. 4 7. 0 En el dibujo superior derecho se representan dos características ácidobase que debe señalar 1. - Una alteración metabólica 2. - Una alcalosis 3. - Un proceso compensado 4. - Una acidosis 5. - Una alteración respiratoria. VOLVER

Un valor de p. H 7. 4 en plasma indica normalidad Porque La caracterización ácido-base puede realizarse con una sola de las variables involucradas : p. H, PCO 2 o HCO 3 VV VF FF FV VOLVER

Un valor de p. H 7. 4 en plasma indica normalidad en el estado ácido-base Porque La caracterización ácido-base puede realizarse con una sola de las variables involucradas : p. H, PCO 2, HCO 3 FF VOLVER

En el diagrama de Davenport se grafican como valores normales en el área azul: 1. - Bicarbonato 24 m. Eq/l 2. - (H+) 50 nano Moles 3. - PCO 2 40 mm. Hg 4. -CO 2 disuelto 40 m. Mol / l 5. - p. H 7. 5 unidades 0 H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. VOLVER
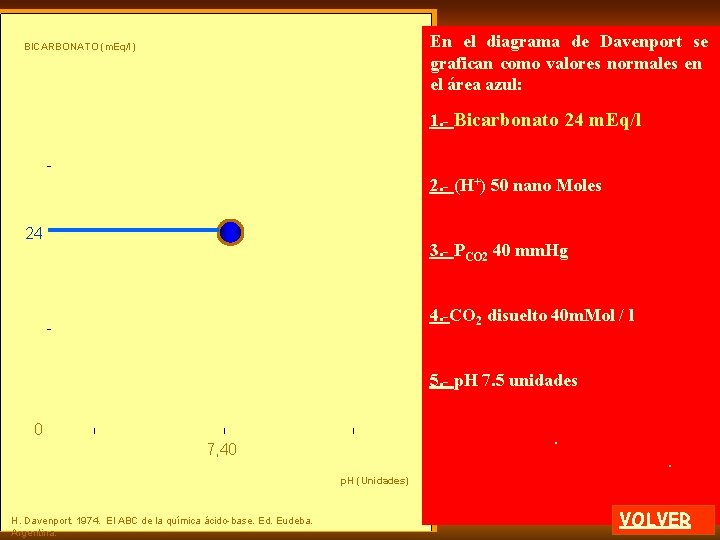
En el diagrama de Davenport se grafican como valores normales en el área azul: BICARBONATO (m. Eq/l) 1. - Bicarbonato 24 m. Eq/l 2. - (H+) 50 nano Moles 24 3. - PCO 2 40 mm. Hg 4. -CO 2 disuelto 40 m. Mol / l 5. - p. H 7. 5 unidades 0 . 7, 40 . p. H (Unidades) H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. VOLVER
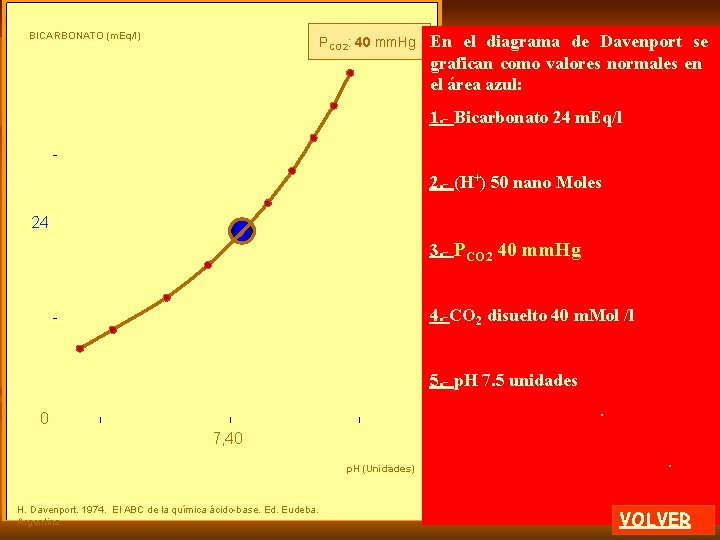
BICARBONATO (m. Eq/l) PCO 2: 40 mm. Hg En el diagrama de Davenport se grafican como valores normales en el área azul: 1. - Bicarbonato 24 m. Eq/l 2. - (H+) 50 nano Moles 24 3. - PCO 2 40 mm. Hg 4. -CO 2 disuelto 40 m. Mol /l 5. - p. H 7. 5 unidades. 0 7, 40 p. H (Unidades) H. Davenport. 1974. El ABC de la química ácido-base. Ed. Eudeba. Argentina. . VOLVER

Los parámetros utilizados en el diagrama de Davenport, tienen habitualmente una representación que muestra: 1. - Una escala logarítmica de p. H con escala de hidrogeniones lineal 2. - p. H como logaritmo de la concentración de hidrogeniones 3. - p. H en escala lineal con hidrogeniones en escala lineal 4. - p. H en escala lineal con hidrogeniones en escala logarítmica 5. - concentración de hidrogeniones como logaritmo de p. H VOLVER

7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 p. H (Unidades) 7, 60 7, 70 7, 80 p. H = log (H+) -1 = log 1/ (H+) 100 80 60 50 40 30 25 20 15 + [H ] (n. M/l) Los parámetros utilizados en el diagrama de Davenport, tienen habitualmente una representación que muestra : 1. - Una escala logarítmica de p. H con escala de hidrogeniones lineal 2. - p. H como logaritmo de la concentración de hidrogeniones 3. - p. H en escala lineal con hidrogeniones en escala lineal 4. - p. H en escala lineal con hidrogeniones en escala logarítmica 5. - concentración de hidrogeniones como logaritmo de p. H . VOLVER

Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones - 1. - [H+] = 24* PCO 2 2. - p. H = 6, 1 + log 10 3. - [H+] = 24 *PCO 2 * 4. - [H+] = 5. - [HCO 3 -] a * PCO 2 [HCO 3 -] 24* PCO 2 [HCO 3 -] p. H = 6, 1 + log 10 a * PCO 2 [HCO 3 -] VOLVER

Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones 1. - [H+] = 24* PCO 2 2. - p. H = 6, 1 + log 10 3. - [H+] 4. - [H+] = 5. - = 24 *PCO 2 - [HCO 3 -] a * PCO 2 * [HCO 3 -] 24* PCO 2 [HCO 3 -] p. H = 6, 1 + log 10 a * PCO 2 [HCO 3 -] . VOLVER

Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones 1. - [H+] = 24* PCO 2 2. - p. H = 6, 1 + log 10 3. - [H+] = 24 *PCO 2 4. 5. - [H+] = - [HCO 3 -] a * PCO 2 * [HCO 3 -] 24* PCO 2 [HCO 3 -] p. H = 6, 1 + log 10 a * PCO 2 [HCO 3 -] . VOLVER
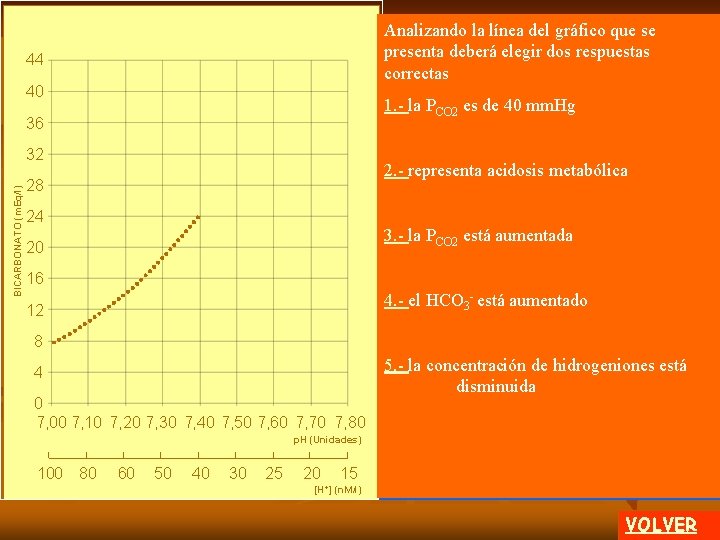
Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 44 40 1. - la PCO 2 es de 40 mm. Hg 36 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 3. - la PCO 2 está aumentada 20 16 4. - el HCO 3 - está aumentado 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - la concentración de hidrogeniones está disminuida p. H (Unidades) 100 80 60 50 40 30 25 20 [H+] 15 (n. M/l) VOLVER
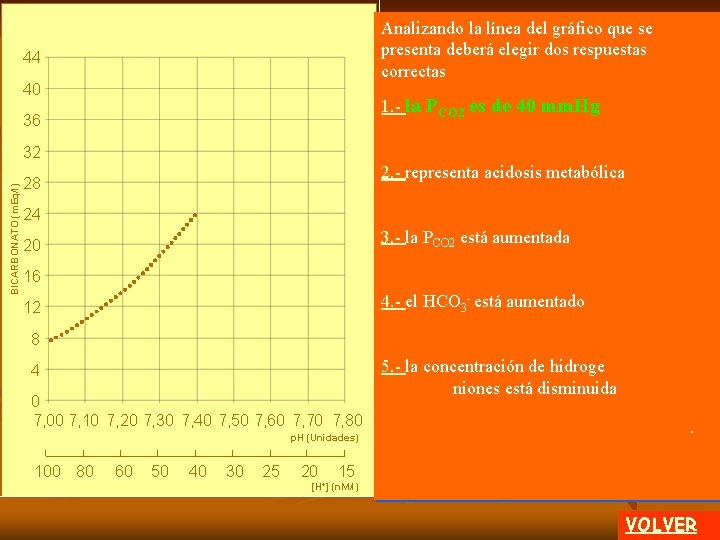
Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 44 40 1. - la PCO 2 es de 40 mm. Hg 36 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 3. - la PCO 2 está aumentada 20 16 4. - el HCO 3 - está aumentado 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 5. - la concentración de hidroge niones está disminuida. 15 [H+] (n. M/l) VOLVER
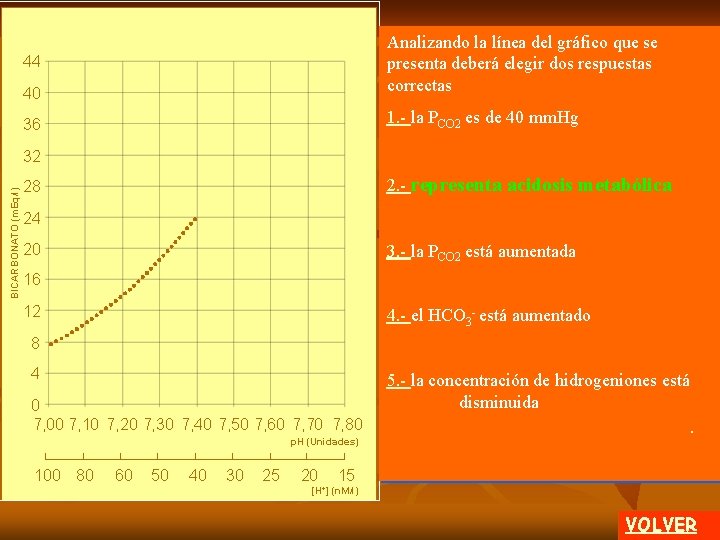
40 Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 36 1. - la PCO 2 es de 40 mm. Hg 44 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 20 3. - la PCO 2 está aumentada 16 12 4. - el HCO 3 - está aumentado 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 5. - la concentración de hidrogeniones está disminuida. 15 [H+] (n. M/l) VOLVER
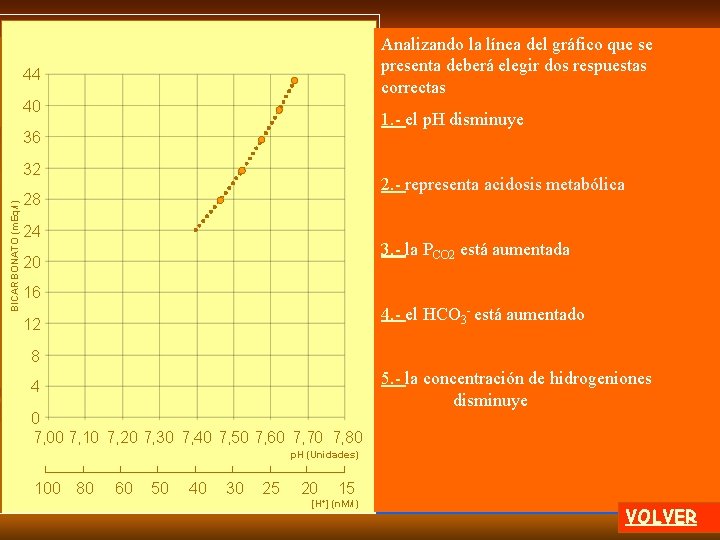
Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 44 40 1. - el p. H disminuye 36 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 3. - la PCO 2 está aumentada 20 16 4. - el HCO 3 - está aumentado 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - la concentración de hidrogeniones disminuye p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
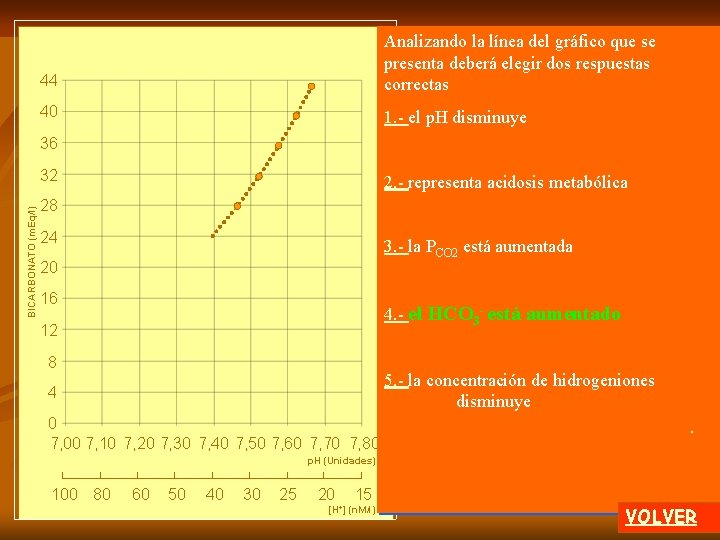
44 Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 40 1. - el p. H disminuye 36 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 3. - la PCO 2 está aumentada 20 16 4. - el HCO 3 - está aumentado 12 8 5. - la concentración de hidrogeniones disminuye 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 [H+] 15 (n. M/l) VOLVER
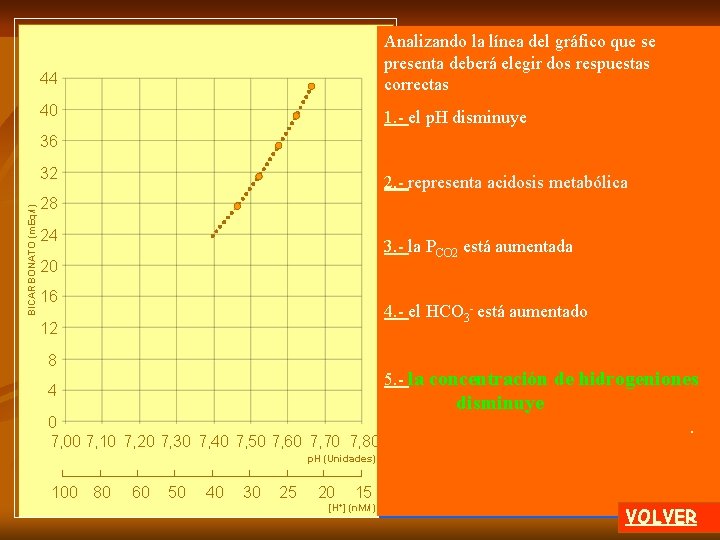
44 Analizando la línea del gráfico que se presenta deberá elegir dos respuestas correctas 40 1. - el p. H disminuye 36 BICARBONATO (m. Eq/l) 32 2. - representa acidosis metabólica 28 24 3. - la PCO 2 está aumentada 20 16 4. - el HCO 3 - está aumentado 12 8 5. - la concentración de hidrogeniones 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 disminuye. p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER

- Toda disminución de la concentración de HCO 3 producido con una PCO 2 de 40 mm. Hg, conduce a una disminución del p. H Porque De esta manera es posible caracterizar una alteración respiratoria compensada con la disminución de p. H VV VF FF FV VOLVER

- Toda disminución de la concentración de HCO 3 producido con una PCO 2 de 40 mm. Hg, conduce a una disminución del p. H Porque De esta manera es posible caracterizar una alteración respiratoria compensada con la disminución de p. H VF VOLVER
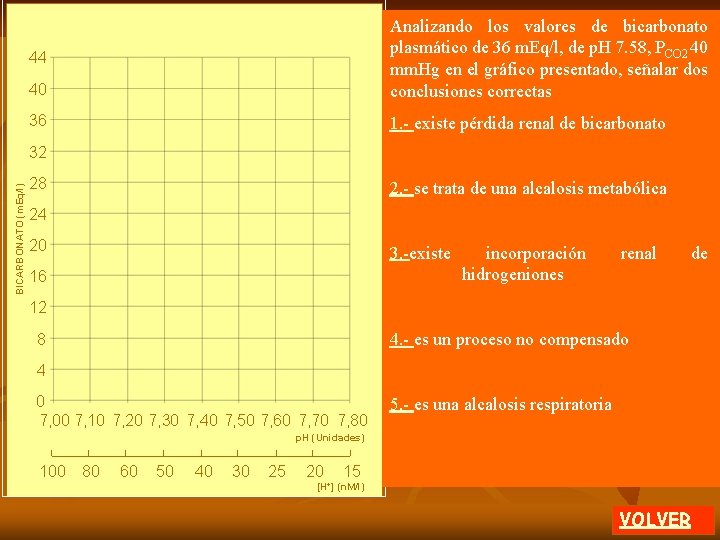
40 Analizando los valores de bicarbonato plasmático de 36 m. Eq/l, de p. H 7. 58, PCO 2 40 mm. Hg en el gráfico presentado, señalar dos conclusiones correctas 36 1. - existe pérdida renal de bicarbonato 44 BICARBONATO (m. Eq/l) 32 28 2. - se trata de una alcalosis metabólica 24 20 3. -existe 16 incorporación hidrogeniones renal 12 4. - es un proceso no compensado 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - es una alcalosis respiratoria p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER de
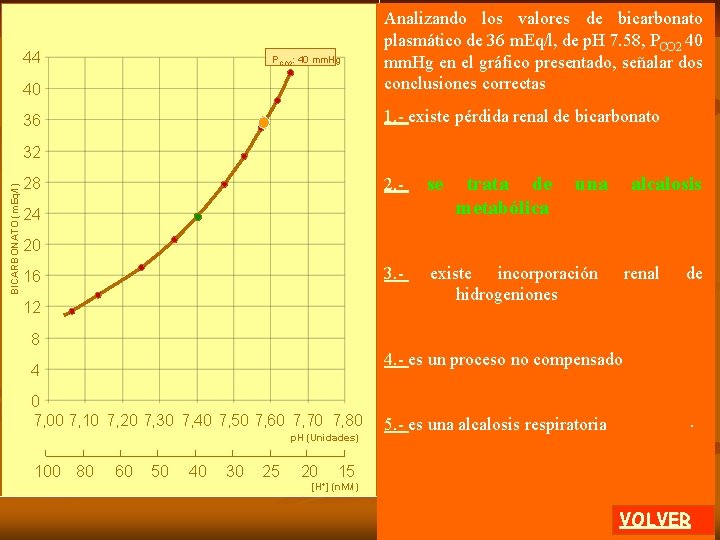
40 Analizando los valores de bicarbonato plasmático de 36 m. Eq/l, de p. H 7. 58, PCO 2 40 mm. Hg en el gráfico presentado, señalar dos conclusiones correctas 36 1. - existe pérdida renal de bicarbonato 44 PCO 2: 40 mm. Hg BICARBONATO (m. Eq/l) 32 28 2. - se 3. - existe incorporación hidrogeniones 24 trata de metabólica una alcalosis 20 16 12 renal de 8 4. - es un proceso no compensado 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 5. - es una alcalosis respiratoria . 15 [H+] (n. M/l) VOLVER
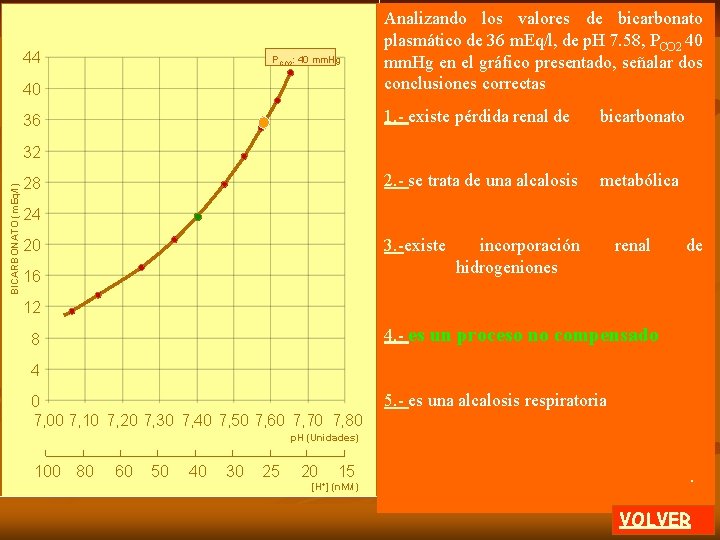
40 Analizando los valores de bicarbonato plasmático de 36 m. Eq/l, de p. H 7. 58, PCO 2 40 mm. Hg en el gráfico presentado, señalar dos conclusiones correctas 36 1. - existe pérdida renal de bicarbonato 2. - se trata de una alcalosis metabólica 44 PCO 2: 40 mm. Hg BICARBONATO (m. Eq/l) 32 28 24 3. -existe 20 16 incorporación hidrogeniones renal de 12 4. - es un proceso no compensado 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - es una alcalosis respiratoria p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) . VOLVER

El valor de bicarbonato plasmático de 24 m. Eq/l es normal solamente cuando la condición respiratoria del individuo mantiene fija una PCO 2 de 40 mm. Hg Porque La concentración de bicarbonato en plasma solo se modifica por trastornos metabólicos. VV VF FF FV VOLVER

El valor bicarbonato plasmático de 24 m. Eq/l es normal solamente cuando la condición respiratoria fija una PCO 2 de 40 mm. Hg Porque La concentración de bicarbonato en plasma solo se modifica por trastornos metabólicos. VF VOLVER
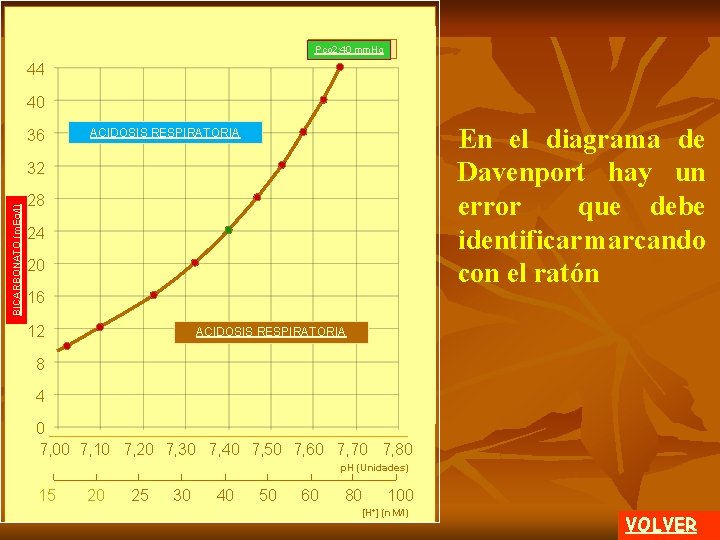
Pco 2: 40 mm. Hg 44 40 36 En el diagrama de Davenport hay un error que debe identificar marcando con el ratón ACIDOSIS RESPIRATORIA BICARBONATO (m. Eq/l) 32 28 24 20 16 12 ACIDOSIS RESPIRATORIA 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 15 20 25 30 40 50 60 80 100 [H+] (n. M/l) VOLVER
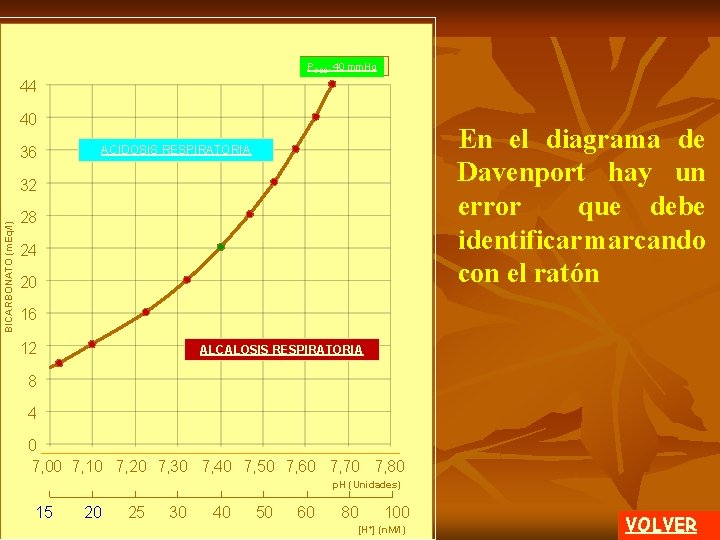
PCO 2: 40 mm. Hg 44 40 36 En el diagrama de Davenport hay un error que debe identificar marcando con el ratón ACIDOSIS RESPIRATORIA BICARBONATO (m. Eq/l) 32 28 24 20 16 12 ALCALOSIS RESPIRATORIA 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 15 20 25 30 40 50 60 80 [H+] 100 (n. M/l) VOLVER

Ante el aumento del ácido carbónico se produce disminución del bicarbonato plasmático, como ocurre en cualquier tipo de acidosis Porque Cuando en el organismo se produce un aumento continuado de PCO 2 se está añadiendo un ácido volátil, el ácido carbónico (H 2 CO 3) y se produce una variación del p. H. VV VF FF FV VOLVER

Ante el aumento del ácido carbónico se produce disminución del bicarbonato plasmático, como ocurre en cualquier tipo de acidosis Porque Cuando en el organismo se produce un aumento continuado de PCO 2 se está añadiendo un ácido volátil, el ácido carbónico (H 2 CO 3) y se produce una variación del p. H. FV VOLVER
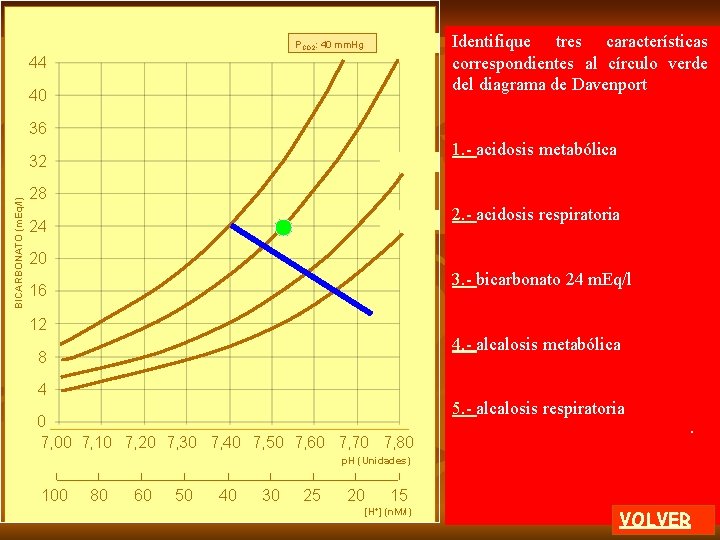
Identifique tres características correspondientes al círculo verde del diagrama de Davenport PCO 2: 40 mm. Hg 44 40 36 1. - acidosis metabólica BICARBONATO (m. Eq/l) 32 28 2. - acidosis respiratoria 24 20 3. - bicarbonato 24 m. Eq/l 16 12 4. - alcalosis metabólica 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - alcalosis respiratoria . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
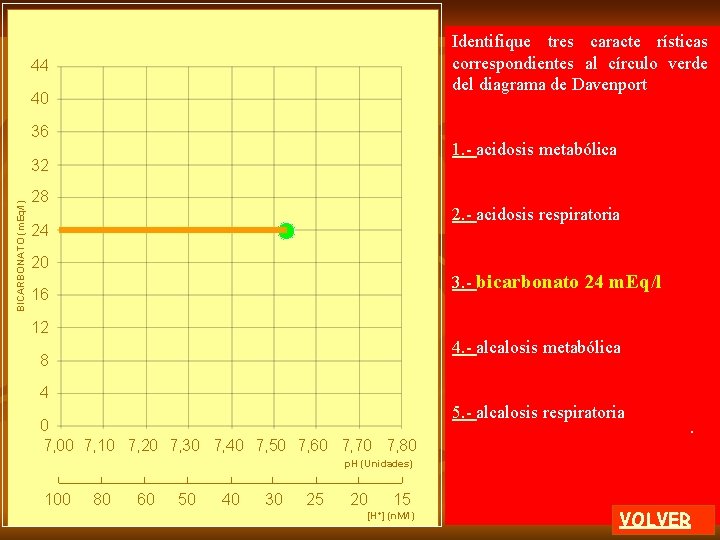
Identifique tres caracte rísticas correspondientes al círculo verde del diagrama de Davenport 44 40 36 1. - acidosis metabólica BICARBONATO (m. Eq/l) 32 28 2. - acidosis respiratoria 24 20 3. - bicarbonato 24 m. Eq/l 16 12 4. - alcalosis metabólica 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - alcalosis respiratoria . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
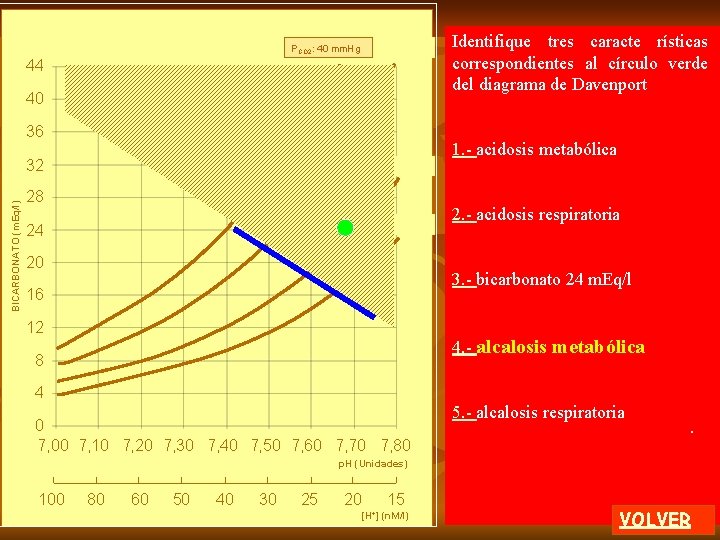
Identifique tres caracte rísticas correspondientes al círculo verde del diagrama de Davenport PCO 2: 40 mm. Hg 44 40 36 1. - acidosis metabólica BICARBONATO (m. Eq/l) 32 28 2. - acidosis respiratoria 24 20 3. - bicarbonato 24 m. Eq/l 16 12 4. - alcalosis metabólica 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - alcalosis respiratoria . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
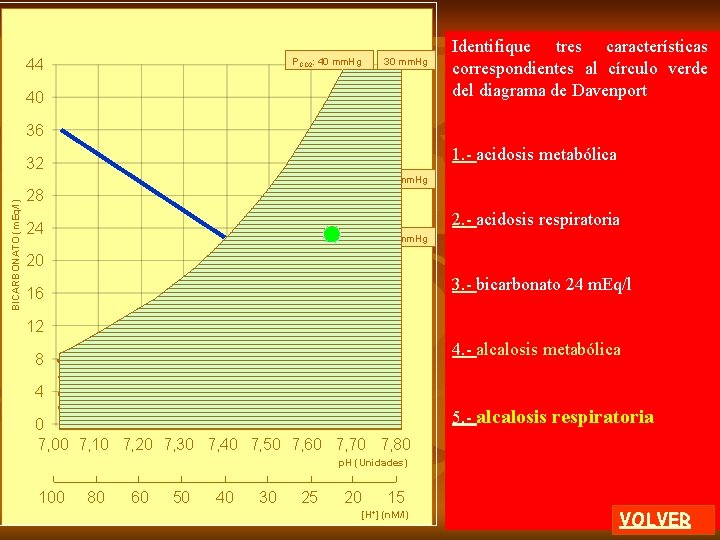
44 PCO 2: 40 mm. Hg 30 mm. Hg 40 Identifique tres características correspondientes al círculo verde del diagrama de Davenport 36 1. - acidosis metabólica 32 BICARBONATO (m. Eq/l) 20 mm. Hg 28 2. - acidosis respiratoria 24 15 mm. Hg 20 3. - bicarbonato 24 m. Eq/l 16 12 4. - alcalosis metabólica 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 5. - alcalosis respiratoria . p. H (Unidades) 100 80 60 50 40 30 25 20 [H+] 15 (n. M/l) VOLVER

En la curva amortiguadora se observa que al aumentar la PCO 2 aumenta la concentración de bicarbonato Porque Cuando en el organismo se produce un aumento continuado de PCO 2 se está añadiendo un ácido volátil, el ácido carbónico (H 2 CO 3) que se disocia en hidrogeniones y bicarbonato VV VF FF FV VOLVER

En la curva amortiguadora se observa que al aumentar la PCO 2 aumenta la concentración de bicarbonato Porque Cuando en el organismo se produce un aumento continuado de PCO 2 se está añadiendo un ácido volátil, el ácido carbónico (H 2 CO 3) que se disocia en hidrogeniones y bicarbonato VV VOLVER
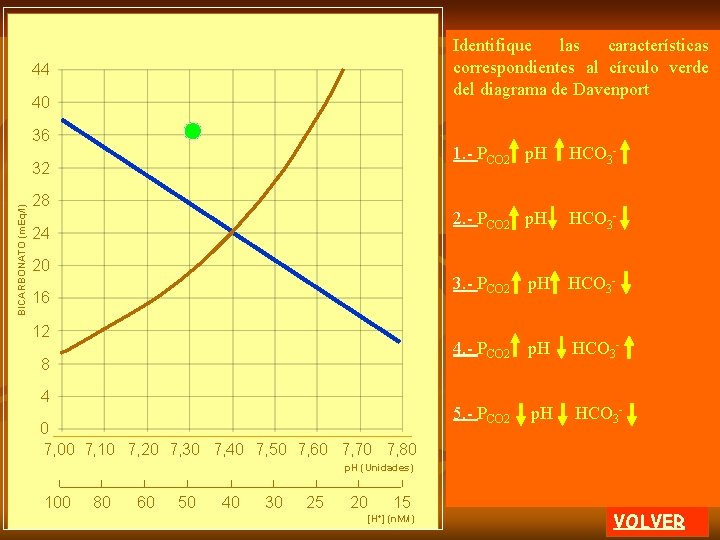
Identifique las características correspondientes al círculo verde del diagrama de Davenport 44 40 36 BICARBONATO (m. Eq/l) 32 28 24 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 1. - PCO 2 p. H HCO 3 - 2. - PCO 2 p. H HCO 3 - 3. - PCO 2 p. H HCO 3 - 4. - PCO 2 p. H HCO 3 - 5. - PCO 2 p. H HCO 3 - . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
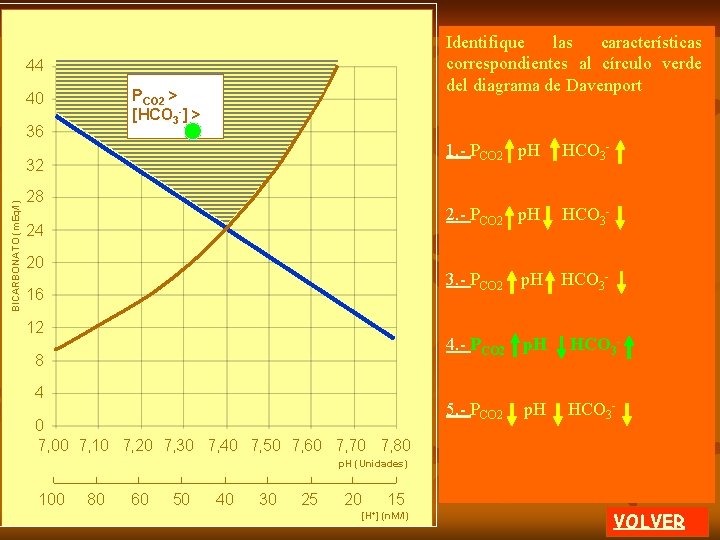
Identifique las características correspondientes al círculo verde del diagrama de Davenport 44 PCO 2 > [HCO 3 -] > 40 36 BICARBONATO (m. Eq/l) 32 28 24 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 1. - PCO 2 p. H HCO 3 - 2. - PCO 2 p. H HCO 3 - 3. - PCO 2 p. H HCO 3 - 4. - PCO 2 p. H HCO 3 - 5. - PCO 2 p. H HCO 3 - . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER

Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones 1. - [H+] = 24* PCO 2 2. - p. H = 6, 1 + log 10 3. 4. 5. - [H+] = 24 *PCO 2 24* PCO 2 [H+] = [HCO 3 -] p. H = 6, 1 + log 10 - [HCO 3 -] a * PCO 2 * [HCO 3 -] a * PCO 2 [HCO 3 -] VOLVER

64 Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones 1. - - [H+] = 24* PCO 2 [HCO 3 -] 2. - p. H = 6, 1 + log 10 3. - [H+] = 24 *PCO 2 * 4. - [H+] 5. - = [HCO 3 -] a * PCO 2 [HCO 3 -] 24* PCO 2 [HCO 3 -] p. H = 6, 1 + log 10 a * PCO 2 [HCO 3 -] . VOLVER

Elija dos ecuaciones correctas para expresar la concentración o el potencial de hidrogeniones 1. 2. 3. 4. 5. - [H+] = 24* PCO 2 - p. H = 6, 1 + log 10 [H+] = 24 *PCO 2 24* PCO 2 [H+] = [HCO 3 -] p. H = 6, 1 + log 10 [HCO 3 -] a * PCO 2 * [HCO 3 -] a * PCO 2 [HCO 3 -] . VOLVER

En la curva amortiguadora se observa que en la acidosis respiratoria la concentración de bicarbonato es de 24 m. Eq/l Porque La concentración de bicarbonato no cambia cuando se produce un aumento de la PCO 2. VV VF FF FV VOLVER

En la curva amortiguadora se observa que en la acidosis respiratoria la concentración de bicarbonato es de 24 m. Eq/l Porque La concentración de bicarbonato no cambia cuando se produce un aumento de la PCO 2. FF VOLVER

Para lograr la compensación de una alcalosis metabólica pura es necesario producir una disminución continua de la PCO 2 Porque De acuerdo a la ecuación de Henderson–Hasselbalch al aumentar la PCO 2 el p. H aumenta VV VF FF FV VOLVER

Para lograr la compensación de una alcalosis metabólica pura es necesario producir una disminución continua de la PCO 2 Porque De acuerdo a la ecuación de Henderson–Hasselbalch al aumentar la PCO 2 el p. H aumenta FF VOLVER
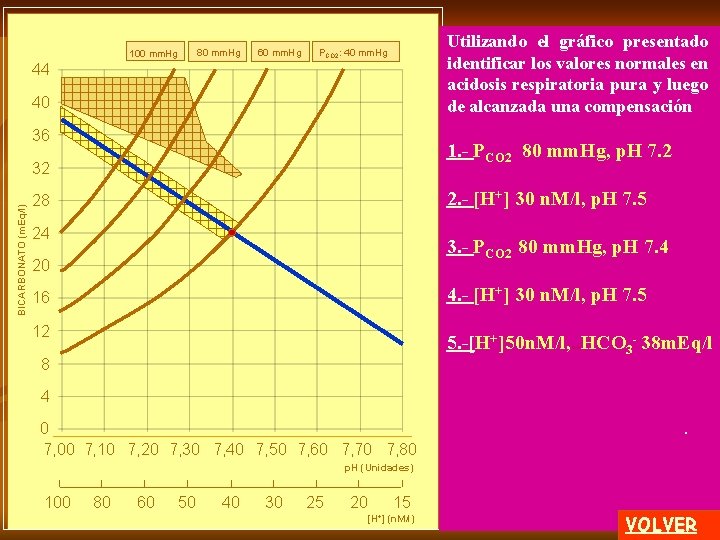
80 mm. Hg 100 mm. Hg 60 mm. Hg Utilizando el gráfico presentado identificar los valores normales en acidosis respiratoria pura y luego de alcanzada una compensación PCO 2: 40 mm. Hg 44 40 36 1. - PCO 2 80 mm. Hg, p. H 7. 2 BICARBONATO (m. Eq/l) 32 2. - [H+] 30 n. M/l, p. H 7. 5 28 24 3. - PCO 2 80 mm. Hg, p. H 7. 4 20 4. - [H+] 30 n. M/l, p. H 7. 5 16 12 5. -[H+]50 n. M/l, . . HCO 3 - 38 m. Eq/l 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
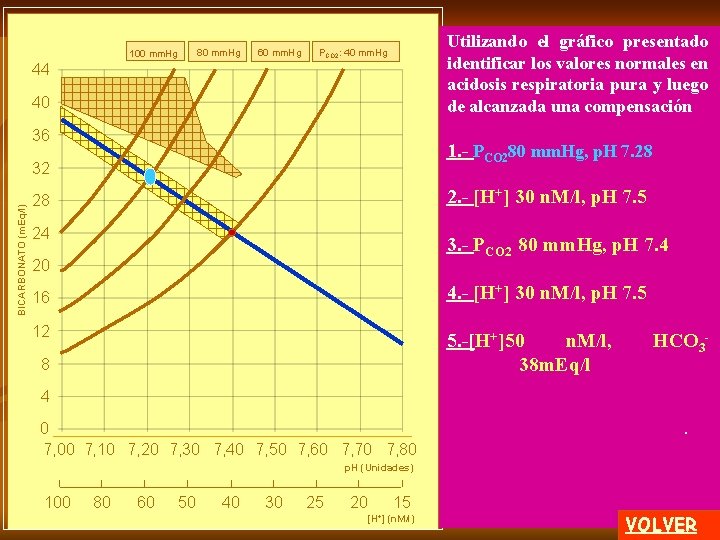
80 mm. Hg 100 mm. Hg 60 mm. Hg Utilizando el gráfico presentado identificar los valores normales en acidosis respiratoria pura y luego de alcanzada una compensación PCO 2: 40 mm. Hg 44 40 36 1. - PCO 280 mm. Hg, p. H 7. 28 BICARBONATO (m. Eq/l) 32 2. - [H+] 30 n. M/l, p. H 7. 5 28 24 3. - PCO 2 80 mm. Hg, p. H 7. 4 20 16 4. - [H+] 30 n. M/l, p. H 7. 5 12 5. -[H+]50 n. M/l, 38 m. Eq/l 8 HCO 3 - 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
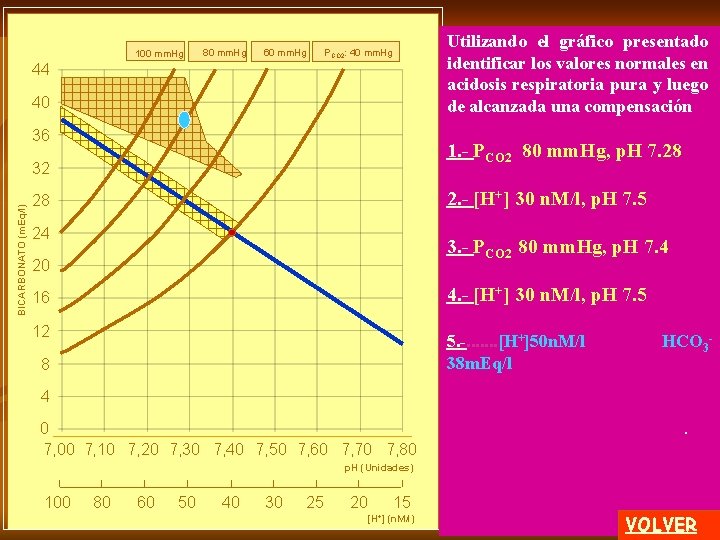
100 mm. Hg 80 mm. Hg 60 mm. Hg PCO 2: 40 mm. Hg 44 40 36 1. - PCO 2 80 mm. Hg, p. H 7. 28 32 BICARBONATO (m. Eq/l) Utilizando el gráfico presentado identificar los valores normales en acidosis respiratoria pura y luego de alcanzada una compensación 2. - [H+] 30 n. M/l, p. H 7. 5 28 24 3. - PCO 2 80 mm. Hg, p. H 7. 4 20 4. - [H+] 30 n. M/l, p. H 7. 5 16 12 5. -. . . . [H+]50 n. M/l 38 m. Eq/l 8 HCO 3 - 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER

Para identificar una alcalosis respiratoria pura sólo es necesario conocer el valor de PCO 2 Porque La curva amortiguadora normal determina los únicos valores normales de bicarbonato ante aumentos o disminuciones de PCO 2 VV VF FF FV VOLVER

Para identificar una alcalosis respiratoria pura sólo es necesario conocer el valor de PCO 2 Porque La curva amortiguadora normal determina los únicos valores normales de bicarbonato ante aumentos o disminuciones de PCO 2 FV VOLVER
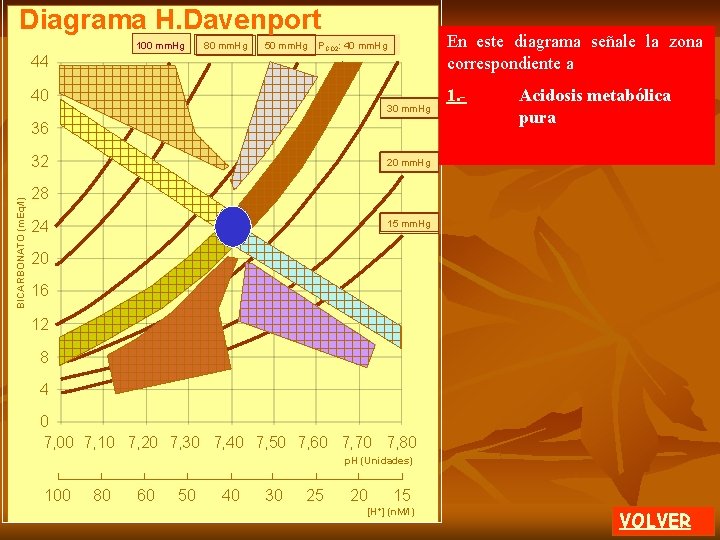
Diagrama H. Davenport 100 mm. Hg 80 mm. Hg 50 mm. Hg En este diagrama señale la zona correspondiente a PCO 2: 40 mm. Hg 44 40 30 mm. Hg 36 BICARBONATO (m. Eq/l) 32 1. - Acidosis metabólica pura 20 mm. Hg 28 24 15 mm. Hg 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
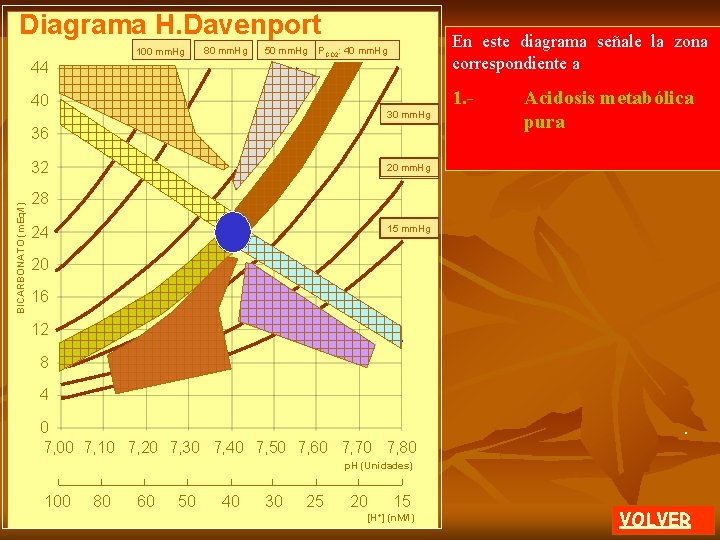
Diagrama H. Davenport 100 mm. Hg 80 mm. Hg 50 mm. Hg En este diagrama señale la zona correspondiente a PCO 2: 40 mm. Hg 44 40 30 mm. Hg 36 BICARBONATO (m. Eq/l) 32 1. - Acidosis metabólica pura 20 mm. Hg 28 24 15 mm. Hg 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 [H+] 15 (n. M/l) VOLVER
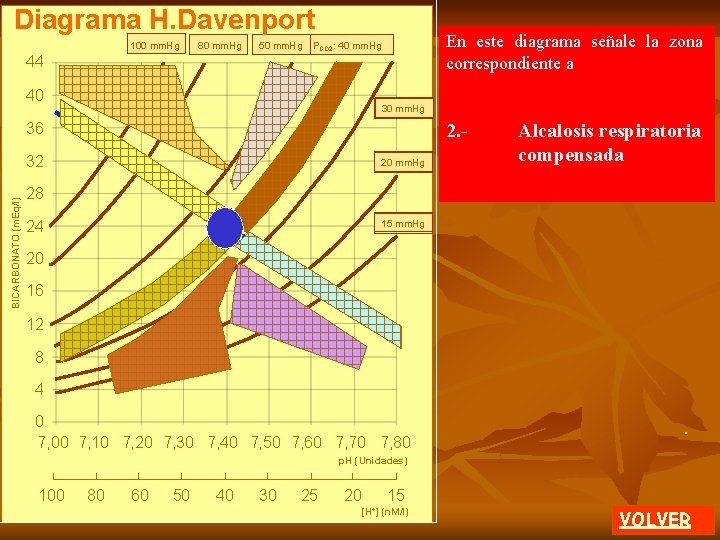
Diagrama H. Davenport 100 mm. Hg 80 mm. Hg 50 mm. Hg En este diagrama señale la zona correspondiente a PCO 2: 40 mm. Hg 44 40 30 mm. Hg 2. - 36 BICARBONATO (m. Eq/l) 32 20 mm. Hg Alcalosis respiratoria compensada 28 24 15 mm. Hg 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
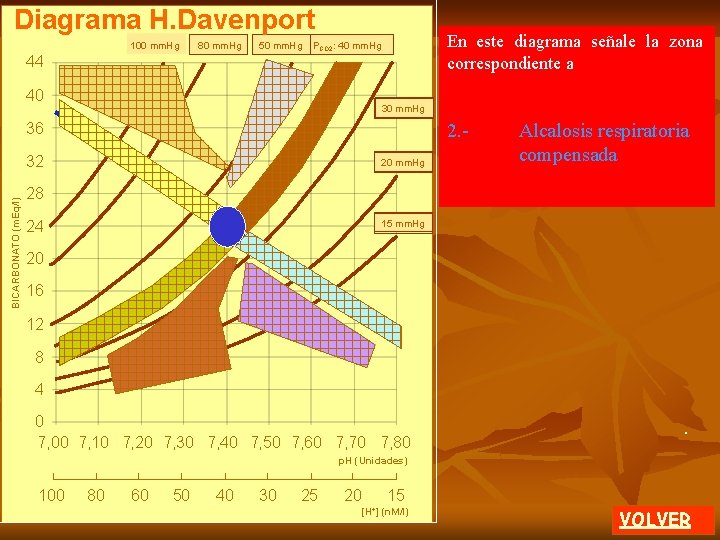
Diagrama H. Davenport 100 mm. Hg 80 mm. Hg 50 mm. Hg En este diagrama señale la zona correspondiente a PCO 2: 40 mm. Hg 44 40 30 mm. Hg 2. - 36 BICARBONATO (m. Eq/l) 32 20 mm. Hg Alcalosis respiratoria compensada 28 24 15 mm. Hg 20 16 12 8 4 0 7, 00 7, 10 7, 20 7, 30 7, 40 7, 50 7, 60 7, 70 7, 80 . p. H (Unidades) 100 80 60 50 40 30 25 20 15 [H+] (n. M/l) VOLVER
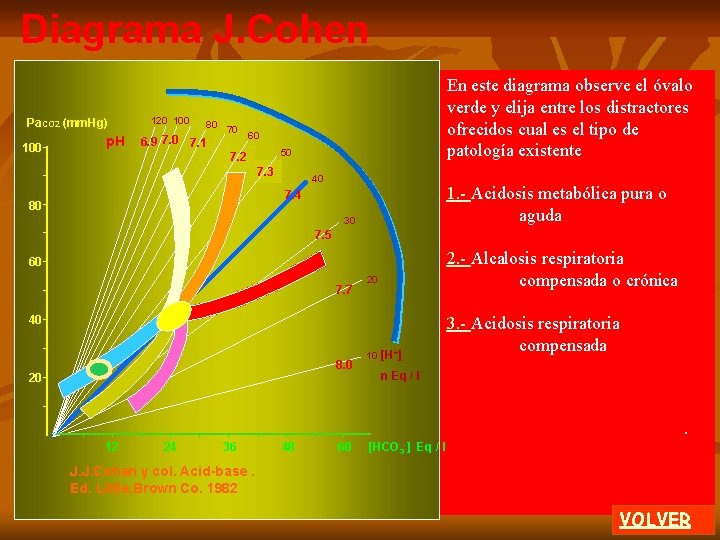
Diagrama J. Cohen Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 En este diagrama observe el óvalo verde y elija entre los distractores ofrecidos cual es el tipo de patología existente 60 50 7. 2 7. 3 40 1. - Acidosis metabólica pura o aguda 7. 4 80 30 7. 5 2. - Alcalosis respiratoria compensada o crónica 60 7. 7 20 3. - Acidosis respiratoria compensada 40 8. 0 20 10 [H+] n Eq / l . 12 24 36 48 60 [HCO 3 -] Eq / l J. J. Cohen y col. Acid-base. Ed. Little, Brown Co. 1982 VOLVER
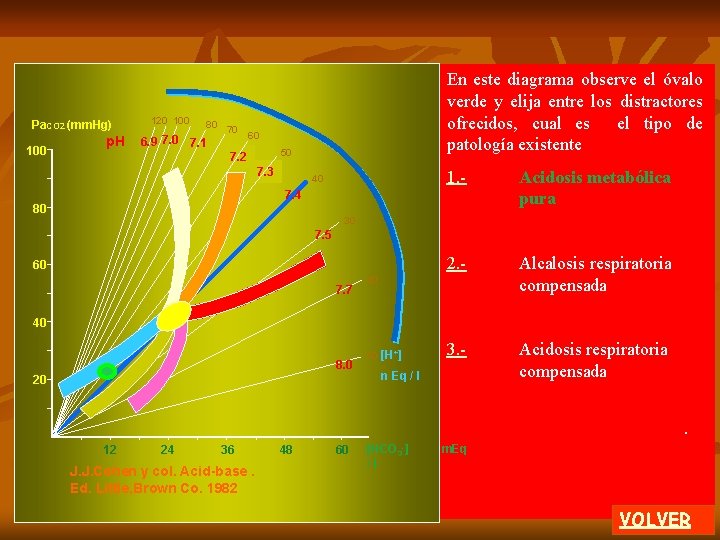
Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 En este diagrama observe el óvalo verde y elija entre los distractores ofrecidos, cual es el tipo de patología existente 60 50 7. 2 7. 3 40 1. - Acidosis metabólica pura 2. - Alcalosis respiratoria compensada 3. - Acidosis respiratoria compensada 7. 4 80 30 7. 5 60 7. 7 20 40 8. 0 20 10 [H+] n Eq / l . 12 24 36 J. J. Cohen y col. Acid-base. Ed. Little, Brown Co. 1982 48 60 [HCO 3 -] /l m. Eq VOLVER
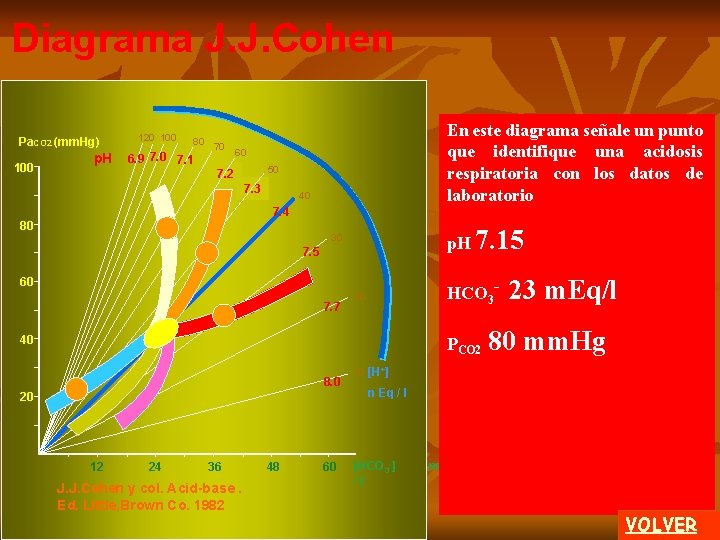
Diagrama J. J. Cohen Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 En este diagrama señale un punto que identifique una acidosis respiratoria con los datos de laboratorio 60 50 7. 2 7. 3 40 7. 4 80 p. H 7. 15 30 7. 5 HCO 3 - 60 7. 7 20 40 PCO 2 8. 0 20 10 23 m. Eq/l 80 mm. Hg [H+] n Eq / l . 12 24 36 J. J. Cohen y col. Acid-base. Ed. Little, Brown Co. 1982 48 60 [HCO 3 -] /l m. Eq VOLVER
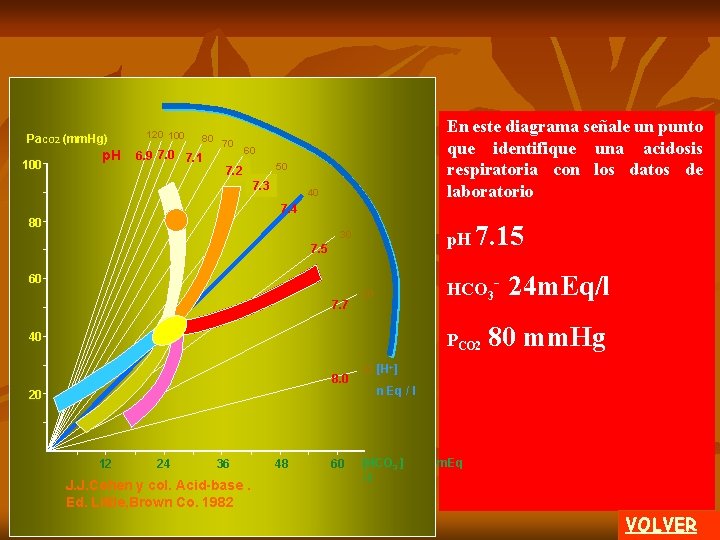
Pa. CO 2 (mm. Hg) 100 p. H 120 100 80 70 6. 9 7. 0 7. 1 En este diagrama señale un punto que identifique una acidosis respiratoria con los datos de laboratorio 60 50 7. 2 7. 3 40 7. 4 80 p. H 7. 15 30 7. 5 HCO 3 - 60 7. 7 20 PCO 2 40 8. 0 20 10 24 m. Eq/l 80 mm. Hg [H+] n Eq / l . 12 24 36 J. J. Cohen y col. Acid-base. Ed. Little, Brown Co. 1982 48 60 [HCO 3 -] /l m. Eq VOLVER
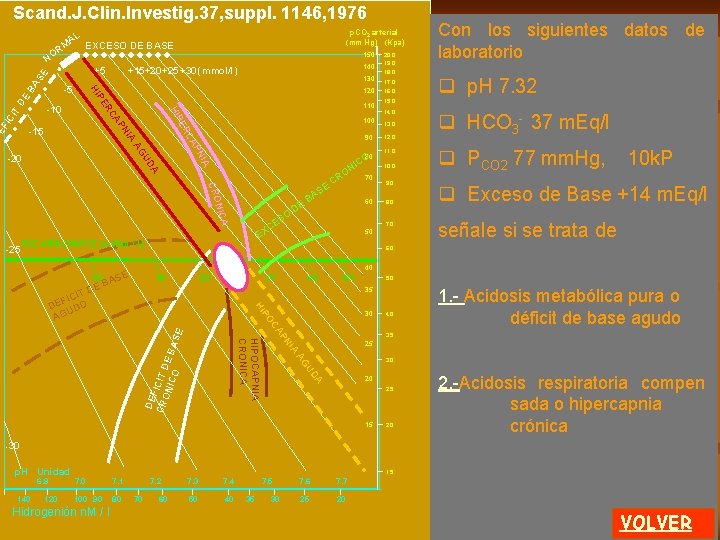
Scand. J. Clin. Investig. 37, suppl. 1146, 1976 85 p. CO 2 arterial (mm Hg) (Kpa) AL M EXCESO DE BASE R BA DE CI T FI DE 100 90 80 O A NI UD AG AP IA -20 110 RC N AP -15 130 PE HI -10 140 120 RC PE HI -5 150 +15+20 +25 +30 (mmol/l) +5 SE NO A RO NIC CRO SO C B BICARBONATO (m. Mol / l) 70 60 CE EX A -25 DE E AS C NI 50 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 9. 0 8. 0 7. 0 Con los siguientes datos de laboratorio q p. H 7. 32 q HCO 3 - 37 m. Eq/l q PCO 2 77 mm. Hg, 10 k. P q Exceso de Base +14 m. Eq/l señale si se trata de 6. 0 40 10 ASE EB IT D 15 20 30 40 50 5. 0 35 P HI FIC DE DO U AG 30 4. 0 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE 3. 5 25 IA HIPOCAPNIA CRONICA N AP OC 1. - Acidosis metabólica pura o déficit de base agudo 20 2. 5 15 2. 0 2. -Acidosis respiratoria compen sada o hipercapnia crónica -30 p. H Unidad 6. 9 140 120 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 VOLVER
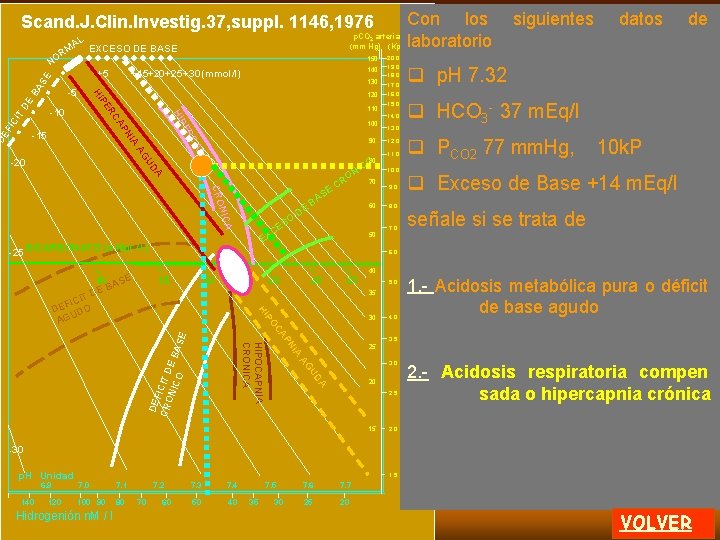
85 Scand. J. Clin. Investig. 37, suppl. 1146, 1976 AL EXCESO DE BASE M R NO SE BA DE FI CI T DE 100 90 NI UD AG AP IA N RO A E NIC CRO O ES C X A -25 80 CO I A -20 110 RC N AP -15 130 PE HI -10 140 120 RC PE HI -5 150 +15+20 +25 +30 (mmol/l) +5 Con los laboratorio siguientes datos de p. CO 2 arterial (mm Hg) (Kpa) DE S BA C 60 50 E BICARBONATO (m. Mol / l) 70 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 9. 0 8. 0 7. 0 q p. H 7. 32 q HCO 3 - 37 m. Eq/l q PCO 2 77 mm. Hg, 10 k. P q Exceso de Base +14 m. Eq/l señale si se trata de 6. 0 40 10 ASE EB IT D 15 20 30 40 50 5. 0 35 P HI FIC DE DO U AG 30 4. 0 1. - Acidosis metabólica pura o déficit de base agudo IA 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE N AP OC HIPOCAPNIA CRONICA 3. 5 25 20 2. 5 15 2. 0 2. - Acidosis respiratoria compen sada o hipercapnia crónica. -30 p. H Unidad 6. 9 140 120 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 VOLVER
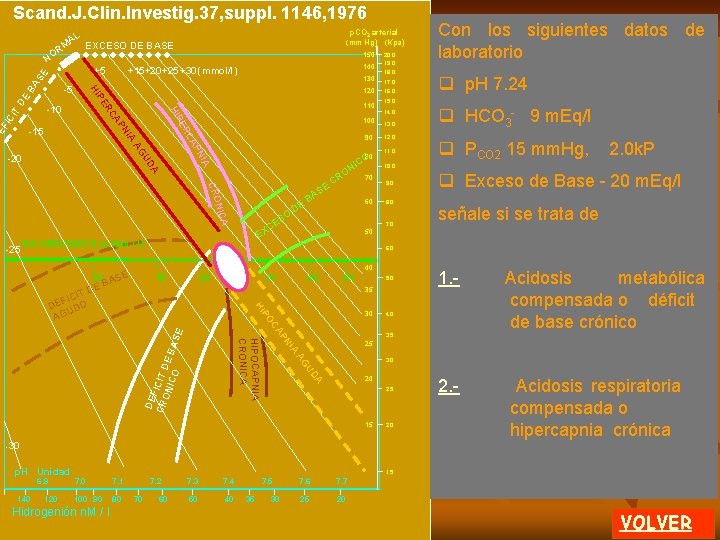
Scand. J. Clin. Investig. 37, suppl. 1146, 1976 85 p. CO 2 arterial (mm Hg) (Kpa) AL M EXCESO DE BASE R BA DE CI T FI DE 100 90 80 O A NI UD AG AP IA -20 110 RC N AP -15 130 PE HI -10 140 120 RC PE HI -5 150 +15+20 +25 +30 (mmol/l) +5 SE NO A NIC CRO E A O ES -25 DE S BA O CR C NI 60 C EX BICARBONATO (m. Mol / l) 70 50 20. 0 19. 0 18. 0 17. 0 16. 0 q p. H 7. 24 15. 0 14. 0 13. 0 12. 0 11. 0 q HCO 3 - 9 m. Eq/l q PCO 2 15 mm. Hg, 2. 0 k. P 10. 0 9. 0 8. 0 7. 0 q Exceso de Base - 20 m. Eq/l señale si se trata de 6. 0 40 10 ASE EB IT D Con los siguientes datos de laboratorio 15 20 30 40 50 5. 0 35 P HI FIC DE DO U AG 30 1. - Acidosis metabólica compensada o déficit de base crónico 2. - Acidosis respiratoria compensada o hipercapnia crónica 4. 0 IA 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE N AP OC HIPOCAPNIA CRONICA 3. 5 25 20 2. 5 15 2. 0 -30 p. H Unidad 6. 9 140 120 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 VOLVER
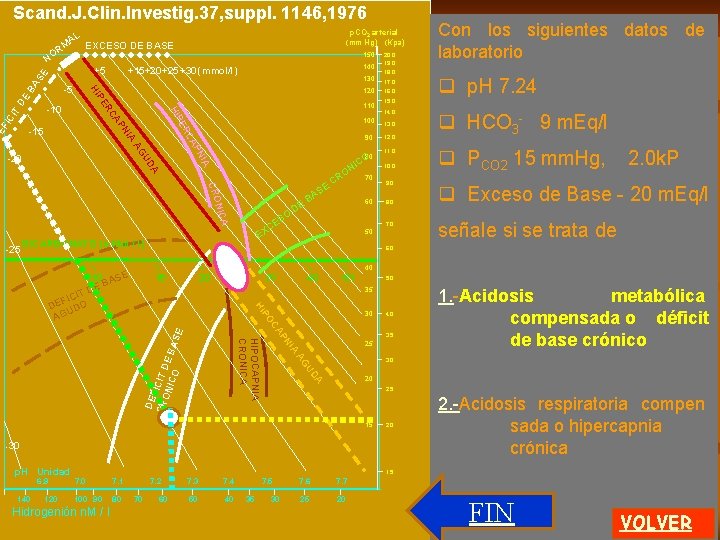
Scand. J. Clin. Investig. 37, suppl. 1146, 1976 85 p. CO 2 arterial (mm Hg) (Kpa) AL M EXCESO DE BASE R BA DE CI T FI DE 100 90 80 O A NI UD AG AP IA -20 110 RC N AP -15 130 PE HI -10 140 120 RC PE HI -5 150 +15+20 +25 +30 (mmol/l) +5 SE NO A RO NIC CRO SO C B BICARBONATO (m. Mol / l) 70 60 CE EX A -25 DE E AS C NI 50 20. 0 19. 0 18. 0 17. 0 16. 0 15. 0 14. 0 13. 0 12. 0 11. 0 10. 0 9. 0 8. 0 7. 0 15 20 30 40 50 P HI 30 4. 0 IA 2. 0 k. P q Exceso de Base - 20 m. Eq/l señale si se trata de 1. -Acidosis metabólica compensada o déficit de base crónico 3. 0 DA U AG DE F CR ICIT D ON ICO E BA SE N AP OC HIPOCAPNIA CRONICA 3. 5 25 20 2. 5 2. 0 -30 120 q PCO 2 15 mm. Hg, 5. 0 35 15 140 q HCO 3 - 9 m. Eq/l 6. 0 FIC DE DO U AG 6. 9 q p. H 7. 24 40 10 ASE EB IT D p. H Unidad Con los siguientes datos de laboratorio 2. -Acidosis respiratoria compen sada o hipercapnia crónica 1. 5 7. 0 7. 1 100 90 80 Hidrogenión n. M / l 7. 2 70 60 7. 3 7. 4 50 40 7. 5 35 30 7. 6 7. 7 25 20 FIN VOLVER
- Slides: 180