DIGITLN UEBN MATERIL slo projektu CZ 1 071

DIGITÁLNÍ UČEBNÍ MATERIÁL Číslo projektu CZ. 1. 07/1. 5. 00/34. 0969 Název školy Gymnázium Česká a Olympijských nadějí, České Budějovice, Česká 64 Název materiálu VY_32_INOVACE_CH_1_BAR_09_OBECNACHEMIE Autor Ivan Bartoš Tematický okruh Redoxní reakce Ročník 1. Datum tvorby 1. 6. 2012 Anotace Tento materiál objasňuje srozumitelnou formou podstatu redoxních reakcí. Grafická názornost se podílí na inovativnost i podání látky spolu s jednoduchostí grafických prvků. Metodický pokyn Prezentace je určena jako výklad do hodiny i jako materiál k samostudiu Možnosti využití: promítání, práce jednotlivců nebo dvojic u PC Pokud není uvedeno jinak, použitý materiál je z vlastních zdrojů autora

Oxidačně-redukční reakce Oxidace – zvýšení oxidačního stupně – odevzdání e – Redukce – snížení oxidačního stupně – příjem e – Aox + Bred 2 Fe 3+ + Sn 2+ redukce oxidace Ared + Box 2 Fe 2+ + Sn 4+ a) 2 Fe 3+ + 2 e – b) Sn 2+ Redukční činidlo – samo se oxiduje (Sn 2+ ) Oxidační činidlo – samo se redukuje (Fe 3+ ) 2 Fe 2+ Sn 4+ + 2 e – -

Oxidačně-redukční reakce - míra oxidačně redukčních schopností látek – oxidační potenciál Nernstova rovnice E = E 0 – (RT/z. F). ln (a. Ared/a. Box) E – potenciál E 0 – standardní potenciál F – Faradayova konstanta – 9, 65. 103 J. V-1. mol-1 a – aktivitní konstanta – charakteristika počtu elektronů vyměněných při parciální redoxní reakci z – počet elektronů vyměněných při parciální redoxní reakci T – termodynamická teplota R – Molární plynová konstanta – 8, 314 J. K-1. mol-1

Oxidačně redukční reakce Čím vyšší je hodnota potenciálu, tím snáze se daný kation oxiduje na částici s ox. Číslem 0 3 Cd 2+ + Al 3 Cd + 2 Al 3+ E 0 Al 3+/Al = -1, 66 V činidlo E 0 Cd 2+/Cd = -0, 4 V Cd – oxidační činidlo, Al – redukční

Oxidačně- redukční reakce Standardní oxidačně redukční potenciály některých látek Obr. 1

Oxidačně-redukční reakce - dysproporcionační reakce – tatáž látka se současně redukuje a oxiduje Cl 20 + Na. OH - Na. Cl-I + Na. Cl. IO + H 2 O synproporcionační reakce - oxidace i redukce vede na týž oxidační stav jednoho produktu 5 H I-I +HIVO 3 3 I 20 + 3 H 2 O Využití oxidačně-redukčních reakcí v chemické analýze: 1) Skupinové reakce – průkaz skupin aniontů a redukovadel (SO 32 -, I-, Br-, CN-, NO 2 -, S 2 -)- reakce s manganistanem v kyselém prostředí, za vzniku bezbarvé manganaté soli 10 I- + Mn. O 4 - + 16 H+ 5 I 2 + 2 Mn 2+ + 8 H 2 O
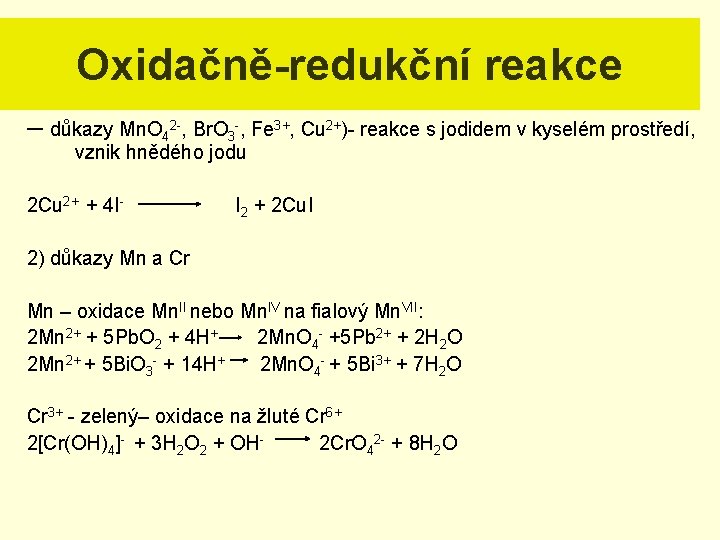
Oxidačně-redukční reakce – důkazy Mn. O 42 -, Br. O 3 -, Fe 3+, Cu 2+)- reakce s jodidem v kyselém prostředí, vznik hnědého jodu 2 Cu 2+ + 4 I- I 2 + 2 Cu. I 2) důkazy Mn a Cr Mn – oxidace Mn. II nebo Mn. IV na fialový Mn. VII: 2 Mn 2+ + 5 Pb. O 2 + 4 H+ 2 Mn. O 4 - +5 Pb 2+ + 2 H 2 O 2 Mn 2+ + 5 Bi. O 3 - + 14 H+ 2 Mn. O 4 - + 5 Bi 3+ + 7 H 2 O Cr 3+ - zelený– oxidace na žluté Cr 6+ 2[Cr(OH)4]- + 3 H 2 O 2 + OH 2 Cr. O 42 - + 8 H 2 O

Oxidačně-redukční reakce Další selektivní reakce – důkaz Sn 2+ a Hg 2+ Sn 2+ + Hg 2 Cl 2 + Sn 2+ Sn 4+ + Hg 22+ 2 Hg + Cl- Bílá šedá Důkaz aldehydů a redukujících cukrů – Fehlingovo činidlo (Cu. SO 4, vínan sodno draselný a alkalický peroxid) 2 Cu 2+ + RCH=O + 5 OHCu 2 O + RCOO- + 3 H 2 O rezavý Důkaz arsenu (Gutzeitova zkouška) As 3+ + 3 Zn + 3 H+ H 3 As + 3 Zn 2+ H 3 As + 6 Ag. NO 3 Ag 3 As. Ag. NO 3 + 3 H+ + 3 NO 3 Ag 3 As. Ag. NO 3 + 3 H 2 O 6 Ag + H 3 As. O 3 + 3 H+ + 3 NO 3černé

Oxidačně-redukční reakce Využití v odměrné analýze – oxidačně redukční titrace Indikace bodu ekvivalence – oxidačně-redukční indikátory Feroinový komplex – oxidovaný (ferin) – modrý, redukovaný (feroin) – červený Oxidimetrie 1) permanganometrie (Mn 7+ Mn 2+, , Mn 4+) 2) bichromatometrie (Cr 2 O 72 Cr 3+) 3) cerimetrie (Ce 4+ Ce 3+) 4) jodometrie (I 2 2 I-) 5) bromatometrie (Br. O 3 Br-) Reduktometrie – titanometrie (Ti 4+ Ti 3+)
![Použité zdroje • Obr. 1 na snímku č. 5 [online]. [cit. 26. 5. 2012]. Použité zdroje • Obr. 1 na snímku č. 5 [online]. [cit. 26. 5. 2012].](http://slidetodoc.com/presentation_image/104e1469138b7dd383906316e66aeaea/image-10.jpg)
Použité zdroje • Obr. 1 na snímku č. 5 [online]. [cit. 26. 5. 2012]. Dostupný na WWW: http: //image. tutorvista. com/content/redox-reactions/standard-reduction-electrode-potentials. gif Malijevský, A. a kol. : Breviář z fyzikální chemie. Praha: VŠCHT, 2000. Klikorka, J. , Hájek, B. , Votínsk, ý J. : Obecná a anorganická chemie. Praha: SNTL/Alfa, 1985. Brown, G. I. : Úvod do studia anorganické chemie. Praha: SNTL, 1982. Šrámek, V. : Kosina L. : Obecná a anorganická chemie. Olomouc: FIN, 1996. Greenwood, N. N. , Earnshaw, A. : Chemie prvků I. a II. Praha: Informatorium, 1993. Olmsted, J. III. , Williams, G. M. : Chemistry - the Molecular Science. Mosby: St. Louis, USA 1994.
- Slides: 10