DIGITLN UEBN MATERIL slo projektu CZ 1 071
DIGITÁLNÍ UČEBNÍ MATERIÁL Číslo projektu CZ. 1. 07/1. 5. 00/34. 0969 Název školy Gymnázium Česká a Olympijských nadějí, České Budějovice, Česká 64 Název materiálu VY_32_INOVACE_CH_2_Kod_16_kyslíkaté kyseliny fosforu Autor Pavla Kodríková Tematický okruh p - prvky Ročník 2. ročník, sexta Datum tvorby 15. listopadu 2012 Anotace Práce slouží k popisu a odvození kyslíkatých kyselin fosforu Metodický pokyn Prezentace je určena jako výklad do hodiny i jako materiál k samostudiu Možnosti využití: promítání, práce s interaktivní tabulí, práce jednotlivců nebo dvojic u PC, samostudium Pokud není uvedeno jinak, použitý materiál je z vlastních zdrojů autora

Metodický pokyn Prezentaci lze použít při výkladu frontálním, práci ve dvojicích či skupinách i samostudiu s důrazem na odvozování reaktivity prvku a sloučenin žáky. Snahou je nepředkládat hotová fakta a řešení, ale vést žáky k maximální spolupráci při výuce a aktivnímu přístupu. Při frontální práci s celou třídou na interaktivní tabuli lze vepisovat do prezentace v programu Activb. Studio nebo Activ. Inspire, a to přetažením anotace přes plochu. Pro kontrolu je vždy zařazen jako následující správně vyplněný slide. Práci je možno přizpůsobit schopnostem žáků ve třídě a využít nápovědy, která upozorňuje na zákonitosti chemických dějů a principy odvozování reakcí. Při práci ve dvojicích nebo skupinách může učitel vést hodinu tak, aby zadával jednotlivé části prezentace k řešení a podle schopností členů skupiny či dvojic doporučil či vynechal nápovědu. Takto mohou žáci pracovat u svých PC nebo podle prezentace puštěné pro celou třídu. Pokaždé je k dispozici kontrola práce na slidech s uvedeným řešením. Prezentaci lze použít k samostudiu nebo přípravě na výuku – obsahuje návody k řešení. Prezentaci lze použít k prověřování učiva – učitel použije nevyplněné slidy. Podle prezentace lze vytvořit pracovní listy – k vytištění jsou nevyplněné slidy. Nápověda se zobrazí kliknutím na tlačítko nápověda, poznámky vedoucí k řešení se zobrazují postupně, klikem myší se lze vrátit kdykoliv zpět.
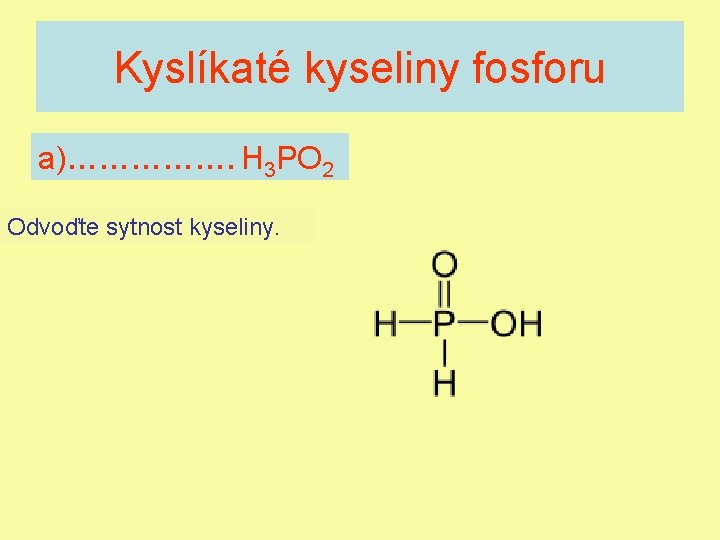
Kyslíkaté kyseliny fosforu a)……………. H 3 PO 2 Odvoďte sytnost kyseliny.
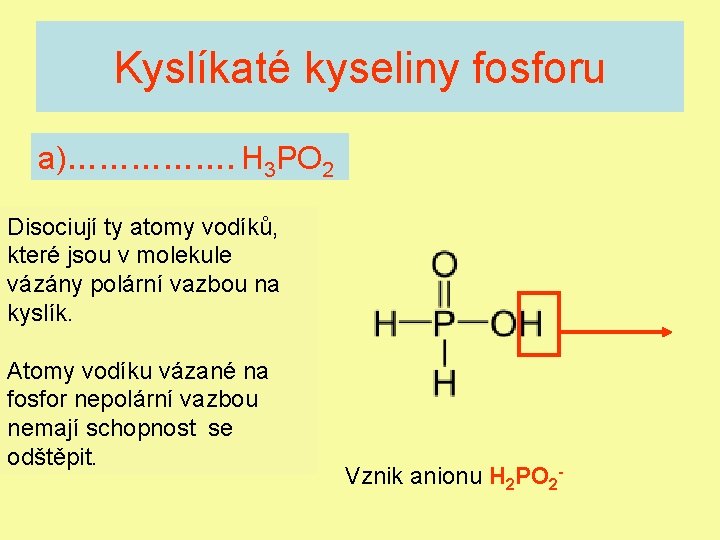
Kyslíkaté kyseliny fosforu a)……………. H 3 PO 2 Disociují ty atomy vodíků, které jsou v molekule vázány polární vazbou na kyslík. Atomy vodíku vázané na fosfor nepolární vazbou nemají schopnost se odštěpit. Vznik anionu H 2 PO 2 -

Kyslíkaté kyseliny fosforu a) Fosforná H 3 PO 2 jednosytná bílá krystalická látka teplem se rozkládá vznik: PH 3 + I 2 + H 2 O dobře rozpustná ve vodě Soli - …………………. . , např. fosfornan sodný ………(vzorce) Mají silné ……………(jaké redoxní) vlastnosti

Kyslíkaté kyseliny fosforu a) Fosforná H 3 PO 2 jednosytná bílá krystalická látka teplem se rozkládá vznik: PH 3 + I 2 + H 2 O dobře rozpustná ve vodě Soli – H 2 PO 2 -, např. fosfornan sodný Na. H 2 PO 2 Mají silné redukční vlastnosti
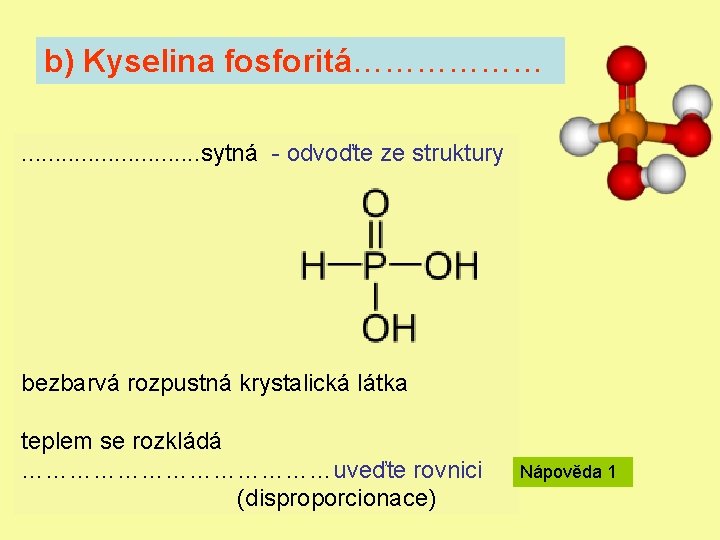
b) Kyselina fosforitá………………. . . . sytná - odvoďte ze struktury bezbarvá rozpustná krystalická látka teplem se rozkládá …………………uveďte rovnici (disproporcionace) Nápověda 1
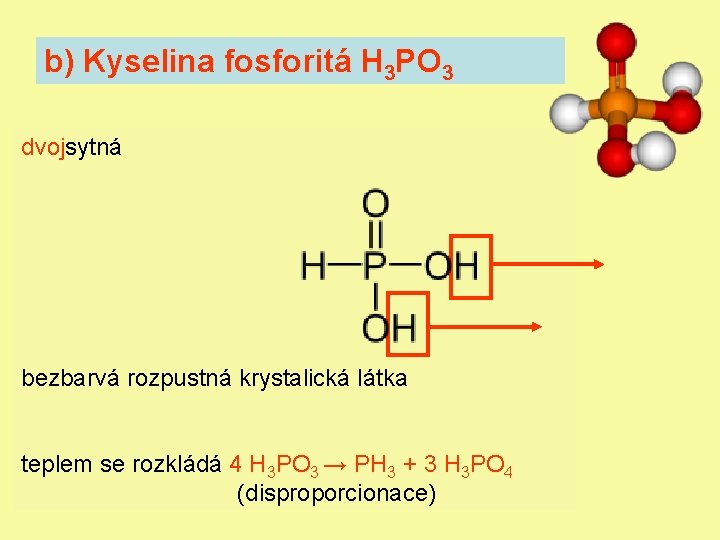
b) Kyselina fosforitá H 3 PO 3 dvojsytná bezbarvá rozpustná krystalická látka teplem se rozkládá 4 H 3 PO 3 → PH 3 + 3 H 3 PO 4 (disproporcionace)
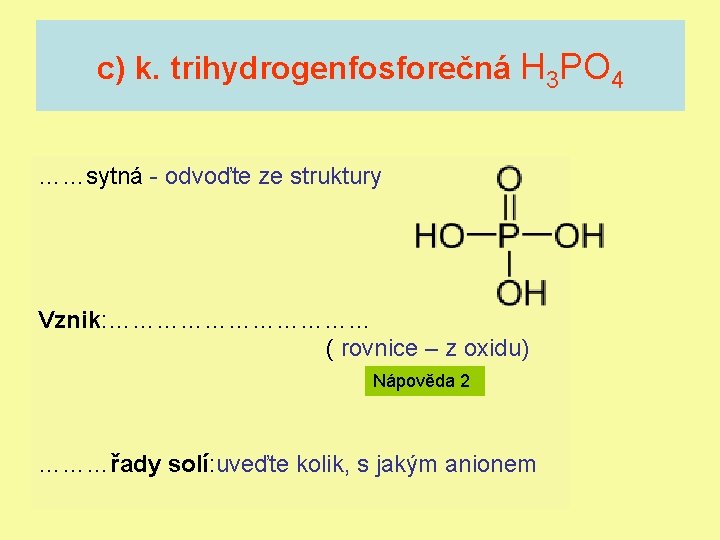
c) k. trihydrogenfosforečná H 3 PO 4 ……sytná - odvoďte ze struktury Vznik: ……………… ( rovnice – z oxidu) Nápověda 2 ………řady solí: uveďte kolik, s jakým anionem
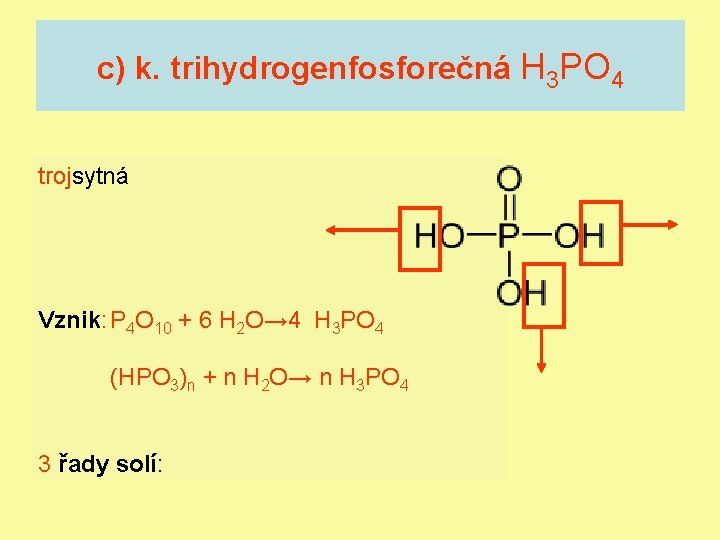
c) k. trihydrogenfosforečná H 3 PO 4 trojsytná Vznik: P 4 O 10 + 6 H 2 O→ 4 H 3 PO 4 (HPO 3)n + n H 2 O→ n H 3 PO 4 3 řady solí:
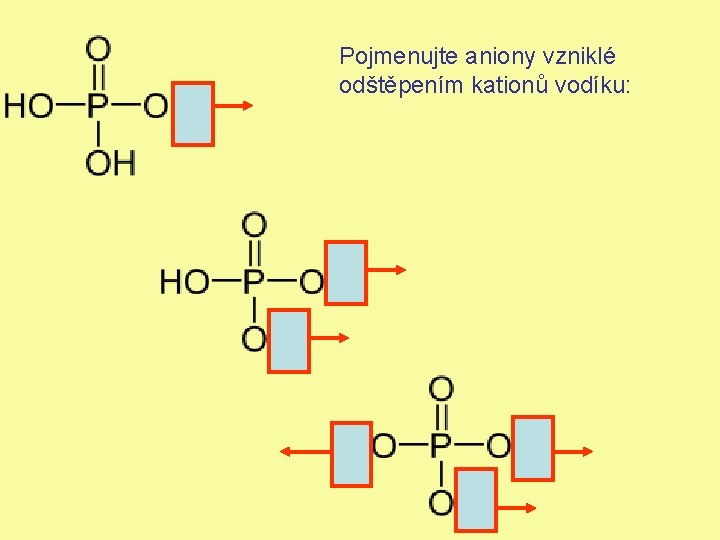
Pojmenujte aniony vzniklé odštěpením kationů vodíku:
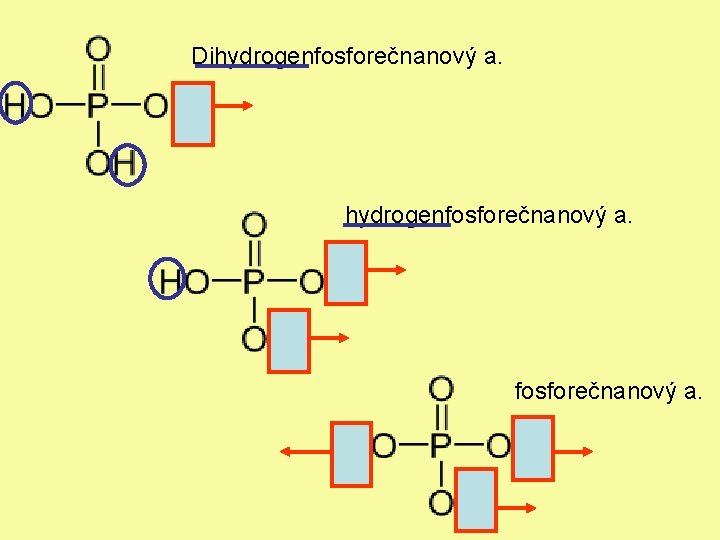
Dihydrogenfosforečnanový a.

Vlastnosti kyseliny trihydrogenfosforečné bezbarvá krystalická látka, rozpustná ve vodě (85% roztok) vrstevnatá struktura středně silná většina kovů se v ní pasivuje – na povrchu kovů vznikají nerozpustné fosforečnany použití: 1) fosfatace - povrchová úprava kovů 2) okyselení nápojů – hořká chuť (nápoje)
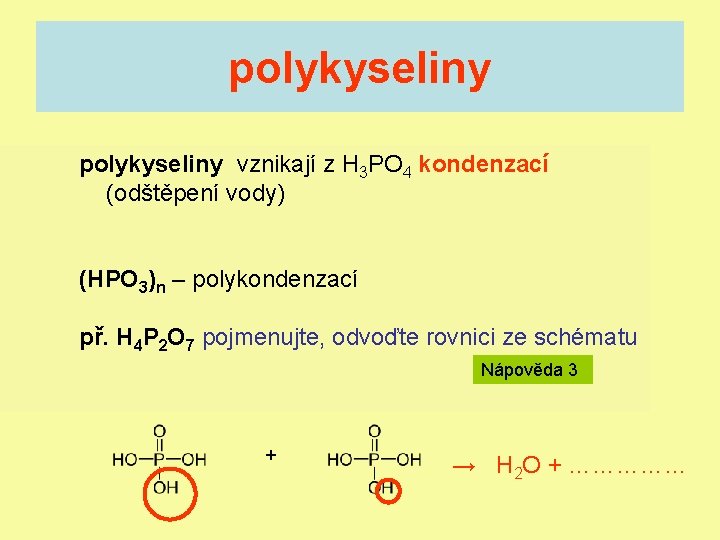
polykyseliny vznikají z H 3 PO 4 kondenzací (odštěpení vody) (HPO 3)n – polykondenzací př. H 4 P 2 O 7 pojmenujte, odvoďte rovnici ze schématu Nápověda 3 + → H 2 O + ……………
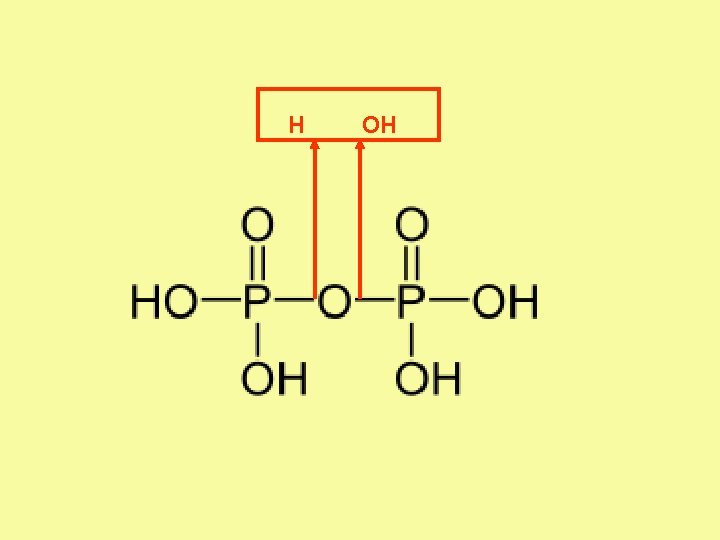
H OH
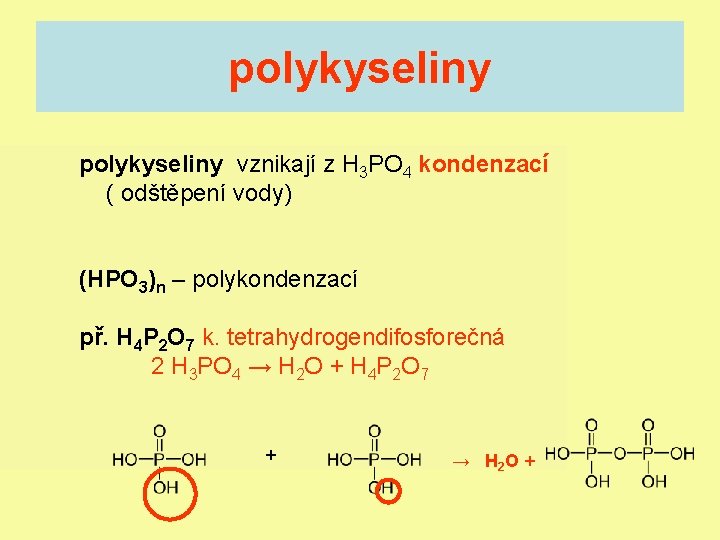
polykyseliny vznikají z H 3 PO 4 kondenzací ( odštěpení vody) (HPO 3)n – polykondenzací př. H 4 P 2 O 7 k. tetrahydrogendifosforečná 2 H 3 PO 4 → H 2 O + H 4 P 2 O 7 + → H 2 O +
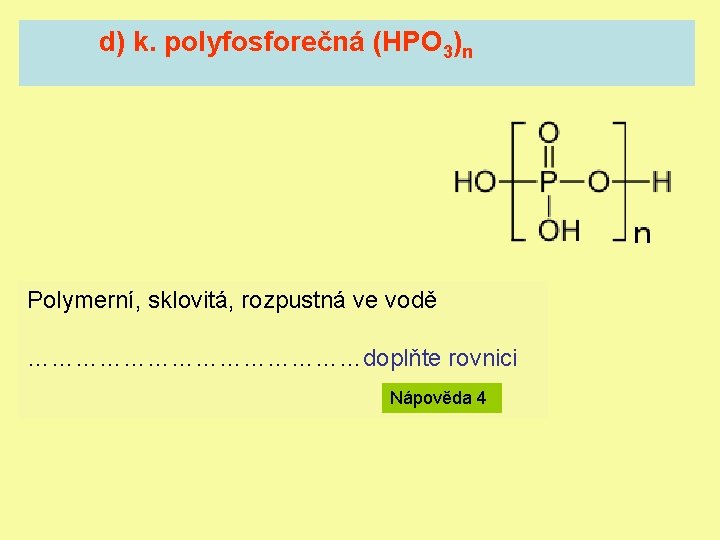
d) k. polyfosforečná (HPO 3)n Polymerní, sklovitá, rozpustná ve vodě …………………doplňte rovnici Nápověda 4
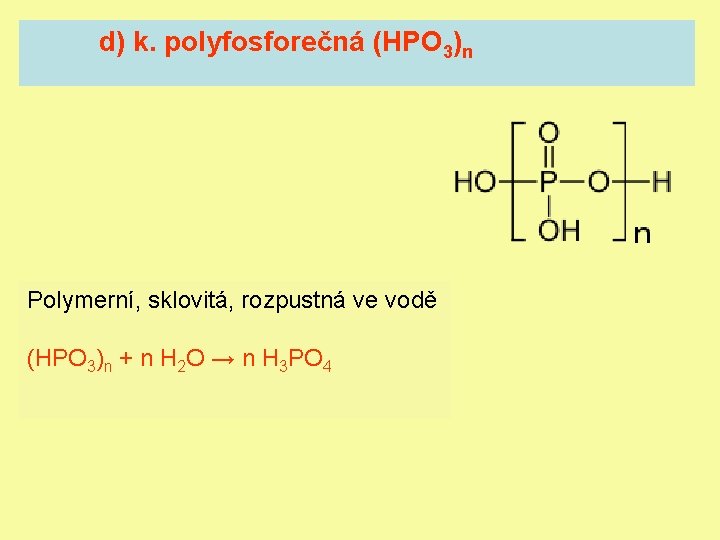
d) k. polyfosforečná (HPO 3)n Polymerní, sklovitá, rozpustná ve vodě (HPO 3)n + n H 2 O → n H 3 PO 4

Nápověda 1 Fosfor je ve sloučenině v ox. čísle III, může ho zvýšit Nejvyšší ox. číslo je V Vznikne kyselina trihydrogenfosforečná Došlo k oxidaci, musí proběhnout redukce Redukce probíhá opět na P III, redukuje se na -III P -III je obsažen ve fosfanu PH 3 Reakce je disproporcionační, koeficienty píšeme vpravo, pak dopočítáme 4 H 3 PO 3 → PH 3 + 3 H 3 PO 4 zpět

Nápověda 2 Kyselina fosforečná – tedy příprava z oxidu fosforečného oxid fosforečný tvoří dimér Dimér = 2 x oxid fosforečný = P 4 O 10 Kyselinotvorný oxid poskytuje reakcí s vodou kyselinu P 4 O 10 + 6 H 2 O→ 4 H 3 PO 4 Prohlédněte si v prezentaci kyselinu polyfosforečnou Vzniká z kyseliny trihydrogenfosforečné kondenzací – spojením molekul odštěpením vody Přidáním vody vznikne opět kyselina trihydrogenfosforečná (HPO 3)n + n H 2 O→ n H 3 PO 4 zpět
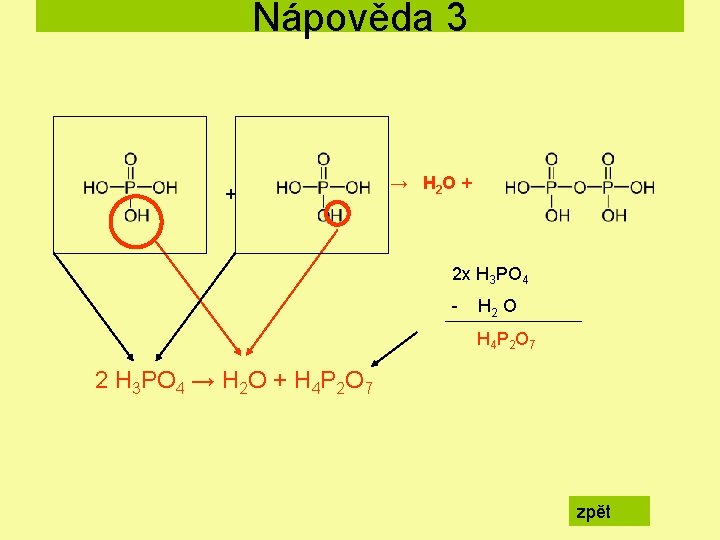
Nápověda 3 + → H 2 O + 2 x H 3 PO 4 - H 2 O H 4 P 2 O 7 2 H 3 PO 4 → H 2 O + H 4 P 2 O 7 zpět
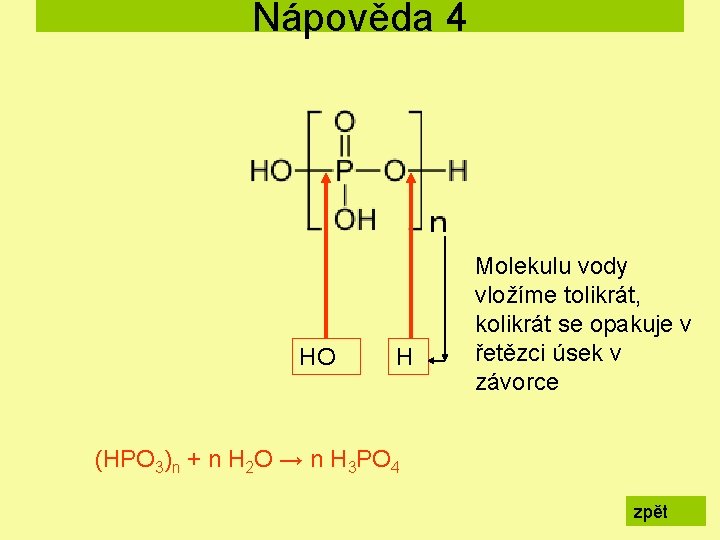
Nápověda 4 HO H Molekulu vody vložíme tolikrát, kolikrát se opakuje v řetězci úsek v závorce (HPO 3)n + n H 2 O → n H 3 PO 4 zpět
![Zdroje: NEUROTIKER. sk. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: Zdroje: NEUROTIKER. sk. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http:](http://slidetodoc.com/presentation_image_h/8792faf13e9d78ad079618d971ef2ee5/image-23.jpg)
Zdroje: NEUROTIKER. sk. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //sk. wikipedia. org/wiki/S%C 3%BAbor: Phosphins%C 3%A 4 ure_-_Hypophosphorous_acid. svg NEUROTIKER. sk. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //sk. wikipedia. org/wiki/S%C 3%BAbor: Phosphons%C 3%A 4 ure_-_Phosphorous_acid. svg AUTOR NEUVEDEN. cs. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //cs. wikipedia. org/wiki/Soubor: Phosphonic-acid-3 D-balls. png NEUROTIKER. sk. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //sk. wikipedia. org/wiki/S%C 3%BAbor: Phosphors%C 3%A 4 ure_-_Phosphoric_acid. svg MILLS, Benjamin. cs. wikipedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //cs. wikipedia. org/wiki/Soubor: Phosphoric-acid-3 D-vd. W. png NEUROTIKER; AUSHULZ. commons. wikimedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //commons. wikimedia. org/wiki/File: Polyphosphoric_acid. svg NEUROTIKER. commons. wikimedia. org [online]. [cit. 15. 11. 2012]. Dostupný na WWW: http: //commons. wikimedia. org/wiki/File: Diphosphors%C 3%A 4 ure_-_Diphosphoric_acid. svg HONZA, Jaroslav; MAREČEK, Aleš. Chemie pro čtyřletá gymnázia 1. díl. Brno: vlastním nákadem, 1995, ISBN 80900066 -6 -3. ŠRÁMEK, Vratislav. Obecná a anorganická chemie. Olomouc: OLOMOUC, 2000, ISBN 80 -7182 -099 -7.
- Slides: 23