Digitln uebn materil Kofaktory Mgr Blanka Janiczkov leden

Digitální učební materiál Kofaktory Mgr. Blanka Janiczková leden 2013

Digitální učební materiál Číslo projektu CZ. 1. 07/1. 5. 00/34. 0606 Název programu OP 1. 5 Vzdělávání pro konkurenceschopnost Název projektu Inovace vzdělávacího procesu Číslo materiálu VY_32_INOVACE-6 -17 -CHE-1 Název školy Střední zdravotnická škola, Brno, Jaselská 7/9 Autor Mgr. Blanka Janiczková Vzdělávací oblast Chemie Tematická oblast Biochemie Téma Kofaktory Ročník 4. L Datum tvorby 2. ledna 2013 Anotace DUM tvoří powerpointová prezentace. Materiál navazuje na probrané učivo o enzymech a je určen k seznámení žáků s některými významnými zástupci kofaktorů oxidoreduktas a transferas. Metodický pokyn Doporučuji použít k zopakování základních pojmů o enzymech a k výkladu nového učiva.

Kofaktory
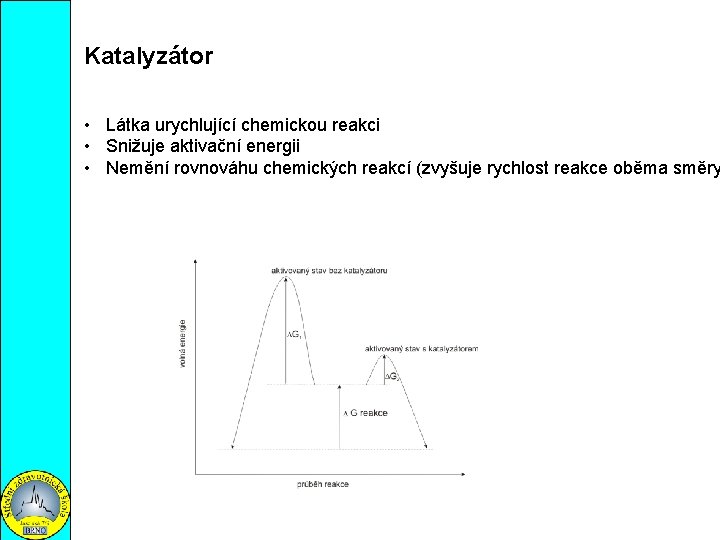
Katalyzátor • Látka urychlující chemickou reakci • Snižuje aktivační energii • Nemění rovnováhu chemických reakcí (zvyšuje rychlost reakce oběma směry
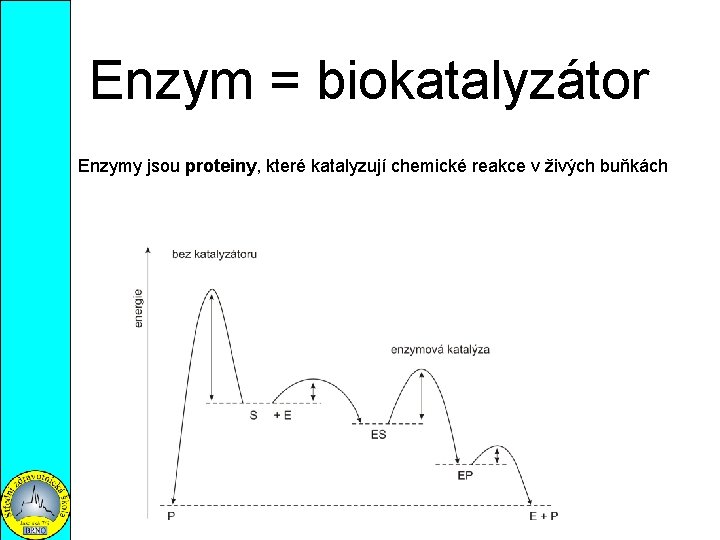
Enzym = biokatalyzátor Enzymy jsou proteiny, které katalyzují chemické reakce v živých buňkách
substrát enzym Látky, které se účinkem enzymů mění, se nazývají substráty produkt

(holo)enzym=kofaktor+apoenzym Enzym se skládá z bílkovinné složky – apoenzymu a nízkomolekulární nebílkovinné struktury - kofaktoru. Reverzibilně vázaný kofaktor se nazývá koenzym. Pevně vázaný kofaktor se nazývá prostetická skupina

Rozdělení enzymů 1. Oxidoreduktasy - enzymy biologické oxidace a redukce 2. Transferasy - enzymy přenášející skupiny 3. Hydrolasy – enzymy katalyzující hydrolytická štěpení 4. Lyasy – enzymy katalyzující eliminační reakce 5. Isomerasy – enzymy katalyzující přeskupení uvnitř molekul 6. Ligasy – enzymy katalyzující tvorbu vazby za štěpení ATP

Kofaktory 1. Kofaktory přenášející vodík – kofaktory oxidoreduktas 2. Kofaktory přenášející skupiny- kofaktory transferas 3. Kofaktory isomeras a lyas

Kofaktory oxidoreduktas 1. Pyridinové (nikotinamidové) nukleotidy 2. Flavinové nukleotidy 3. Biopterin 4. a-lipoát 5. Benzochinony s isoprenoidním postranním řetězcem 6. Hem 7. Ionty železa vázané přímo na bílkovinu 8. Glutathion
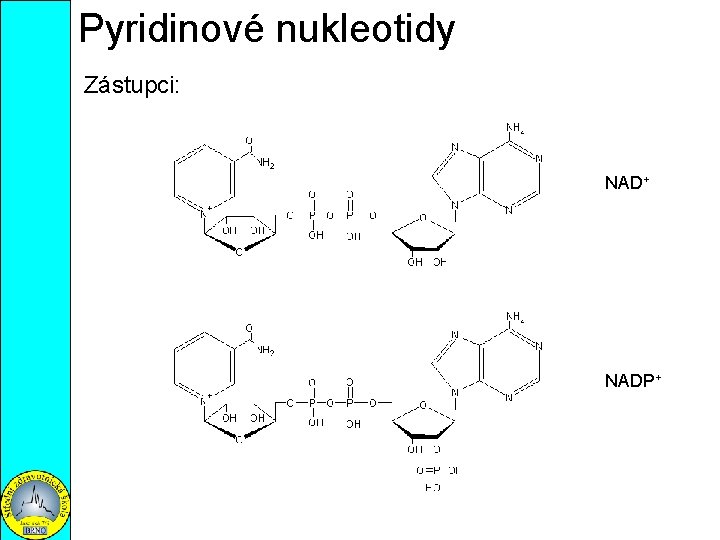
Pyridinové nukleotidy Zástupci: NAD+ NADP+
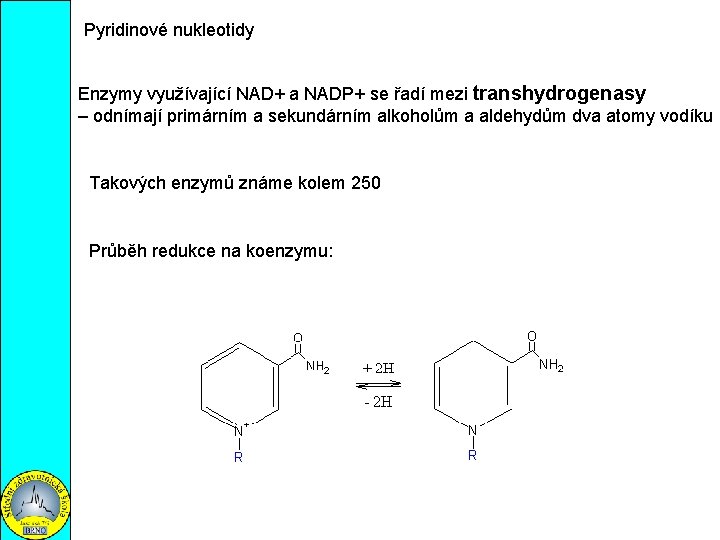
Pyridinové nukleotidy Enzymy využívající NAD+ a NADP+ se řadí mezi transhydrogenasy – odnímají primárním a sekundárním alkoholům a aldehydům dva atomy vodíku Takových enzymů známe kolem 250 Průběh redukce na koenzymu:
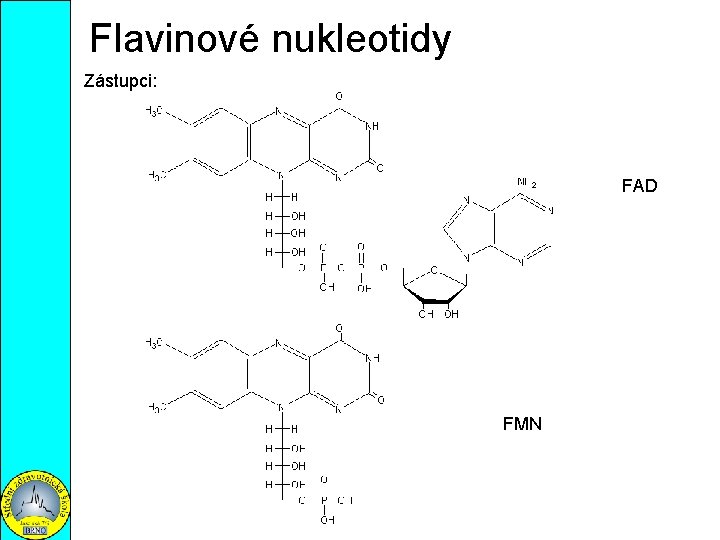
Flavinové nukleotidy Zástupci: FAD FMN
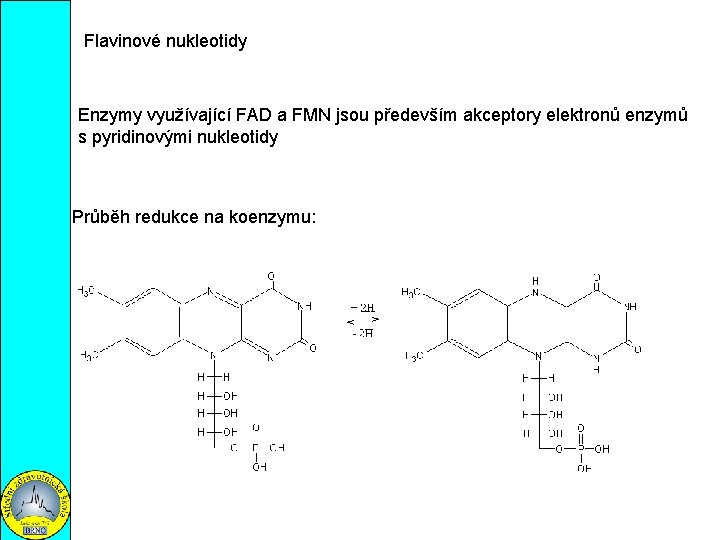
Flavinové nukleotidy Enzymy využívající FAD a FMN jsou především akceptory elektronů enzymů s pyridinovými nukleotidy Průběh redukce na koenzymu:
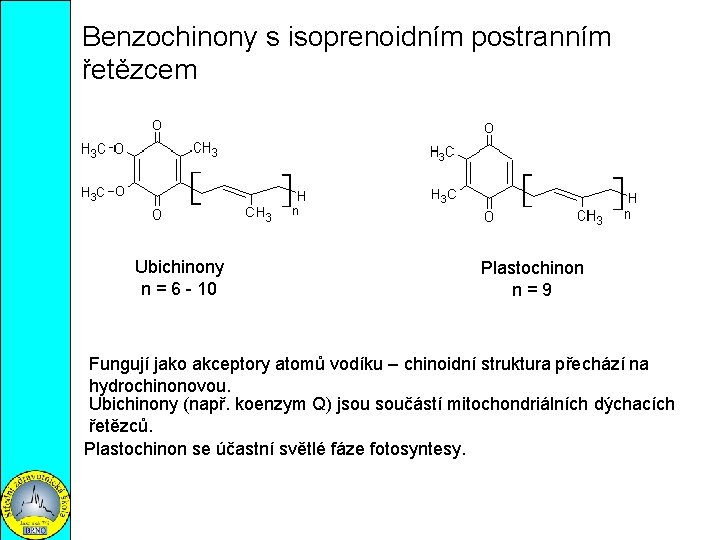
Benzochinony s isoprenoidním postranním řetězcem Ubichinony n = 6 - 10 Plastochinon n=9 Fungují jako akceptory atomů vodíku – chinoidní struktura přechází na hydrochinonovou. Ubichinony (např. koenzym Q) jsou součástí mitochondriálních dýchacích řetězců. Plastochinon se účastní světlé fáze fotosyntesy.
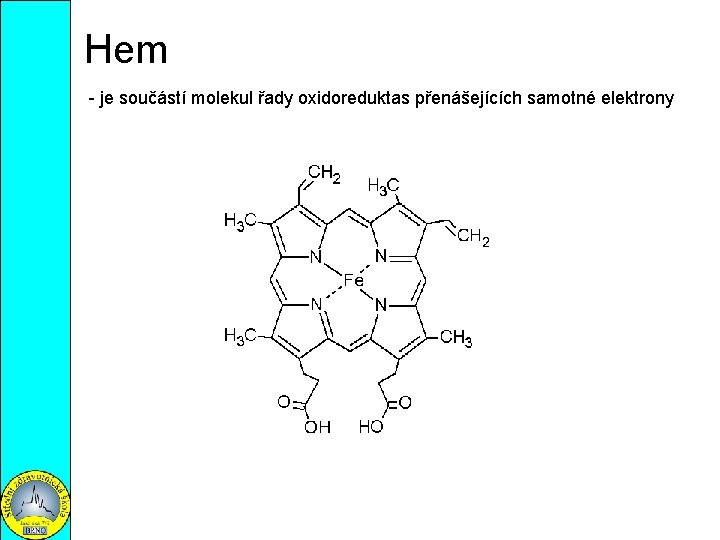
Hem - je součástí molekul řady oxidoreduktas přenášejících samotné elektrony

Kofaktory přenášející skupiny 1. Adenosintrifosfát 2. Aktivní sulfát 3. Kofaktory přenášející jednouhlíkaté štěpy 4. Kofaktory přenášející dvojuhlíkaté štěpy 5. Kofaktor přenášející aminoskupiny 6. Kofaktory přenášející rozsáhlé struktury
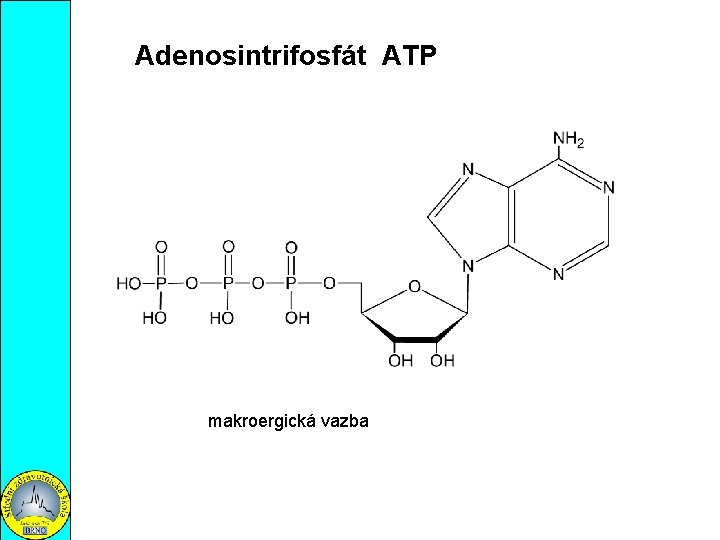
Adenosintrifosfát ATP makroergická vazba
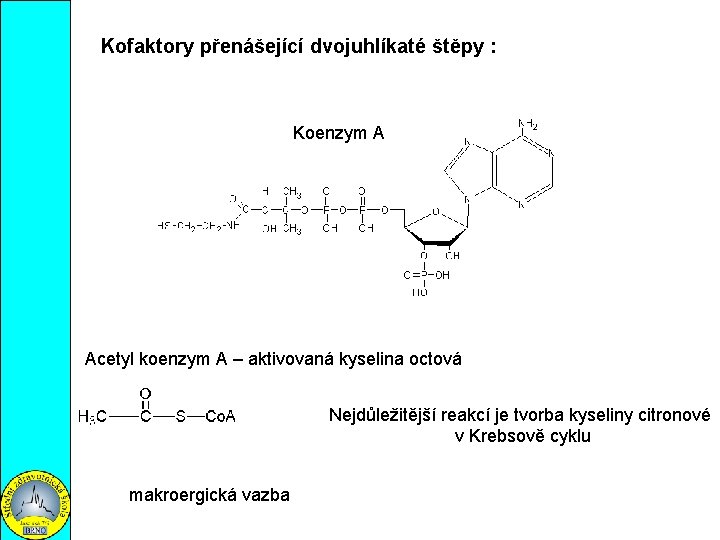
Kofaktory přenášející dvojuhlíkaté štěpy : Koenzym A Acetyl koenzym A – aktivovaná kyselina octová Nejdůležitější reakcí je tvorba kyseliny citronové v Krebsově cyklu makroergická vazba

Použitá literatura : MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia. 1. vyd. Olomouc: Nakladatelství Olomouc, 2000, 250 s. ISBN 80 -718 -2057 -1. VODRÁŽKA, Zdeněk. Biochemie. 2. oprav. vyd. Praha: Academia, 1999, Přer. str. ISBN 80 -200 -0600 -1. VOET, Donald. Biochemie. 1. vyd. Praha, 1995, 1325 s. ISBN 80 -856 -0544 -9. KARLSON, P. Základy biochemie. Praha : Academia, 1981. S. 323. Vzorce a grafy dílem autorky.
- Slides: 20