Digitln uebn materil Kinetika chemickch reakc Mgr Blanka

Digitální učební materiál Kinetika chemických reakcí Mgr. Blanka Janiczková prosinec 2013

Digitální učební materiál Číslo projektu CZ. 1. 07/1. 5. 00/34. 0606 Název programu OP 1. 5 Vzdělávání pro konkurenceschopnost Název projektu Inovace vzdělávacího procesu Číslo materiálu VY_32_INOVACE-6 -16 -CHE-19 Název školy Střední zdravotnická škola, Brno, Jaselská 7/9 Autor Mgr. Blanka Janiczková Vzdělávací oblast Chemie Tematická oblast Obecná a anorganická chemie Téma Kinetika chemických reakcí Ročník 1. Datum tvorby 29. 12. 2013 Anotace Materiál tvoří prezentace, která seznamuje žáky s průběhem chemických reakcí a s faktory, které ovlivňují rychlost chemických reakcí Metodický pokyn Doporučuje se použít k výkladu nového učiva a k následnému zopakování a procvičení důležitých pojmů.

Kinetika chemických reakcí

Chemická kinetika : Je vědní obor, který studuje rychlost chemických reakcí. Pro vysvětlení průběhu chemických reakcí byly vytvořeny dvě teorie :

Teorie aktivních srážek Pro uskutečnění chemické reakce je nutná srážka molekul reagujících látek. Molekuly musí mít také dostatečnou energii : AKTIVAČNÍ ENERGII = minimální energie, kterou musí molekuly mít aby srážka byla účinná.

Teorie aktivních srážek Velikost aktivační energie je dána součtem energií všech vazeb které při reakci zanikají. Jednotkou aktivační energie je KJ. mol-1 Reagující částice musí mít při srážce kromě energie i vhodnou prostorovou orientaci.
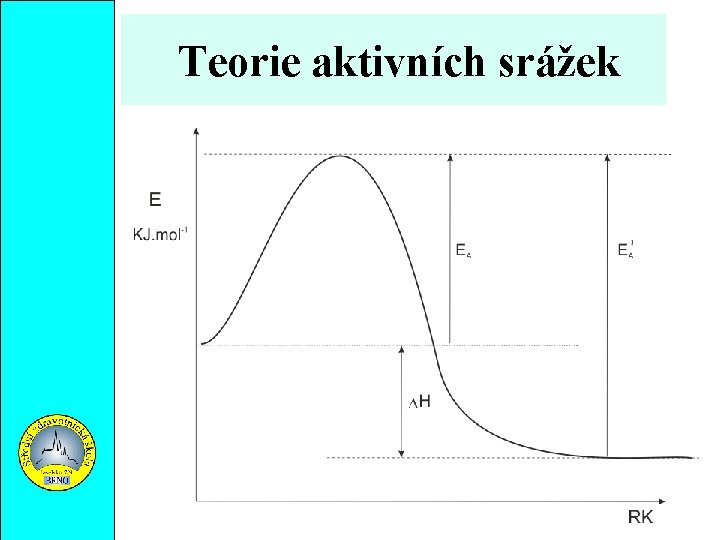
Teorie aktivních srážek
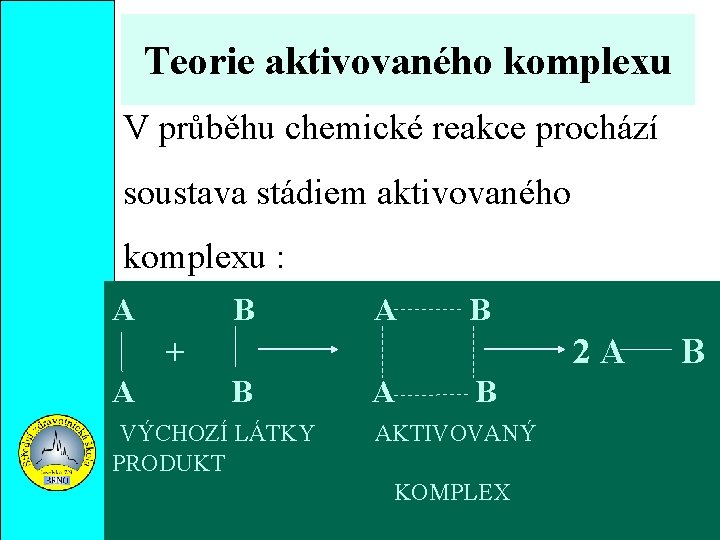
Teorie aktivovaného komplexu V průběhu chemické reakce prochází soustava stádiem aktivovaného komplexu : A B + A 2 A B VÝCHOZÍ LÁTKY PRODUKT A B AKTIVOVANÝ KOMPLEX B

Teorie aktivovaného komplexu Aktivační energie potřebná k vytvoření aktivovaného komplexu je mnohem nižší než aktivační energie potřebná k úplné disociaci molekul výchozích látek.
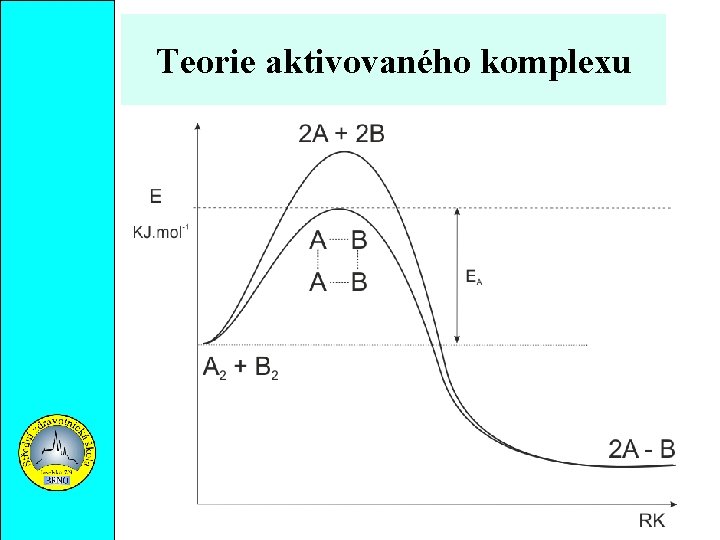
Teorie aktivovaného komplexu

Vliv teploty na rychlost chemické reakce Rostoucí teplota zvyšuje počet molekul, které dosáhnou na aktivační energii. Zvýšení teploty výchozích látek o 100 C zvýší rychlost reakce 2 x až 4 x

Vliv koncentrace na průběh chemické reakce Rostoucí koncentrace výchozích látek zvyšuje rychlost chemické reakce. Rychlost chemické reakce můžeme definovat jako časový úbytek molární koncentrace některého z reaktantů nebo přírůstek molární koncentrace libovolného produktu.
![Vliv koncentrace na průběh chemické reakce a. A + b. B v= ∆[A] a∆t Vliv koncentrace na průběh chemické reakce a. A + b. B v= ∆[A] a∆t](http://slidetodoc.com/presentation_image_h2/856b2ae4a8829a04d1e063c6190813e7/image-13.jpg)
Vliv koncentrace na průběh chemické reakce a. A + b. B v= ∆[A] a∆t c. C + d. D = ∆[B] b∆t = ∆[C] c∆t = ∆[D] d∆t v - rychlost reakce ∆ [A, B. C, D] - změna molární koncentrace látky A, B, C, D a, b, c, d - stechiometrické koeficienty látky A, B, C, D ∆ t - časový interval
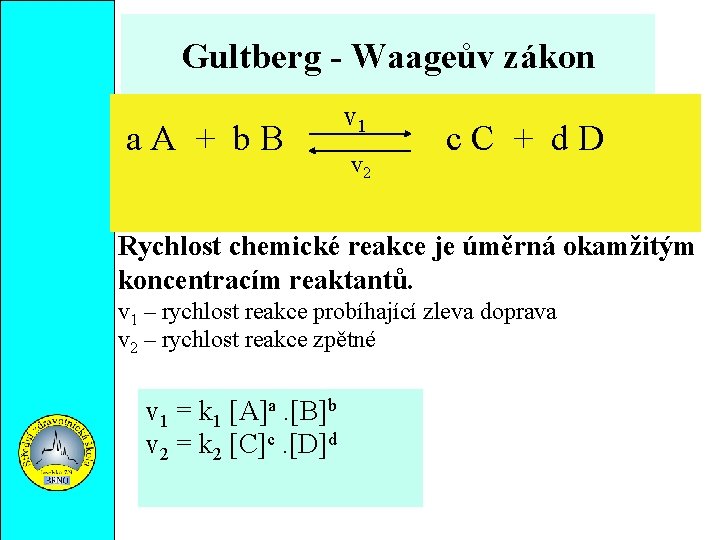
Gultberg - Waageův zákon a. A + b. B v 1 v 2 c. C + d. D Rychlost chemické reakce je úměrná okamžitým koncentracím reaktantů. v 1 – rychlost reakce probíhající zleva doprava v 2 – rychlost reakce zpětné v 1 = k 1 [A]a. [B]b v 2 = k 2 [C]c. [D]d

Gultberg - Waageův zákon V průběhu reakce ubývá výchozích látek a přibývá produktů. Reakce se postupně zpomaluje. U reakcí, které jsou vratné, se soustava po určité době dostane do DYNAMICKÉ ROVNOVÁHY kdy se rychlosti obou reakcí vyrovnají : v 1 = v 2

Gultberg - Waageův zákon Při dosažení rovnováhy se koncentrace látek A, B, C, D nemění ale reakce probíhají stále. Pro rovnovážné koncentrace platí : K = [C]c. [D]d [A]a. [B]b K - rovnovážná konstanta reakce Tento vztah je známý jako Gultberg- Waageův zákon

Vliv katalyzátorů na rychlost chemické reakce Katalyzátory jsou látky, které se při reakci Nespotřebovávají, nemění složení systému ani neposunují chemickou rovnováhu. Katalyzátory snižují aktivační energii reakce a tak reakci urychlují.
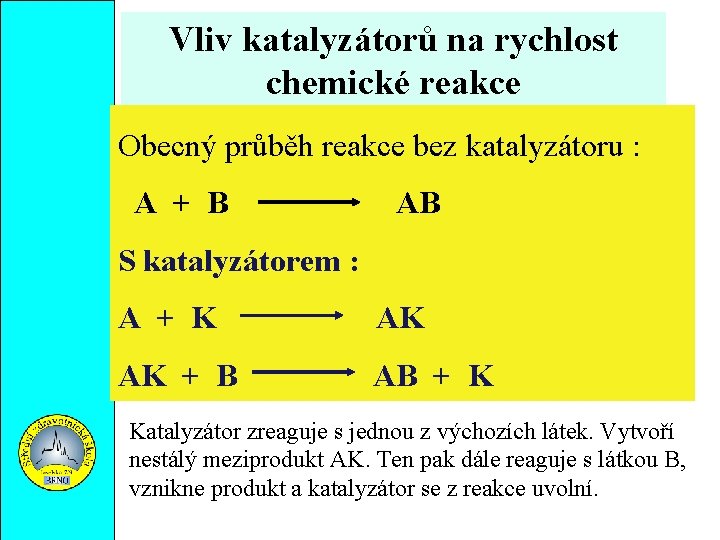
Vliv katalyzátorů na rychlost chemické reakce Obecný průběh reakce bez katalyzátoru : A + B AB S katalyzátorem : A + K AK AK + B AB + K Katalyzátor zreaguje s jednou z výchozích látek. Vytvoří nestálý meziprodukt AK. Ten pak dále reaguje s látkou B, vznikne produkt a katalyzátor se z reakce uvolní.

Vliv katalyzátorů na rychlost chemické reakce Homogenní katalýza – reaktanty a katalyzátor jsou ve stejném skupenství Heterogenní katalýza – reaktanty a katalyzátor jsou v různých skupenských fázích INHIBITORY = negativní katalyzátory zvyšují aktivační energii reakce a tím reakci zpomalují BIOKATALYZÁTORY – ENZYMY látky, které katalyzují reakce probíhající v živých organismech

Použitá literatura MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia: 1. díl. 3. , přeprac. vyd. Olomouc: Nakladatelství Olomouc, 1998, 240 s. ISBN 80 -7182 -055 -51. BANÝR, Jiří. Chemie pro střední školy: obecná, anorganická, analytická, biochemie. 2. vyd. Praha: SPN - pedagogické nakladatelství, 1996, 160 s. ISBN 80 -859 -3746 -8.
- Slides: 20