Digitln uebn materil edn roztok Mgr Blanka Janiczkov

Digitální učební materiál Ředění roztoků Mgr. Blanka Janiczková listopad 2013
Digitální učební materiál Číslo projektu CZ. 1. 07/1. 5. 00/34. 0606 Název programu OP 1. 5 Vzdělávání pro konkurenceschopnost Název projektu Inovace vzdělávacího procesu Číslo materiálu VY_32_INOVACE-6 -16 -CHE-12 Název školy Střední zdravotnická škola, Brno, Jaselská 7/9 Autor Mgr. Blanka Janiczková Vzdělávací oblast Chemie Tematická oblast Obecná a anorganická chemie Téma Ředění roztoků Ročník 1. L ( 4 L seminář) Datum tvorby 17. 11. 2013 Anotace Materiál tvoří prezentace, která seznamuje žáky se chemickými výpočty v oblasti složení roztoků. Metodický pokyn Doporučuje se použít k výkladu nového učiva a k následnému zopakování a procvičení.

Ředění roztoků

Ředění roztoků Roztoky požadovaného složení můžeme připravit i pomocí ředění roztoků o různých koncentracích.

Ředění roztoků Při výpočtech potřebných hmotností látek a roztoků využijeme následující vztahy : 1. KŘÍŽOVÉ PRAVIDLO 2. ZŘEĎOVACÍ ROVNICE

Křížové pravidlo

Příklad : Kolik cm 3 40 % kyseliny dusičné (ϱ =1, 25 g. cm-3) a kolik cm 3 vody je třeba na přípravu 250 cm 3 10 % roztoku HNO 3 ( ϱ= 1, 054 g. cm-3) ? Řešení : 1. Vstupní koncentrace roztoků napíšeme vedle sebe. 1. Do středu pomyslného čtverce vepíšeme požadovanou koncentraci 3. V úhlopříčkách odečteme od sebe vstupní a požadovanou koncentraci. (Výsledná čísla jsou v absolutních hodnotách. )
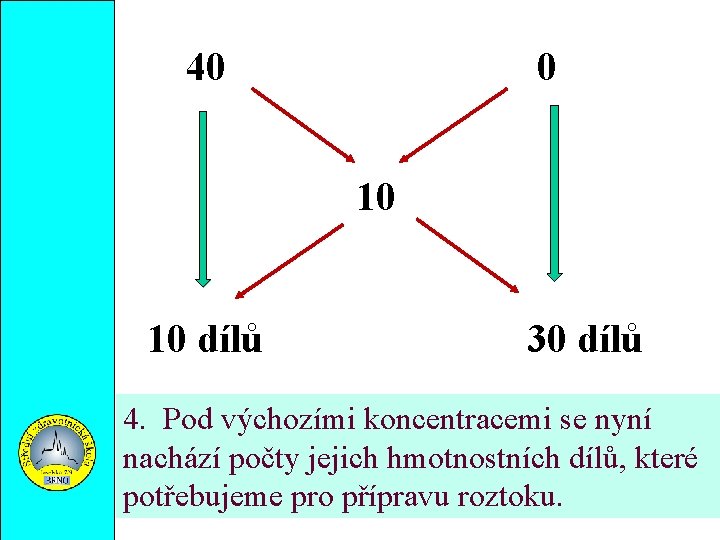
40 0 10 10 dílů 30 dílů 4. Pod výchozími koncentracemi se nyní nachází počty jejich hmotnostních dílů, které potřebujeme pro přípravu roztoku.

5. Nyní vypočítáme hmotnost připravovaného roztoku pomocí vztahu : m=ϱ. V m = 1, 054. 250 = 263, 5 g 6. 263, 5 g roztoku tedy vzniklo smísením 10 hmotnostních dílů 40% roztoku kyseliny a 30 hmotnostních dílů vody. Celkově je roztok tvořen 40 díly. Vypočítáme hmotnost jednoho dílu. 263, 5 : 40 = 6, 5875 g 10 dílů 40% HNO 3 … 10. 6, 5875= 65, 875 g 30 dílů vody………… 30. 6, 5875 =197, 625 g

7. Nakonec přepočítáme hmotnosti obou složek na objem : VHNO 3 = 65, 875 : 1, 25 = 52, 700 cm 3 VH 2 O = 197, 625 : 1, 0 = 197, 625 cm 3 (hustota vody = 1) Na přípravu 250 cm 3 roztoku 10 % HNO 3 potřebujeme 52, 700 cm 3 40% HNO 3 a 197, 625 cm 3 vody.

Zřeďovací rovnice

Zřeďovací rovnice : m 1 c 1 + m 2 c 2 = (m 1 + m 2)c nebo m 1 c 1 + m 2 c 2 = m c c 1, c 2 - procentové koncentrace výchozích roztoků c koncentrace vzniklého roztoků m 1, m 2 - hmotnosti výchozích roztoků m - celková hmotnost roztoku

Příklad : Pomocí zřeďovací rovnice vypočítejte kolik cm 3 60% kyseliny dusičné (ϱ= 1, 3667 g. cm 3) je potřeba na přípravu 550 cm 3 jejího 10 % roztoku ( ϱ= 1, 054 g. cm 3) Řešení : Voda má koncentraci 0 %. Hodnotu m 2 získáme tak, že od celkové hmotnosti roztoku odečteme m 1 : m 2 = m – m 1

Celkový objem roztoku převedeme na hmotnost pomocí vztahu : m=ϱ. V m = 1, 054. 550 = 579, 7 g Nyní dosadíme do zřeďovací rovnice : m 1 ∙ 60 + (m-m 1) ∙ 0 = 579, 7 ∙ 10 m 1 = 96, 62 g m 2 = 579, 7 – 96, 62 = 483, 08 g

Hmotnosti kapalin převedeme na objem : VHNO 3 = 96 , 62 : 1, 3667 =70, 69 cm 3 VH 2 O = 483 , 08 cm 3 Na přípravu 550 cm 3 roztoku 10 % HNO 3 použijeme 70, 69 cm 3 60% HNO 3 a 483, 08 cm 3 H 2 O.

Příklady k procvičení : 1. Vypočítejte kolik cm 3 80% kyseliny sírové (ϱ = 1, 7272 g. cm 3) je potřeba na přípravu 500 cm 3 jejího 20 % roztoku (ϱ = 1, 1394 g. cm 3). 2. Jaká bude výsledná koncentrace roztoku který vznikne smísením 250 cm 3 50 % kyseliny sírové ( ϱ = 1, 3951 g. cm 3 ) s 300 g 15 % roztoku této kyseliny ?

Příklady k procvičení : 3. Kolik g 30 % roztoku hydroxidu draselného a kolik cm 3 vody potřebujeme na přípravu 2 dm 3 10 % roztoku ( ϱ = 1, 0904 g. cm 3) této látky ? 1. Kolik gramů vody je nutno přidat ke 3 kg roztoku glukosy abychom získali 10 % roztok ? 5. Určete hmotnost chloridu sodného, který je nutno rozpustit ve 2 kg vody, abychom získali 40 % roztok Na. Cl.

Použitá literatura MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia: 1. díl. 3. , přeprac. vyd. Olomouc: Nakladatelství Olomouc, 1998, 240 s. ISBN 80 -7182 -055 -51. MAREČEK, Aleš a Jaroslav HONZA. Chemie: sbírka příkladů pro studenty středních škol. Vyd. 1. Brno: Proton, 2001, 146 s. ISBN 80 -902 -4022 -4. BANÝR, Jiří. Chemie pro střední školy: obecná, anorganická, analytická, biochemie. 2. vyd. Praha: SPN - pedagogické nakladatelství, 1996, 160 s. ISBN 80 -859 -3746 -8.
- Slides: 18