Digitln uebn materil Chemick vazba Mgr Blanka Janiczkov

Digitální učební materiál Chemická vazba Mgr. Blanka Janiczková prosinec 2013

Digitální učební materiál Číslo projektu CZ. 1. 07/1. 5. 00/34. 0606 Název programu OP 1. 5 Vzdělávání pro konkurenceschopnost Název projektu Inovace vzdělávacího procesu Číslo materiálu VY_32_INOVACE-6 -16 -CHE-15 Název školy Střední zdravotnická škola, Brno, Jaselská 7/9 Autor Mgr. Blanka Janiczková Vzdělávací oblast Chemie Tematická oblast Obecná a anorganická chemie Téma Chemická vazba Ročník 1. Datum tvorby 07. 12. 2013 Anotace Materiál tvoří prezentace, která seznamuje žáky se schopností atomů vytvářet složitější útvary. Metodický pokyn Doporučuje se použít k výkladu nového učiva a k následnému

Chemická vazba

Chemická vazba : Atomy většiny prvků nejsou schopny samostatné existence a spojují se do větších celků – molekul. Molekuly prvků - H 2 , P 4 , O 2 sloučenin - H 2 O, Na. Cl

Chemická vazba : Je spojení mezi atomy, které je realizováno prostřednictvím valenčních elektronů. Typy chemické vazby : vazba kovalentní vazba polární vazba iontová vazba kovová

Vazba kovalentní : Předpoklady vzniku vazby : přiblížení atomů dostatečná energie vhodné uspořádání valenčních elektronů Pak dojde k překrytí orbitalů valenčních elektronů a ke vzniku vazebných elektronových párů
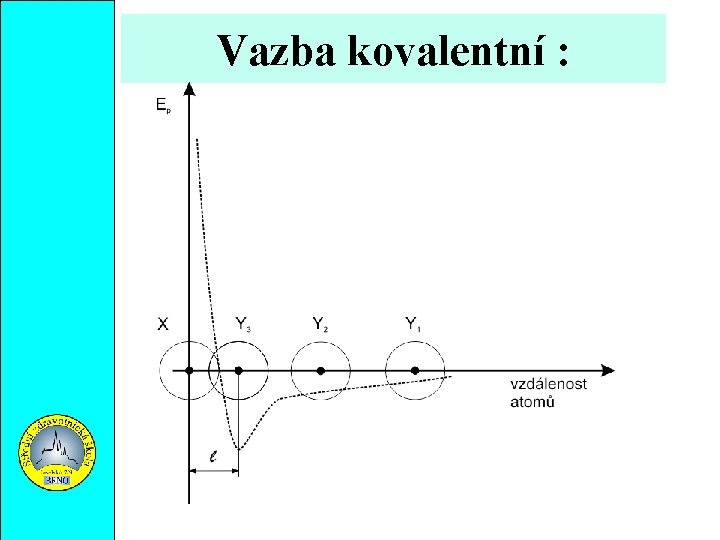
Vazba kovalentní :

Vazba kovalentní : Vzniká sdílením elektronových párů Vazebná energie : energie, která se uvolní při vzniku vazby udává se v KJ/mol Disociační energie : energie potřebná ke zrušení vazby, je stejně velká jako vazebná, má opačné znaménko

Vazba kovalentní : Podle počtu valenčních elektronů, které tvoří vazbu rozlišujeme : Vazba jednoduchá : je tvořena jedním elektronovým párem H˙ + ˙H H-H

Vazba kovalentní : Vazba dvojná : je tvořena dvěma elektronovými páry : O : + : O O=O Vazba trojná : je tvořena třemi elektronovými páry : N⋮ + ⋮ N N ≡ N
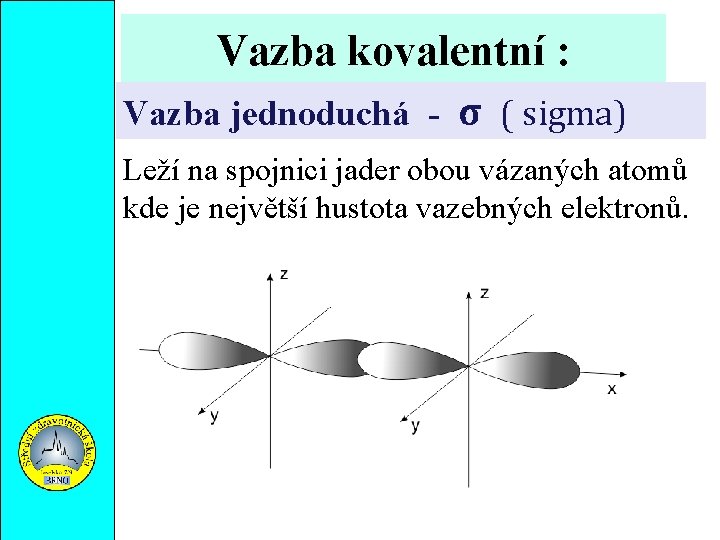
Vazba kovalentní : Vazba jednoduchá - σ ( sigma) Leží na spojnici jader obou vázaných atomů kde je největší hustota vazebných elektronů.
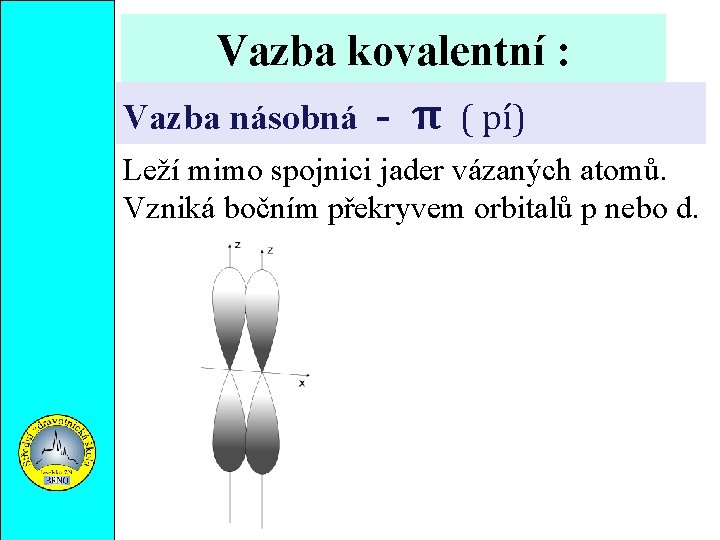
Vazba kovalentní : Vazba násobná - π ( pí) Leží mimo spojnici jader vázaných atomů. Vzniká bočním překryvem orbitalů p nebo d.

Vazba polární : Vzniká mezi atomy s rozdílnou schopností přitahovat elektrony : ELEKTRONEGATIVITOU Elektronegativita se vyjadřuje číselnou hodnotou – podle L. Paulinga. Čísla najdeme v chemické tabulce.

Vazba polární : Čím víc daný prvek přitahuje elektrony, tím vyšší je hodnota jeho elektronegativity. U vazby polární je rozdíl hodnot elektronegativit větší než 0, 4.

Vazba iontová : Vzniká jestliže je rozdíl hodnot elektronegativit vázaných atomů větší než 1, 7. Pak je valenční elektron jednoho z atomů vtažen do valenční vrstvy druhého atomu a vzniká kation a anion. Na+ Cl –

Vazba kovalentní - nepolární Rozdíl hodnot elektronegativit vázaných atomů je v intervalu 0 - 0, 4 Vazba polární Rozdíl elektronegativit mezi vázanými atomy je větší než 0, 4 ale menší než 1, 7 Vazba iontová Rozdíl elektronegativit vázaných atomů je větší než 1, 7

Výpočtem urči typ vazby v těchto molekulách : H 2 O KBr N 2 Ca. O NH 3 Mg. S

Vazba kovová : kationty kovu jsou pravidelně rozmístěny v uzlových bodech krystalové mřížky valenčními elektrony, které se mezi nimi volně pohybují ve formě elektronového plynu. Valenční elektrony jsou společné všem členům mřížky. ⨁ ⨁ ⨁ ⨁ ⨁ ⨁

Použitá literatura MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia: 1. díl. 3. , přeprac. vyd. Olomouc: Nakladatelství Olomouc, 1998, 240 s. ISBN 80 -7182 -055 -51. BANÝR, Jiří. Chemie pro střední školy: obecná, anorganická, analytická, biochemie. 2. vyd. Praha: SPN - pedagogické nakladatelství, 1996, 160 s. ISBN 80 -859 -3746 -8.
- Slides: 19