Digitln uebn materil Acidobazick reakce Mgr Blanka Janiczkov

Digitální učební materiál Acidobazické reakce Mgr. Blanka Janiczková duben 2013

Digitální učební materiál Číslo projektu CZ. 1. 07/1. 5. 00/34. 0606 Název programu OP 1. 5 Vzdělávání pro konkurenceschopnost Název projektu Inovace vzdělávacího procesu Číslo materiálu VY_32_INOVACE-6 -16 -CHE-2 Název školy Střední zdravotnická škola, Brno, Jaselská 7/9 Autor Mgr. Blanka Janiczková Vzdělávací oblast Chemie Tematická oblast Obecná a anorganická chemie Téma Acidobazické reakce Ročník 1. L Datum tvorby 25. dubna 2013 Anotace Materiál tvoří prezentace, která seznamuje žáky s významnou skupinou chemických reakcí. Metodický pokyn Doporučuje se použít k výkladu nového učiva a k následnému zopakování a procvičení důležitých pojmů.

Acidobazické reakce (Protolytické reakce) Reakce, které probíhají mezi kyselinami a zásadami

Acidobazické reakce : 1. Arrheniova teorie 2. Brönsted-Lowryho teorie 3. Síla kyselin a zásad
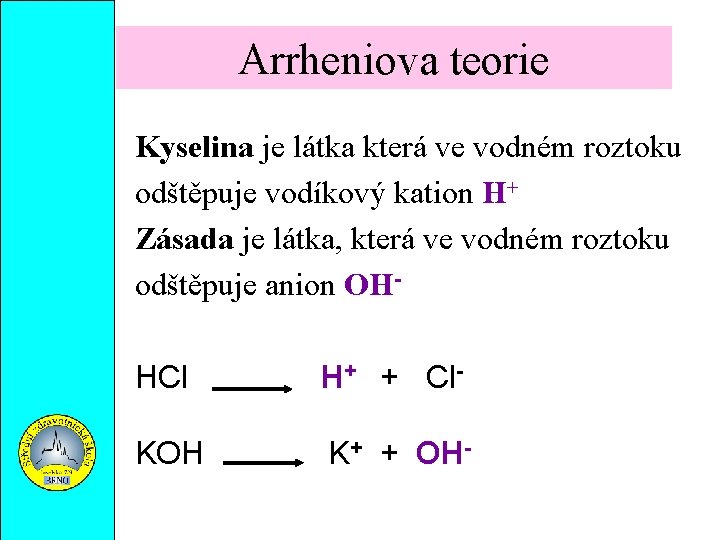
Arrheniova teorie Kyselina je látka která ve vodném roztoku odštěpuje vodíkový kation H+ Zásada je látka, která ve vodném roztoku odštěpuje anion OH HCl H+ + Cl KOH K+ + OH

Brönsted-Lowryho teorie • Je obecnější • Bere v úvahu i rozpouštědlo Kyselina je látka která je schopna odštěpit proton H+. Zásada je látka, která je schopna vázat proton H+.
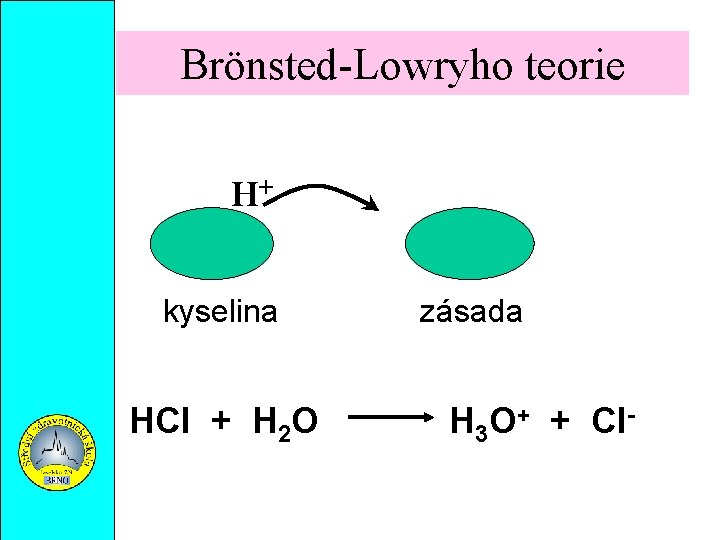
Brönsted-Lowryho teorie H+ kyselina HCl + H 2 O zásada H 3 O+ + Cl

Určete částici, která se podle Brönstedovy teorie může chovat ve vodném roztoku jako kyselina : SO 42 - , NH 3 , PO 43 - , NO 3 Určete částici, která se ve vodném roztoku nemůže projevovat jako kyselina : HPO 42 - , HCOO- , H 2 S , NH 4+
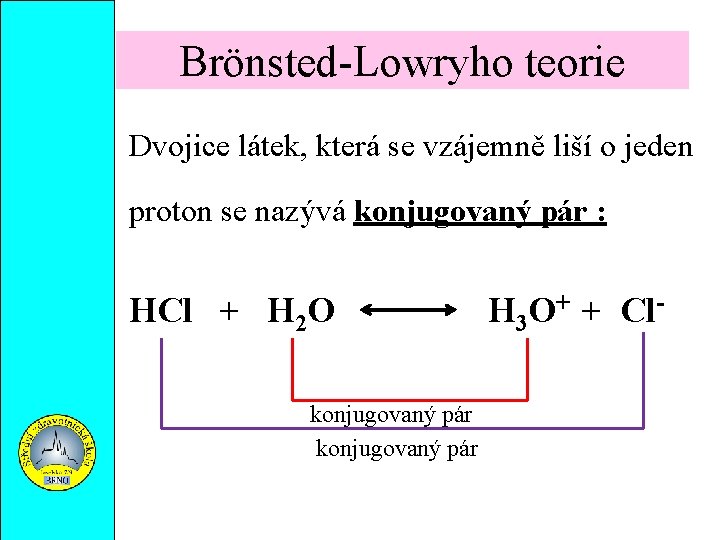
Brönsted-Lowryho teorie Dvojice látek, která se vzájemně liší o jeden proton se nazývá konjugovaný pár : HCl + H 2 O konjugovaný pár H 3 O+ + Cl
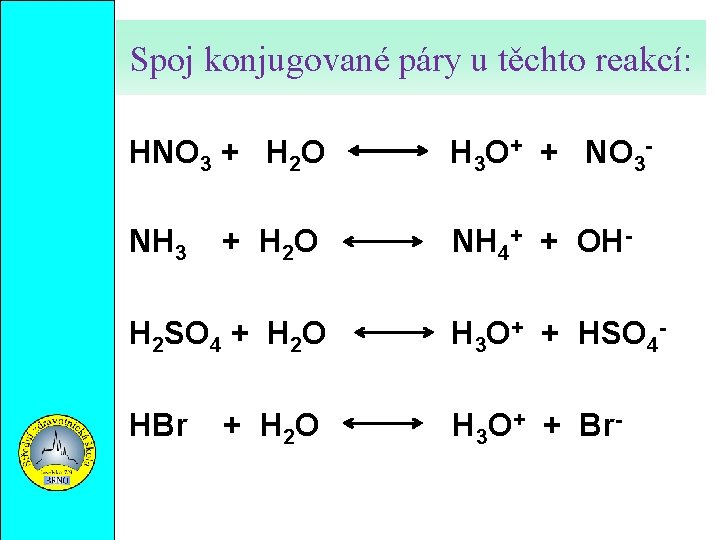
Spoj konjugované páry u těchto reakcí: HNO 3 + H 2 O H 3 O+ + NO 3 NH 3 NH 4+ + OH + H 2 O H 2 SO 4 + H 2 O H 3 O+ + HSO 4 HBr H 3 O+ + Br + H 2 O

K předání protonu může dojít i mezi molekulami rozpouštědla. Rozpouštědlo se chová jako kyselina i jako zásada. Toto chování nazýváme amfoterní charakter a tomuto ději říkáme autoprotolýza H 2 O + H 2 O H 3 O+ + OH NH 3 + NH 3 NH 4+ + NH 2
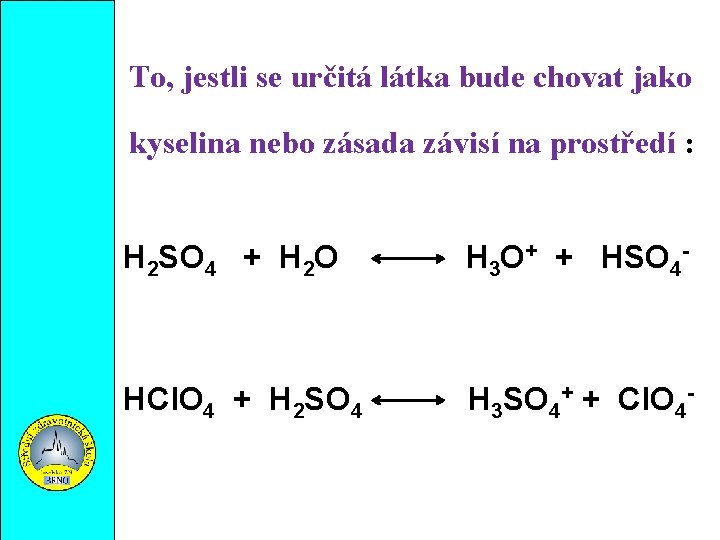
To, jestli se určitá látka bude chovat jako kyselina nebo zásada závisí na prostředí : H 2 SO 4 + H 2 O H 3 O+ + HSO 4 HCl. O 4 + H 2 SO 4 H 3 SO 4+ + Cl. O 4

Síla kyselin a zásad • Kyselina je tím silnější, čím snadněji odštěpuje proton. • Sílu kyseliny můžeme kvantitativně popsat pomocí konstanty acidity KA HB + H 2 O KA = [H 3 O+]. [B ] [ HB] H 3 O + + B

Síla kyselin a zásad • Zásada je tím silnější, čím snadněji váže proton • Sílu zásady můžeme kvantitativně vyjádřit pomocí konstanty bazicity KB Z+ + OH ZOH [ Z+]. [ OH ] KB = [ ZOH]
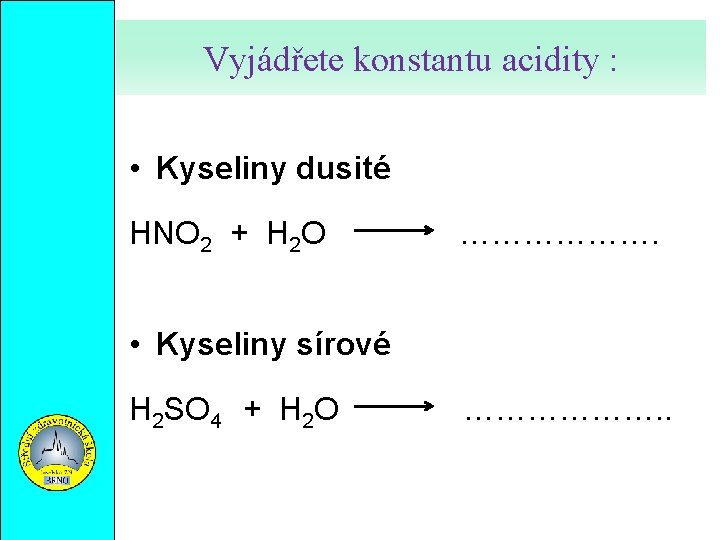
Vyjádřete konstantu acidity : • Kyseliny dusité HNO 2 + H 2 O ………………. • Kyseliny sírové H 2 SO 4 + H 2 O ………………. .

Použitá literatura MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia: 1. díl. 3. , přeprac. vyd. Olomouc: Nakladatelství Olomouc, 1998, 240 s. ISBN 80 -7182 -055 -51. MAREČEK, Aleš a Jaroslav HONZA. Chemie: sbírka příkladů pro studenty středních škol. Vyd. 1. Brno: Proton, 2001, 146 s. ISBN 80 -902 -4022 -4.
- Slides: 16