Die Brennstoffzelle Energie der Zukunft Christina Clemens Thomas

Die Brennstoffzelle Energie der Zukunft? Christina Clemens, Thomas Arand

Übersicht Geschichte ¢ Aufbau ¢ Chemie ¢ Verschiedene Arten der Brennstoffzelle ¢ Anwendungen in der Praxis ¢ Zukunft ¢

Geschichte ¢ Vor mehr als 160 Jahren entdeckte der Engländer William R. Grove das Prinzip der Brennstoffzelle. Erst in den vergangenen Jahrzehnten erlebt die Brennstoffzelle als "neue" Technik eine Renaissance.

Aufbau der Brennstoffzelle ¢ Das bekannteste Beispiel für eine Brennstoffzelle ist die mit Wasserstoff und Sauerstoff betriebene Wasserstoff -Sauerstoff-BZ (Polymer Elektrolyt Brennstoffzelle (PEM), PEM-BZ. Sie gehört zu den Niedertemperatur-BZ.
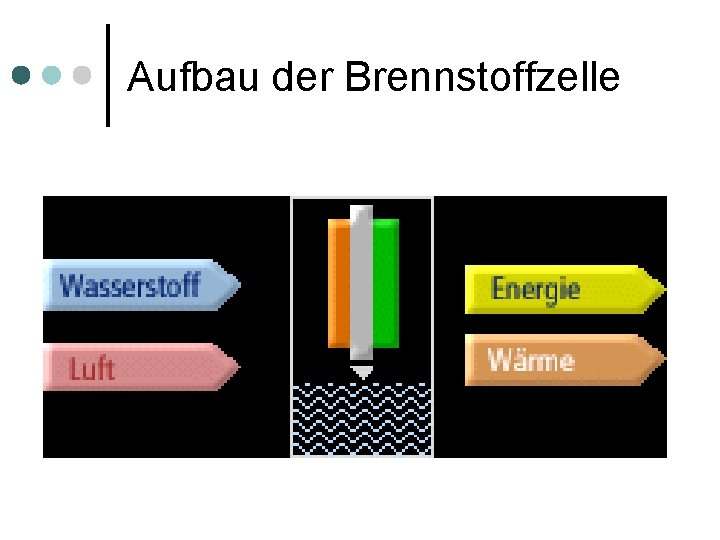
Aufbau der Brennstoffzelle
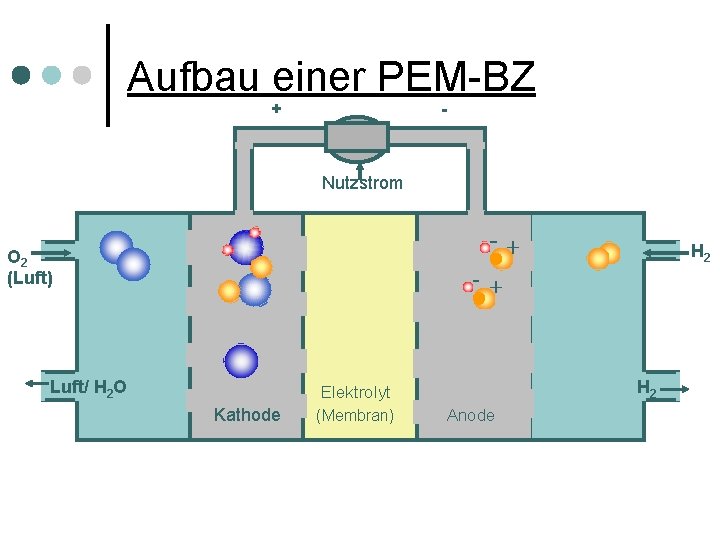
Aufbau einer PEM-BZ + - Nutzstrom H 2 O 2 (Luft) Luft/ H 2 O H 2 Elektrolyt Kathode (Membran) Anode

Chemie am Beispiel der PEM Bei einer PEM-Brennstoffzelle wird ein edelmetallhaltiger Katalysator eingesetzt, meistens handelt es sich hierbei um Platin. Mit Nafion als Membranmaterial. ¢ Erst die Zufuhr der Aktivierungsenergie, z. B. durch einen Funken, lässt die Reaktion ablaufen. ¢ Die hierbei stattfindende Aufladung der Elektroden bezeichnet man als Elektrodenpotential. ¢

Chemie am Beispiel der PEM ¢ Theoretisch lässt sich an einer PEM-Brennstoffzelle eine Ruhespannung von 1, 23 V messen. E = E 0(Kathode) - E 0 (Anode) U = E 0 (Sauerstoff) - E 0 (Wasserstoff) = 1, 23 V - 0 V = 1, 23 V. ¢ Anode: 2 H 2(g) 4 H+ + 4 e¢ ¢ Kathode: O 2(g) +4 H+ + 4 e- 2 O 2 - ¢ Gesamtreaktion: 2 H 2(g) + O 2(g) 2 H 2 O(g) ¢ Die Brennstoffzelle kann je nach Typ und Brennstoff einen theoretischen Wirkungsgrad von 70% bis ca. 100% erreichen Tatsächliche Wirkungsgrad liegt zwischen 20% und 70%. ¢
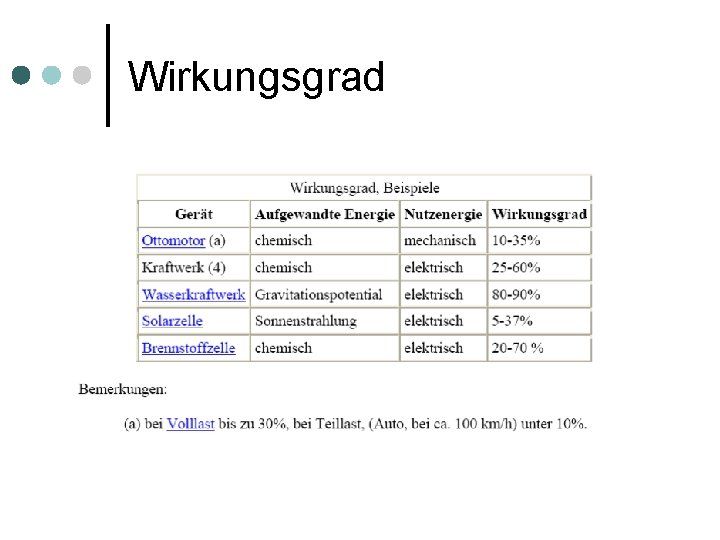
Wirkungsgrad

Verschiedene Arten der Brennstoffzelle ¢ Polymer Elektrolyt Brennstoffzelle (PEM) ( Polymer Electrolyte Fuel Cell) ¢ Alkalische Brennstoffzelle (AFC) (Alkaline Fuel Cell) ¢ Phosphorsäure Brennstoffzelle (PAFC) (Phosphoric Acid Fuel Cell) ¢ Schmelzkarbonat Brennstoffzelle (MCFC) (Molten Carbonate Fuel Cell) ¢ Oxidkeramische Brennstoffzelle ( SOFC) (Solid Oxide Fuel Cell) ¢ Direkt Methanol Brennstoffzelle (DMFC) (Direct Methanol Fuel Cell)

Alkalische Brennstoffzelle (AFC)

Alkalische Brennstoffzelle (AFC) ¢ Die in zwei Kreisläufen getrennten Gase Sauerstoff und Wasserstoff wandern vom Gasraum in den Katalysator. ¢ Die Wasserstoffmoleküle werden durch den Katalysator gespalten. ¢ Die Elektronen fließen von der Anode zur Kathode und bewirken einen elektrischen Stromfluß. ¢ Jeweils vier Elektronen an der Kathode rekombinieren mit einem Sauerstoffmolekül. ¢ Die entstandenen Sauerstoff-Ionen reagieren mit Wasser zu OH- -Ionen. ¢ Die Hydroxid-Ionen wandern durch den Elektrolyten (Kalilauge) zur Anode. ¢ Die Hydroxidionen reagieren an der Anode mit den Protonen zu Wasser. Ein Teil des entstandenen Wassers wird wieder an die Kathode transportiert, wo es für eine weitere Reaktion zur Verfügung steht.

Anwendung der AFC ¢ Alkalische Brennstoffzellen wurden in der bemannten Raumfahrt eingesetzt, die ohne die Brennstoffzellen nicht möglich gewesen wäre. Im Skylab und in den Space Shuttles wurden bzw. werden alkalische Brennstoffzellen eingesetzt. ¢ AFCs wurden auch für den Einsatz als Fahrzeugantrieb erprobt. Allerdings besteht hier der Nachteil, dass die AFC nicht mit Luft direkt betrieben werden kann. ¢ Dies ist ein genereller Nachteil der AFC. Das in der Luft enthaltene Kohlendioxid ist vorher zu entfernen, um eine "Vergiftung" des Elektrolyten zu vermeiden. Dies erfordert einen zusätzlichen technischen Aufwand. ¢ Mit reinem Sauerstoff betrieben verfügt die AFC allerdings über eine sehr gute Haltbarkeit, was sie insbesondere für Nischenanwendungen qualifiziert.

Phosphorsäure Brennstoffzelle (PAFC)

Phosphorsaure Brennstoffzelle (PAFC) Auch bei dieser Brennstoffzelle werden die Gase getrennt in den Katalysator gegeben ¢ Die Protonen wandern durch den Elektrolyten ¢ Die Sauerstoff-Ionen geben ihre negativen Ladungen an die Protonen ab und oxidieren zu Wasser ¢

Anwendung PAFC ¢ ¢ Die PAFC wird ausschließlich für die Kraft. Wärme-Kopplung eingesetzt. Die PAFC war die erste kommerziell verfügbare Brennstoffzelle. In Einheiten mit einer elektrischen Leistung von 200 k. W und einer thermischen Leistung von 220 k. W wurde sie von der amerikanischen Firma ONSI angeboten. Bisher wurden weltweit rund 200 PAFC-Anlagen installiert.

Schmelzkarbonat-Brennstoffzelle (MCFC)

Schmelzkarbonat-Brennstoffzelle (MCFC) ¢ ¢ Der Sauerstoff und das Kohlendioxid an der Kathode und Wasserstoff an der Anode - wandern vom Gasraum in den Katalysator. Die Sauerstoff-Ionen reagieren mit Kohlendioxid zu Karbonat-Ionen. Die Karbonat-Ionen wandern durch den Elektrolyten (Salzschmelze) zu den Protonen Die Karbonat-Ionen geben Ladungen an zwei Protonen ab und oxidieren mit diesen zu Wasser. Durch die Abspaltung der Sauerstoff-Ionen vom Karbonat entsteht wieder Kohlendioxid.

Anwendung MCFC ¢ ¢ Schmelzkarbonat-Brennstoffzellen werden für den stationären Einsatz entwickelt eignen sich besonders für die Kraft-Wärme-Kopplung in industriellen und gewerblichen Anwendungen, wo hohe Temperaturen benötigt werden (Prozesswärme) ¢ Es werden Anlagen im Leistungsbereich von 300 k. W entwickelt, aber auch größere Leistungen von mehreren Megawatt sind möglich ¢ Neben diesen stationären Anwendungen werden auch Schiffsantriebe auf der Basis von MCFCs entwickelt.

Oxidkeramische Brennstoffzelle (SOFC)

Oxidkeramische Brennstoffzelle (SOFC) ¢ ¢ ¢ Die in zwei Kreisläufen getrennten Gase Sauerstoff und Wasserstoff wandern vom Gasraum in den Katalysator Die nun entstandenen Sauerstoff-Ionen wandern durch den Elektrolyten (Yttriumdotiertes Zirkondioxid)) zur Anodenseite Die Sauerstoff-Ionen geben ihre beiden negativen Ladungen an zwei Protonen ab und oxidieren mit diesen zu Wasser

Anwendung SOFC ¢ ¢ ¢ Festoxid-Brennstoffzellen sind sowohl für stationäre als auch für mobile Anwendungen geeignet. Stationäre Anlagen zur Kraft-Wärme-Kopplung werden sowohl für Ein- und Mehrfamilienhäuser als auch für große Gebäude und gewerbliche oder industrielle Anwendungen entwickelt. Die Wärme kann auf einem hohen Temperaturniveau entnommen und als Prozesswärme genutzt werden. Daneben werden kleine Kraftwerke auf der Basis der SOFC entwickelt. Hier wird die Abwärme zur Stromerzeugung in Gasturbinen genutzt. Solche Kraftwerke sollen zukünftig Wirkungsgrade von 70% erreichen können. Im mobilen Bereich werden SOFCs bisher nicht für den Fahrzeugantrieb entwickelt, sondern als Ersatz für die Fahrzeugbatterie. Der Grund liegt zum einen in der ständig steigenden Anzahl von elektrischen Verbrauchern im Auto, und zum anderen in der Möglichkeit, auch bei abgeschaltetem Motor über lange Zeit Strom zur Verfügung zu haben. Als Betriebsmittel dient Benzin, das vor der Brennstoffzelle einem technisch einfachen Reformer und einer Entschwefelung zugeführt werden muss.

Direkt-Methanol-Brennstoffzelle (DMFC)

Direkt-Methanol-Brennstoffzelle (DMFC) ¢ ¢ ¢ Die getrennten Gase Sauerstoff Methanol und Wasser, wandern vom Gasraum in den Katalysator. Das Methanol reagiert mit dem Wasser zu Kohlendioxid und Wasserstoff. Die Protonen wandern durch den Elektrolyten (Protonenleitende Polymer-Elektrolyt-Membran) zur Kathode Jeweils vier Elektronen an der Kathode rekombinieren mit einem Sauerstoffmolekül. Die entstandenen Sauerstoff-Ion reagieren mit den Protonen zu Wasser.

Anwendung DMFC ¢ ¢ Die Direktmethanol-Brennstoffzelle wird derzeit für kleine, tragbare Anwendungen entwickelt. Die Toxizität von Methanol erfordert ein sehr sicheres Speichersystem in Form von Patronen oder Kartuschen. Da derzeit weltweit intensiv an der DMFC entwickelt wird, ist in den nächsten Jahren mit einer breiten Markteinführung zu rechnen. Insbesondere im Bereich der mobilen Computer, wo die Akkulaufzeit weiterhin die größte Einschränkung bedeutet. Mit einer Methanol-Patrone rechnet man mit einer bis zu fünffachen Laufzeit gegenüber Akkus und der Wechsel der Patrone geschieht in Sekunden. Kaufen kann man bereits DMFC Systeme für den Campingbereich und für industrielle Notebooks. Insbesondere japanische Hersteller wollen in den nächsten 2 -3 Jahren mit sehr kompakten Systemen auf dem Markt sein. Für den Einsatz im Mobiltelefon ist noch ein weiter Schritt in der Miniaturisierung notwendig. Bis dieser erfolgt ist, gibt es zumindest so genannte Power-Packs, mit denen lassen sich Akkus z. B. auch von Digitalkameras unterwegs nachladen.

Anwendung in der Praxis In Krefeld wird der Energiebedarf einer ganzen Siedlung mit Brennstoffzellen gedeckt ¢ Dies ist ein europaweit einzigartiges Projekt ¢

Entwicklungsstand ¢ Vorteile Hoher Wirkungsgrad bei Voll- und (je nach Anwendung) bei Teillast der Brennstoffzelle; Gute Regelbarkeit; Hohe Stromkennzahl; Gute Leistungsstaffelung durch modularen Aufbau; Geringer zu erwartender Wartungsaufwand; Geringe Schadstoffund Lärmemissionen; Hohes Entwicklungspotenzial ¢ Nachteile Hoher Investitionsaufwand; Wenig Betriebserfahrungen; Fehlender Nachweis hoher Lebensdauer; Wenig Anbieter ¢ Die genannten Nachteile dürften allerdings zukünftig aufgrund weiterer Entwicklungsfortschritte an Bedeutung verlieren. Vor allem bei den Investitionskosten wird mit einem deutlichen Rückgang zu rechnen sein, wenn die Systeme technisch optimiert sind und größere Stückzahlen produziert werden können

Ausblick ¢ Was wird die Zukunft bringen? ¢ Werden auch aus ökologischer Sicht immer wichtiger

Quellen www. die-brennstoffzelle. de ¢ www. innovation-brennstoffzelle. de ¢ www. brennstoffzelle-nrw. de ¢
- Slides: 29