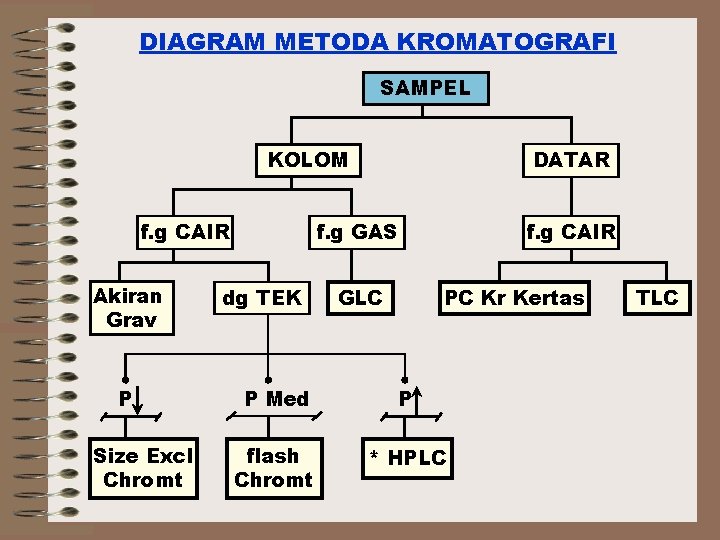
DIAGRAM METODA KROMATOGRAFI SAMPEL KOLOM f g CAIR


























![Signal A B t t 1 [ ] A B t 2 B Jarak Signal A B t t 1 [ ] A B t 2 B Jarak](https://slidetodoc.com/presentation_image_h/2eba1dedbbc78b827573bc15f3e05e79/image-33.jpg)


























































- Slides: 115

DIAGRAM METODA KROMATOGRAFI SAMPEL KOLOM f. g CAIR Akiran Grav P Size Excl Chromt DATAR f. g GAS dg TEK GLC f. g CAIR PC Kr Kertas P Med P flash Chromt * HPLC TLC

Group Ion Excl HPCL Basa Kuat CH 2 N(CH 3)3, Cl. Med Basa N(CH 3)3, Cl. Basa Lmh NH(R)2, Cl. Asam Kuat SO 3 -, H+ Med Asam HPO 3 -, Na+ Excl Chromt LC berdasar pemisahan/per perbedaan dimensi molekul. Contoh kompl camp protein dan estrogen BM beda, dpt dipisahkan dg Chromatografi

KROMATOGRAFI salah satu cara pemisahan dengan dasar analisis menggunakan : Dua Fasa F. Tetap (Stationary) F. Gerak (Mobile) ~ F. Cair Pemisahan tergantung pada gerakan relatif dua fasa tersebut. Dari sifat-sifat kedua fasa Kromatografi dapat digolongkan :

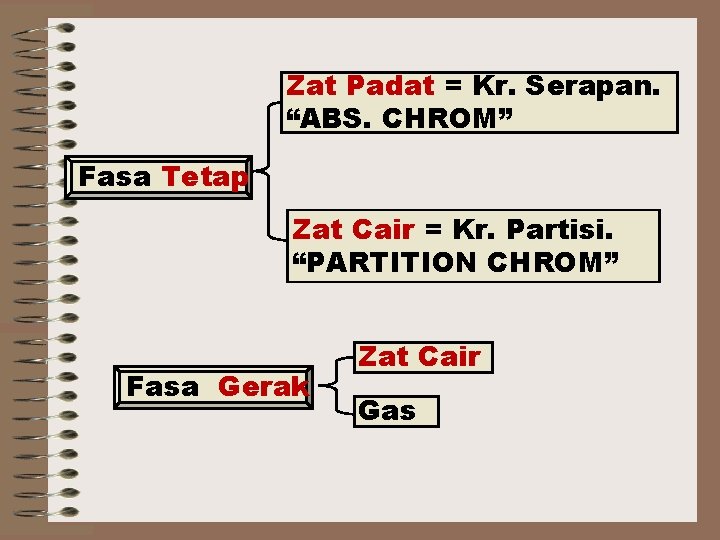
Zat Padat = Kr. Serapan. “ABS. CHROM” Fasa Tetap Zat Cair = Kr. Partisi. “PARTITION CHROM” Fasa Gerak Zat Cair Gas

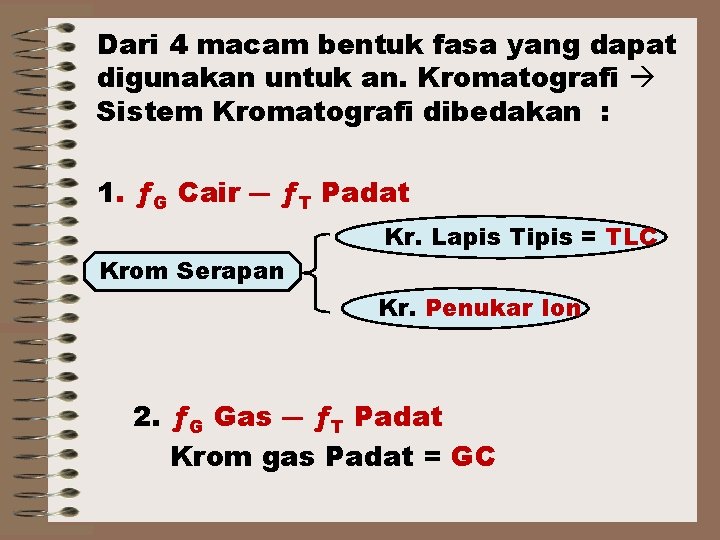
Dari 4 macam bentuk fasa yang dapat digunakan untuk an. Kromatografi Sistem Kromatografi dibedakan : 1. ƒG Cair ― ƒT Padat Kr. Lapis Tipis = TLC Krom Serapan Kr. Penukar Ion 2. ƒG Gas ― ƒT Padat Krom gas Padat = GC

3. ƒG Cair ― ƒT Cair Krom Partisis Krom Kertas 4. ƒG Gas ― ƒT Cair Krom. Gas Cair = GLC Krom. Kolom Kapiler. Semua pemisahan dg kromatografi tgt pada kenyataan bahwa senyawa-senyawa yang dipisahkan, terdistribusi sendiri diantara fasa-fasa gerak dan tetap dalam perbandingan yang sangat berbeda-beda satu sama lain.

KROMATOGRAFI SERAPAN ƒT = Zat padat berfungsi sebagai adsorben ƒG = Zat cair Permukaan partikel padat biasanya lebih aktif daripada bagian dalam. Yang pada umumnya dikatakan mempunyai “aktivitas permukaan” = “Survace Activity”. Bila partikel dimasukkan dalam larutan permukaan partikel mempunyai daya tarik baik terhadap zat larut atau pelarutnya.

Daya tarik / absorbsi dalam bentuk : Ø Ø Elektrostastik (Ionik) Daya tarik dua dipol Antara dipol dan dipol induksi Kekuatan Vander Waals Partikel padat yang mempunyai aktivitas permukaan dalam kromatografi dinamakan “Adsorben”.

KESEIMBANGAN ADSORBSI Bila larutan mengalir melalui permukaan aktif terjadi proses adsorbsi dan desorbsi. Hubungan antara konsentrasi zat yang ada dalam larutan (CM) dan yang teradsorbsi (CS) terlukis sebagai berikut : Cm A Cs Bentuk (A) bentuk konveks, terjadi karena adanya variasi aktivitas dari permukaan yang ada. Hubungan demikian sering dinamakan “Freunddlich Isotherm” yang terjadi umumnya pada sistem padat – cair.

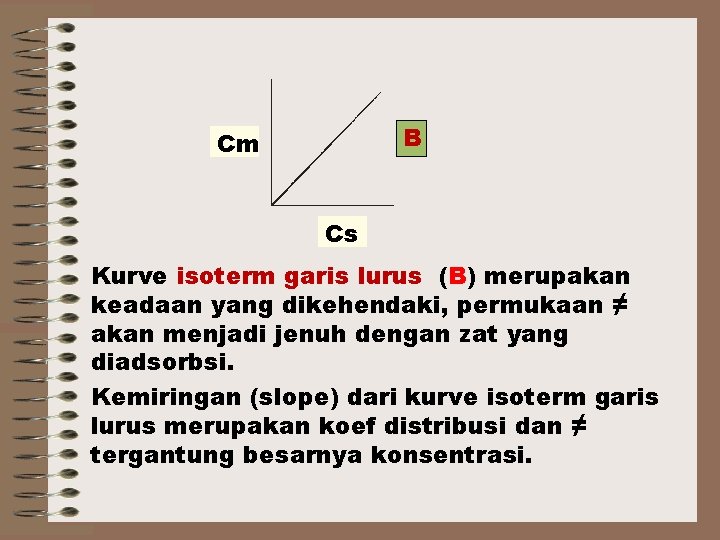
B Cm Cs Kurve isoterm garis lurus (B) merupakan keadaan yang dikehendaki, permukaan ≠ akan menjadi jenuh dengan zat yang diadsorbsi. Kemiringan (slope) dari kurve isoterm garis lurus merupakan koef distribusi dan ≠ tergantung besarnya konsentrasi.

C Cm Cs Kurve isoterm bentuk konkaf (bentuk C) dihasilkan dari reaksi yang terjadi sedemikian sehingga menyebabkan mempercepat proses adsorbsi secara keseluruhan.

Ketiga macam perbedaan proses adsorbsi menyebabkan terjadinya distorsi puncak yang dihasilkan. Respon Konveks Lurus Konkaf Puncak bentuk condong (Tailing) biasanya diakibatkan adsorben terlalu aktif. Hal ini dpt dikurangi *) menutup sisi aktif dengan zat lain *)menaikkan suhu, *) me(-) banyaknya sampel yang akan dipisahkan.

ADSORBEN Alumina dan silika gel. merupakan dua adsorben yang paling populair penggunaannya. Contoh : urutan absorben sesuai kemampuan adsorbsi 1. 2. 3. 4. Alumina Charcoal / Arang Silika Gel Magnesia 5. 6. 7. 8. Kalium Karbonat Sukrosa Starch / Pati Serbuk Selulosa Aktivitas permukaan setiap adsorben berbeda. Perlakuan pendahuluan menurut cara-cara yang ditentukan dapat menghilangkan perbedaan aktivitas tersebut.

Contoh : Daya adsorbsi alumina, dapat diatur dengan mengatur kandungan air. Alumina ---- 3600 C / 5 jam, ----- , dibiarkan menyerap air sampai kadar tertentu yang dinyatakan dalam skala “Brockmann”. Alumina berkadar air 3% mempunyai aktifitas yang umum digunakan. Luas permukaan alumina 150 m 2/g, kadar air cukup 5% untuk pelapisannya.

Silika gel yang memp luas permukaan 500 m 2/g tetapi mempunyai aktivitas kimia lebih kecil, banyak digunakan untuk pemisahan senyawa organik yang peka terhadap perubahan-perubahan karena aktivitas permukaan yang mempunyai sifat katalik. Hubungan skala Brockmann dan kadar air alumina Skala Brockmann I II IV V % Kadar Air 1 3 6 10 15

ZAT PELARUT *) Zat pelarut mempunyai peranan penting dalam Elusi yang dapat menentukan baikburuknya pemisahan. *) Zat pelarut yang mampu menjalankan Elusi terlalu cepat ≠ akan mampu memisahkan secara sempurna. *) Elusi yang terlalu lambat menyebabkan waktu Retensi lama. Sebaiknya zat pelarut ≠ tergantung dari kekuatan elusinya. Kekuatan zat elusi : daya penyerapan pada penyerap (zat pengisi) kolom.

Penyabab Ke Polaran Alumina Silika Gel. Kekuatan Penyerap Kekuatan penyerapan dg me polaritas zat yang diserap. Menurut TRAPPE, kekuatan elusi dari deretan pelarut dalam kolom dg silika gel, Air Murni Metanol Etanol Propanol Aseton Etil Asetat Dietil Eter Kloroform Metilenia Cl Benzana Toluena Trikloretilen Karbon Tetra Cl Sikloheksan Heksan.

Menurut Williams pelarut-pelarut dalam kolom menggunakan “carbon aktif” untuk pemisahan asam-asam amino dan sakarida dalam larutan : Adalah : Etil Asetat , Dietil Eter , Propanol , Aseton , Etanol , Metanol , Air Murni . Catatan pelarut harus betul-betul murni. Pipet Kertas Saring Gambar Penanganan Cuplikan

PENGISIAN DAN CARA KERJA KOLOM Pengisian kolom harus dikerjakan dengan seragam. *) Penyeragaman kepadatan dalam kolom dengan vibrator atau planger, *)atau adsorben dimasukkan ke dalam kolom dalam bentuk bubur (Slurry) dan partikelnya dibiarkan me. Pengisian ≠seragam menimbulkan rongga di tengah-tengah kolom. Bagian dasar / bawah dan atas dari isian kolom diberi glasswool atau sintered glass disc untuk menyangga isian.

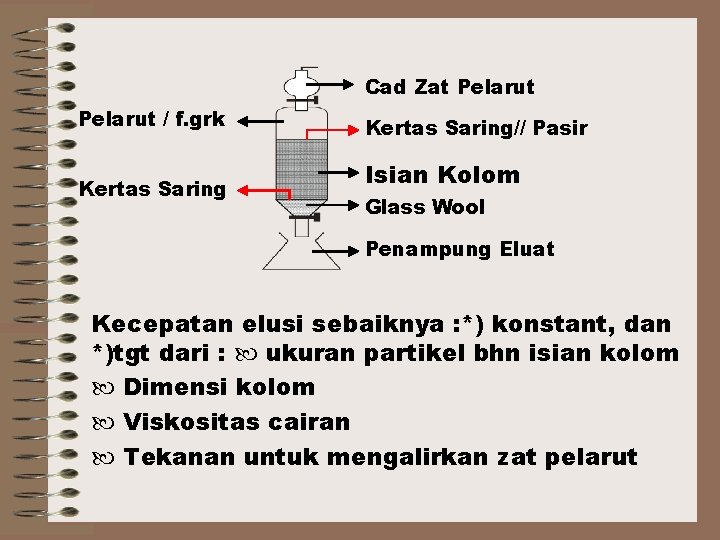
Cad Zat Pelarut / f. grk Kertas Saring// Pasir Isian Kolom Glass Wool Penampung Eluat Kecepatan elusi sebaiknya : *) konstant, dan *)tgt dari : ukuran partikel bhn isian kolom Dimensi kolom Viskositas cairan Tekanan untuk mengalirkan zat pelarut

PENANGANAN CUPLIKAN Memasukkan cuplikan dari atas kolom merupakan hal yang sangat penting Cuplikan harus rata Dlm keadaan larutan yg sepekat mungkin? ? ? Dicegah terjadinya penggoncangan kolom Untuk mendapatkan permukaan rata permukaan penyerap / bahan isian diberi kertas saring atau pasir yang bersih hingga membentuk lapisan tipis.

Pemasukan cuplikan melalui pipet kecil – ujung pipet ditempelkan pada dinding kolom. Selama zat cair lepas dari pipet, ujung pipet digerakkan berkeliling dalam kolom, dan diupayakan ≠ menyentuh penyerap / bahan isian. Cuplikan yang tertinggal dalam dinding kolom dicuci dengan cara yang sama menggunakan pelarut murni. Bila semua cuplikan telah turun ke bagian bahan penyerap, bahan pelarut / ƒG dapat dimasukkan melalui corong pisah.

Kromatografi Partisi ƒG Cair ƒT Cair Dlm kromatografi ini fasa tetap / stasioner ≠ berupa zat padat tetapi cairan. Fasa geraknya juga berupa cairan ~ HPLC “High Performance Liquid Chromatography”. = Liq-liq Partition Chromatogra phy Zat yang dilarutkan akan terdistribusi dg sendirinya diantara 2 fasa zat cair

Dan sesuai dengan koef partisinya. Perbedaan koef partisi dari berbagai komponen campuran dapat dipisahkan. Keuntungan kromatografi partisi dengan adsorbsi, karena : - Daya ulangnya lebih baik - Dari data kelarutan, hasil dapat diramalkan - Koef distribusi konstant dalam jangka [ ] yang agak luas dapat menghasilkan puncak yang simetris lebih tajam

Keunggulan “HPLC” 1. Dapat menangani senyawa-2 yang stabilitas terhadap suhu dan volatilitasnya terbatas, bila tanpa menggunakan derivatisasi. Contoh : analisis beberapa jenis gula, dg HPLC tanpa derivatisasi 2. t pemisahan singkat 5 – 10 menit untuk satu sampel. 3. Dapat digunakan untuk anal. Kuantitatif dg presisi yang cukup tinggi. 4. Merup teknisi analisis yg peka, mempunyai resolusi yang baik untuk pemisahan senyw serupa.

Efisiensi maksimal dapat dicapai dg *) mengatur kecepatan aliran fasa gerak yang kecil, sehingga analisis memakan waktu yang lama. Untuk menanggulangi hal ini perlu diperhatikan : *) Me P aliran ƒ gerak *) Me(-)jarak tempuh zat yg dianalisis *) dlm proses partisi, dg menggunakan bahan isian atau penyangga (Packing Material)

Bahan isian sebagai penyangga harus inert thd senyawa-2 yang akan dipisahkan. f. T (stasr). Berupa cairan yang dilapiskan pada permukaan bahan penyangga (Packing Material). Ikatan antara bahan penyangga dg ƒT , dapat berupa ikatan fisik maupun kimiawi. Dua tipe bahan isian yang ada dipasaran Pellicular Beads dan Microporous Prarticle. Pellicula Beads terdiri dari bagian dalam yg padat, ≠ berpori, biasanya dari bahan silika, kulit luar tipis bersifat porous, dg ketebalan 1/30 – 1/40 dari bagian dalam. Besar partikel keseluruhan 40 . m.

Kelemahan tipe ini luar permukaan dari kulit yang berpori 1 -25 m 2/g jarang dipakai Microporous Particle / Mikropartikel Ukuran antara 3 -10 . m memberikan luas permukaan besar antara 200 -300 m 2/g Efisiensi tinggi karena plat teoritis dapat mencapai 10. 000 dalam kolom sepanjang 25 cm. Kromatografi partisi cair - cair ƒT dan ƒG harus ≠ bercampur.

Pelarut lebih polar digunakan sebagai ƒStat sistem dinamakan Krom Fase Normal. Contoh : Air sebagai ƒT yang melapisi silika gel secara tipis. Air ter-ads. 50% dari berat silika gel. kadang-2 dipakai sistem buffer. Untuk menghasilkan t. R yang diharapkan jumlah fraksi terlarut dalam ƒG berkisar 0, 05 – 0, 5. Bila ƒT dipakai senyawa non polar, dan ƒG polar merupakan kebalikan fase normal. “Reverse Phase Chromatography” untuk ini penyangga padat yang non polar dapat digunakan bubuk karet dengan lapis tipis benzen sebagai ƒT dan air sebagai ƒG.

SUSUNAN PERALATAN Pada HPLC dan GLC ≠ jauh berbeda. Komponen utama : Reservoir pelarut untuk fase gerak Pompa untuk mengalirkan fase gerak / mobile dg kecepatan dan tekanan tetap Injector untuk memasukkan sampel Ada 2 macam On Coloum Injection / Langsung Holding Loop Injection / ≠ langsung

Kolom Detector : D. Ultraviolet D. Fluoresens D. Konduktivitas D. Indeks Refraksi D. FID. “Flame Ionitation Detector”. Recorder

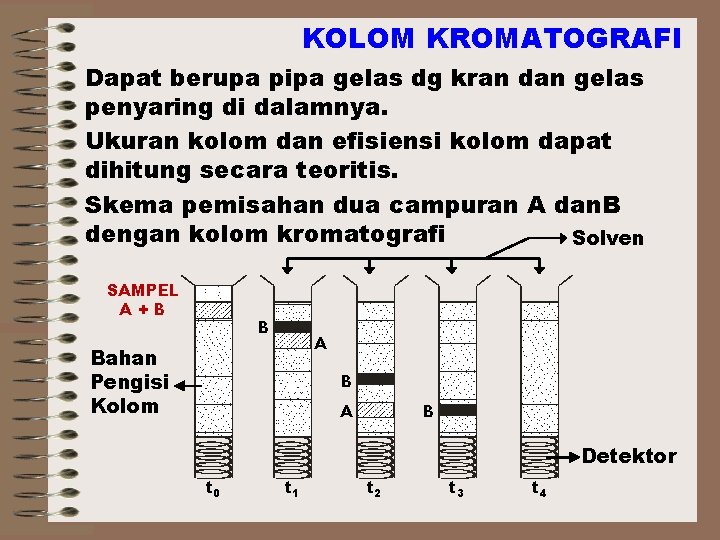
KOLOM KROMATOGRAFI Dapat berupa pipa gelas dg kran dan gelas penyaring di dalamnya. Ukuran kolom dan efisiensi kolom dapat dihitung secara teoritis. Skema pemisahan dua campuran A dan. B dengan kolom kromatografi Solven SAMPEL A+B B A Bahan Pengisi Kolom B A B Detektor t 0 t 1 t 2 t 3 t 4
![Signal A B t t 1 A B t 2 B Jarak Signal A B t t 1 [ ] A B t 2 B Jarak](https://slidetodoc.com/presentation_image_h/2eba1dedbbc78b827573bc15f3e05e79/image-33.jpg)
Signal A B t t 1 [ ] A B t 2 B Jarak Migrasi A

KESEIMBANGAN DISTRIBUSI Perbedaan migrasi merup hsl distribusi keseimbangan dr senyawa A, B, C, … diantara f. Tdan f. G. Distribusi molekul cuplikan antara dua fasa dinyatakan dlm tetapan keseimbangan dikenal sbg koef Distr atau partisi = KD 1 CS = Kadar senyawa dlm f. T (Diam), (fo) CM = Kadar senyawa dlm f. G (Mobil), (fa)

K, meliputi berbagai macam mekanisme tgt sifat-2 fasa dan interaksi cuplikan dengan setiap fasa. Proses : Penukaran ion Serapan Partisi Harga K merupakan populasi relatif Senyawa dlm 2 fasa k populasi CS CM Mol cuplikan akan tinggal lebih lama di ƒSts = ƒo

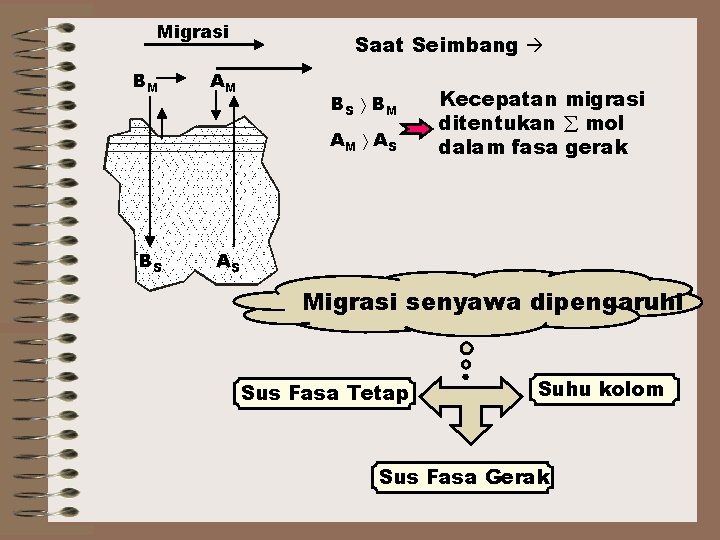
Migrasi BM AM Saat Seimbang BS B M AM A S BS Kecepatan migrasi ditentukan mol dalam fasa gerak AS Migrasi senyawa dipengaruhi Sus Fasa Tetap Suhu kolom Sus Fasa Gerak

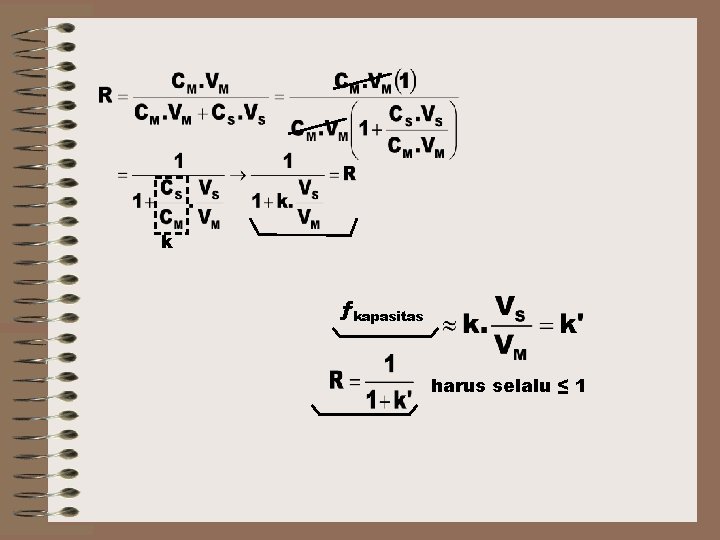
Sebagai dasar retensi Keseimbangan dinamik sebenarnya yang ada 2 3 faktor kapasitas yang setara dengan CS. VS / CM. VM

k ƒkapasitas harus selalu ≤ 1

4 Harus selalu ≤ 1, karena k’≥ 0, maka kecepatan solut tidak pernah lebih besar dari kecepatan ƒM Ciri khas kedua pemisahan kromatografi penyebaran Mol yang menyebabkan perbedaan puncak kromatogram. Molekul-molekul membentuk garis sempit ~ luas puncak awal.

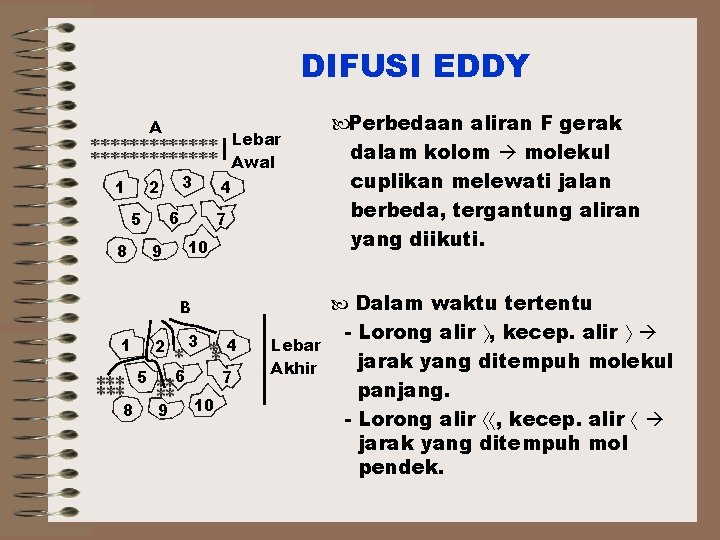
DIFUSI EDDY A 1 3 2 4 6 5 8 Lebar Awal 7 10 9 Dalam waktu tertentu B 1 6 5 8 3 2 9 Perbedaan aliran F gerak dalam kolom molekul cuplikan melewati jalan berbeda, tergantung aliran yang diikuti. 4 7 10 Lebar Akhir - Lorong alir , kecep. alir jarak yang ditempuh molekul panjang. - Lorong alir , kecep. alir jarak yang ditempuh mol pendek.

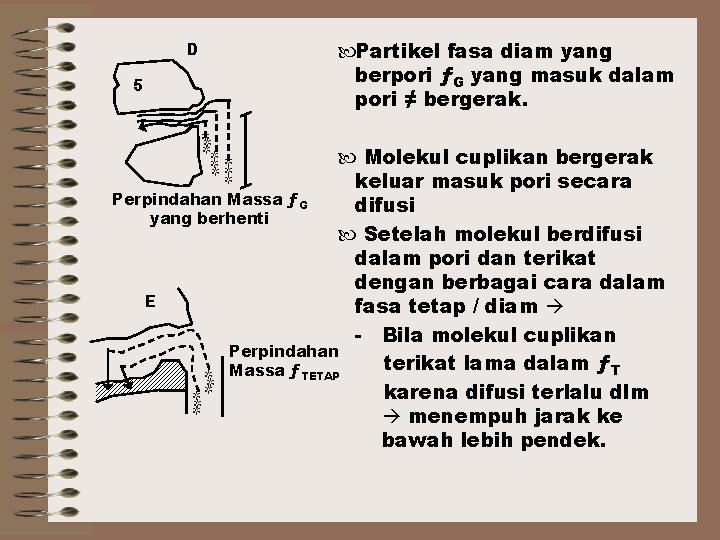
Perpindahan massa ƒG berhubungan dg perbedaan kecepatan alir setiap bagian 1 2 dari suatu lorong. ƒG berdekatan dg partikel, 5 akan bergerak lambat / ≠ Perpindahan bergerak. Massa ƒG ditengah aliran bergerak lebih cepat dlm rentang waktu tertentu ~ molekul cuplikan dekat partikel menempuh jarak lebih pendek. ~ molekul cuplikan di tengah aliran menempuh jarak lebih panjang. C

D 5 Partikel fasa diam yang berpori ƒG yang masuk dalam pori ≠ bergerak. Molekul cuplikan bergerak keluar masuk pori secara Perpindahan Massa ƒG difusi yang berhenti Setelah molekul berdifusi dalam pori dan terikat dengan berbagai cara dalam E fasa tetap / diam - Bila molekul cuplikan Perpindahan terikat lama dalam ƒT Massa ƒTETAP karena difusi terlalu dlm menempuh jarak ke bawah lebih pendek.

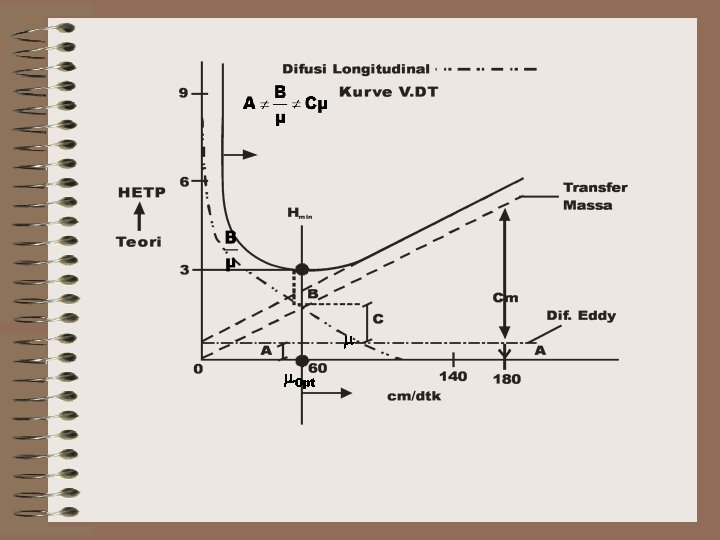
TEORI KELAJUAN / KECEPATAN Dikembangkan oleh “Van Deemter” orang Belanda Pers Van Deemter 5 Pers ini berguna untuk meningkat kan peranan kolom kromatografi efisiensi kolom. diukur dengan :

A = Difusi Eddy / Dif. Olakan B = Difusi Longitudinal C = Transfer. Massa = Kecepatan aliran ƒG dlm kolom (cm/dtk)

Opt

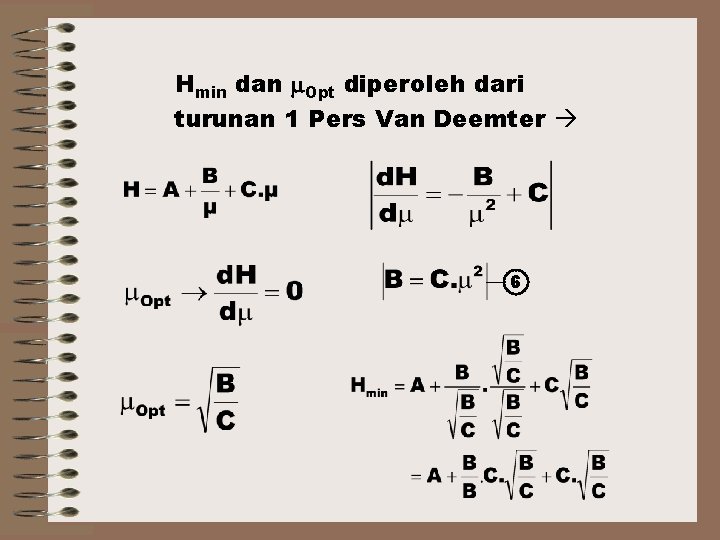
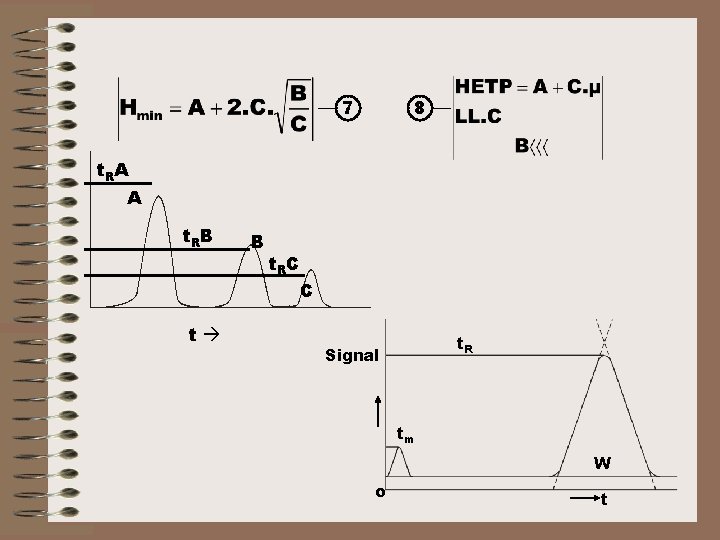
Hmin dan Opt diperoleh dari turunan 1 Pers Van Deemter 6

8 7 t. RA A t. RB B t. RC C t t. R Signal tm W o t

Ciri Khas Kurve / Peak. Kromatogram • Setiap senyawa meninggalkan kolom dalam bentuk simetri, sebagai kurve gaus • Setiap puncak keluar dlm waktu tertentu, yang dapat dipakai sebagai identifikasi senyawa t. R = waktu retensi diukur mulai waktu injeksi cuplikan waktu puncak maksimum meninggalkan kolom • Perbedaan waktu retensi t. R berdekatan. Semakin besar ∆t. R dari campuran semakin mudah dipisahkan

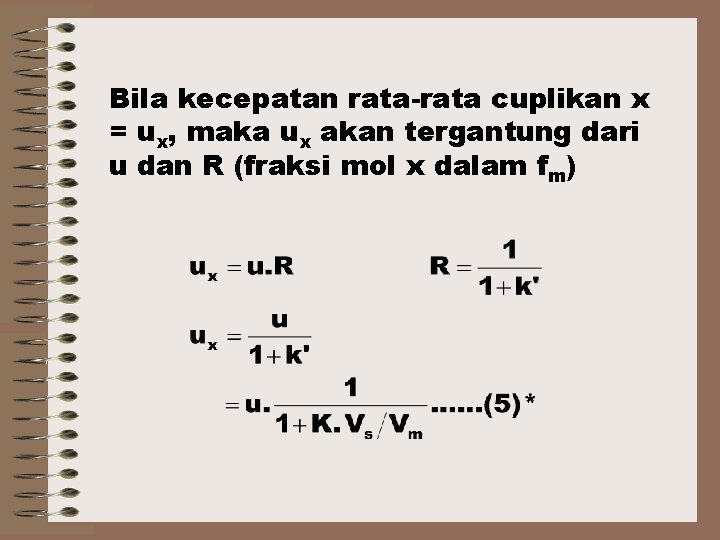
RETENSI Jika kecpt aliran ƒG dlm kolom μ cm/dtk kecepatan rata-rata cuplikan x = μx tgt dari μ dan R (Fraksi Mol X dalam ƒG )

Hub : μ , t. R dan panjang kolom L. (cm) t. R = waktu retensi waktu yang diperlukan fraksi solut bermigrasi sepanjang lintasan kolom

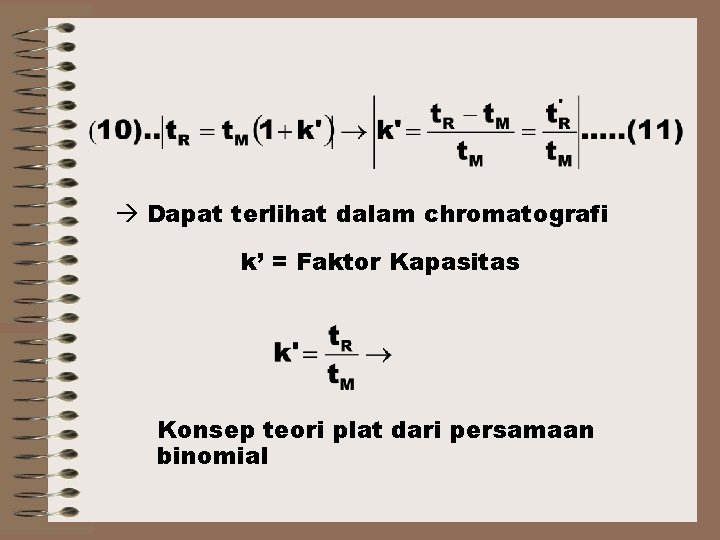
Dapat terlihat dalam chromatografi k’ = Faktor Kapasitas Konsep teori plat dari persamaan binomial

Retensi kadang-kadang diukur dengan satuan Volume VR Vol total ƒG yang diperlukan untuk mengelusi puncak senyawa x. VR = t. R x kecepatan alir ƒG melalui kolom F = ml/dtk VR = t. R. F Vol Total ƒG dalam kolom VM = t. M. F VR lebih disenangi dari t. R karena t. R berubah dengan berubahnya kecep. alir (F, μ), sedang VR tidak tergantung pada (F, μ). μ = cm/dtk

Konsep Teori Lempeng / Plat Teori lempeng plat, perlu untukmenerangkan proses terjadinya suatu pemisahan secara kromatografi. Karena proses yang terjadi pada kromatografi anlog dengan proses ekstraksi bertingkat yang dilakukan oleh Craig. Dimana fasa diam dalam kromatografi dianggap terdiri dari sejumlah ruang yang mempunyai ukuran sama dan tiap ruang mengandung sejumlah fasa mobil dan fasa diam. Dengan teori ekspansi binomial, distribusi sampel dalam ruang dinyatakan dalam rumus.

Distribusi sampel dlm ruang tersebut merupakan fungsi dari koef distribusi (KD). Perbandingan volume pelarut yang digunakan (Vs / Vm) dan jumlah pemindahan atau transfer (n). Teori plat dapat menggambarkan kecepatan migrasi secara kuantitatif tetapi tidak dapat menerangkan bagaimana terjadinya pelebaran pik. Sehingga teori tersebut dilengkapi dengan teori kinetik / teori kecepatan. sampel.

Fraksi waktu tinggal dalam fasa gerak, sbg dasar RETENSI dinyatakan dlm pers 2, 3, 4 Fraksi waktu tinggal dalam fasa mobil sama dengan jumlah molekul dalam fasa mobil dibagi dengan jumlah total molekul dalam sampel Fraksi dlm fasa gerak (R) = k’ = K. Vs/Vm …. . (3)* faktor kapasitas setara Cs. Vs/Cm. Vm Besaran-besaran dlm kromatografi

WAKTU RETENSI Apabila kecepatan alir fm (u, cm/dtk) diatur tetap, t tetap, perbandingan fasa diam dan fasa mobil tetap, setiap komponen dalam suatu sampel akan mempunyai waktu tinggal yang tetap, yaitu waktu yang diperlukan oleh suatu komponen untuk melintasi suatu fasa diam dengan panjang L. (cm) waktu retensi (t. R)

Bila kecepatan rata-rata cuplikan x = ux, maka ux akan tergantung dari u dan R (fraksi mol x dalam fm)

Hubungan u dg t. R dan panjang lintasan L(cm) tm = waktu yang diperlukan oleh fasa mobil itu sendiri (tanpa sampel) untuk keluar dari fasa diam Konsep teori lempeng / plat

FAKTOR SELEKTIFITAS = Untuk pemisahan 2 zat terlarut A, B melalui kolom kromatografi perlu diketahui faktor selektivitas A, B KB, KA adalah Koef Partisi A dan B k’ = Faktor Kapasitas Dalam eksperimen t’R t terkoreksi

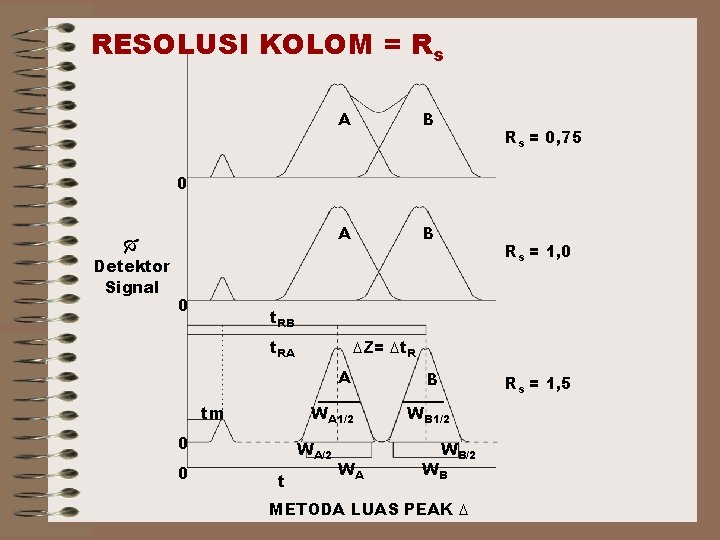
RESOLUSI KOLOM = Rs A B Rs = 0, 75 0 Detektor Signal 0 t. RB t. RA ∆Z= ∆t. R A WA 1/2 tm 0 0 Rs = 1, 0 WA/2 t WA B Rs = 1, 5 WB 1/2 WB METODA LUAS PEAK ∆

Resolusi = perubahan nyata antara dua spesies B, A dalam kolom Dari grafik resolusi terbaca 3 bentuk resolving power yang ≠ sama. Rs = 1, 5 Memisahkan A dan B secara komplit, meskipun masih ada over lap 0, 3%. ~ Resolusi Base Line Rs = 1, 0 Daerah peak B masih mengandung A 4% - 2, 5% dan sebaliknya Rs = 0, 75 A dan B belum sama sekali terpisahkan

Utk pemisahan yg baik R ≥ 1, 5 ≥ 99, 7% Pemisahan spesies dlm kromatografi erat hubungannya dengan faktor-faktor : 1. Efisiensi kolom 2. Efisiensi pelarut Eff kolom diukur sbg ∑ plat teoritis = N, Ketinggian ekivalen terhadap plat teoritis = HETP

L = Panjang Kolom dari pers. Gauss stand deviasi pengamatan Pers. Gauss = standard deviasi Peak Kromatografi

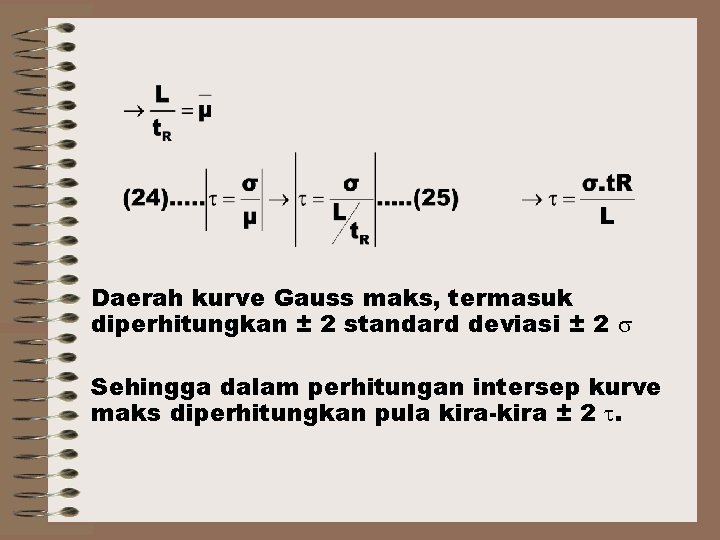
Daerah kurve Gauss maks, termasuk diperhitungkan ± 2 standard deviasi ± 2 Sehingga dalam perhitungan intersep kurve maks diperhitungkan pula kira-kira ± 2 .

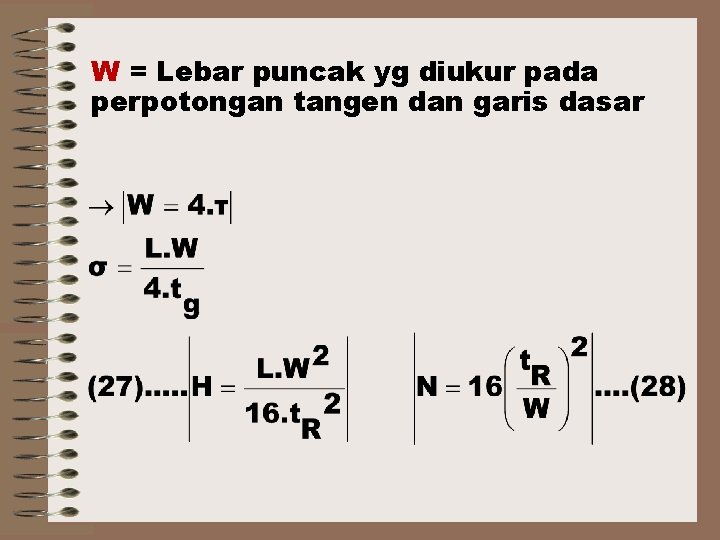
W = Lebar puncak yg diukur pada perpotongan tangen dan garis dasar

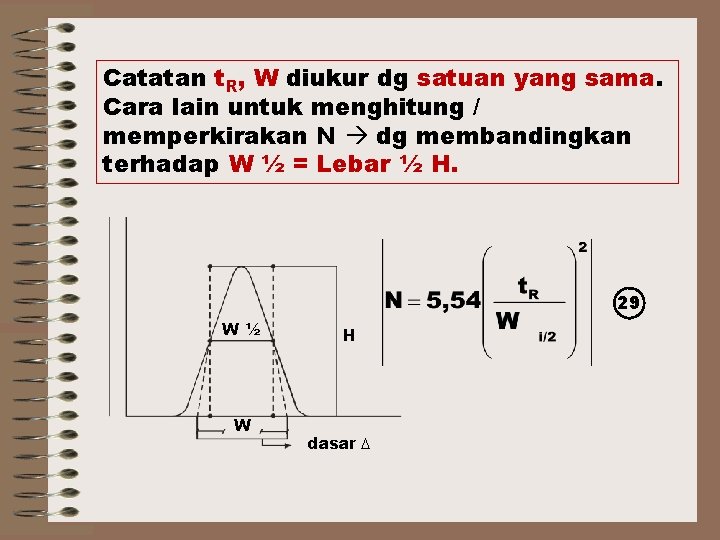
Catatan t. R, W diukur dg satuan yang sama. Cara lain untuk menghitung / memperkirakan N dg membandingkan terhadap W ½ = Lebar ½ H. 29 W½ W H dasar ∆

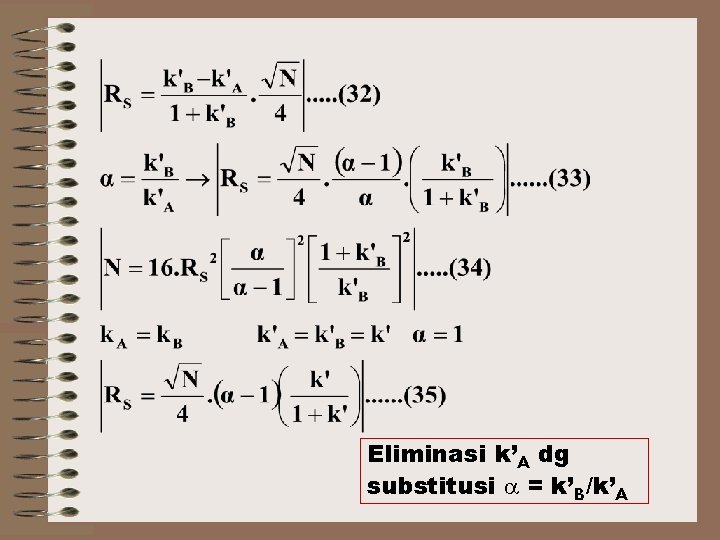
Hubungan Antara Rs dan Kolom Hub matematis antara RS, k. B, k. A, dan N. Dengan asumsi WA ≈ W∆ ≈ W Maka Pers (18) RS Pers (28) N =

Eliminasi k’A dg substitusi = k’B/k’A

Bila diasumsikan WA = WB = W

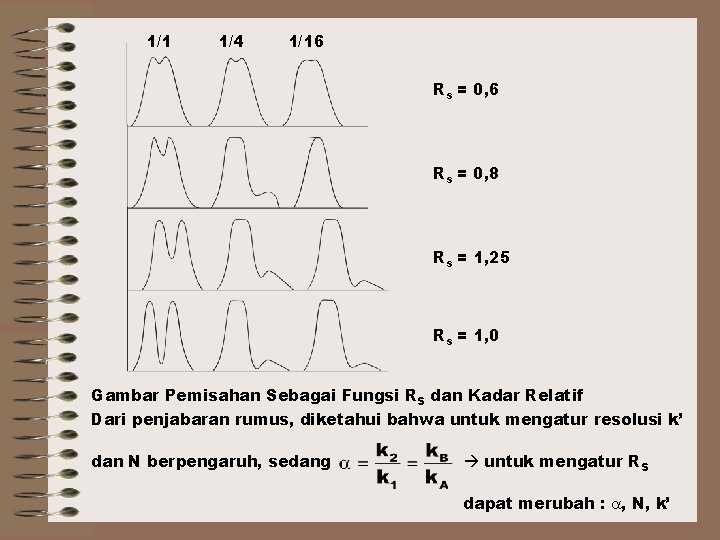
1/1 1/4 1/16 Rs = 0, 8 Rs = 1, 25 Rs = 1, 0 Gambar Pemisahan Sebagai Fungsi RS dan Kadar Relatif Dari penjabaran rumus, diketahui bahwa untuk mengatur resolusi k’ dan N berpengaruh, sedang untuk mengatur RS dapat merubah : , N, k’

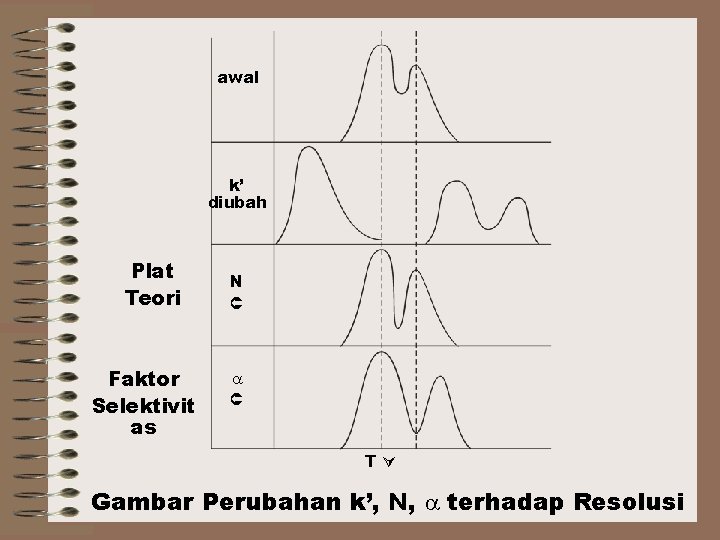
awal k’ diubah Plat Teori Faktor Selektivit as N T Gambar Perubahan k’, N, terhadap Resolusi

Dari rumus RS = i ii iii N K’ Dari pers. RS terhadap , N, k’, ternyata faktor (i), (ii), dan (iii) ≠ saling bergantung, dengan demikian dapat dioptimalkan dulu faktor (i) baru yang lain. Selektivitas pemisahan ditunjukkan faktor yang berubah dengan mengatur susunan ƒgerak dan ƒtetap. Me pergeseran satu puncak relatif terhadap lainnya. Waktu pemisahan dan tinggi dua puncak ≠ begitu berubah untuk perub yang wajar.

Efisiensi pemisahan ditunjukkan faktor (ii) = N, dengan mengubah L dan μ, N suatu kolom di , menghasilkan penyempitan dua puncak dan menaikkan tinggi puncak. Waktu pemisahan ≠ langsung dipengaruhi. Faktor (iii), k’ berubah dengan mengubah kekuatan fasa gerak. Perubahan k’ dapat berpengaruh besar pada pemisahan. k’ perubahan jelek, t. R pendek. k’ terjadi kenaikan nyata resolusi, meskipun tinggi puncak turun cepat dan waktu pemisahan naik.

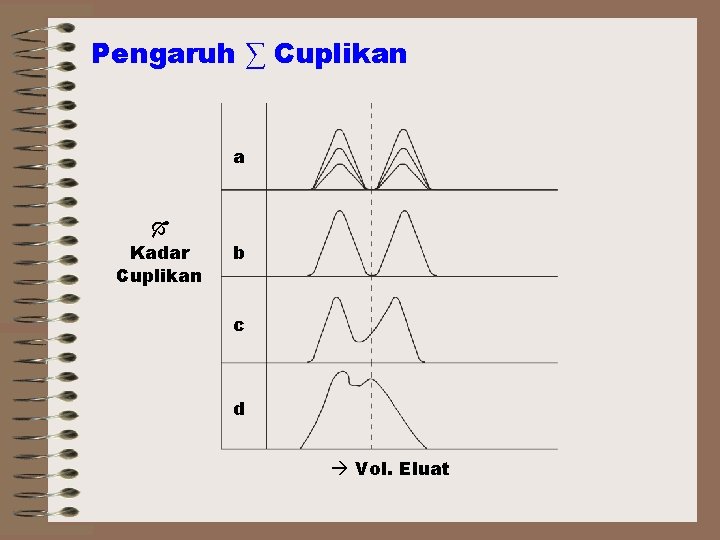
Pengaruh ∑ Cuplikan a Kadar Cuplikan b c d Vol. Eluat

Dari gambar cuplikan kromatogram terlihat / terbaca a. Cuplikan sedikit, Tinggi puncak naik dg bertambahnya cuplikan t. R ≠ dipengaruhi RS tetap b. Jumlah Cuplikan Kritik, - waktu retensi menurun c. d. Pe (+) cuplikan berlanjut, Terjadi penurunan nyata pada pemisahan dan t R. Untuk pemisahan analitik, lebih baik bekerja pada daerah dimana k’ tetap, yaitu ∑ cuplikan harus kurang dari kapasitas linear kolom.

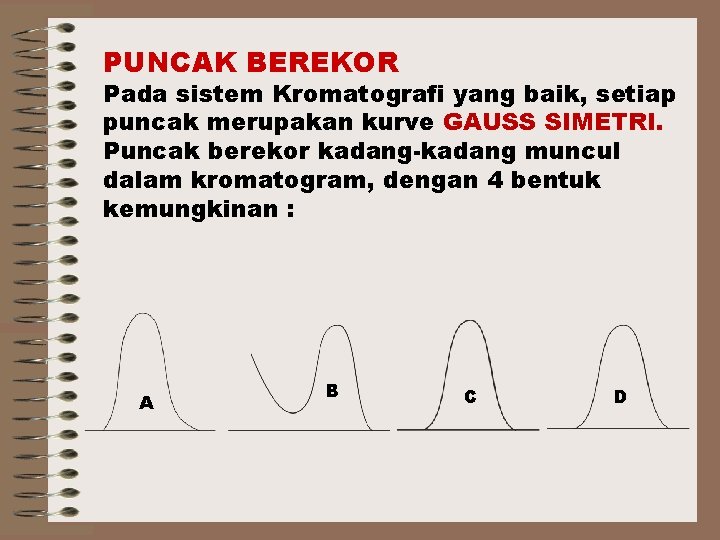
PUNCAK BEREKOR Pada sistem Kromatografi yang baik, setiap puncak merupakan kurve GAUSS SIMETRI. Puncak berekor kadang-kadang muncul dalam kromatogram, dengan 4 bentuk kemungkinan : A B C D

Bentuk A Berekor Kimia A Terjadi karena ketidak cocokan antara cuplikan dengan ƒG atau ƒT. Ditandai dengan lambat kembali ekor puncak pada garis dasar Pemisahan terhadap puncak berikutnya jadi jelek Jika terjadi puncak berekor tipe ini, perlu dicoba ƒG, ƒT yang lain atau dicoba metoda lain

Bentuk B Berekor Pelarut B Akibat dari puncak pelarut cuplikan Penggunaan cuplikan sedikit mungkin, atau menaikkan RS Bentuk C Poisson C Terjadi karena kolom kurang efisien, efisiensi kolom . Jarang terjadi pada kromatografi cairan Bentuk D Eksponansial Normal D Puncak sedikit kurang simetri dan ini biasa terjadi pada semua kromatografi

KROMATOGRAFI PLANAR Dua tipe Kromatografi Planar Thin Layer Chrom “TLC” Paper Chromatography Thin Layer Chromatography ≈ TLC ≈ KLT. Teknik ini dikembangkan oleh “EGON STAHL” dengan menghamparkan penyerap pada lempeng gelas sehingga merupakan lapisan tipis. Kromatografi Serapan KLT / TLC merup Kromatografi Partisi Karena absorben telah dilapisi air dari udara

KLT cepat populair karena memberikan banyak keuntungan : -Peralatan sederhana -Murah -Waktu analisis cepat -Daya pisah cukup baik Sebagian besar teori kolom dapat diterapkan pada KLT. Pemisahan dilakukan oleh keseimbangan berturutan cuplikan terhadap dua fasa, satu diantaranya bergerak terhadap yang lain.

Derajat retensi pada KLT dinyatakan sebagai : Jarak yg telah ditempuh pelarut dapat diukur dengan mudah dan jarak tempuh cuplikan diukur pada pusat kerapatan maksimum.

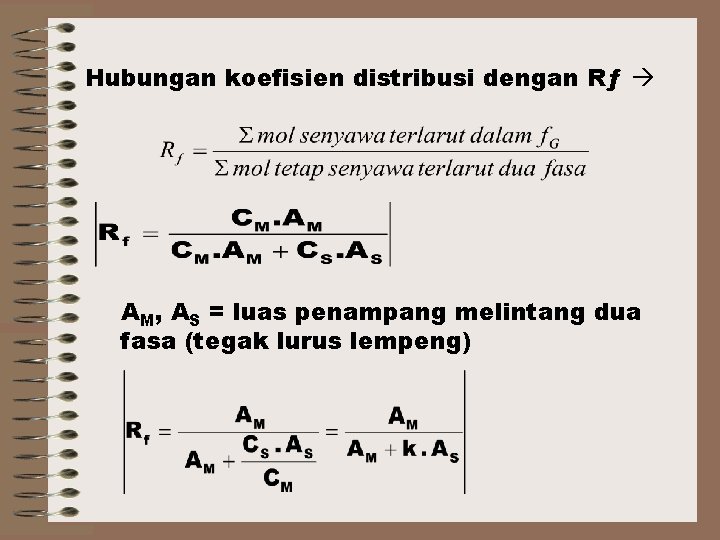
Hubungan koefisien distribusi dengan Rƒ AM, AS = luas penampang melintang dua fasa (tegak lurus lempeng)

Luas penampang melintang sukar diukur persamaan di atas kurang praktis, Rƒ merupakan bentuk modifikasi dari tetapan keseimbangan. Rƒ terbentuk dari: *macam adsorben, *ketebalan, *metoda arah pengembangan, *kadar dan jumlah cuplikan, serta *jarak yang ditempuh / noda.

Dengan melihat ketergantungan harga Rƒ akan lebih mudah dan tepat menggunakan harga Rƒ relataif atau R standard. Dimana suatu senyawa standard di (+) ke cuplikan. Harga RSTD adalah angka banding jarak tempuh dua bercak tersebut dalam waktu pengembangan yang sama.

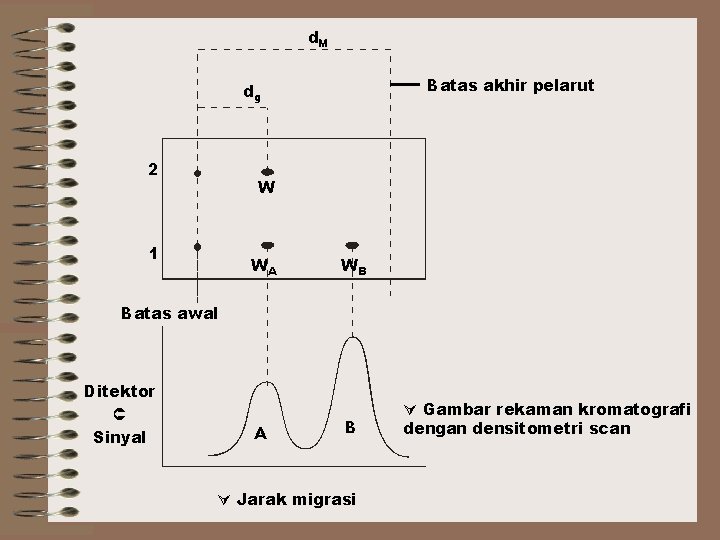
d. M Batas akhir pelarut dg 2 W 1 WA WB Batas awal Ditektor Sinyal A B Jarak migrasi Gambar rekaman kromatografi dengan densitometri scan

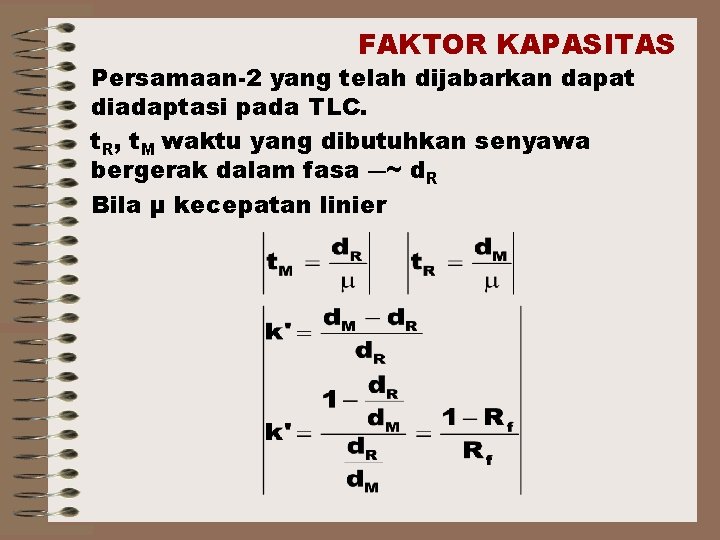
FAKTOR KAPASITAS Persamaan-2 yang telah dijabarkan dapat diadaptasi pada TLC. t. R, t. M waktu yang dibutuhkan senyawa bergerak dalam fasa ―~ d. R Bila μ kecepatan linier


Semua prosedur kromatografi, kondisi optimum untuk suatu pemisahan merupakan kecocokan antara f tetap dan f gerak. KLT / TLC fasa tetap berupa lapis tipis, pada umumnya digunakan silika gel. Untuk penggunaan dalam suatu tipe pemisahan perbedaan fasa tetap terletak pada : Struktur Pori-pori Struktur lubang

Silika gel perdagangan : Ukuran 10 - 40μ berpengaruh pada μ dan pemisahan Ukuran 20 – 1500 A Berpengaruh pd 80 – 150 = pori besar proses serapan Luas permukaan 300 – 1000 m 2/g Kelembaban relatif 45 – 75% mengikat air 7 – 20% Sangat higroskopis Deaktivasi ditentukan kelembaban relatif kamar dan penyimpanan lempeng silika gel perlu diperhatikan

Macam-macam gel di perdagangan : 1. Silika gel dg pengikat silika gel G dg pengikat - Ca. SO 4 [5 -15%] silika gel S dg pengikat - pati 2. Silika gel dg pengikat dan indikator flourisense Silika gel GF atau GF 24 Berflourisens kehijauan jika dilihat dg UV pendek. Indikator yg digunakan timah-kadmium sulfida atau mangan-timah silikat aktif. 3. Silika gel tanpa pengikat Silika gel H atau silika gel N. Lebih stabil dibanding bentuk I.

4. Silika gel tanpa pengikat dengan indikator flourisense. 5. Silika gel untuk pemisahan preparatif. Silika gel PF 254 + 366 6. Alumina dengan p. H 9, 7, 4 Dengan pengikat Cu. SO 4 7. Selulosa, sebagai fasa diam KLT diperoleh mekanisme sama pada krom. kertas Selulosa untuk KLT ada 2 bentuk : - serat asli - Monokristal Pemilihan fasa gerak pada KLT dengan silika gel / alumina sebagai ft, mengikuti aturan kromatografi serapan.

PELARUT SEMI MIKROSTOP (Menurut kenaikan sifat Hidrofob) banyak digunakan. Kloroform biasanya distabilkan dengan Etanol ) Air n. Anil Alkohol Formanida Etil Asetat Metanol Eter Asam Asetat n. Butil Asetat Etanol Kloroform )) Benzena Isopropanol Aseton Siklo Heksan n. Propanol Eter Petroleum Tert-butanol Petroleum Fenol m. Parafin n. Butanol ) Untuk pemisahan senyawa Hidrofil )) Untuk pemisahan senyawa Lipofil

METODOLOGI 1. Pembuata Lempeng Lapis Tipis Ukuran lempeng gelas yang biasa digunakan 20 x 20, 20 x 10, 20 x 5 cm Pencucian : Air (+) deterjen Keringkan - Aseton keringkan Pelapisan : 30 g bahan pelapis dibuat bubur dengan air atau pelarut lain - Pindahkan dengan segera dalam alat perata. - Ratakan bubur pada lempeng dengan ketebalan 0, 25 mm Untuk pemisahan preparatif tebal lapisan 0, 5 – 2, 0 mm. Pindahkan lempeng pada rak dengan hati -hati, diamkan ± 30 menit ------- t 100 – 1200 C ± 1 jam

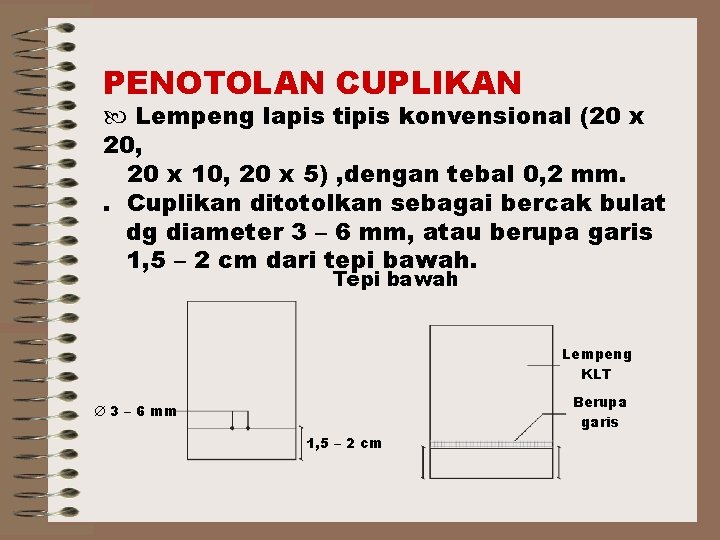
Perbandingan Bahan dan Pelarut untuk Lempeng PENOTOLAN CUPLIKAN Lempeng lapis tipis konvensional (20 x 20, 20 x 10, 20 x 5) dengan tebal 0, 2 mm. Cuplikan ditotolkan sebagai bercak bulat dengan diameter 3 – 6 mm, atau berupa garis; 1, 5 – 2 cm dari tepi bawah. Tepi bawah Lempeng KLT Berupa garis 3 – 6 mm 1, 5 – 2 cm

PENOTOLAN CUPLIKAN Lempeng lapis tipis konvensional (20 x 20, 20 x 10, 20 x 5) , dengan tebal 0, 2 mm. . Cuplikan ditotolkan sebagai bercak bulat dg diameter 3 – 6 mm, atau berupa garis 1, 5 – 2 cm dari tepi bawah. Tepi bawah Lempeng KLT Berupa garis 3 – 6 mm 1, 5 – 2 cm

• Penotolan dengan mikro pipet atau microsyringe diperlukan 1 – 20 μL. Kelebihan bahan totolan menyebabkan bercak asimetri danperubahan harga Rƒ. • HETP pada KLT biasanya 10 x 10, 10 x 20 cm. diperlukan cuplikan dalam nano pikogram setiap bercak. Diameter bercak harus tidak lebih 1, 0 – 1, 5 mm dan vol cuplikan ± 0, 2 μL.

PENGEMBANGAN KROMATOGRAM Teknik naik linier (ascending) Teknik turun / horisontal (descending) Kromatogram biasanya dikembangkan dlm bejana pengembang gelas atau logam yg tertutup dan jenuh dengan uap pelarut.

Teknik Perbaikan Pemisahan • Pengembangan Berkelanjutan ƒ gerak dialirkan pada bagian atas lempengembang. Teknik ini digunakan untuk senyawa dengan Rƒ 0, 05 – 0, 2 setelah pengembangan pertama.

Pengembangan Dua Dimensi Cuplikan ditotolkan di salah satu pojok kemudian dikembangkan seperti biasa. Kemudian diputar 900 sehingga pita pemisahan I terletak pada bagian bawah lempeng dilakukan pengembangan II sehingga terjadi pemisahan berbeda pada arah kedua. Teknik ini berguna untuk cuplikan yg mengandung banyak penyusun.

Pengembangan Serkuler Fasa gerak dialirkan dengan sumbu atau pompa melalui pipa kapiler ditengah lapisan / tetap. Senyawa terlarut bergerak dari tengah penotolan menghasilkan lingkaran sempit. Pengembangan Beberapa Kali Fasa gerak biasanya mudah menguap, diuapkan setelah terjadi pengembangan. Lempeng dikembangkan lagi dengan ƒG yang sama atau berbeda.

METODA IDENTIFIKASI Untuk melihat senyawa ≠ berwarna pada lempengembang, biasanya dilakukan metoda sebagai berikut : 1. Dengan UV (254 – 366 mm) a. Pada lap berfluorisensi (S GF 254) bercak muncul sebagai bercak hitam. b. Senyawa berfluorisensi, pd lapisan biasa bercak akan terlihat berfluorisensi.

2. Disemprot pereaksi yg menghasilkan warna atau berfluorisensi. Digunakan utk deteksi asam sulfat, (H 2 SO 4 p. , 50% H 2 SO 4 dlm Metanol). Reaksi ini terbentuk dlm keadaan dingin atau dg ----100 -1200 C - ≠ dapat digunakan pada ft organik atau sbg bahan pendukung “pati” - Pereaksi lain yg banyak igunakan uap iodium

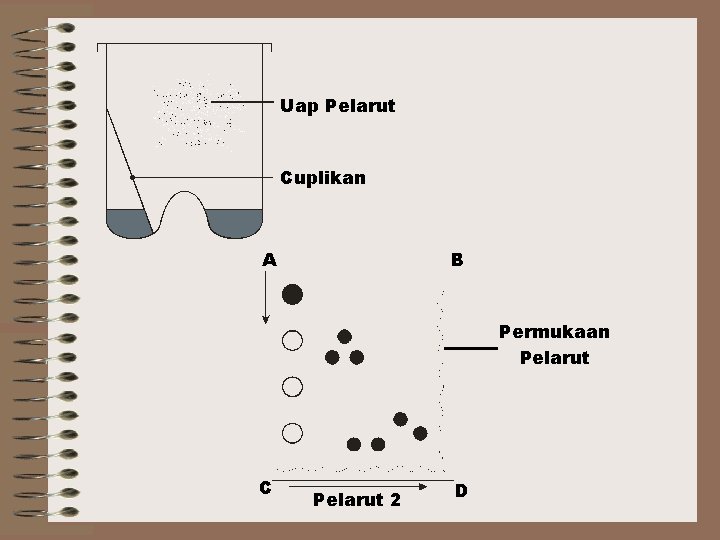
Uap Pelarut Cuplikan A B Permukaan Pelarut C Pelarut 2 D

Faktor yg mempengaruhi gerakan noda dlm KLT yang juga berpengaruh terhadap Rƒ 1. Struktur kimia senyawa yang dipisahkan. 2. Sifat adsorben dan derajat aktivitasnya. Aktivitas di kan dg pemanasan dlm oven. 3. Tebal dan kerataan lapisan penyerap. 4. Pelarut & [o kemurnian] f gerak. - Kemurnian pelarut sangat penting - Perbandingan campuran pelarut perlu diperhatikan. 5. Derajat kejenuhan uap dalam bejana pengembangan. 6. ∑ cuplikan yang digunakan Tetesan cuplikan Tendensi penyebaran noda Kesalahan harga Rƒ Terbentuknya ekor Efek kesetimbangan lain

7. Suhu, pemisahan sebaiknya pada suhu tetap Hal ini terutama untuk mencegah perubahan-perubahan dalam komposisi pelarut karena penguapan, ( perubahan fasa). 8. Kesetimbangan dalam KLT lebih penting dalam krom. kertas perlu diupayakan atmosfer dalam bejana jenuh dengan uap pelarut. Gejala atm. bejana ≠ jenuh pengembangan dengan permukaan pelarut cekung, fasa gerak bergerak lebih berat di bagian tepi . . harus dihindarkan.

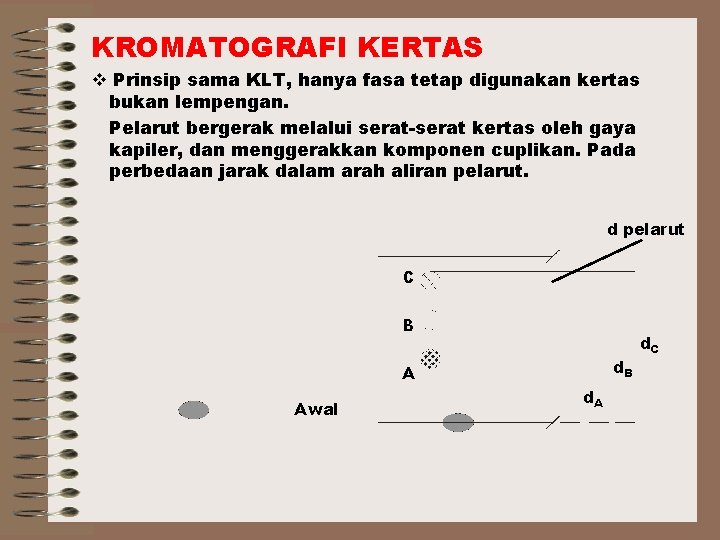
KROMATOGRAFI KERTAS Prinsip sama KLT, hanya fasa tetap digunakan kertas bukan lempengan. Pelarut bergerak melalui serat-serat kertas oleh gaya kapiler, dan menggerakkan komponen cuplikan. Pada perbedaan jarak dalam arah aliran pelarut. d pelarut C B d. B A Awal d. A d. C

Bila permukaan pelarut mulai bergerak sampai waktu tetentu/ditetapkan, kertas Diambil dan dikeringkan. Kedudukan dari permukaan pelarut dibe ri tanda. Jika senyawa campuran berwarna akan terlihat noda yang terpisah Bila tdk berwarna perlu diteksi dg UV, di Metoda identifikasi yg plg mudah dengan Berdasar kedudukan noda relatif terhadap Permukaan pelarut dg harga Rf


BEBERAPA FAKTOR PENENTU Rƒ 1. Pelarut pentingnya koefisien partisi 2. Suhu perubahan suhu merubah koefisien partisi dan kecepatan alir 3. Ukuran bejana vol. bejana mempengaruhi homogenitas atmosfer jadi mempengaruhi kecepatan penguapan komponen pelarut. 4. Kertas sesuai jenis berpengaruh thd keseimbangan partisi. 5. Sifat campuran.

APLIKASI DATA ANALISIS 1. Substan A dan B mempunyai waktu retensi t. RA = 16, 40 t. RB = 17, 63 menit pada kolom 30 cm. Lebar dasar puncak A = 1, 11 dan B = 1, 21 menit. Hitung : a. RS resolusi kolom b. N = ∑ rata-rata plate dalam kolom c. H = tinggi plate orisinil d. Panjang kolom untuk mencapai RS = 1, 5 e. Berapa waktu yang dibutuhkan untuk mengelusi B dari kolom (d) f. Berapa tinggi plate dibutuhkan untuk R S = 1, 5 pada kolom orisinil 30 cm dan waktu orisinil

Penyelesaian :

d. k’ dan ≠ berubah dengan kenaikan N ataupun L substitusikan N 1 dan N 2 pada persamaan :

Elusi B dalam kolom ( ) dengan RS = 1, 5 membutuhkan waktu 35 menit.

f. Dari persamaan (e) H 1 dan H 2 disubstitusikan H 1 = H orisinil H 2 = H baru untuk mencapai RS = 1, 5 dg L. t. R. orisinil

2. KLT dipakai untuk memisahkan campuran 3 carbamate insektisida 1) Carbofuran 2) Carbaryl 3 3) Metalkamate 2 Sampel 5 μL larutan mengandung 1 1 mg/m. L setiap komponen dalam CHCl 3 Fasa gerak toluen / isoprophyl ether 70% / 30%. KLT 20 x 20 cm Cuplikan ditotolkan sebelah kanan KLT Standard dari 3 komponen sebelah kiri KLT Dari pengamatan dengan ukuran cm diperoleh data : d. M = 9, 8 d. R)1 = 1, 7 W 1 = 0, 57 d. R)2 = 2, 5 W 2 = 0, 54 Hitung : d. R)3 = 3, 9 W 3 = 0, 75 a. Rƒ untuk ketiga carbamate b. Tinggi plate untuk setiap spot (noda)