Diagnostico Virolgico HIV HCV HBV en Dilisis Interpretacin

Diagnostico Virológico HIV, HCV, HBV en Diálisis. Interpretación de test Diagnósticos de Screening Dra. Noemí del Pino | Diagnobio Laboratorio | Congreso Argentino de Nefrología 2005 Pto. Iguazú - Misiones

Población a estudiar : DIALISIS – Los pacientes con insuficiencia renal crónico presentan alteraciones en la respuesta inmune tanto especifica como inespecífica. – La hemodiálisis aumenta la exposición del paciente a: • Materiales biocompatibles (membranas) • Endotoxinas • Sustancias en el líquidos de diálisis (inductoras de citoquinas) – Los reactantes de fase aguda están aumentados en pacientes de HD, considerados crónicamente inflamados. – Recientemente se publicó un genotipo de la IL 10 asociada a la baja producción de citoquinas por los monocitos, se correlaciona con la ausencia de respuesta a la vacuna de la Hepatitis B en HD. (Inmunology 2003).

Los pacientes de HD son considerados población de riesgo, por lo que se recomienda testeo periódico para: HCV HBV HIV

Toma de muestras para test de Screening • Pueden ser procesados en Suero o Plasma. • Interferencias propias de las muestras: – Eritrocitos en suspensión. – Fibrina. – Muestras lipémicas. – Contaminación bacteriana. – Congelado y descongelado de muestras. – Muestra inactivadas.

Recomendaciones del CDC sobre los Test de Screening • No hay “standard” ni consensos para reportar los resultados en Test de Screening. (en distintas poblaciones) • Existen variaciones sustanciales en los informes entre laboratorios: – – – Seleccionar pruebas especificas y sensibles. Tomar en cuenta las limitaciones del procedimiento. Considerar los criterios de aceptación de cada Kit. Interpretación de resultados. Confirmar por métodos confirmatorios, en caso de resultados repetidamente positivos con valores de corte bajos. MMWR 2003 RECOMENDA TION AND

Característica de los Test de Screening

Elección de Test de Screening • Sensibilidad. • Especificidad. • Valor Predictivo: Expresa la probabilidad que un resultado muestre el verdadero status del paciente, pudiendo ser positivo o negativo, . • Para test con alta sensibilidad y especificidad el valor predictivo depende de la prevalencia en la población a estudiar • WHO recomienda tres criterios para la elección de los test • I (objetivo para el uso del test) • II (sensibilidad y especificidad) • III (prevalencia en la población a estudiar)
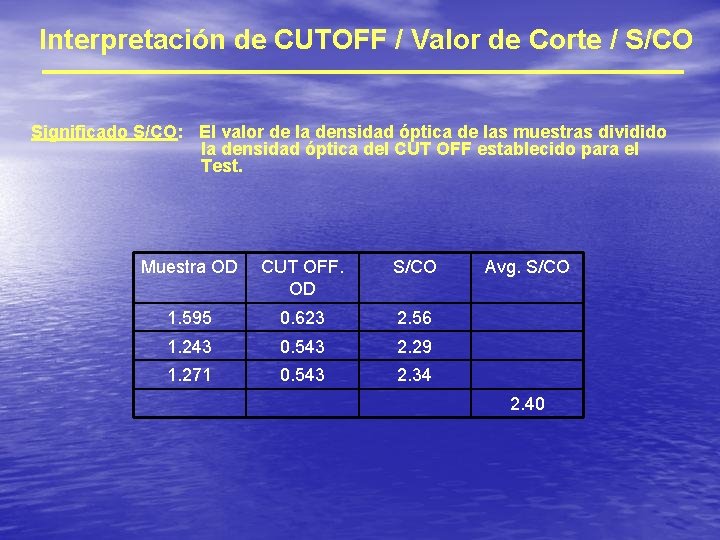
Interpretación de CUTOFF / Valor de Corte / S/CO Significado S/CO: El valor de la densidad óptica de las muestras dividido la densidad óptica del CUT OFF establecido para el Test. Muestra OD CUT OFF. OD S/CO 1. 595 0. 623 2. 56 1. 243 0. 543 2. 29 1. 271 0. 543 2. 34 Avg. S/CO 2. 40
Interpretación de S/CO según: • Consenso Argentino Hepatitis C (2004) Método Modelo de Informe: Resultado informar S/CO => 2 (Pobla. Gral. ) • CDC Evaluación de S/CO Dependiendo de la población en estudio y contexto clínico del paciente MMWR 2003; 52(No. RR-3): 1 -15.

HCV

Marcadores virales en Hepatitis C • Directos: • Indirectos: – HCV RNA – HCc. Ag – anti. HCV Ig. G – anti. HCV Ig. M SCREENING Anti HCV Confirmación + HCV RNA (cualitativo) + HCV genotipo, serotipo Pronostic. + Anti HCV (LIA, RIBA) HCV RNA (cuantitativo) Monitoreo + +
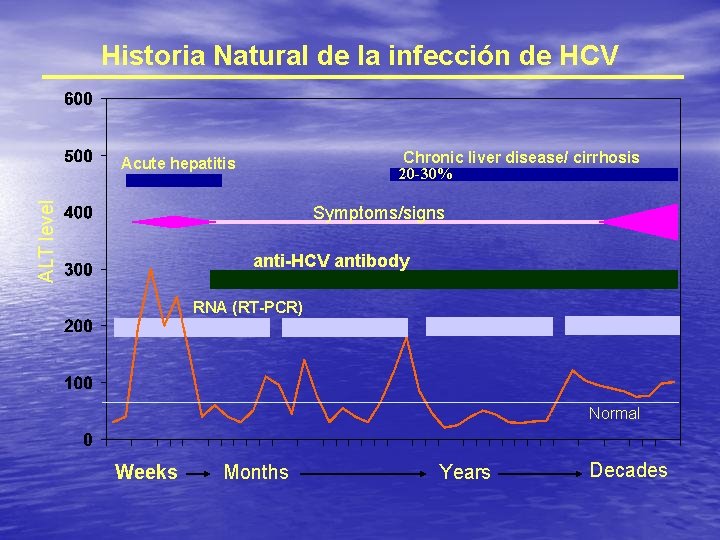
Historia Natural de la infección de HCV Chronic liver disease/ cirrhosis 20 -30% ALT level Acute hepatitis Symptoms/signs anti-HCV antibody RNA (RT-PCR) Normal Weeks Months Years Decades

Relevancia clínica de Ac anti HCV • No distingue infección aguda de crónica. • El Ac HCV core Ig. M no es marcador de HCV aguda. ( este marcador esta presente en el 50 -90% de HCV crónicos) • Los test de Screening en suero no reconocen todas las cuasiespecies de HCV No se ha identificado aún “Ac neutralizante anti. HCV”.
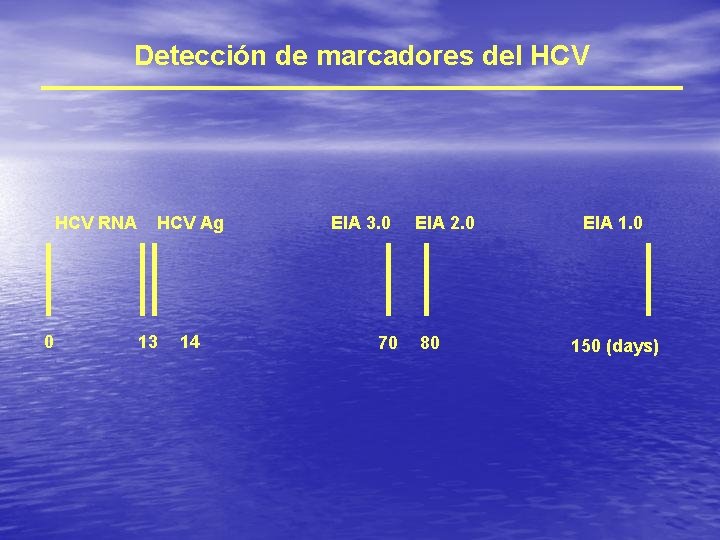
Detección de marcadores del HCV RNA 0 HCV Ag 13 14 EIA 3. 0 70 EIA 2. 0 80 EIA 1. 0 150 (days)

Enzimoinmunoensayos para la detección de anti HCV Genoma HCV Core E 1 E 2/NS 1 NS 2 NS 3 1º Gen NS 4 C-100 -3 2º Gen core NS 3 NS 4 3º Gen core NS 3 NS 4 4º Gen NS 5 Distintos sistemas de expresión CDC
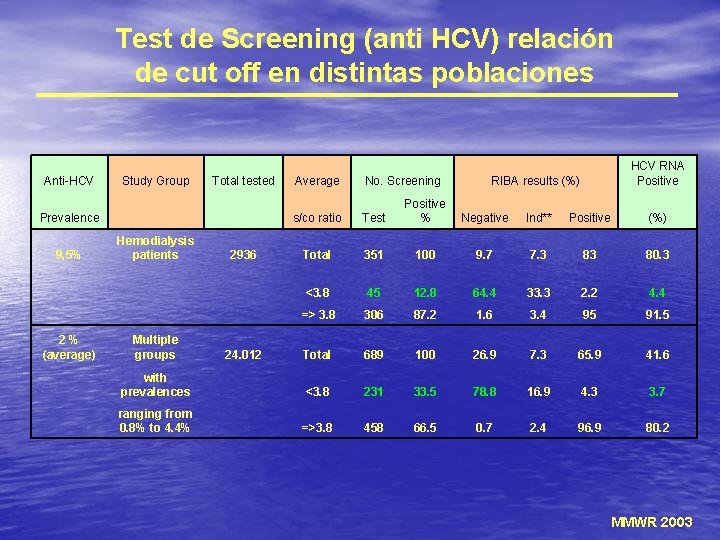
Test de Screening (anti HCV) relación de cut off en distintas poblaciones Anti-HCV Study Group Total tested Average No. Screening RIBA results (%) Positive % Negative Prevalence s/co ratio Test 9, 5% Hemodialysis patients 2936 Total 351 100 <3. 8 45 => 3. 8 2 % (average) Multiple groups 24. 012 HCV RNA Positive Ind** Positive (%) 9. 7 7. 3 83 80. 3 12. 8 64. 4 33. 3 2. 2 4. 4 306 87. 2 1. 6 3. 4 95 91. 5 Total 689 100 26. 9 7. 3 65. 9 41. 6 with prevalences <3. 8 231 33. 5 78. 8 16. 9 4. 3 3. 7 ranging from 0. 8% to 4. 4% =>3. 8 458 66. 5 0. 7 2. 4 96. 9 80. 2 MMWR 2003
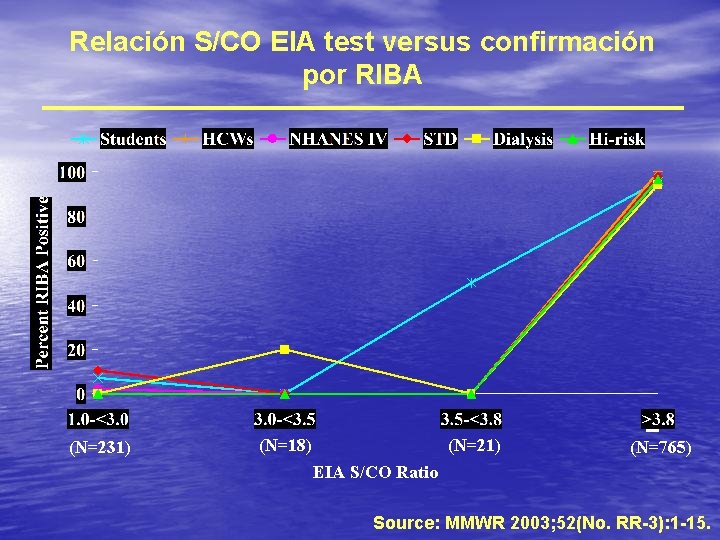
3 Relación S/CO EIA test versus confirmación por RIBA _ (N=231) (N=18) (N=21) (N=765) EIA S/CO Ratio Source: MMWR 2003; 52(No. RR-3): 1 -15.
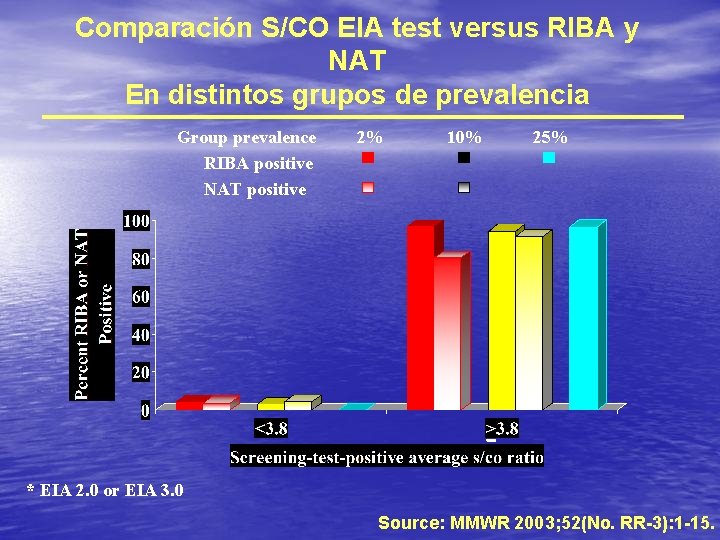
Comparación S/CO EIA test versus RIBA y NAT En distintos grupos de prevalencia Group prevalence RIBA positive NAT positive 2% 10% 25% _ * EIA 2. 0 or EIA 3. 0 Source: MMWR 2003; 52(No. RR-3): 1 -15.
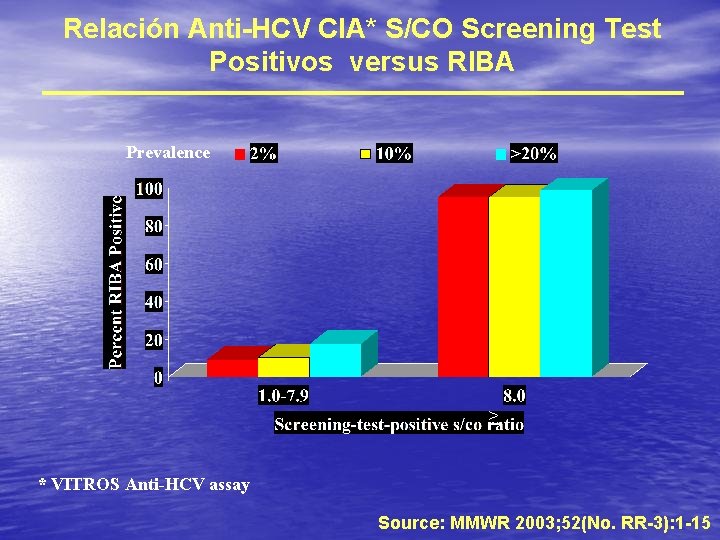
Relación Anti-HCV CIA* S/CO Screening Test Positivos versus RIBA Prevalence > * VITROS Anti-HCV assay Source: MMWR 2003; 52(No. RR-3): 1 -15

Conclusión: • De los pacientes estudiados el 12. 9 % anti HCV negativos resultaron HCV – RNA positivos. • El HCV – RNA precede al anti HCV. • La condición del estado inmunológico de los pacientes Dialisys & Transplantation 1996

HCV Falsos positivos • • Pacientes inmunocomprometidos Todo resultados anti HCV por test de Screening con bajo S/CO deben ser corroborados con un segundo test de screening y confirmados por NAT HCV Falsos negativos • • Periodos de ventana. Pacientes inmunocomprometidos. CDC
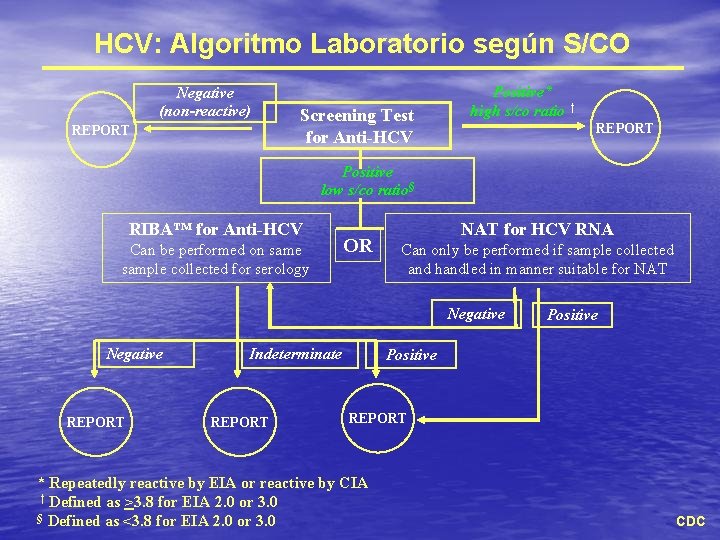
HCV: Algoritmo Laboratorio según S/CO Negative (non-reactive) REPORT Screening Test for Anti-HCV Positive* high s/co ratio † REPORT Positive low s/co ratio§ RIBA™ for Anti-HCV Can be performed on same sample collected for serology OR NAT for HCV RNA Can only be performed if sample collected and handled in manner suitable for NAT Negative REPORT Indeterminate REPORT Positive REPORT * Repeatedly reactive by EIA or reactive by CIA † Defined as >3. 8 for EIA 2. 0 or 3. 0 § Defined as <3. 8 for EIA 2. 0 or 3. 0 CDC

HBV

Marcadores de virus de la Hepatitis B • Ig. M anti-HBc: Marcador de replicación viral. • HBs. Ag: Marcador de infección. • Anti-HBs: Marcador de inmunidad. • HBc. Ag: No presente en suero. • Anti-HBc: Marcador de infección pasada o actual. • Ig. G anti-HBc: Memoria inmunológica. • HBe. Ag: . Marcador de alto grado de infectividad. • Anti-HBe: presente en estadios agudos y crónicos.

Curso clínico del virus Hepatitis B • Hepatitis B Aguda: – Ac HBc Ag Ig. M (marcador de replicación) – HBs. Ag (marcador de inefectividad) – HBV-DNA (marcador de replicación directo) – HBe. Ag (marcador de replicación solo en pacientes infectados con cepas salvajes del HBV) • Hepatitis B Crónica: – HBs. Ag. – Ac anti HBC Total (Ig. G – Ig. M) – Ac anti HBs

Interpretación de presencia de anticuerpo anti -HBc positivo como único marcador de Hepatitis B • Sensibilidad insuficiente en los test de diagnostico para detectar Ac anti HBs. • Hepatitis B en el pasado. • Niveles no detectables de HBs Ag o portadores inactivos. • Falso positivo anti-HBc


Infección oculta del virus de la Hepatitis B en pacientes hemodialisados (Minuk, G et al Hepatology 2004) • 241 pacientes HD estudiados: Ac HBc Positivo – 2 (0. 8%) HBs. Ag (+) – 239 HBs. Ag (-) • 9 HBV-DNA (+) (3. 8%) Baja Carga Viral – 7 Mutaciones (s. G 145 R) Conclusión: La prevalencia en este estudio de HBV oculto fue (3. 8%) asociada a baja carga viral y alta prevalencia de mutantes (s. G 145 R)
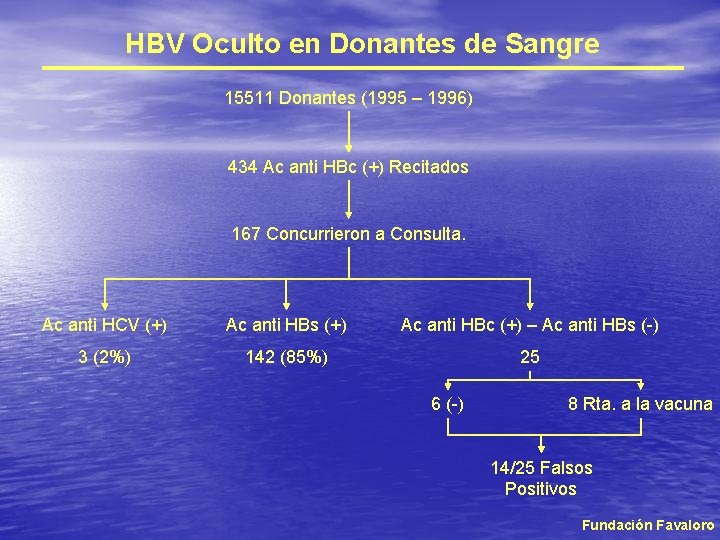
HBV Oculto en Donantes de Sangre 15511 Donantes (1995 – 1996) 434 Ac anti HBc (+) Recitados 167 Concurrieron a Consulta. Ac anti HCV (+) Ac anti HBs (+) Ac anti HBc (+) – Ac anti HBs (-) 3 (2%) 142 (85%) 25 6 (-) 8 Rta. a la vacuna 14/25 Falsos Positivos Fundación Favaloro
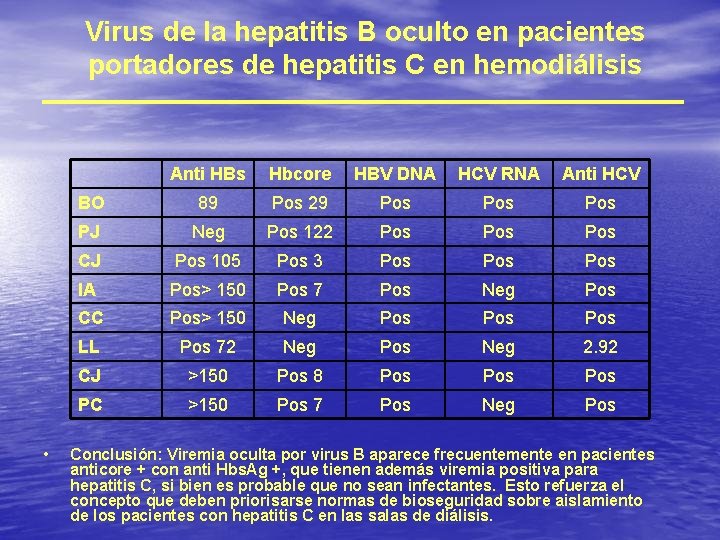
Virus de la hepatitis B oculto en pacientes portadores de hepatitis C en hemodiálisis • Anti HBs Hbcore HBV DNA HCV RNA Anti HCV BO 89 Pos 29 Pos Pos PJ Neg Pos 122 Pos Pos CJ Pos 105 Pos 3 Pos Pos IA Pos> 150 Pos 7 Pos Neg Pos CC Pos> 150 Neg Pos Pos LL Pos 72 Neg Pos Neg 2. 92 CJ >150 Pos 8 Pos Pos PC >150 Pos 7 Pos Neg Pos Conclusión: Viremia oculta por virus B aparece frecuentemente en pacientes anticore + con anti Hbs. Ag +, que tienen además viremia positiva para hepatitis C, si bien es probable que no sean infectantes. Esto refuerza el concepto que deben priorisarse normas de bioseguridad sobre aislamiento de los pacientes con hepatitis C en las salas de diálisis.
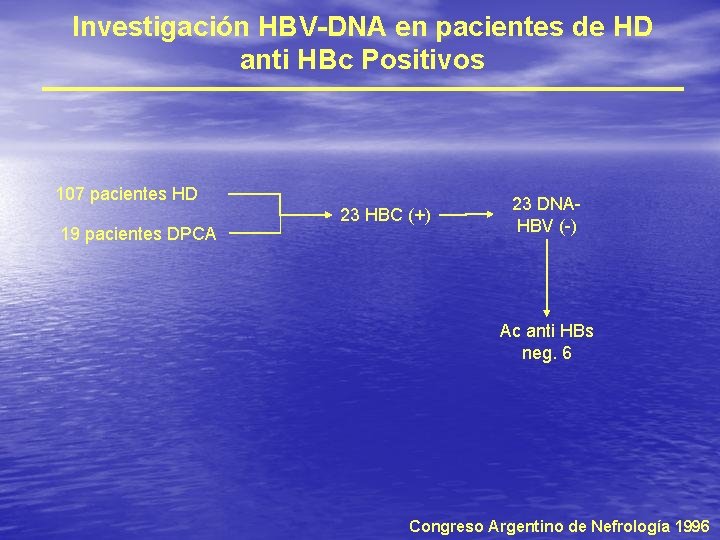
Investigación HBV-DNA en pacientes de HD anti HBc Positivos 107 pacientes HD 19 pacientes DPCA 23 HBC (+) 23 DNA- HBV (-) Ac anti HBs neg. 6 Congreso Argentino de Nefrología 1996

Marcadores Serológicos Inusuales Anti - HBC Ac. HBC HBSAg anti HBS - +/Mutación Core/precore? + - Falso positivo HBC (mutacion HBSAg? ) Marcadores Específicos HBe. Ag anti HBe anti HBc. Ig. M HBV antigeno - + Mutación precore/core con reactivacion? + - Fuente: CDC

Utilidad Clínica de los marcadores del HBV • • Ac anti HBcore en bancos de sangre se usa como marcador subrogante de la infección por HIV y HBV, ya que puede estar presente durante el periodo de ventana de la infección aguda HBV luego de la desaparición de HBs. Ag pero antes de la aparición de Ac protectores anti HBs. Se ha demostrado que una proporción de anti HBcore positivos son virémicos De allí la utilidad de esta prueba en banco de sangre y población de riesgo.

Utilidad Clínica de los marcadores del HBV (2) • Estudios sobre pacientes en HD los cuales muestran compromiso del sistema inmune debido a uremia crónica, la relación entre ALT y actividad de HBs. Ag en HD es imperfecta. – La respuesta inmune celular juega un papel crucial por lo que el aumento de ALT es intermitente, la carga viral del HBV fluctúa. Neophron 1995

Limitaciones de los Test para HBs. Ag • Pueden arrojar resultados FALSOS NEGATIVOS en: – Métodos comerciales de baja sensibilidad. – HBs. Ag con niveles por debajo del limite de detección (portadores inactivos). – Según publicaciones recientes los pacientes con Ac anti HBc como único marcador puede ser considerado portador con baja viremia. – Variantes del virus no reconocidos por los Test empleados en el diagnostico.
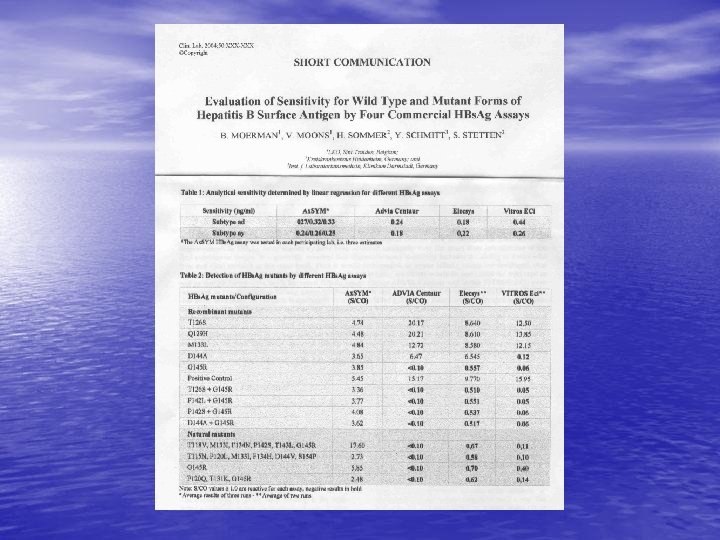
HIV

Test de Screening para HIV • Falsos Positivos: – Tanto en técnicas EIA como WB el rango descripto de falsos positivos (0. 0004% a 0. 0007%) (N. Engl I. Med 1988). – Autoanticuerpos (enfermedades autoinmunes) – Inmunosupresión – Pacientes expuestos recientemente al virus Eptein Barr. – Pacientes tratados con heparina, se pueden coagular parcialmente y producir resultados erróneos debido a la presencia de fibrina. – Tomar muestras antes de la terapia con heparina o en tubos con anticoagulante. – Muestra hemolisados y/o lipémicas. Resultados Falsos Negativos: • • Periodo de Ventana (11 a 22 días): – 0. 3 % en población de alta prevalencia. – < 0. 005 % en población de baja prevalencia. Respuesta atípica del huesped por causas desconocidas (AIDS 1995, MMWR 1996). Agammaglobulina. Subtipos O en HIV 2 (JANAT 1994) (MMWR 1996)
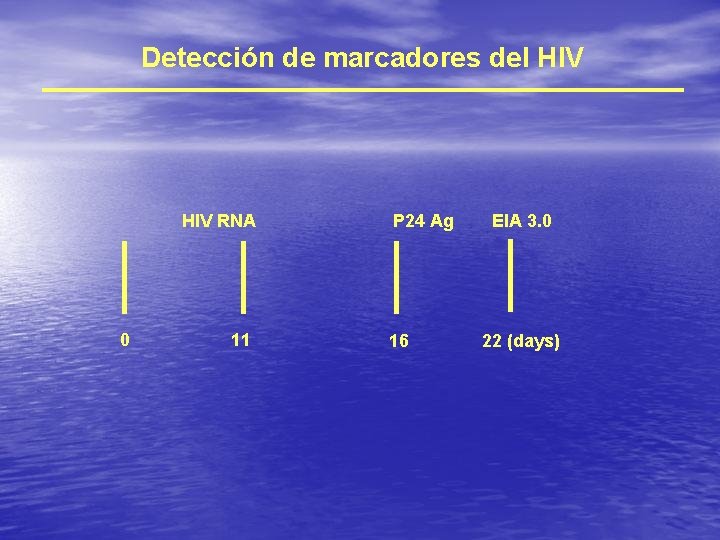
Detección de marcadores del HIV RNA 0 11 P 24 Ag 16 EIA 3. 0 22 (days)
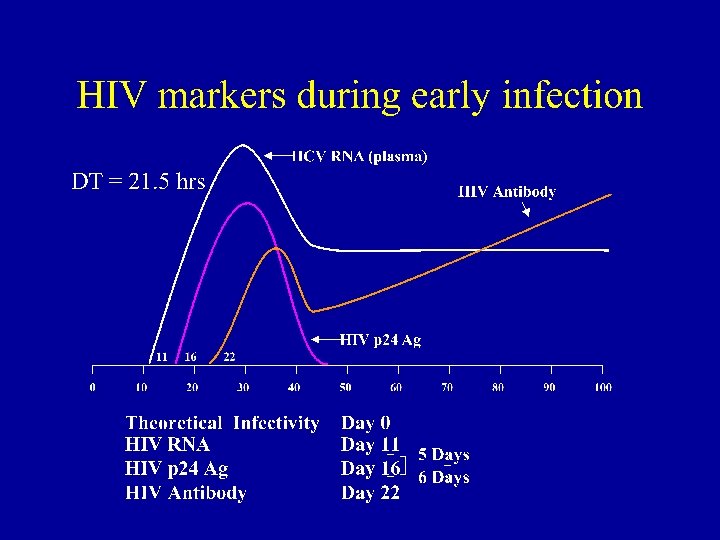

Resumen y Conclusiones • Seleccionar test de alta sensibilidad y especificidad. • Tomar en cuenta las interferencias propias de las muestras y el estado inmune del paciente. • Informar los resultados con, método utilizado, valor S/CO e interpretación del mismo (positivos – negativos). • Evaluar los test de screening y sus valores de corte en distintas poblaciones. (de alto riesgo – bajo riesgo). • Seria de suma utilidad un “consenso sobre diagnostico virológico en diálisis” a fin de estandarizar los informes de laboratorio y establecer las limitaciones de los test de screening comercializados en nuestro país.
- Slides: 41