Diagnostic et Suivi biologique de linfection par le

Diagnostic et Suivi biologique de l’infection par le VIH Professeur Lassana SANGARE UFR-SDS, Université de Ouagadougou 9è Session du DIU "Prise en Charge Globale des Personnes vivant avec le VIH en Afrique Sub-saharienne. Ouagadougou, Burkina Faso: 28 mai au 23 juin 2012

Diagnostic de l’infection à VIH

OBJECTIFS (1/2) • Citer les marqueurs virologiques de l’infection à VIH • Expliquer les courbes d’évolution des marqueurs du VIH chez le sujet adulte infecté • Citer deux produits biologiques permettant la détection des anticorps anti-VIH • Citer deux produits biologiques permettant la détermination de la CV chez un patient sous traitement

OBJECTIFS (2/2) • Énumérer deux tests de dépistage et un test de confirmation • Citer deux techniques permettant le diagnostic précoce chez l’enfant de moins de 18 mois • Citer deux conditions de demande de test de résistance

Rappels virologiques • • Classification & Phylogénie Morphologie structure Réplication virale Diversité génétique

Classification • • Famille: Sous-Famille: Genre: Espèce: Retroviridae Orthoretrovirinae Lentivirus de l’immunodeficience humaine type-1 et type 2 (VIH-1, VIH-2) Très grande diversité du VIH

Origines des VIH
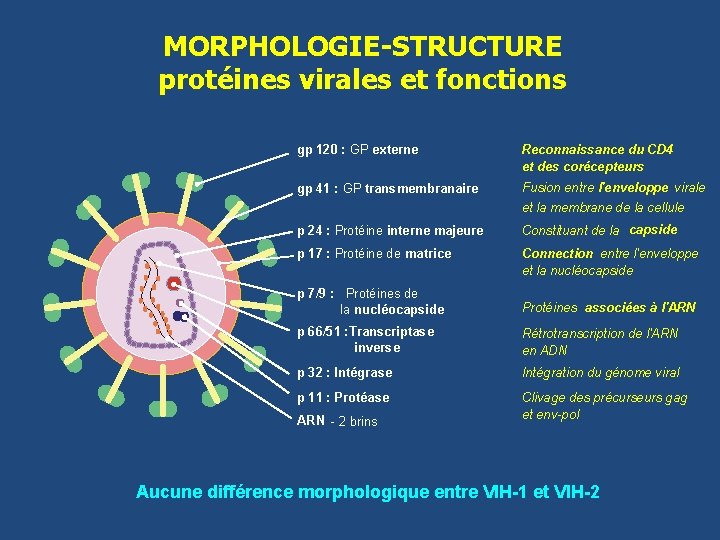
MORPHOLOGIE-STRUCTURE protéines virales et fonctions gp 120 : GP externe Reconnaissance du CD 4 et des corécepteurs gp 41 : GP transmembranaire Fusion entre l'enveloppe virale et la membrane de la cellule p 24 : Protéine interne majeure Constituant de la capside p 17 : Protéine de matrice Connection entre l'enveloppe et la nucléocapside p 7/9 : Protéines de la nucléocapside Protéines associées à l'ARN p 66/51 : Transcriptase inverse Rétrotranscription de l'ARN en ADN p 32 : Intégrase Intégration du génome viral p 11 : Protéase Clivage des précurseurs gag et env-pol ARN - 2 brins Aucune différence morphologique entre VIH-1 et VIH-2

DIVERSITE DU VIH variants VIH-1 VIH-2 • Groupe M, • 8 sous-types (A-H) – 9 sous-types – Sous sous-types • A 1 à A 4 • F 1, F 2 – Plus de 50 CRF • Groupe O (Outlier) • Groupe N • Groupe P
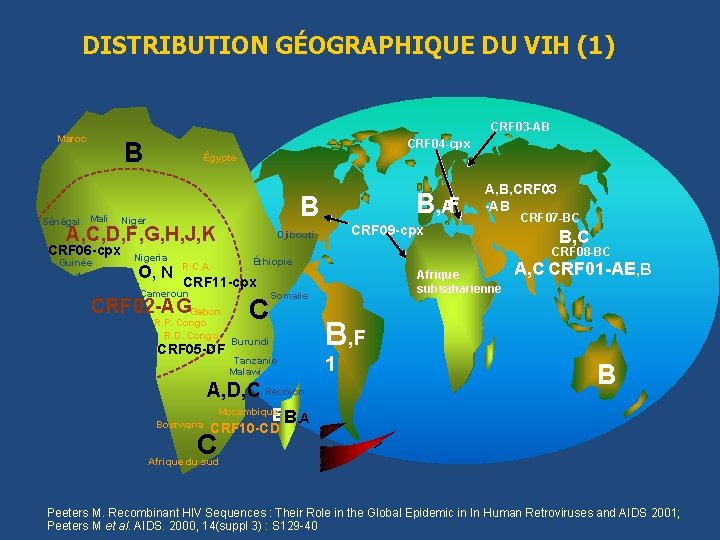
DISTRIBUTION GÉOGRAPHIQUE DU VIH (1) CRF 03 -AB Maroc CRF 04 -cpx B Sénégal Mali Égypte Niger A, C, D, F, G, H, J, K CRF 06 -cpx Guinée Côte d ’Ivoire Nigeria O, N Bénin B, AF B A, B, CRF 03 -AB CRF 09 -cpx Djibouti Afrique subsaharienne CRF 11 -cpx Cameroun CRF 02 -AGGabon R. P. Congo R. D. Congo CRF 05 -DF C Somalie Burundi B, F Tanzanie Malawi 1 A, D, C Réunion B, C CRF 08 -BC Éthiopie R. C. A. CRF 07 -BC A, C CRF 01 -AE, B B BB , A, A Mozambique Bostwana CRF 10 -CD C Afrique du sud Peeters M. Recombinant HIV Sequences : Their Role in the Global Epidemic in In Human Retroviruses and AIDS 2001; Peeters M et al. AIDS. 2000, 14(suppl 3) : S 129 -40

DIVERSITÉ DU VIH Antigènes (anticorps)


Implications de la Diversité du VIH Outils diagnostics • Choix des tests de diagnostic sérologique • Tests de quantification virale (moléculaires) Choix des schémas thérapeutiques (TARV) Conception des vaccins anti-VIH

DIAGNOSTIC DE L’INFECTION A VIH • • • Marqueurs de l’infection à VIH Cinétique/Evolution des marqueurs Définitions opérationnelles Diagnostic direct Diagnostic sérologique
MARQUEURS DE L’INFECTION • Virus entier • Acides nucléiques Diagnostic direct • Antigènes (p 24) • Anticorps Diagnostic indirect (Sérologique)

Cinétique des marqueurs
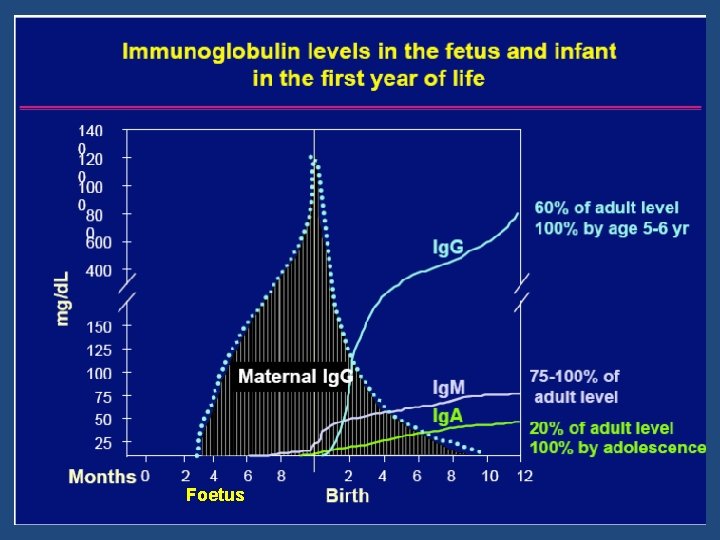
Foetus
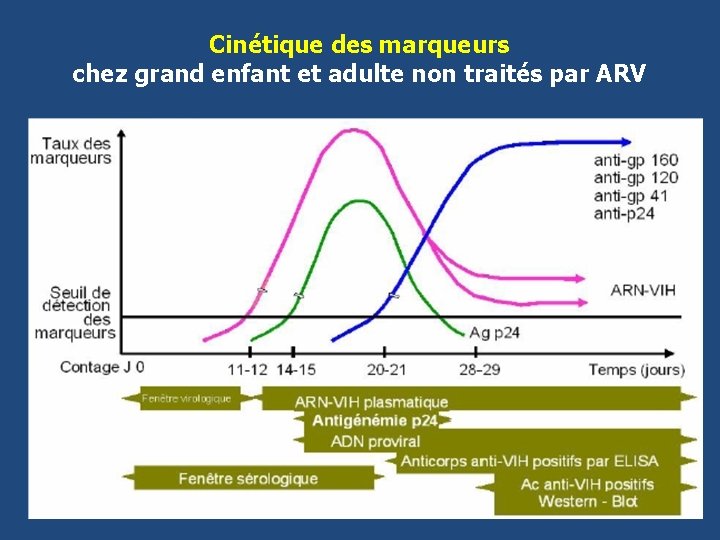
Cinétique des marqueurs chez grand enfant et adulte non traités par ARV
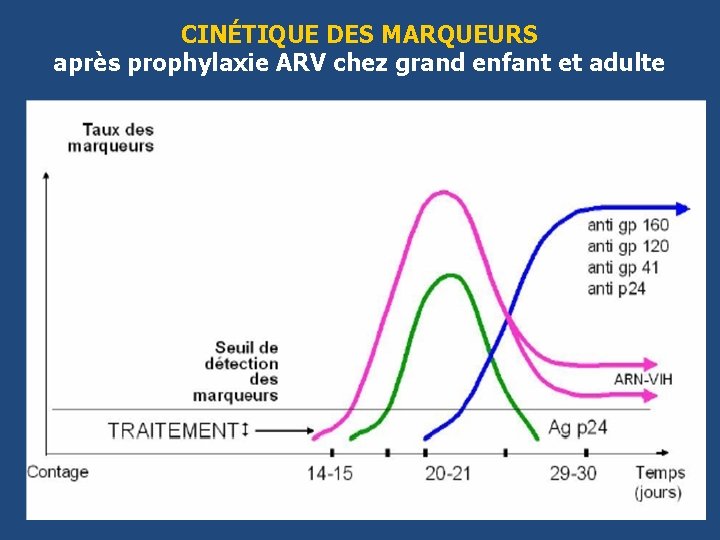
CINÉTIQUE DES MARQUEURS après prophylaxie ARV chez grand enfant et adulte

Fenêtre sérologique • Délai entre la contamination et la date de détection des anticorps anti-VIH • Séroconversion – 3ème semaine au plus tôt – 7ème mois au plus tard – 6 -8 semaines en moyenne • Considérablement réduit avec les nouveaux tests «(3ème et 4ème) générations

Fenêtre sérologique: Réduction selon les générations de tests ELISA • 1ère Génération – Ag naturels de lysats de virus purifiés – Nombreux faux positifs • 2ème Génération – Ag = Protéines recombinantes ou Peptides synthétiques – Réduisent de 10 jrs la fenêtre sérologique des tests de 1ère génération • 3ème Génération – Conjugués d’Ag de VIH marqués – Réduisent de 5 jrs le délai de détection des Ac anti-v. IH par tests de 2ème génération • 4ème Génération – Détection simultanée Ag de VIH et Ac anti-VIH – Détectent l’infection à VIH 5 jrs avant l’apparition des 1 ers Ac

DIAGNOSTIC DIRECT • Prélèvements – Sang (plasma, fraction lymphocytaires) – Taches de sang séché sur papier filtre (DBS) • Détection du virus entier • Détection des antigènes du VIH • Détection des acides nucléiques (ADN proviral, ARN viral)

DIAGNOSTIC DIRECT Isolement du VIH en culture cellulaire • Indications: – Infections du nouveau-né (<18 mois) – Primo-infection • Avantages: – Méthode de référence = Étalon d’or – Caractérisation de la souche virale • Inconvénients: – longue, coûteuse – danger biologique – réservée aux laboratoires spécialisés (référence)
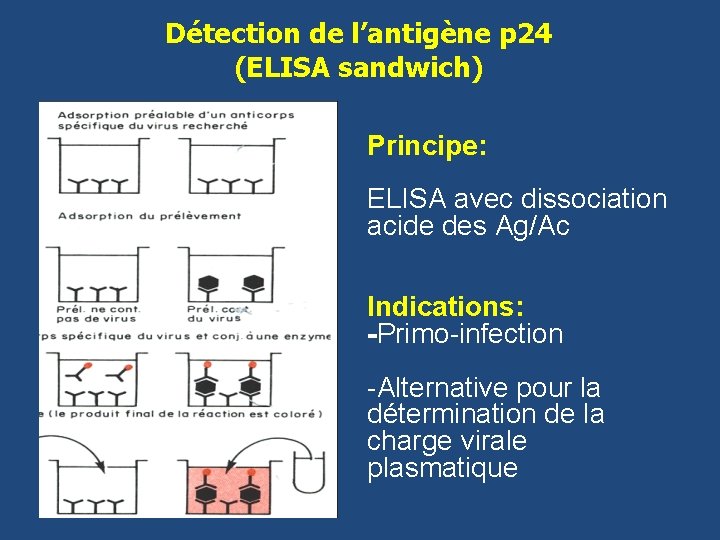
Détection de l’antigène p 24 (ELISA sandwich) Principe: ELISA avec dissociation acide des Ag/Ac Indications: -Primo-infection -Alternative pour la détermination de la charge virale plasmatique

Détection de l’antigène p 24 • Inconvénients: – disponible pour le VIH-1 seul – coût PCR en temps réel • Avantages: – très sensible/ultra-sensible (Schupbach, Perkin-Elmer) • Dissociation des complexes immuns: triton et chaleur • Sensibilisation possible du signal de détection par étape supplémentaire Seuil de sensibilité : 2 -5 pg/ml • 1 pg/ml correspond à 1000 -10. 000 copies d’ARN VIH – réduction de la fenêtre sérologique – pas d’appareillage spécifique nécessaire (laveur de plaque et spectro = chaîne ELISA)
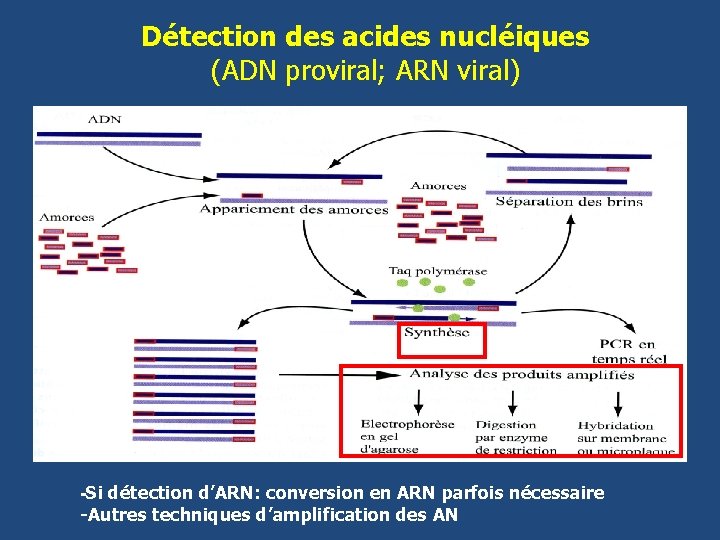
Détection des acides nucléiques (ADN proviral; ARN viral) -Si détection d’ARN: conversion en ARN parfois nécessaire -Autres techniques d’amplification des AN

Détection des acides nucléiques de VIH • Indications: – infection néonatale , – sérologie incertaine, difficultés de discrimination entre VIH-1 et VIH-2 – infections à VIH-1 des groupes O et N – infections mixtes à VIH-1/VIH-2 • Avantages: – très sensible, très spécifique (qualité des amorces) – référence ? • Inconvénients: – infrastructures , équipement, expérience – lourdeur, coût

DIAGNOSTIC INDIRECT • Diagnostic indirect = Sérologique – Prélèvements • Sang (total, sérum, plasma, TSS/DBS) • Autres: Salive, urines, … – Critères de choix – Méthodes d’analyses (Unitaires vs ELISA) – Stratégie conventionnelle – Stratégies alternatives (OMS)
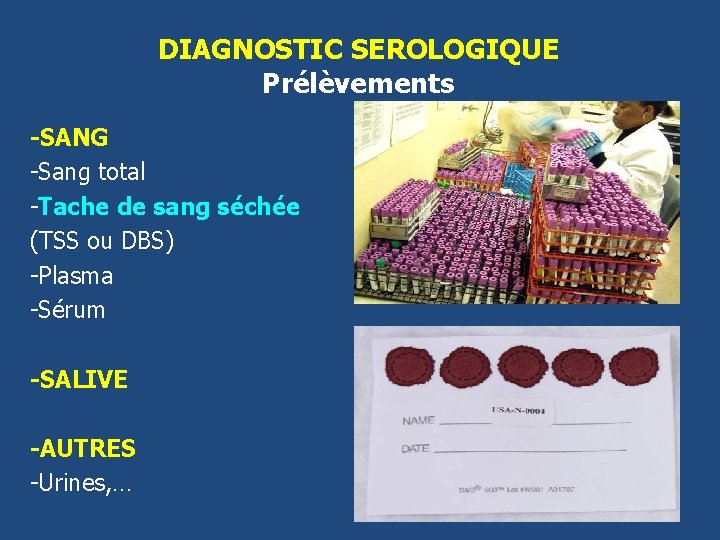
DIAGNOSTIC SEROLOGIQUE Prélèvements -SANG -Sang total -Tache de sang séchée (TSS ou DBS) -Plasma -Sérum -SALIVE -AUTRES -Urines, …
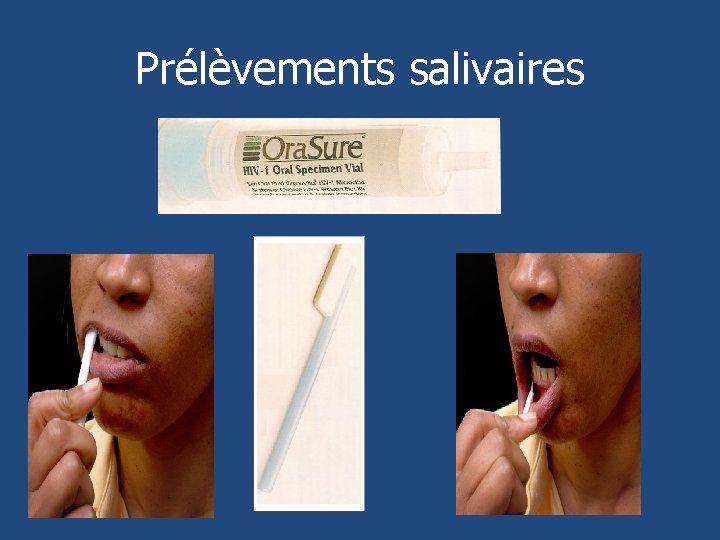
Prélèvements salivaires

DIAGNOSTIC SÉROLOGIQUE • Principaux critères de choix – Objectifs: • transfusion et transplantations • surveillance • diagnostic de l ’infection à VIH – Détection de VIH-1 (M, N, O) et VIH-2 – Sensibilité et spécificité respectant prévalence du VIH dans pays • Tests disponibles – Tests de dépistage • Tests ELISA • Tests rapides, simples ou unitaires – Tests de confirmation • Stratégies de diagnostic sérologique – Stratégie conventionnelle – Stratégies alternatives (OMS/ONUSIDA)

Tests ELISA • 4 Générations • Principes – – – Indirect Compétition Sandwich Immunocapture Combiné (Ag/Ac) ELISA indirect Enzyme Linked Immuno. Sorbent Assay

Caractérisques et évolution des tests sérologiques 1ère gen Antigène utilisé Elisa anti-HIV IG détection 2 nd gen 3ème gen 4ème gen protéines et peptides recombinants Lysat viral protéines et peptides recombinants indirect sandwich Ig. G Ig. M indirect Anticorps Ag p 24 Sensibilité + ++++ Spécificité + +++ 1987 1989 1997 Année 1985

Tests ELISA Avantages et Inconvénients • Avantages – Sensibilité et spécificité – Adaptés aux grandes séries – Coût faibles • Inconvénients – – – Équipements/Appareillage Personnel technique qualifié Électricité Nombre de tests réduits Avec plasma/sérum Température de conservation: +4°C à+ 8°C

Tests unitaires et tests rapides • Principes – Agglutination – Immunofiltration – Flux capillaires sur bandelettes (immunochromatographie) – Dot EIA • Durée: <30 mn (2 -5 mn, voire 15 mn) • Origine des Ag: – 1ère génération = naturels – 2ème génération = protéines recombinantes et/ou peptides synthétiques; tests actuels • Sensibilité et spécificité: comparables à celles des ELISA de 2ème génération

Tests rapides utilisés pour l’étude Test 1: Determine™HIV-1/2 (Abbott) Négatif Positif
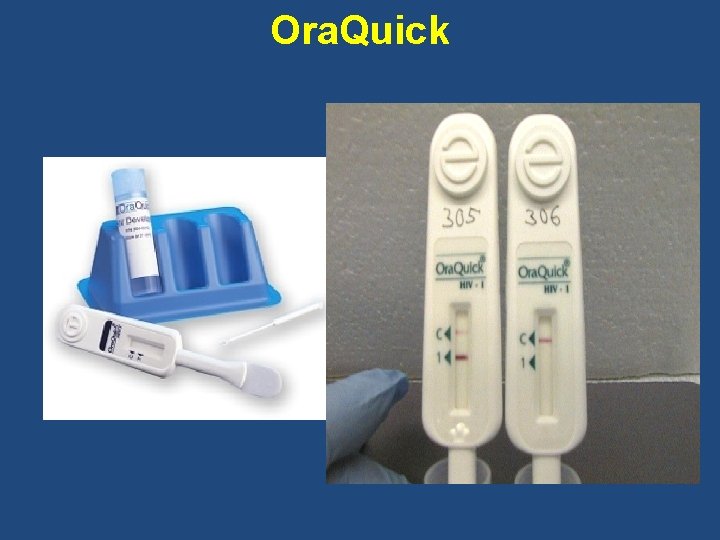
Ora. Quick
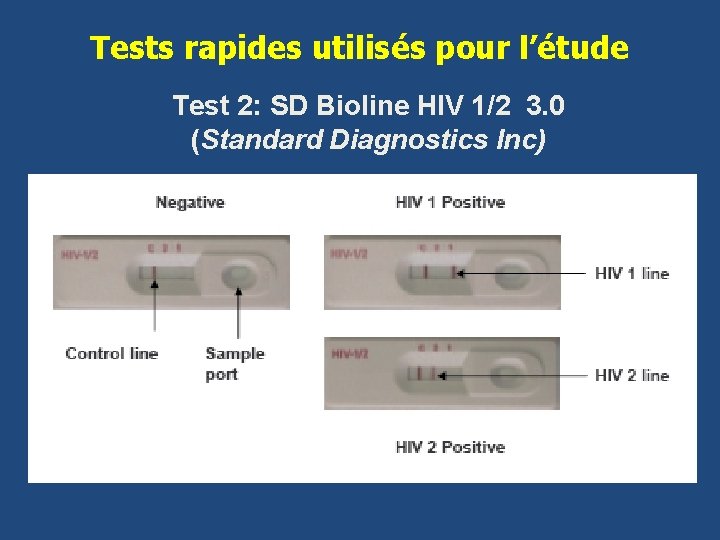
Tests rapides utilisés pour l’étude Test 2: SD Bioline HIV 1/2 3. 0 (Standard Diagnostics Inc)
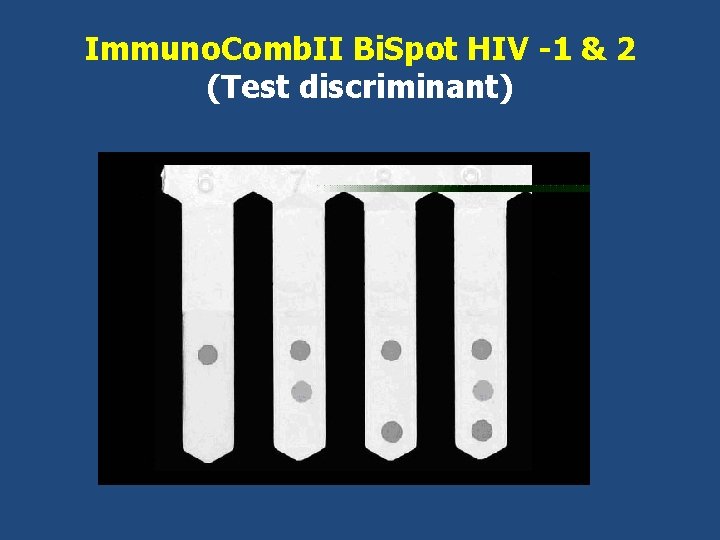
Immuno. Comb. II Bi. Spot HIV -1 & 2 (Test discriminant)

Avantages des Tests rapides Avec sérum, plasma, voire sang total, salive Ne nécessitent pas «d’équipements» de laboratoire Conservation: température du laboratoire (20°C-30°C) Individuel Durée: 10 -30 mn Lecture visuelle Peuvent manquer de sensibilité, en particulier en cas de séroconversion précoce, et aussi de spécificité • Certains sont discriminants • Aide au diagnostic d’urgence • Coût réduit • •

Inconvénients des Tests rapides • Sensibilité « légèrement » inférieure aux nouvelles techniques ELISA (séro-conversions) • Peu adaptés aux grandes séries

Tests de dépistage de 4ème génération • Détection simultanée des anticorps contre le VIH et de l’antigène p 24 – Sensibilités (seuil de détection = 65 -250 pg/ml d’antigène p 24) : inférieures à celles des trousses en immunocapture classiques exclusivement conçues pour détecter l’antigène p 24 (seuil<25 pg/ml) • Permet de gagner environ 2 -5 jours par rapport aux trousses de dépistage des anticorps anti-VIH non combinées • Mais même les plus sensibles ne doivent pas remplacer les trousses de détection de l’antigène p 24 pour le diagnostic de primo-infection • Inversement, une négativité avec un test combiné ne permet pas de rassurer une personne exposée au risque d’infection à VIH

Tests de confirmation sérologique • Tests – Western blot ou Immunoblot – Western blot modifié ou amélioré – Tests d’Immunoanalyse en lignes (LIA) – Test d’Immunofluorescence indirecte (IFA) – Test de Radioimmunoprécipitation (RIPA) • Inconvénients (Technique delicate) – demande une bonne expérience pour son interprétation, qui demeure subjective – fabrication artisanale des lots, ce qui entraîne des charges différentes en protéines, et en particulier en gp 160 – onéreuse : #15 -20 euros
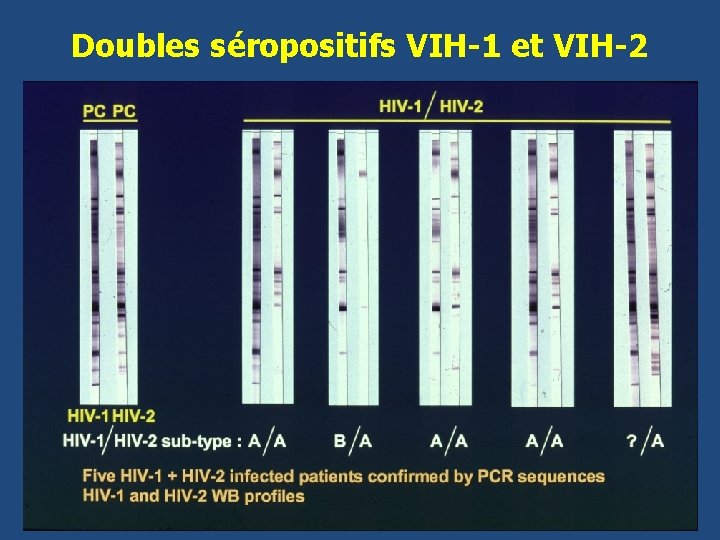
Doubles séropositifs VIH-1 et VIH-2
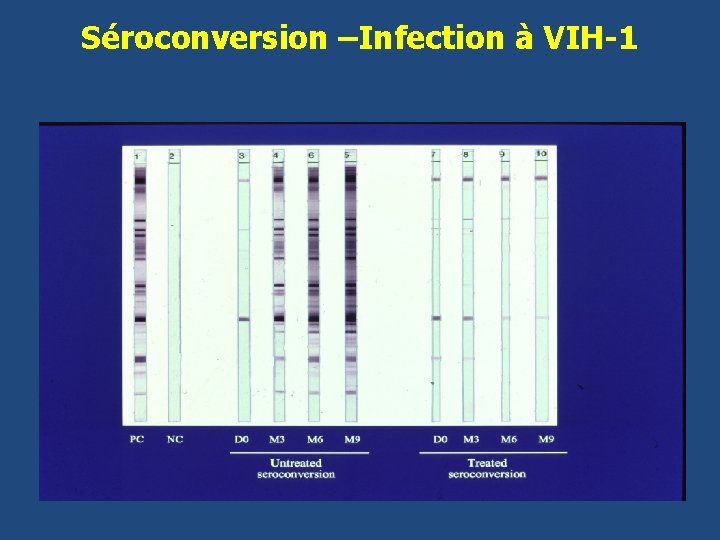
Séroconversion –Infection à VIH-1
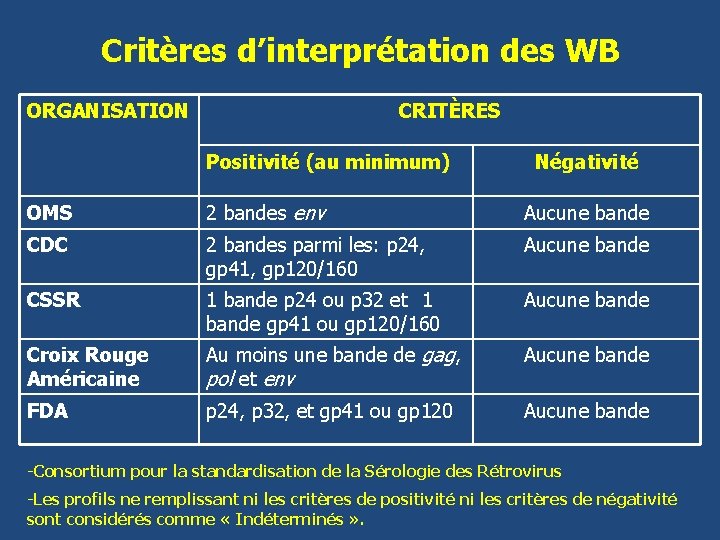
Critères d’interprétation des WB ORGANISATION CRITÈRES Positivité (au minimum) Négativité OMS 2 bandes env Aucune bande CDC 2 bandes parmi les: p 24, gp 41, gp 120/160 Aucune bande CSSR 1 bande p 24 ou p 32 et 1 bande gp 41 ou gp 120/160 Aucune bande Croix Rouge Américaine Au moins une bande de gag, pol et env Aucune bande FDA p 24, p 32, et gp 41 ou gp 120 Aucune bande -Consortium pour la standardisation de la Sérologie des Rétrovirus -Les profils ne remplissant ni les critères de positivité ni les critères de négativité sont considérés comme « Indéterminés » .

WB VIH-1 indéterminé ? • • Séroconversion VIH-1? Infection par VIH-2 ? Erreur de tube ? Variant ?

Stratégies de diagnostic sérologique du VIH • Conventionnelle – Tests de dépistage (ELISA) • + – Western blot (si ELISA+) • Alternative – 3 Algorithmes • I: • III – Equivalente à la conventionnelle

PROBLÉMATIQUE DES SÉROLOGIES INDÉTERMINÉES • Importances: +++ • Stratégies – Conventionnelle (WB et autres tests de confirmation) – Alternatives : qualité des tests • Résolution – Faux positifs (contextes) – Diversité du VIH – Recours à d’autres techniques
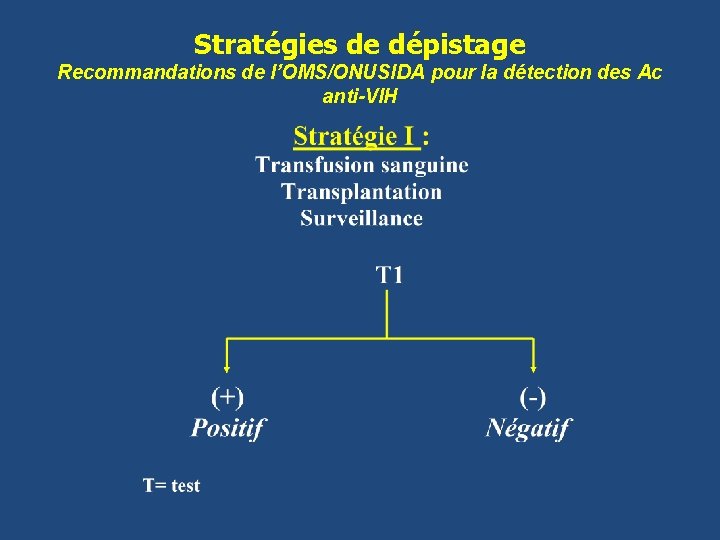
Stratégies de dépistage Recommandations de l’OMS/ONUSIDA pour la détection des Ac anti-VIH
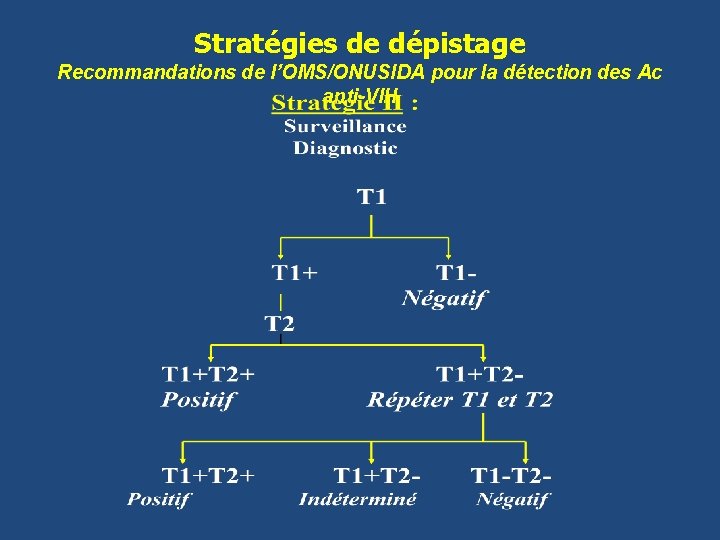
Stratégies de dépistage Recommandations de l’OMS/ONUSIDA pour la détection des Ac anti-VIH
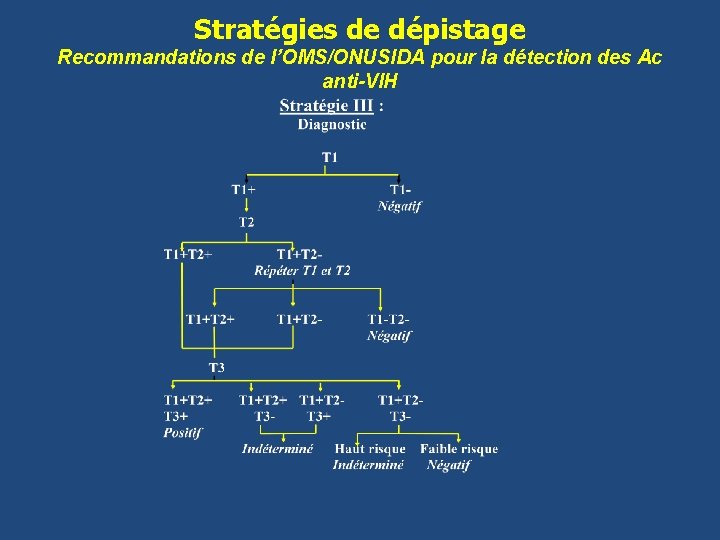
Stratégies de dépistage Recommandations de l’OMS/ONUSIDA pour la détection des Ac anti-VIH

Causes d’erreurs • Diversités antigéniques et des virus • Causes liés aux tests • Causes liées au manipulateur • Causes liées à l’échantillon • Réponses immunitaires de l’hôte infecté


SUIVI BIOLOGIQUE DE L’INFECTION À VIH


Représention de Coffin (1996)

SUIVI BIOLOGIQUE • But – Surveillance de l’efficacité du traitement • Paramètres du suivi – – – Immunologique (Numération lymphocytes T CD 4+) Virologique (CVP) Biochimiques Hématologiques Infections opportunistes

Examens du suivi biologique Analyses Biochimiques • • • Glycémie Azotémie Créatininémie Transaminases Amylasémie CPK • • • PAL Lipasémie Triglycérides Bilirubine Cholestérol

Examens du suivi biologique Examens hématologiques • Numération Formule Sanguine (NFS)

Examens du suivi biologique Bilan initial chez Adultes (M 0) Sérologie VIH Charge virale plasmatique Numération des lymphocytes T CD 4+ Numération formule sanguine Sérologie VHB (Ag. HBs), VHC, Syphilis Analyses biochimiques – Glycémie/Azotémie – Créatininémie – Transaminases – Amylasémie – CPK • Recherche de KAOP • Test immunologique de grossesse (femme) • • •

SUIVI DES PATIENTS (1) Examens du suivi à M 1 • Efficacité du traitement – Numération des lymphocytes T CD 4+ – Charge virale plasmatique • Surveillance de la toxicité des ARV – – Numération formule sanguine Transaminases Créatininémie Phosphatase alcaline • Bilan métabolique – Glycémie Bilan pas obligatoire

SUIVI DES PATIENTS (1) Examens du suivi à M 3 -M 4; tous les 3 -4 mois • Efficacité du traitement – Numération des lymphocytes T CD 4+ – Charge virale plasmatique • Surveillance de la toxicité des ARV – – – Numération formule sanguine Transaminases Créatininémie Phosphatase alcaline, CPK, Lipasémie, Amylasémie Bilirubine • Bilan métabolique – Glycémie – Cholestérol – Triglycérides • Diagnostic des infections opportunistes

Examens du suivi biologique Bilan initial chez enfants<18 mois (M 0) • Sérologie VIH ? • Détection de l’ARN viral par RT-PCR ou Ag p 24 (VIH-1) • Charge virale plasmatique • Numération formule sanguine • Glycémie • Créatininémie

Examens du suivi biologique Bilan initial chez enfants≥ 18 mois (M 0) • Sérologie VIH • Détection de l’ARN viral par RT-PCR ou Antigène p 24 (VIH-1) • Charge virale plasmatique • Numération formule sanguine • Glycémie • Créatininémie • Transaminases

Examens du suivi biologique Bilan à M 1 • Efficacité du traitement – Numération des lymphocytes T CD 4+ – Charge virale plasmatique • Surveillance de la toxicité des ARV – – Numération formule sanguine Transaminases Créatininémie Phosphatase alcaline (PAL) • Bilan métabolique – Glycémie Bilan pas obligatoire

Examens du suivi biologique Bilan à M 3 -4 et tous les 3 -4 mois • Efficacité du traitement – Numération des lymphocytes T CD 4+ – Charge virale plasmatique • Surveillance de la toxicité des ARV – Numération formule sanguine – Transaminases, Créatininémie, Bilirubine – PAL, CPK, Lipasémie, Amylasémie • Bilan métabolique – Glycémie – Cholestérol – Triglycérides • Diagnostic des infections opportunistes

Examens du suivi biologique Accidents d’exposition au VIH • Évaluation du risque (par clinicien) • Sérologie du « patient-source » • Bilan initial dans les 0 -48 heures du blessé (mieux dans les 4 heures) – Sérologie VIH – Ag. HBs et Anti-VHC – Transaminases

Examens du suivi biologique Accidents d’exposition au VIH • Bilan de surveillance – Sérologie VIH: 3ème et 6ème mois – NFS – Transaminases • Autres examens si TARV poursuivi

Examens du suivi biologique Examens de diagnostic des IO • Examens parasitologiques • Examens cytobactériologiques • Examens virologiques

MESURE DE CHARGE VIRALE • Définition : • Détermination de la quantité de virus chez l’individu infecté, dans – Sang (sang total sur tube; DBS) – tissu lymphoïde • Méthodes – Dosage des protéines virales – Quantification des acides nucléiques

Méthodes de mesure de la CV

Outils de suivi virologique Par dosage des protéines virales • Antigène p 24 «sensibilisée» • Détection de l’activité transcriptase inverse (Exa. Vir® Version 2, Cavidi Tech) Techniques « alternatives » aux techniques moléculaires de « référence »
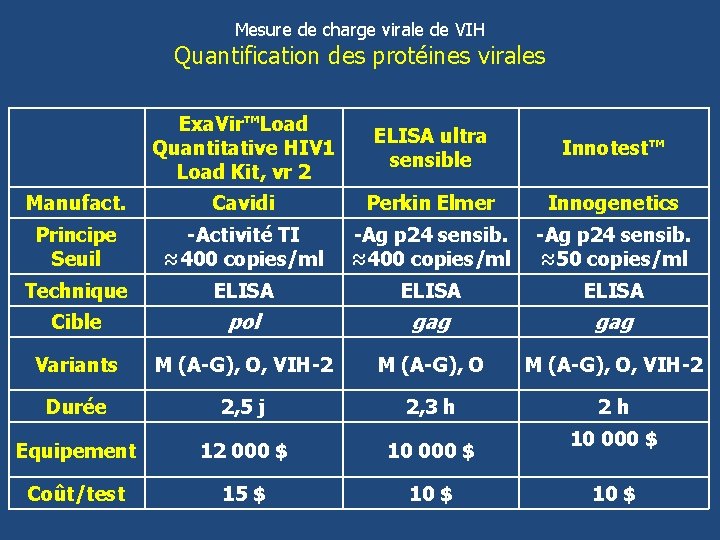
Mesure de charge virale de VIH Quantification des protéines virales Exa. Vir™Load Quantitative HIV 1 Load Kit, vr 2 ELISA ultra sensible Innotest™ Manufact. Cavidi Perkin Elmer Innogenetics Principe Seuil -Activité TI ≈400 copies/ml -Ag p 24 sensib. ≈50 copies/ml Technique ELISA Cible pol gag Variants M (A-G), O, VIH-2 Durée 2, 5 j 2, 3 h 2 h Equipement 12 000 $ 10 000 $ Coût/test 15 $ 10 000 $ 10 $

Mesure de charge virale de VIH Exa. Vir™Load Quantitative HIV-1 Load • Avantages – Equipement peu onéreux – Fonctionne sur tous les sous-types – Sensibilité de l’ordre de 400 copies/ml – Pas de risque de contamination • Inconvénients – Longue : 2, 5 jours – Fastidieuse (étape de capture des particules virales) et série limitée (30 échantillons) – Variation inter-essai élevée : 15% – Relativement coûteuse – Non validée par rapport aux trousses de référence de biologie moléculaire – Non connue et non validée en clinique

Mesure de charge virale de VIH Quantification des acides nucléiques (biologie moléculaire) • Deux principes : – Amplification de la cible • PCR point final, • PCR temps réel – Amplification du signal • Tech commerciales standardisées – RT-PCR ou *RT-PCR en temps réel – ADN branché – Système « ouvert » ou « fermé » • Techniques «maisons» – *RT-PCR en temps réel (protocole ANRS AC 11) * : Tecnniques dites « alternatives » aux techniques dites de « référence »
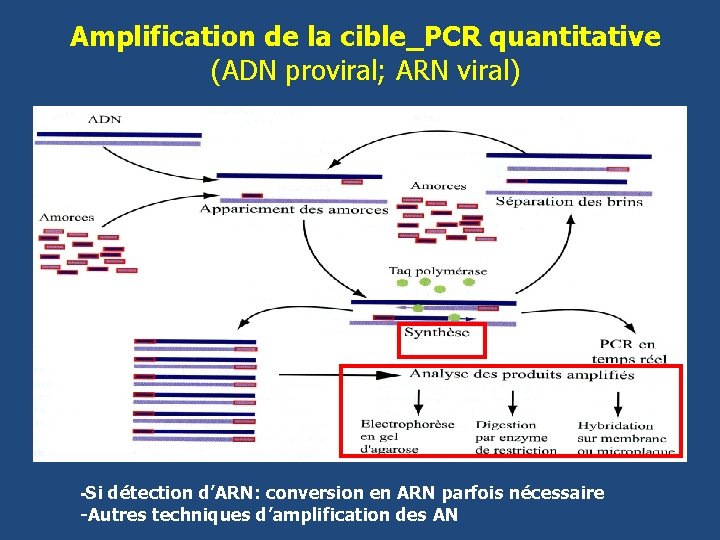
Amplification de la cible_PCR quantitative (ADN proviral; ARN viral) -Si détection d’ARN: conversion en ARN parfois nécessaire -Autres techniques d’amplification des AN
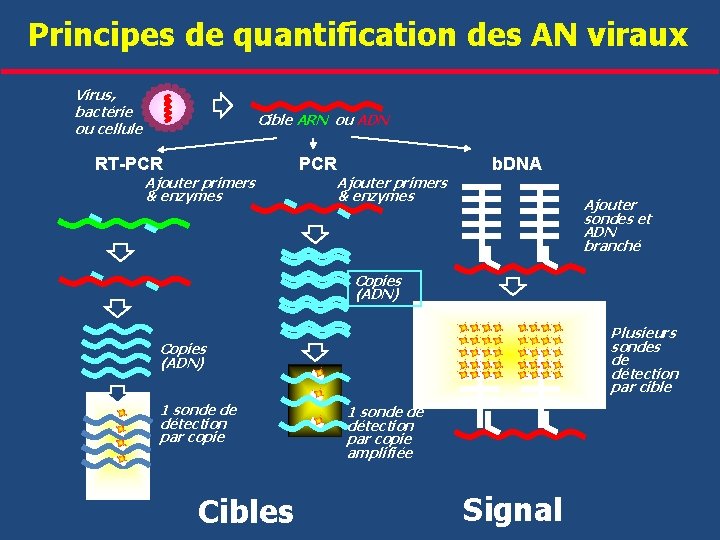
Principes de quantification des AN viraux Virus, bactérie ou cellule Cible ARN ou ADN RT-PCR Ajouter primers & enzymes b. DNA Ajouter sondes et ADN branché Copies (ADN) Plusieurs sondes de détection par cible Copies (ADN) 1 sonde de détection par copie Cibles 1 sonde de détection par copie amplifiée Signal

Outils de suivi Virologique Techniques de mesure des AN de VIH • Mesure du Signal – Quantiplex HIV-1 Vr 3. 0 (Bayer/Chiron) – Versant HIV-1 RNA 3. 0 (Bayer Diagnostics) • Mesure de la Cible – Amplicor Monitor HIV-1 vr 1. 5 (Roche) – Nuclisens HIV-1 QT – Nuclisens Easy Q VIH-1 (Organon/Bio. Mérieux) – Abbott HIV-1 Quantitative rt. PCR
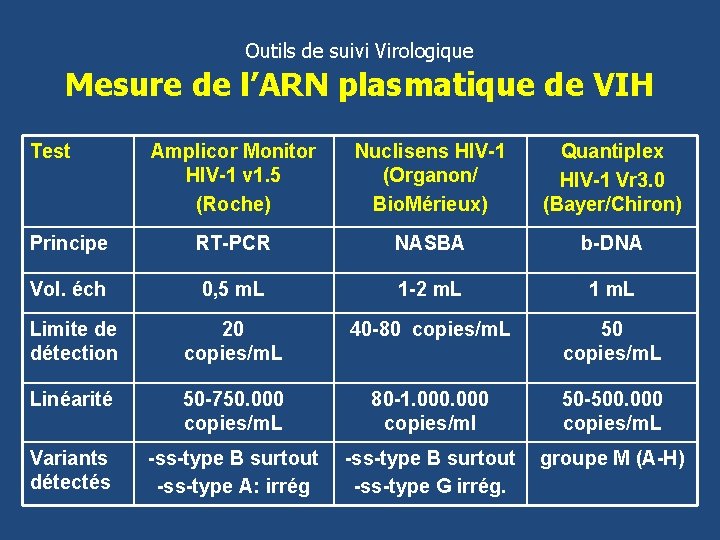
Outils de suivi Virologique Mesure de l’ARN plasmatique de VIH Test Amplicor Monitor HIV-1 v 1. 5 (Roche) Nuclisens HIV-1 (Organon/ Bio. Mérieux) Quantiplex HIV-1 Vr 3. 0 (Bayer/Chiron) Principe RT-PCR NASBA b-DNA Vol. éch 0, 5 m. L 1 -2 m. L 1 m. L Limite de détection 20 40 -80 copies/m. L 50 copies/m. L Linéarité 50 -750. 000 copies/m. L 50 -500. 000 copies/m. L Variants détectés 80 -1. 000 copies/ml -ss-type B surtout -ss-type A: irrég -ss-type G irrég. groupe M (A-H)
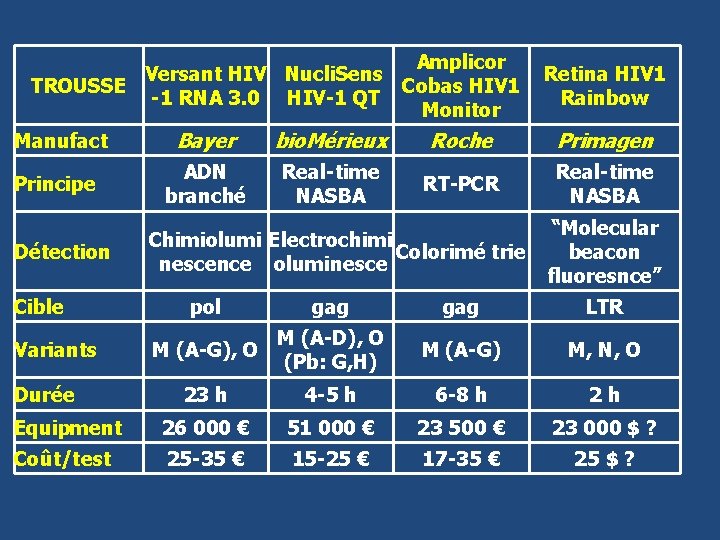
Amplicor Versant HIV Nucli. Sens Retina HIV 1 TROUSSE Cobas HIV 1 -1 RNA 3. 0 HIV-1 QT Rainbow Monitor Manufact Principe Détection Cible Bayer bio. Mérieux Roche Primagen ADN branché Real-time NASBA RT-PCR Real-time NASBA Chimiolumi Electrochimi Colorimé trie nescence oluminesce “Molecular beacon fluoresnce” pol gag LTR M (A-G), O M (A-D), O (Pb: G, H) M (A-G) M, N, O 23 h 4 -5 h 6 -8 h 2 h Equipment 26 000 € 51 000 € 23 500 € 23 000 $ ? Coût/test 25 -35 € 15 -25 € 17 -35 € 25 $ ? Variants Durée
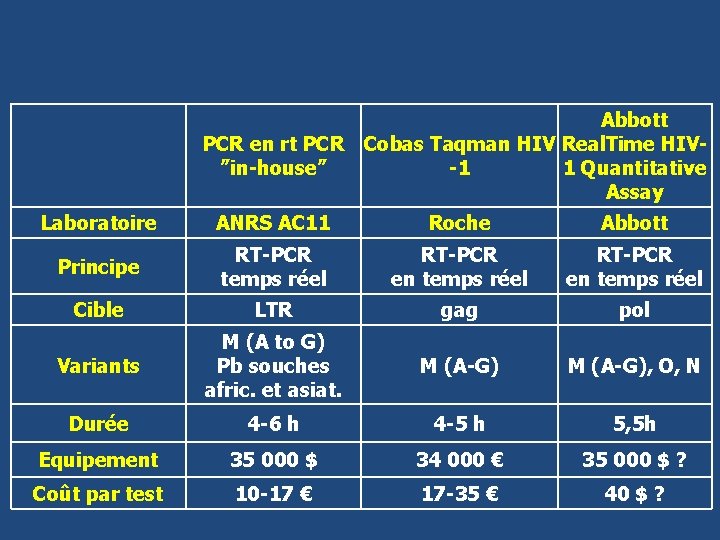
Abbott PCR en rt PCR Cobas Taqman HIV Real. Time HIV”in-house” -1 1 Quantitative Assay Laboratoire ANRS AC 11 Roche Abbott Principe RT-PCR temps réel RT-PCR en temps réel Cible LTR gag pol Variants M (A to G) Pb souches afric. et asiat. M (A-G), O, N Durée 4 -6 h 4 -5 h 5, 5 h Equipement 35 000 $ 34 000 € 35 000 $ ? Coût par test 10 -17 € 17 -35 € 40 $ ?

Résultats des mesures de Charges virale • Résultats exprimés – copies/ml – Log/ml • Interprétation des résultats : – variation biologique: 0. 5 log – Modifications transitoires : • Infections aiguës (grippe, herpes) • Vaccinations

ARN-VIH plasmatique (charge virale » ) interprétation des résultats Variabilité de la mesure : -Liée à l'anticoagulant, aux plaquettes; -Liée aux méthodes; -Variabilité intra individuelle 0, 2 - 0, 3 log = facteur 2 Variations significatives : > 0, 5 log = facteur 3 Les valeurs sont comprises entre 1, 3 et 7 2 Brun-Vezinet F, Dormont J. Méthodes de mesure de la charge virale VIH-1. Med Sci Flammarion, 196 Rapport Dormont, 11. 06. 1998 : p. 5 -8

Intérêts des Charges virales plasmatiques -Inversement proportionnelle au nombre T CD 4 + -Pronostic de l’évolution de la maladie -Corrélation avec stade clinique -Marqueur de l ’efficacité des ARV Contraintes : équipements, choix et coûts des kits, infrastructures. . .

Numération des lymphocytes T CD 4

Outils de suivi immunologique Numération lymphocytes T CD 4 • Collecte des échantillons de sang – Anticoagulant – Stabilisateurs de sang • Cytométrie de flux – Marqueurs monoclonaux – Plateforme double – Plateforme simple • Méthodes Manuelles – Lecture Microscopique – ELISA

Techniques de numération des lymphocytes T CD 4 Cytométrie en flux Plateforme double PARAMÈTRES CARACTÉRISTIQUES Fabricant Partec; Becton Dickinson; Coulter Coût instrument 20 000 -95 000 $ US Coût/test 3 -11 $ US Echantillon Sang total Résultats CD 4, CD 8 (absolu, %, CD 4/CD 8); rapport lymphocytaire; cellules B et NK possible Nbre analysé/jr ≤ 250 Avantages Précision pipettage non requise; Analyse d’ 1 seul tube possible sans pb de CQ; CQE disponibl. Inconvénients Analyseur hémato requis; Erreurs de transcription ou de calcul; Sang frais pour numération absolue

Techniques de numération des lymphocytes T CD 4 Cytométres en flux spécialisés FACSCount (BD) Cy. Flow (Partec) Syst détect° Fluorocchromes conjug aux Ac. M anti-CD 3, CD 4, CD 8 Fluorocchromes conjug aux Ac. M anti-CD 4 Echantillon Sang total Résultats CD 4, CD 8 (absolus, % par rapport aux T; CD 4/CD 8) CD 4 absolu Corrélation avec réf (r) 0, 93 – 0, 98 (plusieurs études 0, 96 – 0, 96 interntles) (quelques études) Coût instrumt 25 000 $ US 20 000 $ US Coût/test 6 – 20 $ US 2 $ US Avantages Automatisation; Peu d’étapes; Coût réactifs; Rapide; moins d’erreurs humaines; CQE CD 4 et CD 8 absolus; Rapide; CQE dispo Inconvénts Coût réactifs; 12 échant à la fois; %CD lymphoctre indispo; Evaluations en cours

BD FACSCount* (Becton Dickinson) • Dédié aux lymphocytes T CD 4/8/3 • Simple à utiliser • Lymphocytes CD 4 en valeur absolue et pourcentage • Réactifs encore onéreux • Coût : 25, 000 $ • >225 appareils en Afrique • Politique commerciale active en Afrique • Maintenance régionale++

Techniques de numération des lymphocytes T CD 4 Autres méthodes en cours d’évaluation • • • Cy. Flow Apogee 40, A 40 (Amplimed) Point Care Lab Now Etc.

A 40
Point Care (Beckman Coulter)

Guava Easy CD 4 System
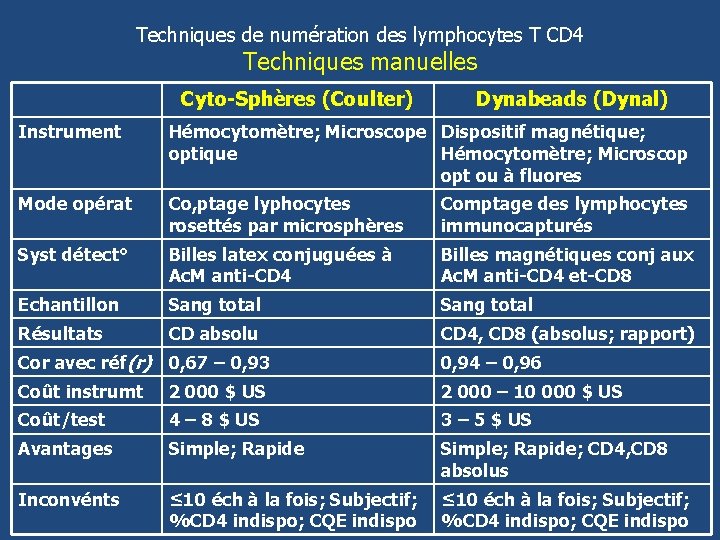
Techniques de numération des lymphocytes T CD 4 Techniques manuelles Cyto-Sphères (Coulter) Dynabeads (Dynal) Instrument Hémocytomètre; Microscope Dispositif magnétique; optique Hémocytomètre; Microscop opt ou à fluores Mode opérat Co, ptage lyphocytes rosettés par microsphères Comptage des lymphocytes immunocapturés Syst détect° Billes latex conjuguées à Ac. M anti-CD 4 Billes magnétiques conj aux Ac. M anti-CD 4 et-CD 8 Echantillon Sang total Résultats CD absolu CD 4, CD 8 (absolus; rapport) Cor avec réf(r) 0, 67 – 0, 93 0, 94 – 0, 96 Coût instrumt 2 000 $ US 2 000 – 10 000 $ US Coût/test 4 – 8 $ US 3 – 5 $ US Avantages Simple; Rapide; CD 4, CD 8 absolus Inconvénts ≤ 10 éch à la fois; Subjectif; %CD 4 indispo; CQE indispo
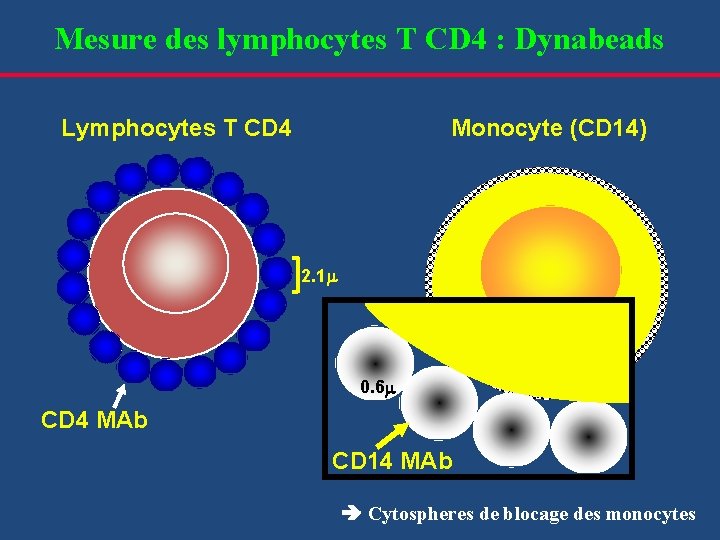
Mesure des lymphocytes T CD 4 : Dynabeads Lymphocytes T CD 4 Monocyte (CD 14) 2. 1 m 0. 6 m CD 4 MAb CD 14 MAb Cytospheres de blocage des monocytes
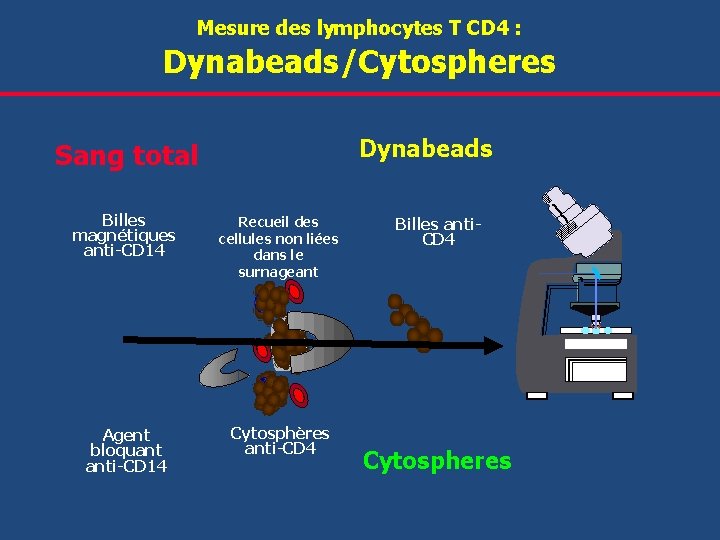
Dynabeads/Cytospheres Mesure des lymphocytes T CD 4 : Dynabeads Sang total Billes magnétiques anti-CD 14 Recueil des cellules non liées dans le surnageant Agent bloquant anti-CD 14 Cytosphères anti-CD 4 Billes anti. CD 4 Cytospheres

Techniques de numération des lymphocytes T CD 4 Méthodes non commercialisées ou obsolètes • • • Capcellia (Bio-Rad) OPTI-CIM (CIMA, Cuba) TRAx. ELISA (Innogenetics) Zummune (Znaxis Inc) Dosage de phosphatase immunoalcaline

Taux de CD 4 chez l'adulte • Valeurs normales: 750 -1180/mm 3 • Perte moyenne/an: 50 à 60/mm 3 • Rendu en mm 3 ou en % • >500/ mm 3 >29% • 200 -500/ mm 3 14 -28% • <200/ mm 3 <14%

Intérêt de mesure des T CD 4+ – Statut immunitaire – Stade de la maladie – Décision de début intervention thérapeutique Ne mesure pas l’activité du virus

Charge virale et LT CD 4+ La C. V. en association avec LTCD 4+ image complète du statut immunitaire et de l’activité virale à tous les stades de la maladie

TESTS DE RÉSISTANCE DU VIH AUX ARV

3 types de Tests de résistance du VIH aux ARV • Tests phénotypiques (biologiques) • Tests génotypiques (moléculaires) • Recombinaison virale (biologique+ moléculaire)
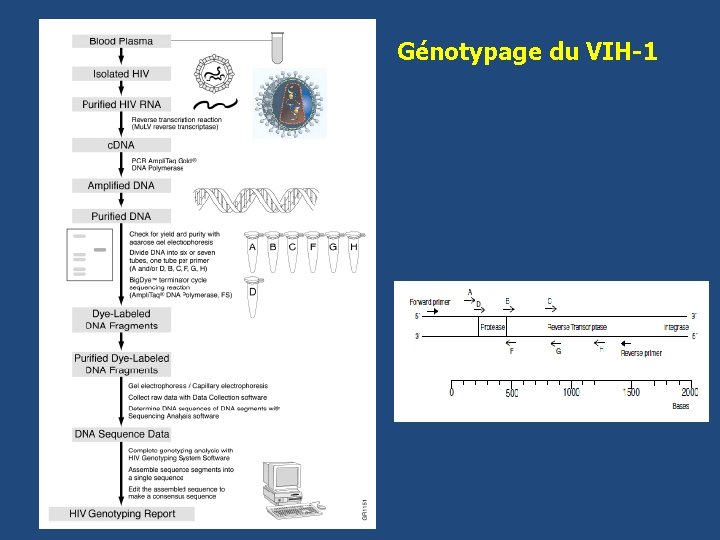
Génotypage du VIH-1
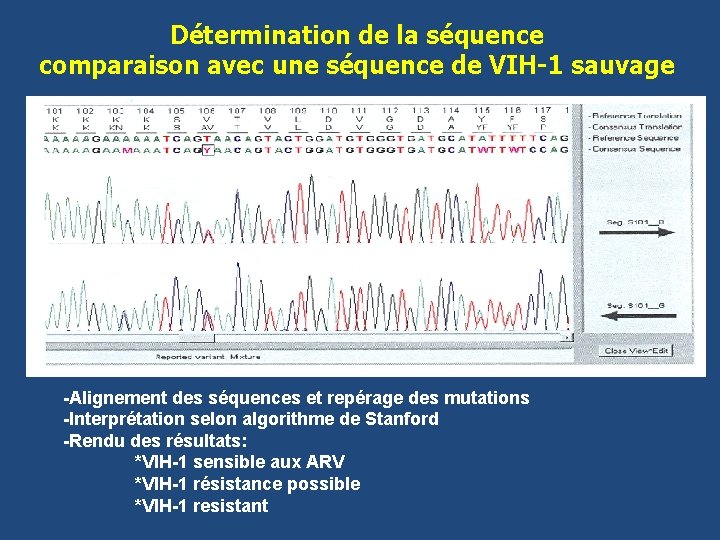
Détermination de la séquence comparaison avec une séquence de VIH-1 sauvage -Alignement des séquences et repérage des mutations -Interprétation selon algorithme de Stanford -Rendu des résultats: *VIH-1 sensible aux ARV *VIH-1 résistance possible *VIH-1 resistant

Génotype de résistance : Techniques disponibles n Tests commerciaux 4 « services » de génotypage Geneseq (Virologic) Genchec (Virco) HIV Geno. Sure (Labcorp) Geno. Type Plus (Labcorp) 2 trousses de génotypage (approuvées par la FDA) Trugene (Visible Genetics/Bayer) Viroseq (Applied Biosystem/Abbott) n Nombreux protocoles « maisons » - Protocole de l’AC 11 de l’ANRS (France)

CONCLUSION • Dépistage = porte d’entrée de la prise en charge de l’infection par le VIH • Diversité du virus un obstacle majeur au diagnostic et au suivi de l’infection par le VIH • Coût des infrastructures, équipements et intrants divers pris en compte par subventions • Surveillances géographiques des virus

Merci
- Slides: 108