DIAGNOSTIC BACTERIOLOGIQUE DR RADJI Cours 2 e anne

DIAGNOSTIC BACTERIOLOGIQUE DR RADJI Cours 2 e année CHIR DENT 2018 -2019

• Devant une infection, le clinicien réalise un prélèvement qu’il envoi au laboratoire. En attendant les résultats, il instaure un traitement probabiliste (en fonction des signes cliniques, de l’âge du patient du germe présumé et de l’épidemiologie des résistances). • Le rôle du laboratoire est d’isoler, d’identifier puis de tester la sensibilité aux antibiotique du germe en cause

INTRODUCTION • Diagnostic direct: mise en évidence de la bactérie responsable du tableau clinique, identification et étude de la sensibilité aux anti -bactériens • Diagnostic indirect: mise en évidence des marqueurs biologiques (Anticorps humoraux) témoins de la multiplication bactérienne dans l’organisme

LES PRELEVEMENTS De la qualité du prélèvement et des conditions de son transport au laboratoire dépend la qualité du résultat

LES PRELEVEMENTS - - Règles générales: Avant toute antibiothérapie si possible, sinon après une fenêtre thérapeutique Asepsie rigoureuse Acheminement rapide ( à +4° polymicrobien, à 37° monomicrobien) Germes fragiles: possibilité d’ensemencement au lit du malade (méningocoque, gonocoque) Milieux de transport

Fiche de renseignements cliniques • Informations utiles sur le malade: âge, sexe, profession, origine géographique, etc. • sur le tableau clinique: début, symptômes majeurs, type d’évolution, traitement reçus avant. • Autres types d’informations spécifiques pouvant orienter le bactériologistes vers une recherche de germes particuliers.

Enregistrement au laboratoire • Sur registre du laboratoire – Numéro – date de réception au laboratoire – Nom, prénom, âge et sexe – Adresse ou service hospitalier, nom du médecin – Nature du prélèvement
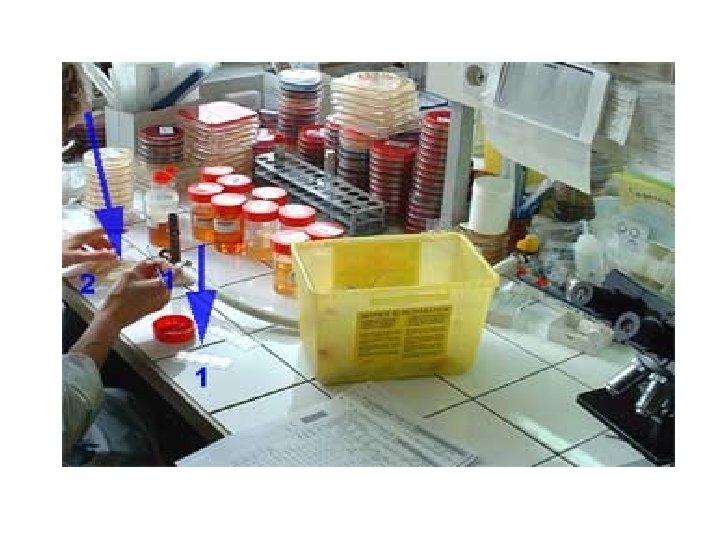

DIAGNOSTIC DIRECT 1. Examen macroscopique : =» aspect du prélèvement la présence d’un trouble, l’odeur (particulièrement pour les anaérobies), la consistance, la granulations… peuvent apporter des premières informations sur l’existence d’une infection ou non.

Il existe différents types de prélèvements: Coproculture LCR Clair trouble Expectorations purulentes clair

2. Examens microscopiques: ü état frais fourni des informations sur la forme et la mobilité des bactéries. ü examen à l’encre de chine : recherche de capsule. ü frottis colorés par le bleu, le Gram, ou coloration spécifique (Ziehl-Neelsen), IFD immunofluorescence directe…… ü Coloration de Gram : Gram (montre l’affinité tinctoriale du micro-organisme)

ü Permettent d’avoir des informations sur la pureté de la population bactérienne, la présence de cellules polynucléaires ou lymphocytaires ü Orientent les recherches ultérieures pour le choix des milieux à ensemencer, les tests à lancer rapidement et ü Permet parfois de donner un diagnostic de forte présomption au clinicien qui peut commencer le bon traitement immédiat
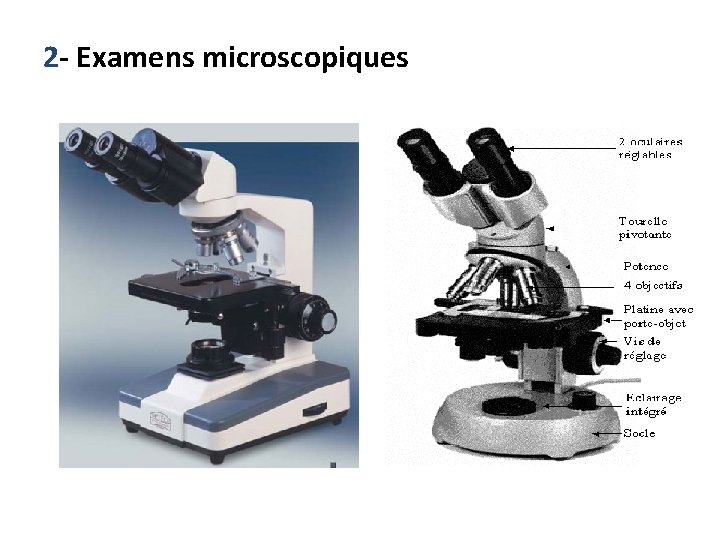
2 - Examens microscopiques
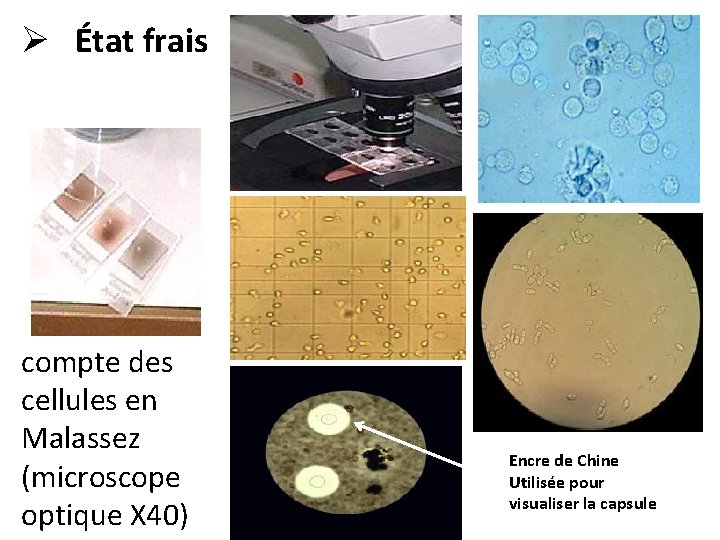
Ø État frais compte des cellules en Malassez (microscope optique X 40) Encre de Chine Utilisée pour visualiser la capsule
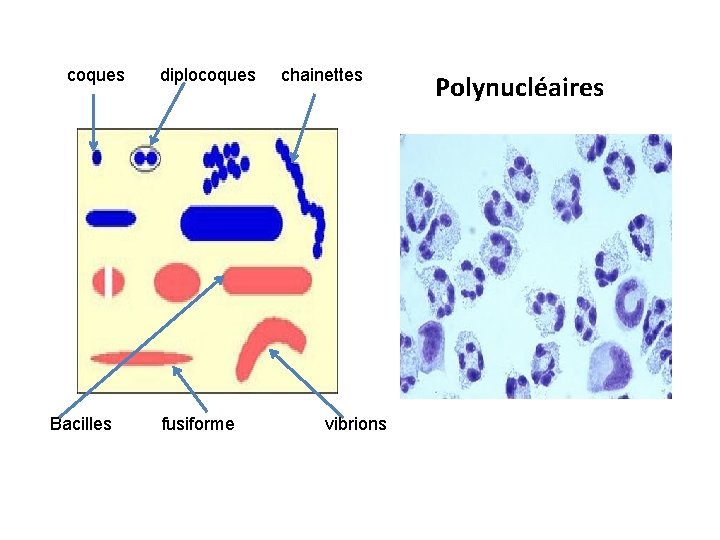
coques Bacilles diplocoques fusiforme chainettes vibrions Polynucléaires

La coloration de Gram • Renseigne sur la présence (ou absence) de bactéries: • leur forme (cocci ou bacille, cocobacille, fusiforme) • leur groupement (amas, chaînettes, diplocoques) • leur gram (+ ou -) ⇒ très utile car oriente l’antibiothérapie.
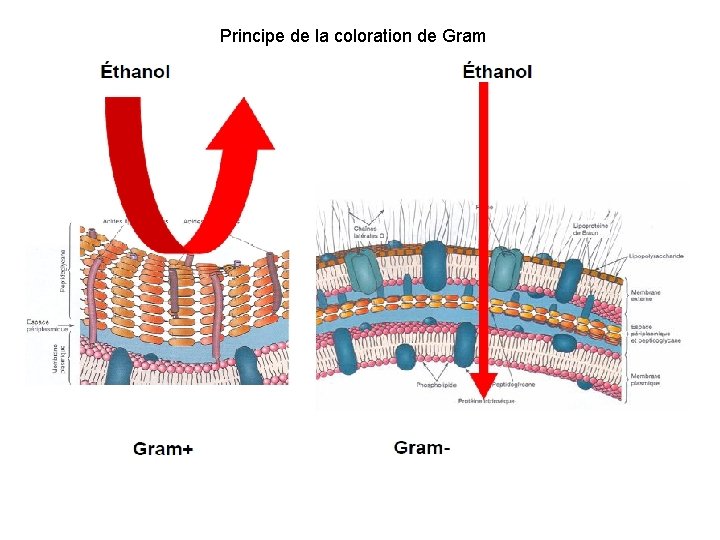
Principe de la coloration de Gram
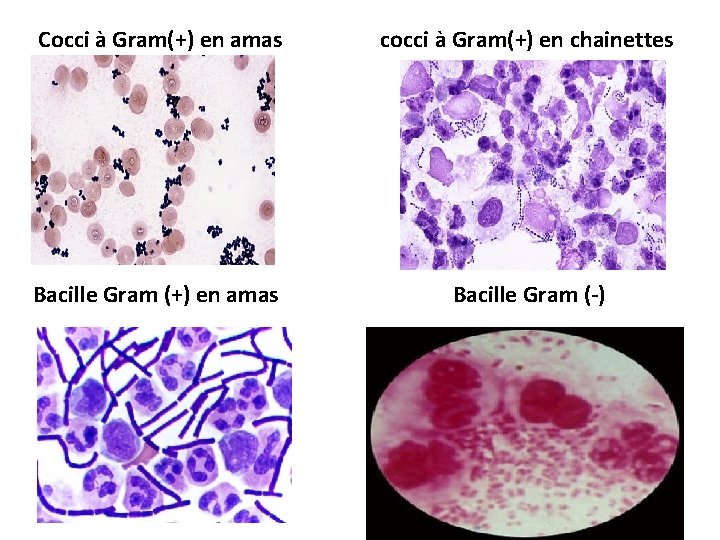
Cocci à Gram(+) en amas cocci à Gram(+) en chainettes Bacille Gram (+) en amas Bacille Gram (-)
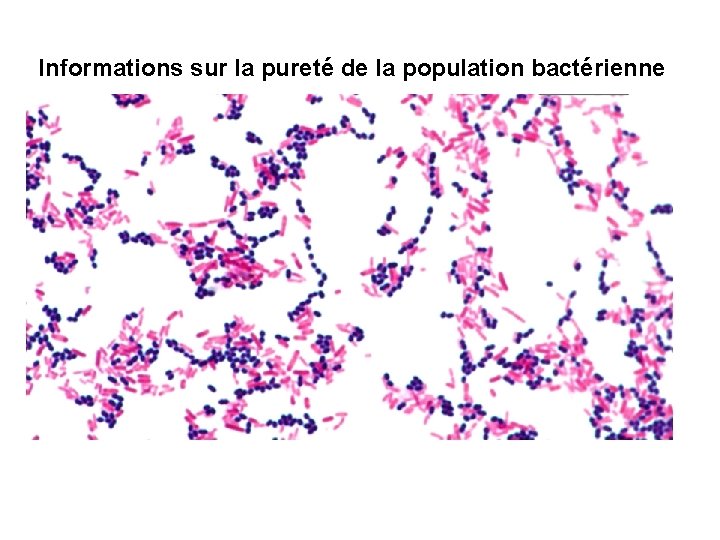
Informations sur la pureté de la population bactérienne
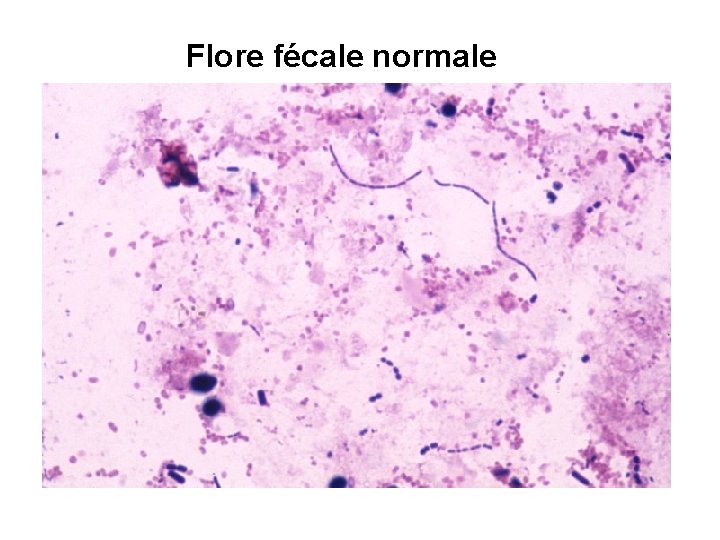
Flore fécale normale
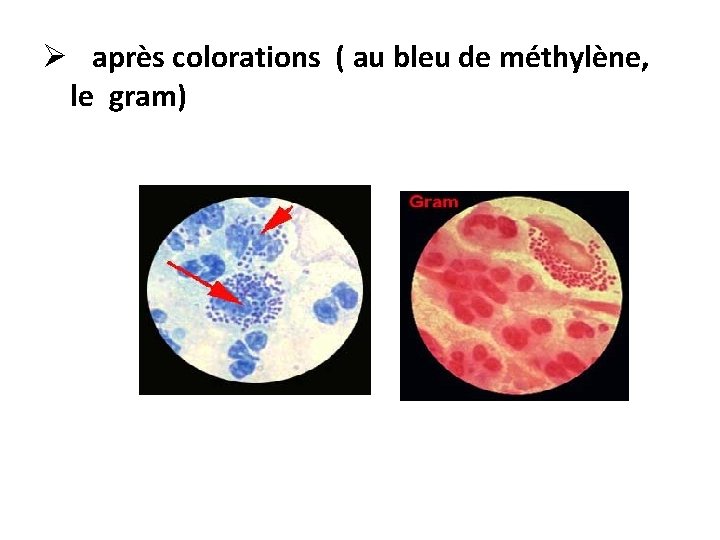
Ø après colorations ( au bleu de méthylène, le gram)



• AUTRES COLORATIONS: Certaines bactéries ne se colorent pas avec la coloration de Gram: Ziehl-Neelsen pour les mycobactéries : coloration des bacilles acido-alcoolo-résistants (BAAR).
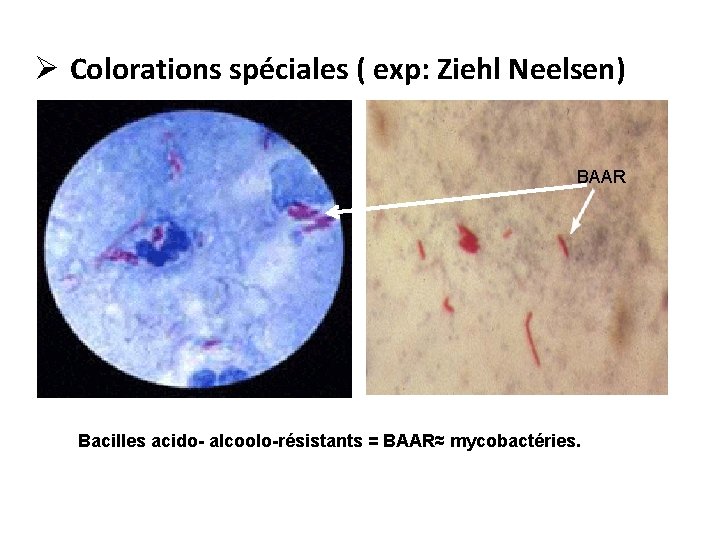
Ø Colorations spéciales ( exp: Ziehl Neelsen) BAAR Bacilles acido- alcoolo-résistants = BAAR≈ mycobactéries.

Coloration à l’auramine lecture au microscope à fluorescence
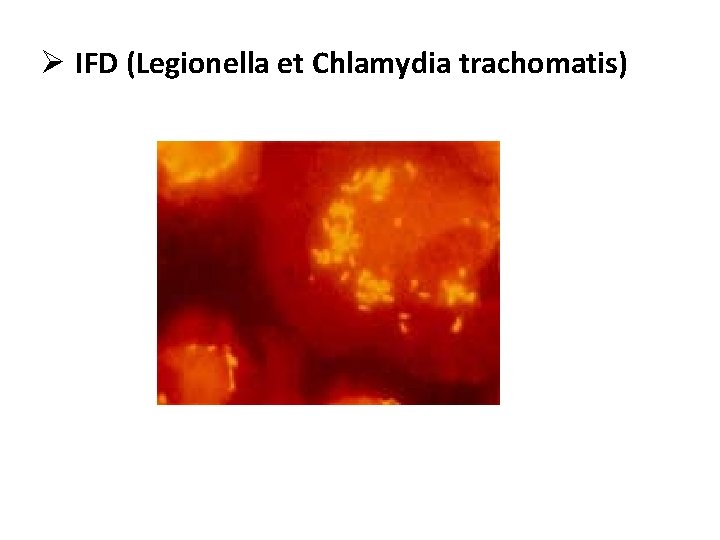
Ø IFD (Legionella et Chlamydia trachomatis)
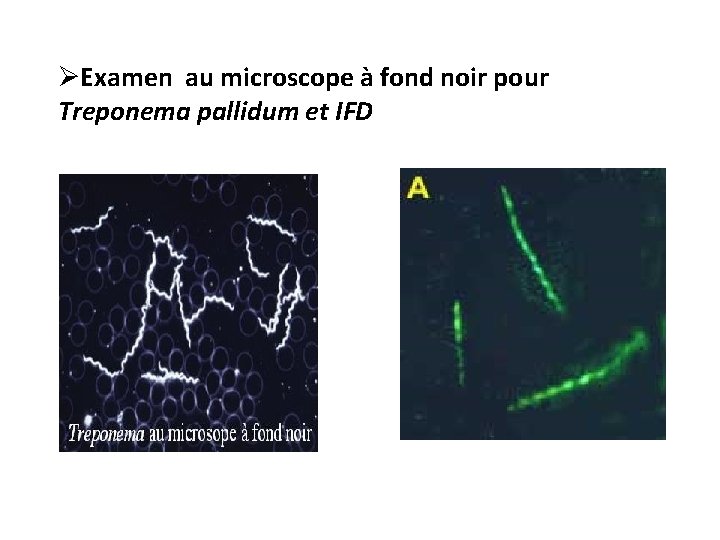
ØExamen au microscope à fond noir pour Treponema pallidum et IFD
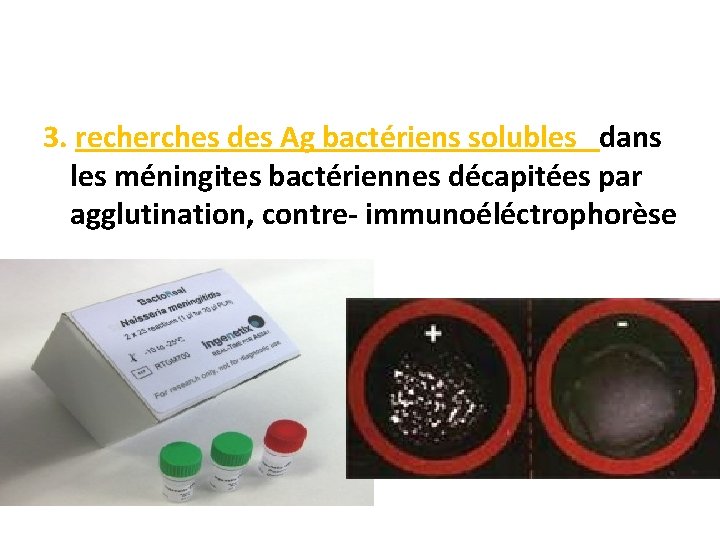
3. recherches des Ag bactériens solubles dans les méningites bactériennes décapitées par agglutination, contre- immunoéléctrophorèse

4. mise en culture et isolement l’isolement sur milieux selon l’orientation clinique, le site anatomique du prélèvement : flore, type d’infection, espèces pathogènes courantes La mise en culture doit être appropriée à la bactérie suspectée Ø Isolement sur milieux de culture - Milieux nutritifs simples - Milieux nutritifs enrichis - Milieux sélectifs Ø Conditions d’incubation - Température ( 37, 30 ou 42° ) - Tension d’oxygène - Tension de CO 2 - Durée d’incubation ( 18 h, 24 h, 48 h, jours ou semaines) Ø obtenir une culture: une bactérie une colonie
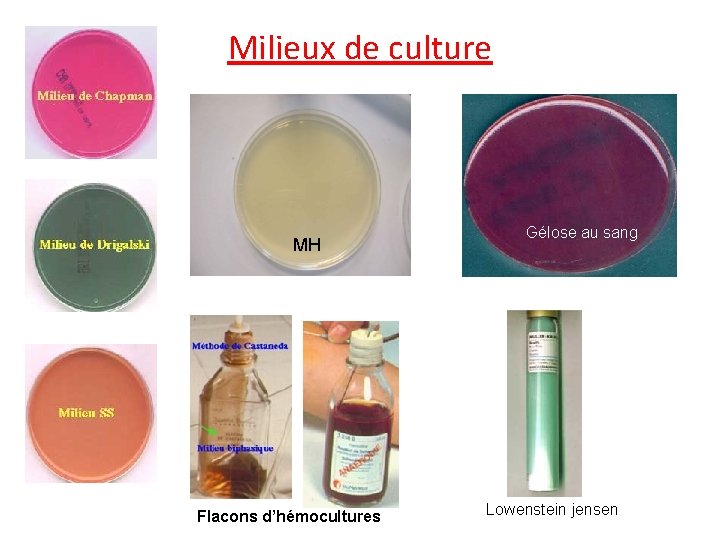
Milieux de culture MH Flacons d’hémocultures Gélose au sang Lowenstein jensen

• Isolement des bactéries : ⇒ milieux solides étalement et isolement en stries pour étaler les bactéries et les isoler les unes des autres. les bactéries se multiplient et donne une colonie visible à l’oeil nu au bout de 18 à 24 h ou plus.

Incubation Etuve Jarres

Automate Bact. Alert® (Biomerieux) pour les hémocultures Leur principal avantage est de détecter automatiquement et très rapidement toute croissance bactérienne en mesurant régulièrement la production de CO 2 due à la multiplication bactérienne

5. Identification des bactéries: à partir de culture pure Ø caractères morphologiques Ø caractères culturaux : ●Aspect des colonies, ●Pigmentation ●Vitesse de croissance Ø caractères biochimiques Ø caractères antigéniques (sérotypie) intérêt épidémiologique exp: salmonella
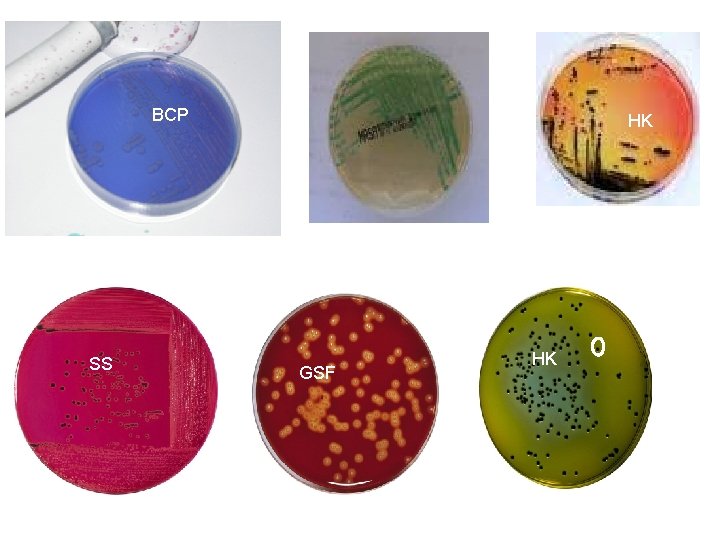
BCP SS HK GSF HK
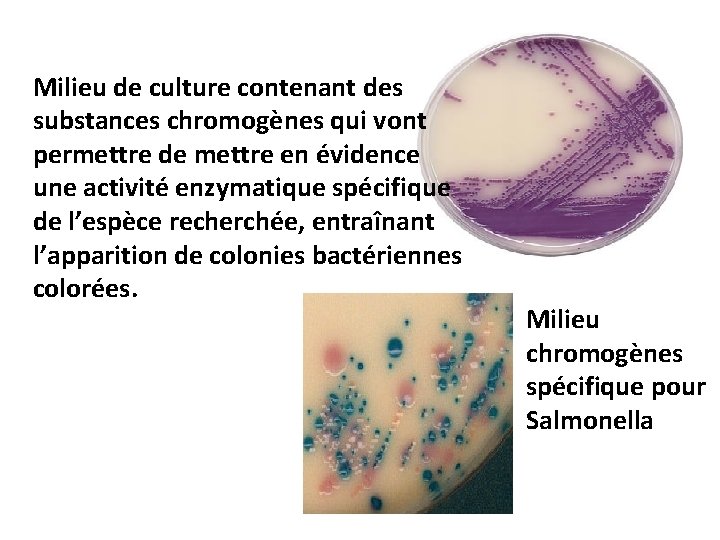
Milieu de culture contenant des substances chromogènes qui vont permettre de mettre en évidence une activité enzymatique spécifique de l’espèce recherchée, entraînant l’apparition de colonies bactériennes colorées. Milieu chromogènes spécifique pour Salmonella
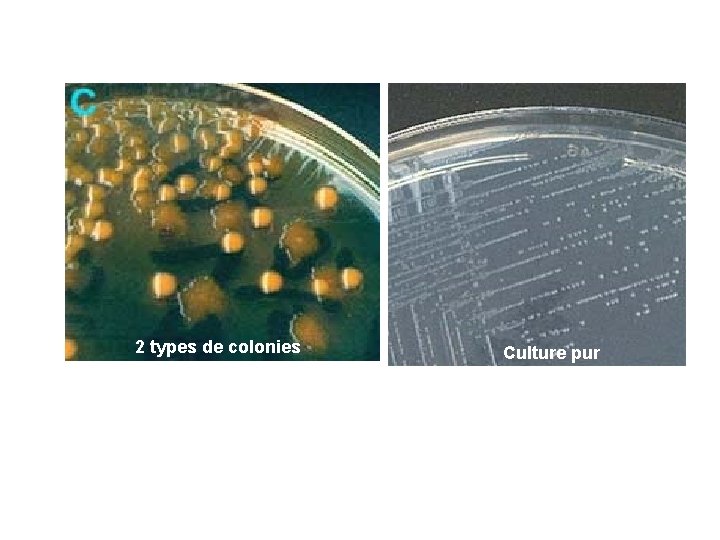
2 types de colonies Culture pur

Corynrbacterium diphteriae
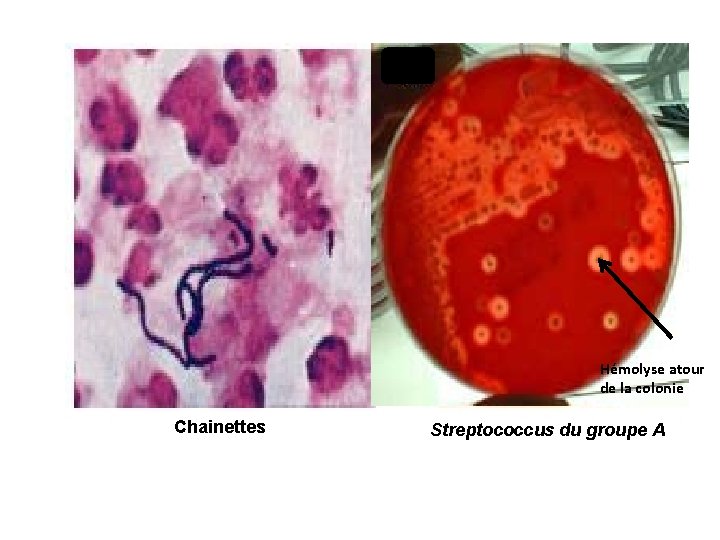
Hémolyse atour de la colonie Chainettes Streptococcus du groupe A
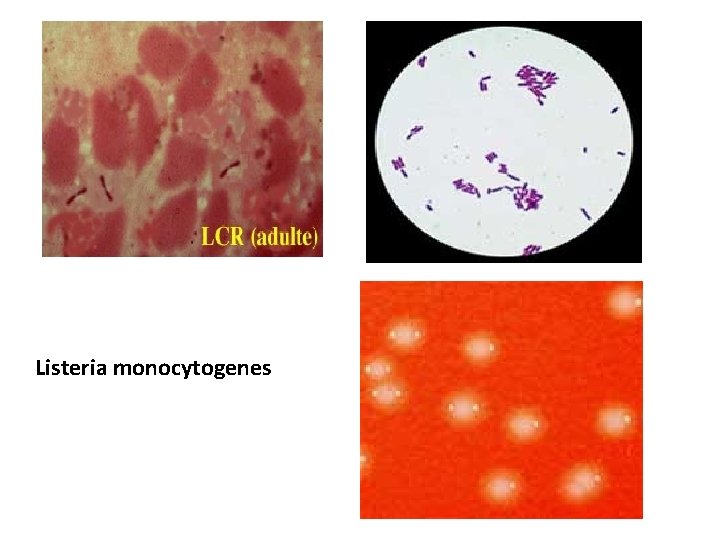
Listeria monocytogenes
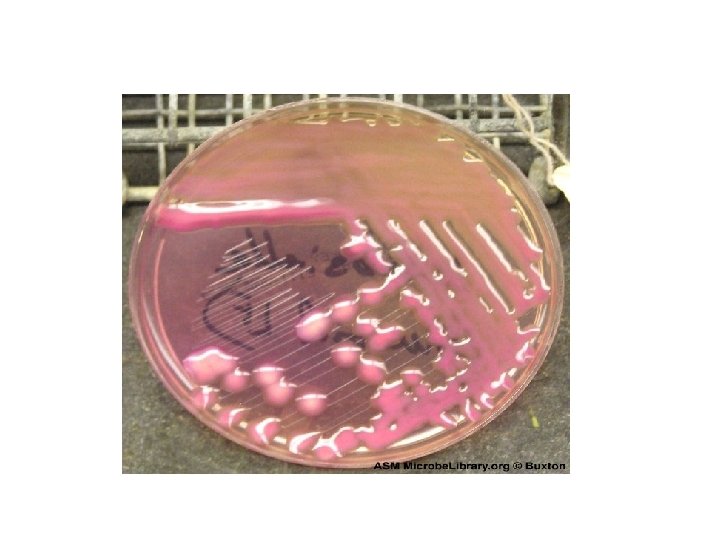
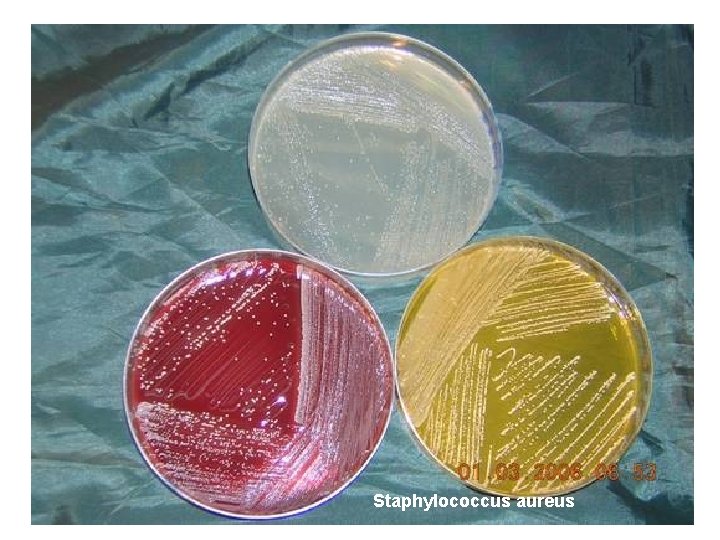
Staphylococcus aureus

Identification de la bactérie (suite) Réalisée sur une population bactérienne « pure » • L’étude microscopique ( état frais et colorations) • Caractères culturaux ( morphologie, durée, conditions physiologiques) • Tests biochimiques explorant le métabolisme glucidique, protidique et lipidique • Tests explorant les conséquences du métabolisme – Détection de produits de dégradation métaboliques ou – d’enzymes impliquées dans la réaction
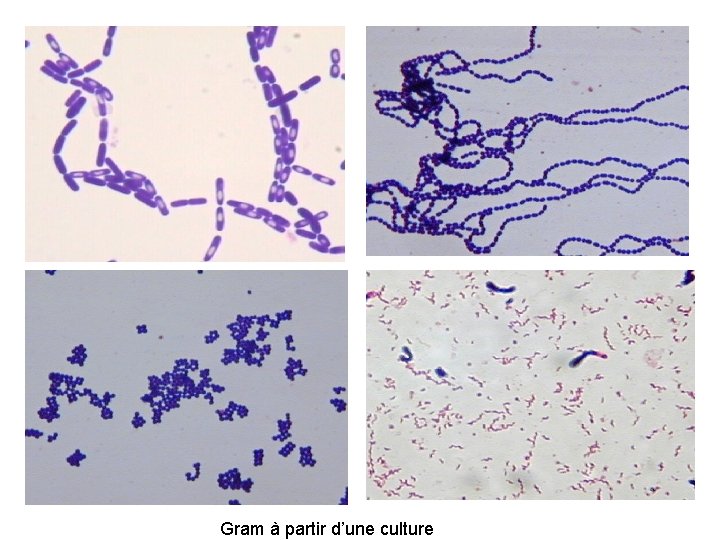
Gram à partir d’une culture
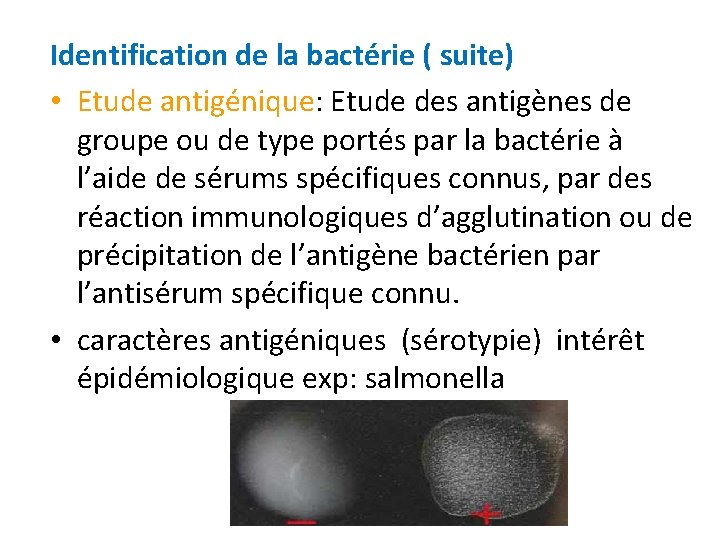
Identification de la bactérie ( suite) • Etude antigénique: Etude des antigènes de groupe ou de type portés par la bactérie à l’aide de sérums spécifiques connus, par des réaction immunologiques d’agglutination ou de précipitation de l’antigène bactérien par l’antisérum spécifique connu. • caractères antigéniques (sérotypie) intérêt épidémiologique exp: salmonella

Tests biochimiques La galerie biochimique d’identification: Contient des tests plus lents (résultat en 4 h à 24 h) basés sur l’étude de la fermentation de sucres et des caractères enzymatiques. + + _ _ +

Automate d'identification Vitek 2® Compact (Bio. Mérieux)
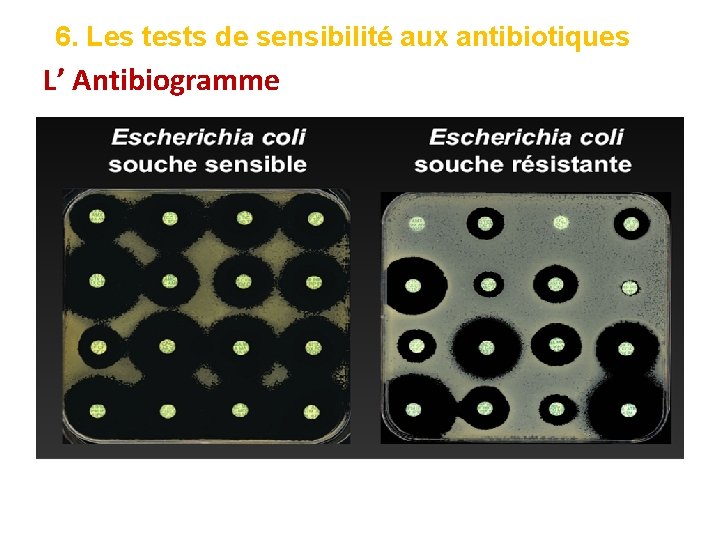
6. Les tests de sensibilité aux antibiotiques L’ Antibiogramme
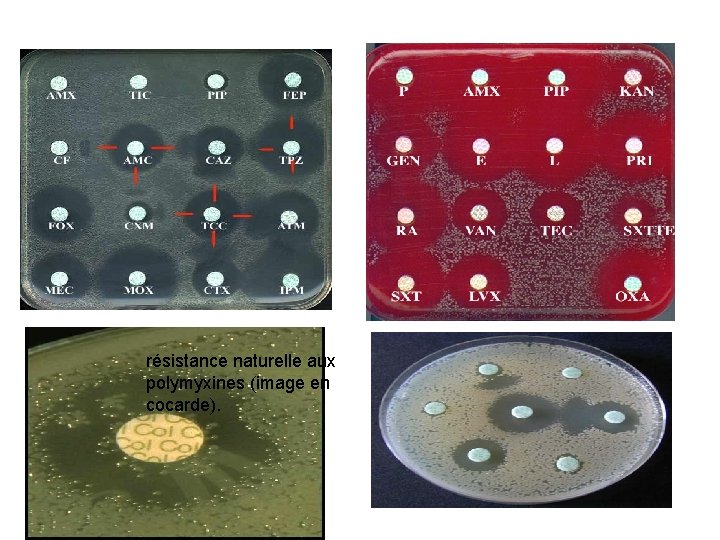
résistance naturelle aux polymyxines (image en cocarde).



DIAGNOSTIC INDIRECT Mettre en évidence la réaction immunitaire de l’organisme infecté: Ø Humorale: production d’anticorps Ø Indications : le diagnostic d’infection due à une bactérie de croissance difficile ou impossible (Syphilis, rickettsiose, leptospirose, maladie de lyme…) Ø Tester 2 sérums à 15 jours d’intervalle.

Recherche des anticorps spécifiques = sérodiagnostic - principe: complexe immun Ag – Ac - Techniques: immuno-précipitation, immunoagglutination, IF et immuno-enzymatique ELISA +++ • Analyse quantitative : titre • Analyse qualitative : classe des Ig, G ou M.
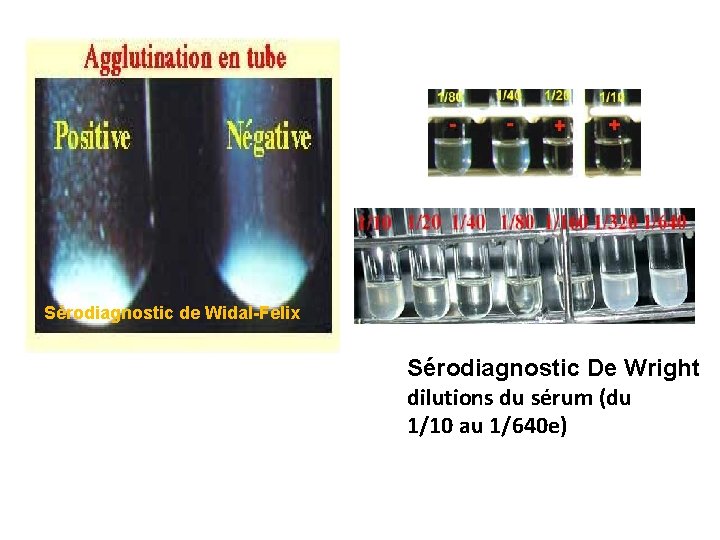
Sérodiagnostic de Widal-Felix Sérodiagnostic De Wright dilutions du sérum (du 1/10 au 1/640 e)
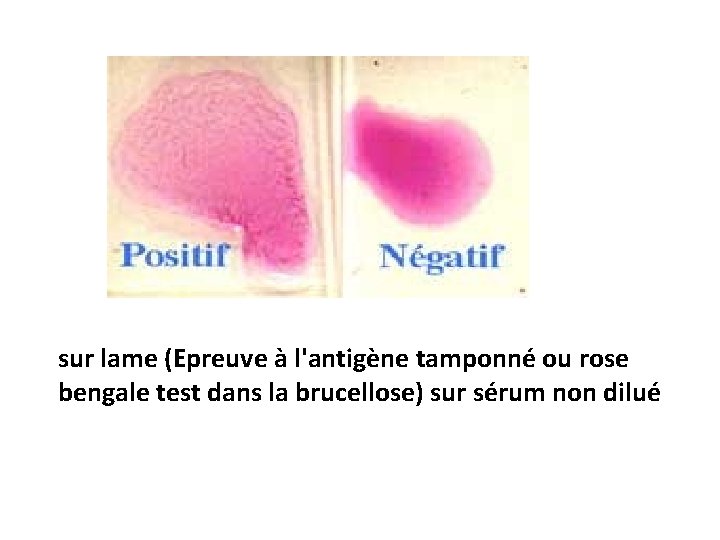
sur lame (Epreuve à l'antigène tamponné ou rose bengale test dans la brucellose) sur sérum non dilué


Quelques exemples de sérodiagnostic: - Brucellose : agglutination (Wright), Antigène tamponné ou Rose bengale - Chlamydioses : ELISA - Legionellose : IFI, ELISA - Lyme (maladie) : ELISA - Mycoplasmes : ELISA - Rickettsioses - Coxiella : IFI - Salmonelloses : anti-typhoparathyphoïdiques (Widal-Félix) par agglutination - Infections à Streptocoques du groupe A : antistreptolysines, anti-strepdornases, antistreptokinases - Syphilis : TPHA, FTA, TPI, ELISA

q La sérologie n’est pas fiable: - Infection ancienne - Vaccination - Antigénnicité croisé pour plus de fiabilité: Ø 02 titrages à 15 jours d’intervalle Ø recherche des Ig. M primo-infection

BIOLOGIE MOLECULAIRE Ø Recherche du génome bactérien: spécificité ++ Ø Intérêt application pour les bactéries non cultivables ou celles à croissance lente ou difficile Ø 02 techniques: - hybridation par les sondes - PCR

Amplification enzymatique in vitro ou polymerase chain réaction (PCR) Ø Consiste à synthétiser in vitro des milliers de copies d’une séquence spécifique de l’ADN bactérien (automates) Ø La révélation du produit amplifié se fait soit par hybridation soit par électrophorèse sur gel d’agarose et visualisation de la bande d’ADN

Principe de la technique PCR 1 - ADN double brin 2 - Dénaturation thermique (ouverture des 2 brins ) 3 - Hybridation des amorces ( sens et anti-sens) 4 - Elongation ou synthèse ( ADN polymérase+ désoxynucléotides) hybridation d’un néo brin d’ADN complémentaire de l’ADN d’origine 5 - Continuation de la réaction par réactions successives de dénaturation/ hybridation sous l’action de la température (chauffage, refroidissement) aboutissant à la fabrication d’un grand nombre de fragments d’ADN copies du fragment original Diagnostic bactériologique. 2007
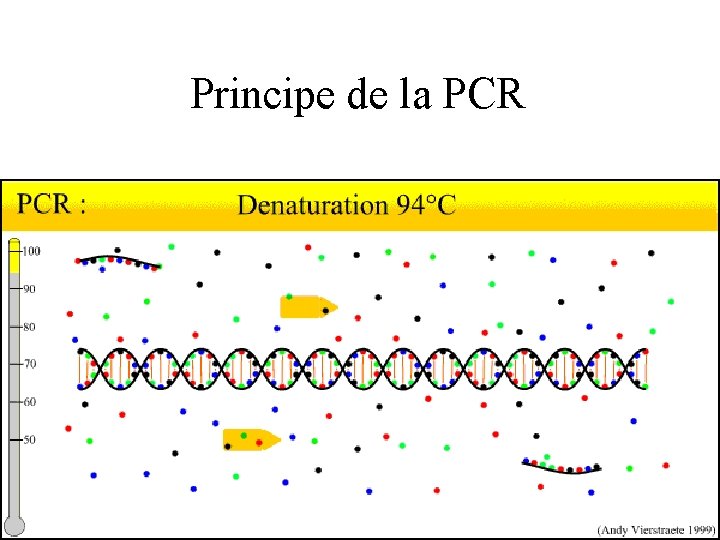
Principe de la PCR
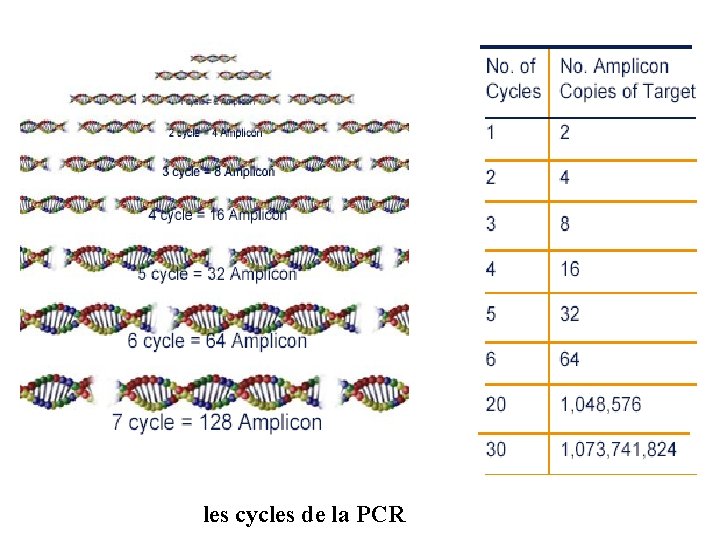
les cycles de la PCR
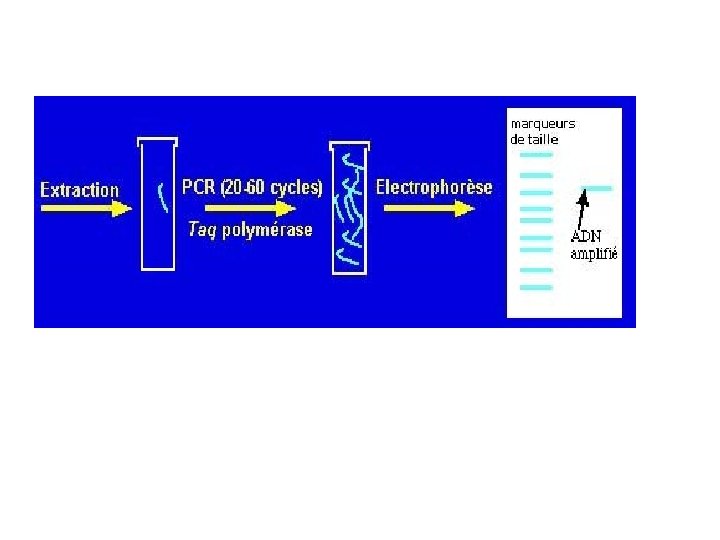

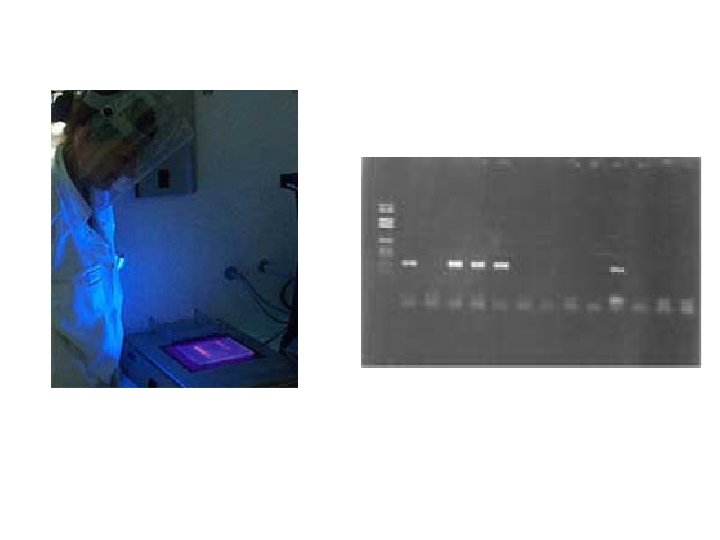

Merci
- Slides: 68