DIABETE MELLITO IN ETA PEDIATRICA Manuela Caruso Dipartimento

DIABETE MELLITO IN ETA’ PEDIATRICA Manuela Caruso Dipartimento di Pediatria Azienda Policlinico Università di Catania

CLASSIFICAZIONE DEL DIABETE (American Diabetes Association) • Diabete tipo 1 o. T 1 DM (diabete insulinodipendente; diabete giovanile) • Diabete tipo 2 o T 2 DM (diabete non insulino-dipendente; diabete dell’adulto) • Tipi specifici di diabete (MODY; LADA; Diabete mitocondriale) • Diabete gestazionale

Diabete Tipo 1 (T 1 DM) Il diabete Tipo 1 è caratterizzato dalla carenza assoluta di insulina, dovuta alla distruzione autoimmunitaria delle beta-cellule pancreatiche, pertanto richiede necessariamente una terapia sostitutiva con insulina

CARATTERISTICHE DEL T 1 DM E DEL T 2 DM • T 1 DM - Tipico del bambino e dell’adolescente - Esordio brusco, spesso in concomitanza con malattie intercorrenti - Tendenza alla chetoacidosi - Produzione di insulina ridotta/assente - Patogenesi: autoimmunitaria - Terapia insulinica sostitutiva indispensabile • T 2 DM - Tipico dell’adulto - Esordio a decorso lento, spesso asintomatico per lungo tempo - Scarsa tendenza alla chetosi - Produzione di insulina normale, o aumentata - Resistenza dei tessuti all’azione dell’insulina (insulinoresistenza) - Spesso associato all’obesità - Curabile con dieta ed antidiabetici orali

EPIDEMIOLOGIA DEL T 1 DM • Incidenza in aumento • Rappresenta il 25% dei casi di diabete • Fattori razziali: più frequente nella razza caucasica • Fattori geografici: gradiente nord-sud

EPIDEMIOLOGIA DEL T 1 DM • In Europa l’incidenza più elevata si osserva nei paesi scandinavi (30 -40 casi/100. 000 anno) • L’incidenza minore si osserva in Grecia • In Italia l’incidenza è molto variabile: § Lombardia 7/100. 000 anno § Sicilia 8 -9/100. 000 anno § Sardegna 30/100. 000 anno
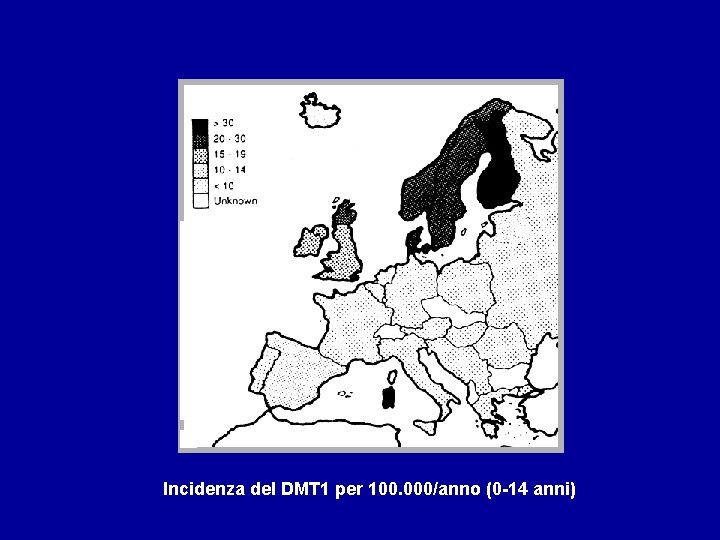
Incidenza del DMT 1 per 100. 000/anno (0 -14 anni)

EZIOPATOGENESI DEL T 1 DM • Fattori genetici • Fattori ambientali • Fattori immunitari

FATTORI GENETICI DEL T 1 DM • Il T 1 DM è una malattia che si sviluppa in soggetti geneticamente predisposti: la predisposizione genetica è conferita da alcuni aplotipi HLA, cioè dalla presenza o dall’assenza di alcuni geni del sistema maggiore di istocompatibilità (MHC)

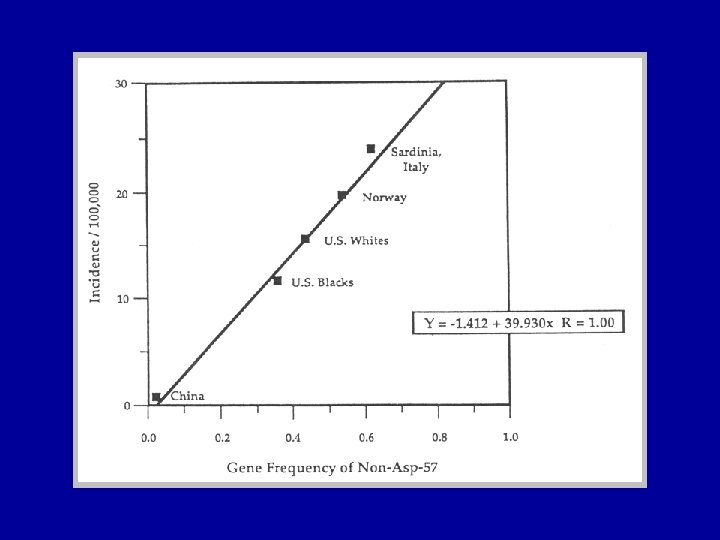
MARKERS GENETICI DI SUSCETTIBILITA’ AL T 1 DM • Rischio aumentato di sviluppare T 1 DM: aplotipo DR 3, DR 4, DQB 1 (non. Asp 57), DQA 1 (Arg 52) • Rischio ridotto di sviluppare. T 1 DM: DR 2, DQB 602

RISCHIO RELATIVO DI SVILUPPARE T 1 DM • • • Omozigoti Eterozigoti DR 3/DR 3 DR 4/DR 4 DR 3/x DR 4/x = 10 = 16 = 33 = 3. 3 = 6. 4

RISCHIO RELATIVO DI SVILUPPARE T 1 DM • • • Popolazione generale 1/400 Nati da madre diabetica 1/66 Nati da padre diabetico 1/40 Fratelli di soggetto diabetico 1/12 – 1/35 Fratelli HLA identici 1/4 Gemelli monocoriali 1/2

FATTORI IMMUNITARI • Fenomeni umorali: presenza di anticorpi ICA (anticorpi antiβcellula), IAA (anticorpi anti -insulina), anti. GAD (anticorpi anti-glutammico decarbossilasi) , IA 2 (anticorpi anti-proteintirosinfosfatasi) , Zn. T 8 (anticorpi anti Zinc Transporter 8) • Fenomeni cellulomediati: ↑ linfociti killers, ↑ linfociti T helper/suppressor • Insulite: infiltrato infiammatorio linfociti T attivati, linfociti B, macrofagi
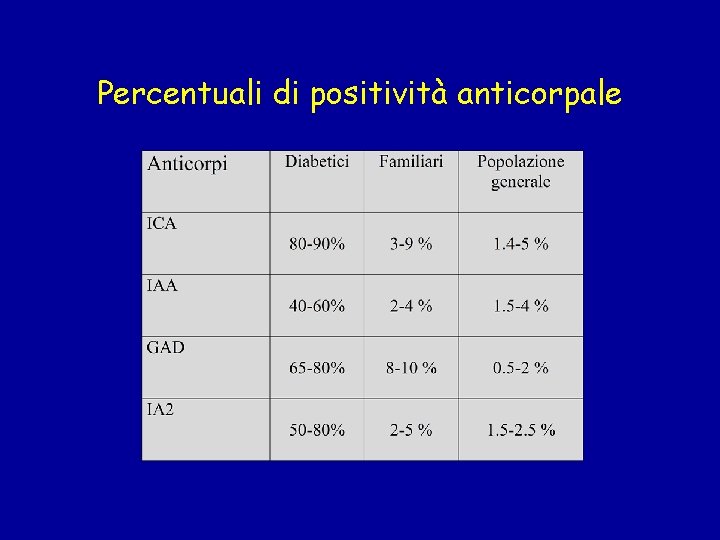
Percentuali di positività anticorpale
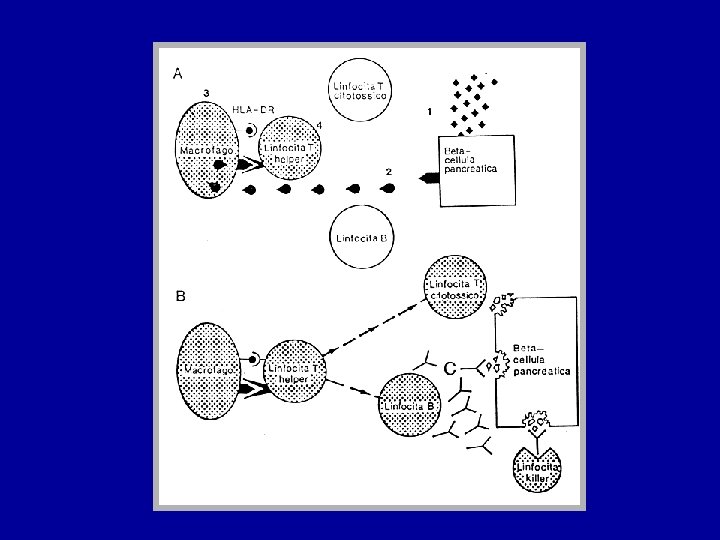

FATTORI AMBIENTALI • Infezioni virali - coxsackie B 1 -B 6 - virus della rosolia - cytomegalovirus - virus della parotite • Dati a favore del ruolo delle infezioni virali - dati anamnestici - stagionalità - isolamento del virus coxsackie B 4 dal pancreas di un paziente - presenza di IFN-α nelle β cellule di pancreas di diabetici

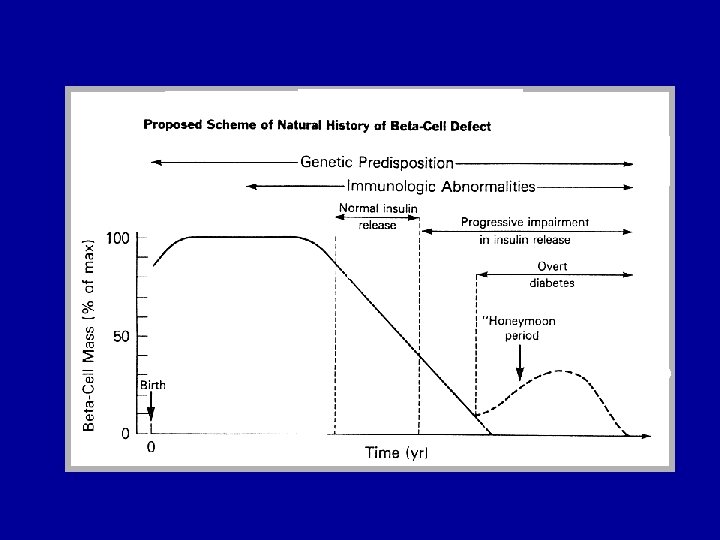
PATOGENESI DEL T 1 DM Genotipo permissivo ↓ e scatenante (insulto virale) ↓ Cellule presentantigeni nuovi/modificati ↓ Risposta autoimmune ↓ Distruzione delle β cellule ↓ DIABETE Fattor

EFFETTI DELL’INSULINA Fegato • Aumento del consumo di glucosio: stimolazione della glicolisi e della glicogenosintesi • Inibizione della gluconeogenesi e della glicogenolisi • Stimolazione della sintesi degli ac. grassi • Inibizione della βossidazione Muscolo/Tessuto Adiposo - Stimolazione del trasporto del glucosio (Glut-1, -4) - Aumento del consumo del glucosio - Inibizione della lipolisi (tessuto adiposo) - Inibizione del catabolismo proteico nel muscolo

EFFETTI DELLA CARENZA DI INSULINA • Iperglicemia→Superamento soglia renale →glicosuria • Glicosuria → Diuresi osmotica→Poliuria • Poliuria →Disidratazione → Polidipsia • Difetto di utilizzazione del glucosio nelle cellule → - Aumento della fame - Astenia - Dimagramento • Uso di substrati energetici alternativi (lipidi) → - Produzione di corpi chetonici (acetone) - Acidosi - Chetonuria

DIAGNOSI DI T 1 DM SINTOMI E SEGNI • • • Polidipsia Poliuria Nicturia Astenia Dimagramento → - iperglicemia - glicosuria - chetonuria

CHETOACIDOSI DIABETCA ALTERAZIONI METABOLICHE • Iperglicemia (>300 mg/dl) • Iperchetonemia (>3 mmol/l) • Acidosi metabolica (p. H < 7. 3 bicarbonati < 15 m. Eq/l) • Manifestazione d’esordio del T 1 DM • Complicanza nel decorso della malattia

FATTORI SCATENANTI LA CHETOACIDOSI DIABETCA • Infezioni • Dose di insulina inadeguata • Omissioni nelle somministrazioni • Esordio della malattia

CHETOACIDOSI DIABETCA QUADRO CLINICO • • • Polidipsia Poliuria Alito acetonemico Vomito Dolori addominali Astenia Obnubilamento del sensorio → Coma Disidratazione Respiro profondo e frequente (respiro di Kussmaul)


CHETOACIDOSI DIABETCA La chetoacidosi diabetica è un’emergenza medica, dovuta ad una condizione dismetabolica grave che può evolvere sino al coma e alla morte se non trattata tempestivamente ed adeguatamente Cardini della terapia sono: • Idratazione • Terapia insulinica • Terapia elettrolitica • Alcalinizzanti (raramente)

CHETOACIDOSI DIABETICA TERAPIA REIDRATANTE • 1°- 2° ora : 5 -8 ml/kg/ora di Na. Cl 0. 9% • Dalla 3° alla 24° ora: 2 -2. 5 ml/kg/ora • Quando la glicemia scende al di sotto di 250 mg% sostituire la fisiologica con glucosata (5 -10%) • L’idratazione favorisce l’utilizzo dell’insulina endogena e aumenta il filtrato glomerulare

CHETOACIDOSI DIABETICA: TERAPIA INSULINICA • Glicemia > 250 mg% e/o p. H < 7. 25 : infusione e. v. di insulina alla dose di 0. 1 U/kg/ora (0. 05 se età < 5 aa) • Glicemia < 250 mg% e/o p. H > 7. 25 : dose di insulina 0. 05 U/kg/ora (0. 03 se età < 5 aa) • La dose di partenza va modificata sulla base del monitoraggio della glicemia (ogni 1 -2 ore) • L’infusione e. v. di insulina va proseguita sino a normalizzazione del p. H e della chetonemia e scomparsa della chetonuria • La terapia insulinica permette l’utilizzazione del glucosio e di conseguenza blocca la chetogenesi, corregge l’acidosi e normalizza il metabolismo glucidico, protidico e lipidico

CHETOACIDOSI DIABETCA TERAPIA ALCALINIZZANTE • Da evitare se p. H > 7. 10 • Se necessaria applicare la formula: BE (eccesso Basi) x kg peso x 0. 05 • Somministrare con cautela: la correzione rapida dell’acidosi favorisce l’edema cerebrale

CHETOACIDOSI DIABETCA TERAPIA CON ELETTROLITI • POTASSIO: somministrare (in presenza di diuresi) dalla 2°-3° ora, indipendentemente dal valore della kaliemia (no se iperkaliemia), alla dose di 0. 1 -0. 2 m. Eq/kg/ora nei liquidi di infusione (50% KCl, 50% KPO 4) • SODIO: se > 150 m. Eq/l utilizzare Na. Cl 0. 45%

TERAPIA del T 1 DM Scopi della terapia sono: • Una crescita regolare • Lo svolgimento delle normali attività di un soggetto di pari età • Un normale sviluppo puberale • Una sopravvivenza più lunga possibile e libera dalle complicanze della malattia

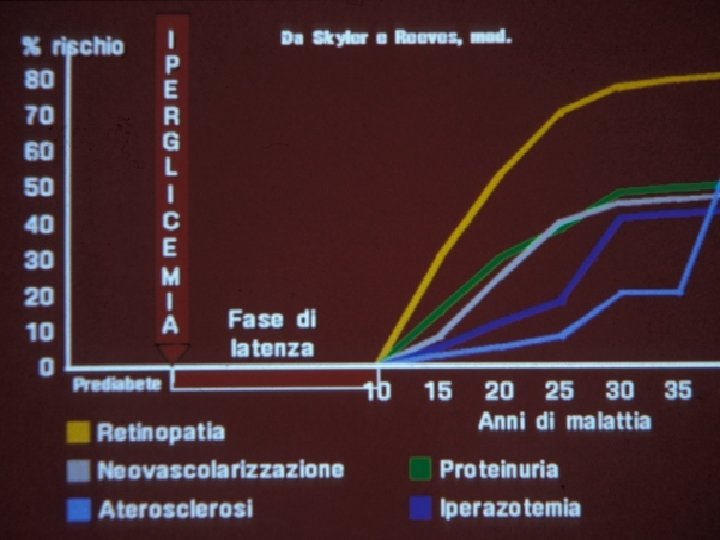
COMPLICANZE • Acute → Metaboliche • Croniche → Macrovascolari → Microvascolari Retinopatia Nefropatia Neuropatia

TERAPIA del T 1 DM Obiettivo a breve termine della terapia, necessario per raggiungere gli scopi finali è: • Ottenere un buon controllo glicemico, cioè valori glicemici e di emoglobina glicosilata (Hb. A 1 c) il più possibile vicini alla norma

CONTROLLO GLICEMICO DEL T 1 DM • Valori glicemici ideali: glicemia preprandiale entro 140 mg/dl; glicemia postprandiale entro 180 mg/dl • L’Hb. A 1 c è la frazione dell’emoglobina circolante legata al glucosio ed è direttamente proporzionale ai valori glicemici medi dei 3 mesi precedenti la determinazione (vita media dei globuli rossi) • L’Hb. A 1 c normale è inferiore al 5 -6%; nei soggetti diabetici l’obiettivo è mantenere l’Hb. A 1 c < 7. 5% • Uno stretto controllo glicemico è in grado di prevenire le complicanze

TERAPIA del T 1 DM Cardini fondamentali della terapia sono: • Insulina • Autocontrollo e autogestione • Alimentazione corretta • Attività fisica

FORME DI INSULINA • Insulina umana Rapida (Pronta, Regolare) Intermedia Ultralenta • Analoghi dell’insulina Analoghi ultrarapidi Analoghi ultralenti
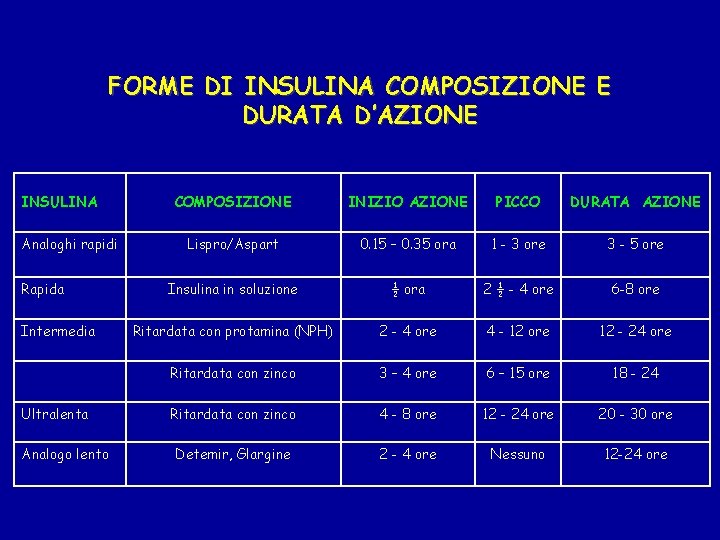
FORME DI INSULINA COMPOSIZIONE E DURATA D’AZIONE INSULINA Analoghi rapidi Rapida Intermedia Ultralenta Analogo lento COMPOSIZIONE INIZIO AZIONE PICCO DURATA AZIONE Lispro/Aspart 0. 15 – 0. 35 ora 1 - 3 ore 3 - 5 ore Insulina in soluzione ½ ora 2 ½ - 4 ore 6 -8 ore Ritardata con protamina (NPH) 2 - 4 ore 4 - 12 ore 12 - 24 ore Ritardata con zinco 3 – 4 ore 6 – 15 ore 18 - 24 Ritardata con zinco 4 - 8 ore 12 - 24 ore 20 - 30 ore Detemir, Glargine 2 - 4 ore Nessuno 12 -24 ore
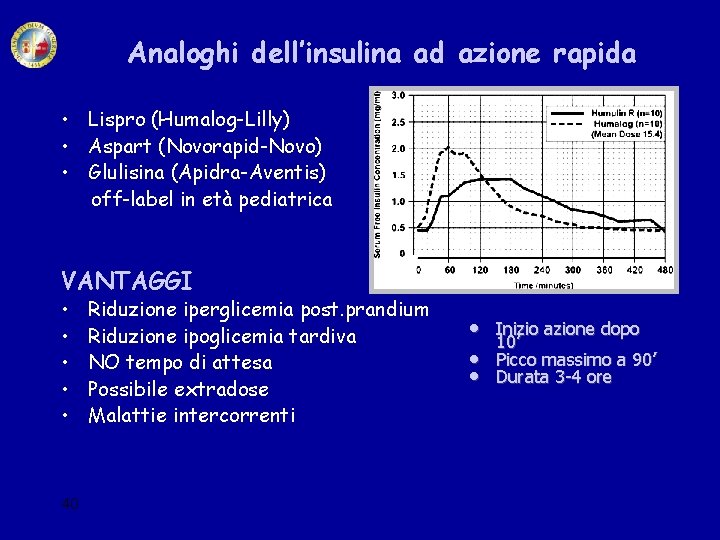
Analoghi dell’insulina ad azione rapida • Lispro (Humalog-Lilly) • Aspart (Novorapid-Novo) • Glulisina (Apidra-Aventis) off-label in età pediatrica VANTAGGI • • • 40 Riduzione iperglicemia post. prandium Riduzione ipoglicemia tardiva NO tempo di attesa Possibile extradose Malattie intercorrenti • • • Inizio azione dopo 10’ Picco massimo a 90’ Durata 3 -4 ore
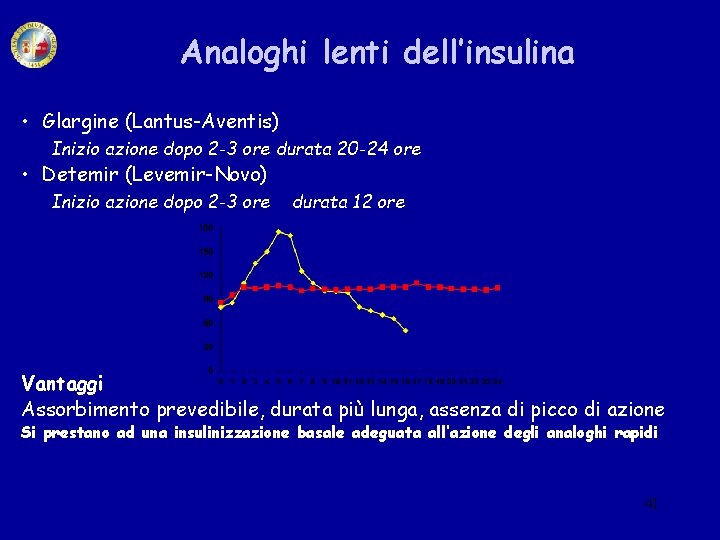
Analoghi lenti dell’insulina • Glargine (Lantus-Aventis) Inizio azione dopo 2 -3 ore durata 20 -24 ore • Detemir (Levemir-Novo) Inizio azione dopo 2 -3 ore durata 12 ore Vantaggi Assorbimento prevedibile, durata più lunga, assenza di picco di azione Si prestano ad una insulinizzazione basale adeguata all’azione degli analoghi rapidi 41

Miscele con analoghi dell’insulina • Humalog mix 25 • Novomix 30 • Humalog mix 50 • Novomix 50 • Novomix 70 • Le miscele sono poco maneggevoli poiché non consentono “l’adattamento dose”, • ma possono rivelarsi utili, specie nei più piccoli, allo scopo di risparmiare qualche puntura 42

INSULINA PER VIA INALATORIA FASE SPERIMENTALE • Biodisponibilità • Variazioni dell’assorbimento • Danno locale da fagocitosi endoalveolare • Frequenza dosi • Quantità per dose • Definizione di strumenti di precisione per l’erogazione

Il microinfusore “gold-standard” della terapia insulinica • Estrema plasmabilità della velocità basale • Adeguamento al diverso fabbisogno insulinico nei vari momenti della giornata • Profili basali diversi nei diversi giorni della settimana • Erogazione di boli (programmati o no) • Efficace compenso di fenomeni alba e crepuscolo • 7 • 1 U/h • 0. 9 U/ 44 h • 14 • 24 • 1. 4 U/h h U/ 2. 1 • • 20
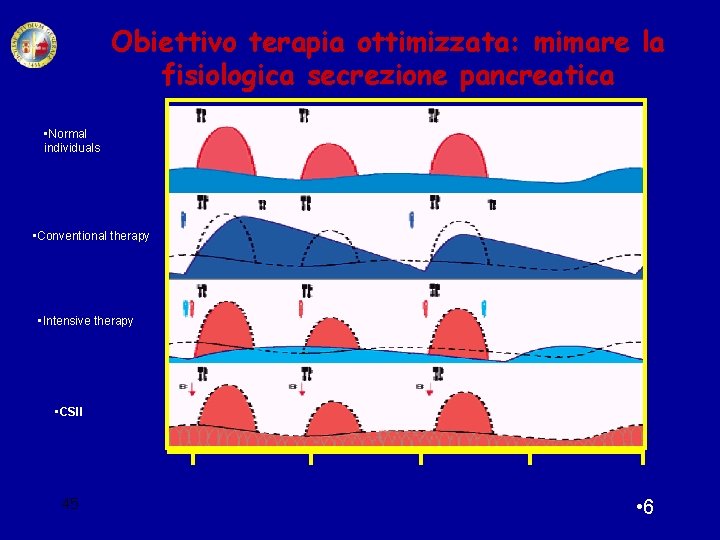
Obiettivo terapia ottimizzata: mimare la fisiologica secrezione pancreatica • Normal individuals • Conventional therapy • Intensive therapy • CSII • 6 45 • 12 • 18 • 24 • 6

………. IL PRESENTE
Set infusionale

DOSE GIORNALIERA DI INSULINA Il fabbisogno quotidiano di insulina varia notevolmente tra gli individui e cambia con il tempo. Pertanto il dosaggio di insulina richiede una regolare revisione ed un periodico aggiustamento Linee guida per il dosaggio • All’esordio: circa 1. 0 U/kg/die (> se chetoacidosi) • Remissione: ≤ 0. 5 U/kg/die • In età prepuberale (periodo di stato): 0. 7 -1. 0 U/kg/die • Pubertà: 1. 0 - 1. 5 U/kg/die

FATTORI INFLUENZANTI IL FABBISOGNO INSULINICO • Aumentata resistenza insulinica alla diagnosi • Residua capacità secretoria β-cellulare • Attività fisica e stile di vita • Tipo di alimentazione • Struttura fisica • Malattie acute e croniche • Alterazioni del sottocutaneo

FATTORI DA VALUTARE NELLA SCELTA DELLO SCHEMA TERAPEUTICO • Residua capacità secretoria β-cellulare • Stile di vita (attività fisica, orario e numero dei pasti) • Capacità di autogestione • Motivazione psicologica al trattamento • Eventuale presenza di complicanze • Eventuale associazione con altre condizioni morbose
Istruzione ↓ Autocontrollo ↓ Autogestione →Adattamento terapia ↓ Buon Controllo Glicemico

AUTOCONTROLLO • E’ il più grande cambiamento avvenuto nella gestione del diabete negli ultimi decenni • Si propone di ottenere uno stretto controllo della malattia senza rendere il bambino e la famiglia totalmente dipendente dalla struttura sanitaria • Richiede per essere effettuato di conoscenze di base e pratiche sul diabete (istruzione) • Passa attraverso tre tappe fondamentali: il controllo della glicemia, il controllo di glicosuria e chetonuria, l’adattamento delle dosi di insulina

AUTOGESTIONE: ADATTAMENTO DELLE DOSI DI INSULINA • E’ il tassello finale del mosaico e presuppone, oltre alle informazioni raccolte tramite l’autocontrollo, una certa esperienza • Partendo dalle dosi prescritte dal pediatra diabetologo la famiglia dovrà imparare ad adattare la dose di insulina sulla base del riscontro di iperglicemia, ipoglicemia o preventivamente in relazione ad una modifica nell’assunzione del cibo e nell’attività fisica • Non è consigliabile comunque variare troppo frequentemente e repentinamente la dose di insulina in relazione all’iper- o all’ipoglicemia, ma dopo aver verificato che il dato si ripresenta ripetutamente agli stessi orari

L’IPOGLICEMIA • E’ la più frequente complicanza acuta del diabete in età pediatrica : dovuta ad una terapia insulinica non adeguata o ad una non corretta stima dell’interazione tra cibo, attività fisica e trattamento insulinico • Sintomi e segni di origine neuroglicopenica: debolezza, cefalea, disturbi della visione, difficoltà nel parlare, capogiro, irrequietezza, irritabilità incubi notturni convulsioni, emiparesi transitoria, coma • Sintomi e segni di origine neurogenica (colinergica o adrenergica): sudorazione, fame, tremore, tachicardia, dolori addominali, pallore, palpitazioni

TRATTAMENTO DELL’IPOGLICEMIA • LIEVE O MODERATA (grado 1 o 2) - Carboidrati semplici a rapido assorbimento: 10 -20 gr di glucosio o saccarosio (zollette di zucchero) o 100 ml di bevande dolci (coca-cola, succo di frutta); aspettare 10 -15 minuti, poi ripetere la somministrazione se la crisi non si risolve - Carboidrati a lento assorbimento: non appena i sintomi di ipoglicemia migliorano somministrare carboidrati complessi (pane, fette biscottate)i • GRAVE (grado 3) (alterazione dello stato di coscienza) - Glucagone: 0. 5 -1. 0 mg per via i. m. o s. c. – Glucosio per via endovenosa: 3 -5 ml/kg di glucosata al 10%
Alimentazione Attività fisica Terapia insulinica

“DIETA PER DIABETICI” PRECONCETTI ERRATI üApporto energetico fisso, non modificabile üRiduzione dei carboidrati üAumento della quota di proteine e grassi üImpiego di “alimenti speciali per diabetici”

COMPOSIZIONE DELLA DIETA NEL DMT 1 ü La dieta deve contenere tutti i nutrienti essenziali in quantità ottimali ü Deve aiutare a controllare i livelli glicemici ü Deve cercare di compensare il rischio aterogenetico
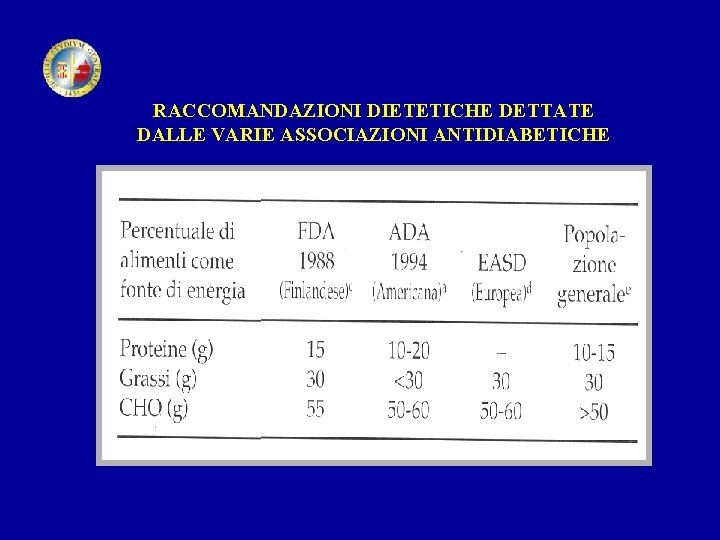
RACCOMANDAZIONI DIETETICHE DETTATE DALLE VARIE ASSOCIAZIONI ANTIDIABETICHE

PRODOTTI PER DIABETICI ü Contengono spesso fruttosio ü Sono ricchi in lipidi e ipercalorici ü Inducono il paziente ad eccessi ü Sono molto costosi ü Possono avere effetto lassativo ü Consigliabili le bevande che contengono dolcificanti non calorici

Alimentazione Attività fisica Terapia insulinica

BENEFICI DELL’ATTIVITÀ FISICA ü Crescita armonica ü Relazione con i coetanei ü Mantenimento del peso ideale ü ↓ Glicemia ü ↓ Colesterolo totale ü ↑ Colesterolo HDL ü Dosi ottimali di insulina

PREVENZIONE DELL’IPOGLICEMIA INDOTTA DALL’ESERCIZIO FISICO ü Educazione - sull’interazione tra insulina, cibo ed esercizio fisico - sui segni e sintomi di ipoglicemia durante l’esercizio ü Aggiustamenti della terapia insulinica ü Supplementi calorici

ALIMENTAZIONE E DIABETE ü L’alimentazione è una pietra miliare nel trattamento del DMT 1 ü L’obiettivo di una corretta alimentazione, che ha sostituito la “dieta per diabetici”, non è facilmente raggiungibile ma è sicuramente il tramite migliore, insieme alla terapia insulinica, per raggiungere l’obiettivo finale che è quello di assicurare un normale sviluppo, una buona qualità di vita e una sopravvivenza scevra da complicanze più lunga possibile

STRATEGIE EDUCAZIONALI ü La “dieta” deve essere facilmente attuabile ü Deve potersi adattare alle abitudini di vita del paziente ü Deve tener conto dello stato socioculturale, economico e delle usanze etniche ü La “dieta” deve basarsi su un processo continuo di educazione alimentare

OBIETTIVI DELL’EDUCAZIONE ALIMENTARE ü Coinvolgimento di tutta la famiglia e graduale responsabilizzazione del paziente sino al raggiungimento dell’autonomia nell’adolescente ü Istruzione su: calorie, nutrienti, piramide alimentare, equivalenti e liste di scambio ü Indurre modifiche del comportamento ü Raggiungere la capacità di autogestire le nozioni acquisite per adattare l’alimentazione a situazioni non routinarie come attività fisica non programmata, feste, vacanze
- Slides: 66