Di Qumica 4 Medio Profesor Bastin Crdenas G

Di. Química 4º Medio Profesor Bastián Cárdenas G
2 Ruta de aprendizaje • Objetivo: Resolver ejercicios de ácido y base de acuerdo a lo planteado en clases. • Contenido 1. 2. 3. 4. 5. Teorías ácido base Ácido y base fuerte o debil Producto iónicos Ph y p. OH Concentraciones • Cierre de clases

Completar la siguiente tabla según corresponda: 3
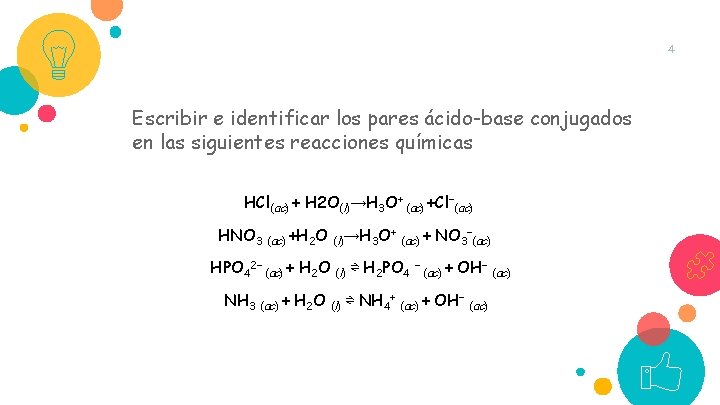
4 Escribir e identificar los pares ácido-base conjugados en las siguientes reacciones químicas HCl(ac) + H 2 O(l)→H 3 O+ (ac) +Cl−(ac) HNO 3 + (ac) +H 2 O (l)→H 3 O (ac) + HPO 42− (ac) + H 2 O (l) ⇌ H 2 PO 4 NH 3 (ac) + H 2 O (l) ⇌ NH 4+ − NO 3−(ac) + OH− (ac)

5 Una avispa al picar vierte un líquido picante, que vira al rojo en el papel tornasol. ¿El líquido expulsado por la avispa es ácido o base? Argumente su respuesta. Escriba la reacción que tendria con agua, si la formula del líquido es HA
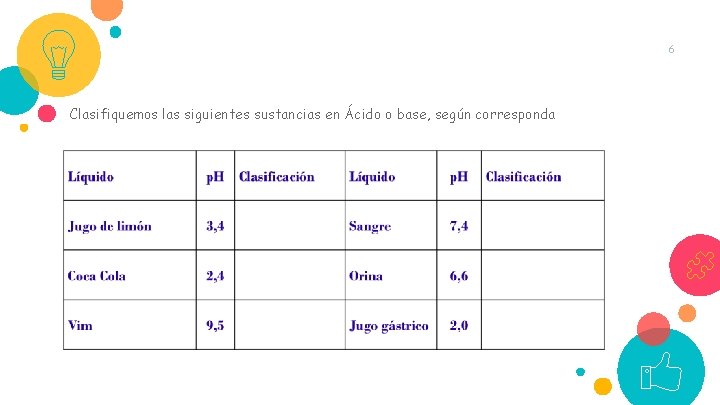
6 Clasifiquemos las siguientes sustancias en Ácido o base, según corresponda
![7 Una disolución tiene una concentración de [OH-] = 3, 56 x 10 -6 7 Una disolución tiene una concentración de [OH-] = 3, 56 x 10 -6](http://slidetodoc.com/presentation_image_h2/00afb802241055da02573fe44c726678/image-7.jpg)
7 Una disolución tiene una concentración de [OH-] = 3, 56 x 10 -6 M, determine la concentración de [H+] Una disolución presenta una concentración de [H+] = 5, 322 x 10 -3 M, determine la concentración de [OH-]

“ Determine el ph y el p. OH de la siguientes disoluciones acuosas: 5, 7× 10 -4 M de HCl 0, 92 M de KOH 3, 9× 10 -3 M de Ba(OH) 2 4, 5× 10 -5 M de HNO 3 8, 5× 10 -2 M de Na. OH 8
![9 Determine la [H+] y la [OH-] en las siguientes disoluciones: Tomate p. H= 9 Determine la [H+] y la [OH-] en las siguientes disoluciones: Tomate p. H=](http://slidetodoc.com/presentation_image_h2/00afb802241055da02573fe44c726678/image-9.jpg)
9 Determine la [H+] y la [OH-] en las siguientes disoluciones: Tomate p. H= 4, 2 Sangre p. OH= 8 Agua p. H= 7 Orina p. H= 5, 3 Jabon liquido p. OH= 10

10 Ácido base Presentes en nuestra cotidianidad
- Slides: 10