Dficit prjonctionnel NN ou prmaturs rinnervation dbutante Dficit


• Déficit pré-jonctionnel : NN ou prématurés • • réinnervation débutante Déficit pré-synaptique: LEMS Déficit post-synaptique : MG Déficit péri-jonctionnel : organophosphorés neuromyotonie Déficit post-jonctionnel : myotonia congenita
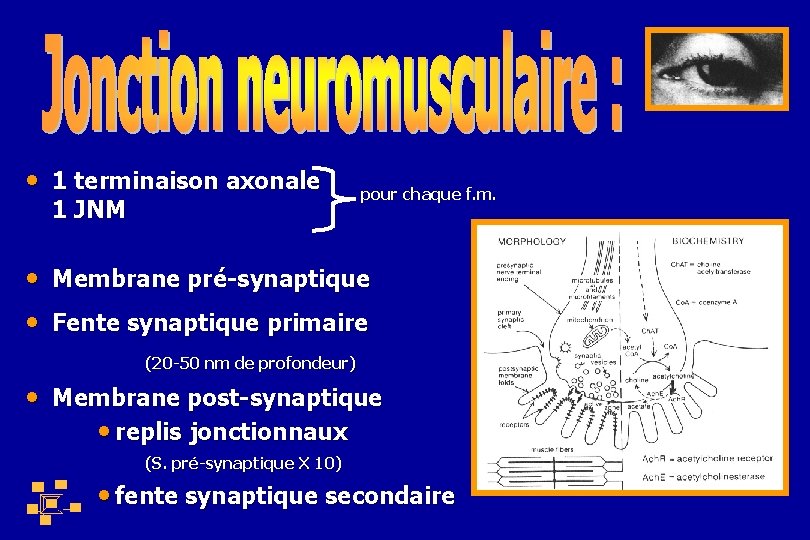
• 1 terminaison axonale 1 JNM pour chaque f. m. • Membrane pré-synaptique • Fente synaptique primaire (20 -50 nm de profondeur) • Membrane post-synaptique • replis jonctionnaux (S. pré-synaptique X 10) • fente synaptique secondaire

• PA axonal • Ouverture de canaux calciques • • pré-synaptiques voltage-dépendants Entrée de Ca 2+ Libération d’Ach par exocytose dans la fente synaptique (100 µs après l’entrée du Ca 2+)

• Ach se fixe sur RAch (canaux ioniques) • Ouverture des RAch pendant 1 -2 ms • Phase acendante du PPM • Em tend vers une valeur intermédiaire entre ENa (+ 45 m. V) et EK (- 80 m. V) : ± - 15 m. V • Courant ionique net entrant (principalement Na+) qui charge la capacité membranaire • Fermeture des RAch • Phase descendante du PPM (décharge passive de la capacité membranaire)

• Courants transmis électrotoniquement de • • la plaque motrice dépolarisée vers la membrane musculaire au repos Déclenchement d’un PAm transmis vers chaque extrémité de la fibre Canaux sodiques, situés dans la profondeur des replis synaptiques secondaires, améliorent la capacité d’un PPM de générer un PAm

• Choline + acétyl~Co. A CAT Ach + Co. A (cytoplasme de la terminaison axonale) • Ach incorporée dans des vésicules (30 -50 nm Ø) • 6. 000 -10. 000 molécules d’Ach/vésicule • 50 -300 vésicules libérées/PAa • 3 types de vésicules : immédiatement libérable (1. 0002. 000), réserve mobilisable (10. 000), réserve principale (300. 000)

• Glycoprotéine (PM : 290. 000) au sommet des • • • replis jonctionnaux 5 sous-unités entourant un pore central 2 sites de fixation pour l’Ach Longueur : 14 nm, Ø : 8 nm Ø de la région la plus étroite du pore : 6, 5 Å 15. 000/20. 000 RAch/µm² Synthèse : 1 h, incorporation dans la m. : 3 h, 1/2 vie : 8 -11 jours

• Couvre les fentes synaptiques secondaires • • ± 23. 000 sites/plaque ± 3. 000 molécules/µm² Ach. E Ach choline + acétate Ach est détruite avant l’induction d’un second PAm

• 1 Quantum = 1 vésicule d ’Ach 1 PPMm (0, 5 -1 m. V) • Au repos : libération spontanée 1 -2 quanta/s 1 -2 PPMm non transmis à la fibre • PAa : 50 -300 quanta 50 -300 PPMm PPM PAm

• Chez le sujet sain, le PAa entraîne toujours un Pam • FS = PPM Seuil PA – Em • FS dépend : quantité d’Ach libérée nombre de RAch LEMS MG {canaux Na+} post-synaptiques MG

• Dépression synaptique (2 -3 Hz) Epuisement des vésicules immédiatement disponibles pour le processus d’éjection • Facilitation synaptique (> 5 Hz) Q Ach libérée = k Q Ca 4 (toute quantité résiduelle de calcium au moment où survient un nouveau PAa facilitera fortement la libération d’Ach)
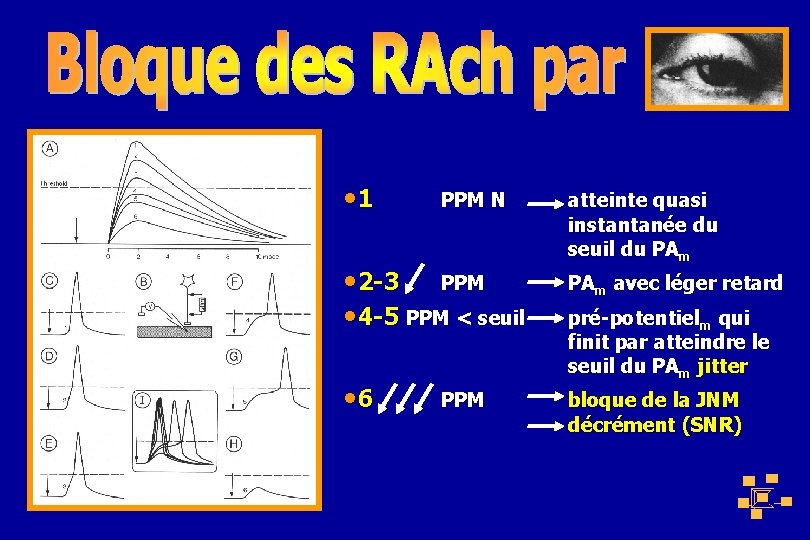
• 1 PPM N • 2 -3 PPM • 4 -5 PPM < seuil • 6 PPM atteinte quasi instantanée du seuil du PAm avec léger retard pré-potentielm qui finit par atteindre le seuil du PAm jitter bloque de la JNM décrément (SNR)

• • Q Ach libérée normale Attaque autoimmune dirigée contre les RAch réduction du PPMm réduction PPM • Destruction de la membrane post-synaptique diminution {canaux Na+} augmentation du seuil PAm FS « débordé » au niveau de certaines JNM

• Le décrément du PPM est physiologique (dépression synaptique) • Certaines JNM sont en bloc partiel qui survient à la 2 e, 3 e, 4 e ou 5 e stimulation • Certaines JNM sont en bloc total • Lors d’une SNR supramaximale, qui sollicite toutes les JNM, le nombre de f. m. qui sont le siège d’un PA diminue de la 1ère à la 5 e stimulation 1 -5 = décrément myasthénique = - 100. 1
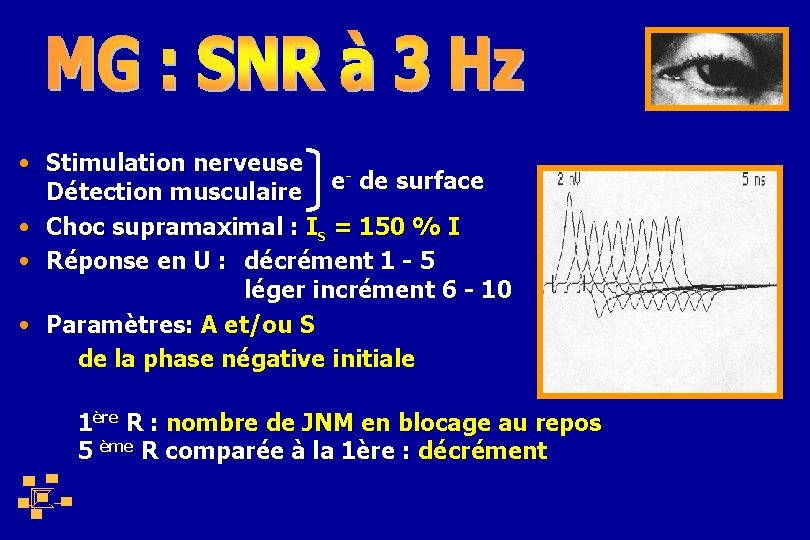
• Stimulation nerveuse - de surface e Détection musculaire • Choc supramaximal : Is = 150 % I • Réponse en U : décrément 1 - 5 léger incrément 6 - 10 • Paramètres: A et/ou S de la phase négative initiale 1ère R : nombre de JNM en blocage au repos 5 ème R comparée à la 1ère : décrément

• Exercice : contraction volontaire 30’’ - 1’ – facilitation post-exercice (< 20’’ ) : facilitation synaptique amplitude réponse M décrément – épuisement post-exercice : désensibilisation RAch ? décrément environ 3 ’ après l ’exercice • Exercice sous ischémie (muscles de la main) - 8’ d’ischémie - chocs supramaximaux à 3 Hz pendant 4 ’ - séries intermittentes de 5 chocs à 3 Hz de la 5 e à la 8 e ’

• Stimulation stable : chocs supramaximaux • Détection stable et muscle relâché • Filtres : 2 Hz - 10 KHz • Température > 32°C le froid améliore la transmission NM • inhibition de l’Ach. E • augmentation de l’amplitude du PPMm

• N’importe quel muscle ; MAIS : • • • de préférence un muscle faible cliniquement réponses M supramaximales fiables et dans des conditions confortables pour le patient faibles mouvements induits par la stimulation m. thénariens, m. hypothénariens, trapèze, m. nasalis, m. anconé deltoïde, orbiculaire de l ’œil, biceps, jambier ant. : muscles techniquement difficiles

• Attaque autoimmune contre les canaux calciques pré-synaptiques - déficit de libération de l’Ach PPM - PPMm normaux • Syn. paranéoplasique ou dysimmunité

• Amplitude de la 1ère réponse M effondrée (grand nombre de JNM bloquées) • Décrément pseudo-myasthénique (dépression synaptique)

• TEST le plus utile - Facilitation post-exercice +++ (<20 ’’) Incrément +++ : facilitation synaptique - ΔΔ : botulisme : souvent pas de décrément à 3 Hz aminosides : décrément à 20 - 50 Hz hypocalcémie MG : décrément à 20 - 50 Hz
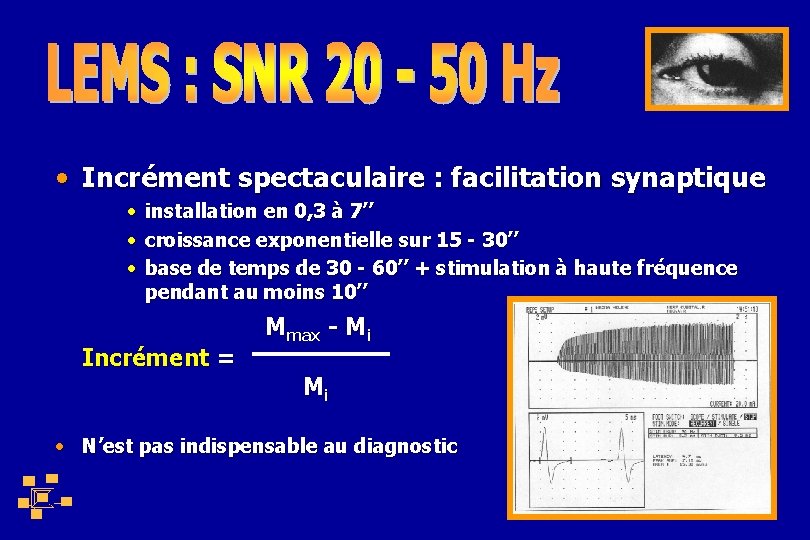
• Incrément spectaculaire : facilitation synaptique • • • installation en 0, 3 à 7’’ croissance exponentielle sur 15 - 30’’ base de temps de 30 - 60’’ + stimulation à haute fréquence pendant au moins 10’’ Incrément = Mmax - Mi Mi • N’est pas indispensable au diagnostic

• Décrément • < 10 % : GODEAUX, KIMURA, KEE • < 10 % m. distaux LANGE < 20 % m. proximaux • < 10 % m. distaux et faciaux < 15 % deltoïde et trapèze • Incrément • < 100 %

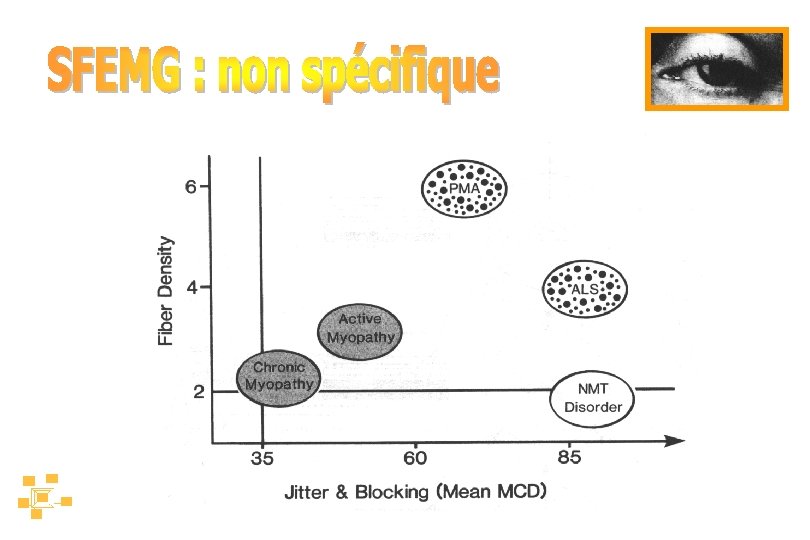
• Jitter = fluctuation de latence ± fluctuation du temps de transmission NM (car l’axone et la f. m. interviennent peu) • • Paramètre = MCD SFEMG avec microstimulation axonale • ne nécessite pas la collaboration du patient • permet de modifier la fréquence d’activation des JNM

• Technique plus sensible que la SNR • Détecte des anomalies même si le muscle examiné n’est pas cliniquement faible • A l’inverse, si le muscle est faible et la SFEMG normale : pathologie de la JNM peu probable • Jitter : sans bloc des JNM Décrément : induit par les blocs des JNM

• 20 JNM sont étudiées • Test pathologique si la moyenne > LSN ou si plus de 10 % des val. individuelles > LSN • MG : Jitter 5 Hz > 1 Hz Stim SFEMG • LEMS : Jitter 1 Hz > 5 Hz > 20 Hz
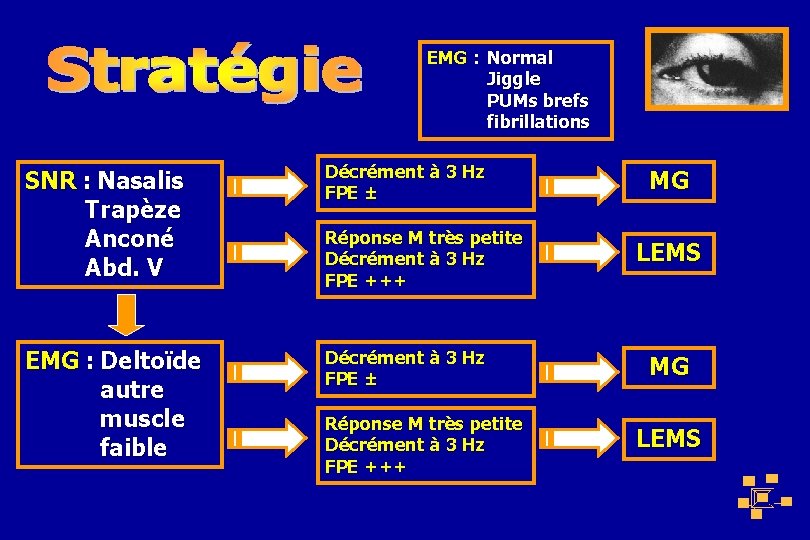
EMG : Normal Jiggle PUMs brefs fibrillations SNR : Nasalis Trapèze Anconé Abd. V Décrément à 3 Hz FPE ± EMG : Deltoïde autre muscle faible Décrément à 3 Hz FPE ± Réponse M très petite Décrément à 3 Hz FPE +++ MG LEMS
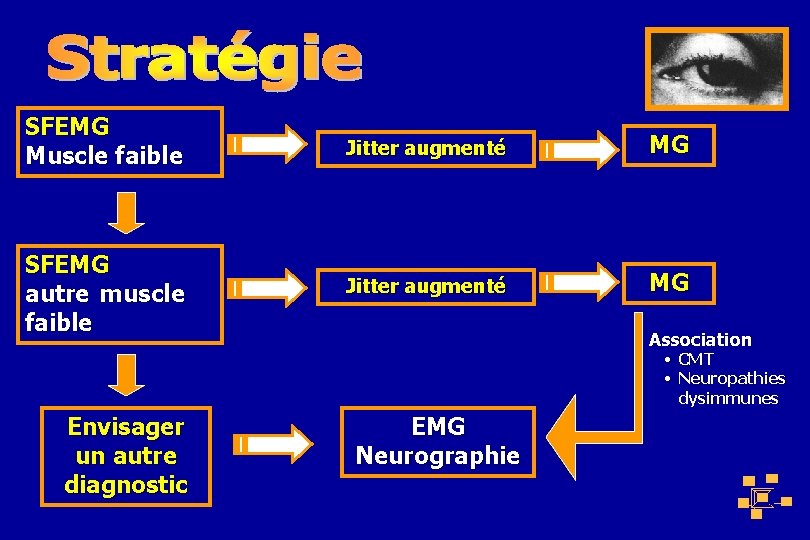
SFEMG Muscle faible Jitter augmenté MG SFEMG autre muscle faible Jitter augmenté MG Association • CMT • Neuropathies dysimmunes Envisager un autre diagnostic EMG Neurographie
- Slides: 30