DETERMINACIN DE LA ACTIVIDAD ENZIMTICA DE LACASAS Y














- Slides: 38

DETERMINACIÓN DE LA ACTIVIDAD ENZIMÁTICA DE LACASAS Y LIGNINA PEROXIDASAS DE HONGOS DEGRADADORES DE COLORANTES SELECCIONADOS PARA EL TRATAMIENTO DE AGUAS RESIDUALES DE LA INDUSTRIA TEXTIL Directora: M. C. Alma Koch Codirectora: Dra. Blanca Naranjo Tesista: Maritza Gardenia Páez Llerena

INTRODUCCIÓN INDUSTRIA TEXTIL Tratamientos: Físicos Químicos Biológicos: efectivos por la remoción de sustancias tóxicas Efluente industrial textil San Antonio de Pichincha Valenzuela, 2012 En el año 2005 la industria textil consumía 182. 000 litros de agua Diez mil colorantes y pigmentos

TRATAMIENTOS BIOLÓGICOS INTRODUCCIÓN HONGOS LIGNINOLÍTICOS ENZIMAS Valenzuela, 2012 (ESPE) Manganeso Peroxidasas (Mn. P) Lignina Peroxidasas (Li. P) Lacasas LACASAS: multicobre oxidasas (p. H 3. 7 -7. 5) LIGNINA PEROXIDASAS: hemo-férrico (p. H menor o igual 3)

OBJETIVOS Objetivo General: Determinar la actividad enzimática de lacasas y lignina peroxidasas de hongos degradadores de colorantes seleccionados para el tratamiento de aguas residuales de la industria textil. Objetivos Específicos: v Determinar la actividad ligninolítica y celulolítica de los hongos seleccionados, mediante una prueba cualitativa con guaiacol y una prueba semi-cuantitativa con agar carboximetilcelulosa. v Determinar la presencia de la enzima lacasa de los hongos degradadores de colorantes mediante una prueba cualitativa utilizando medio con ABTS. v Evaluar la efectividad de tres diferentes medios naturales para la producción de lacasas y lignina peroxidasas de los hongos. v Cuantificar la actividad enzimática de lacasas utilizando dos sustratos, ABTS y Otoluidina. v Cuantificar la actividad enzimática de lignina peroxidasas utilizando como sustrato ABTS.

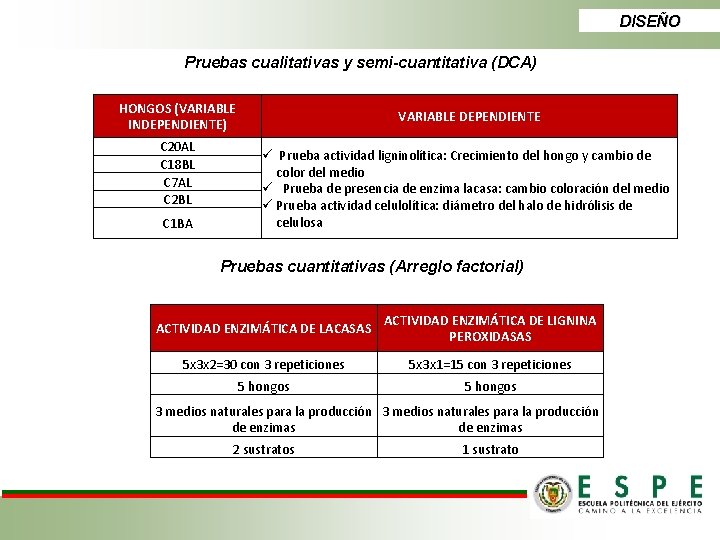
DISEÑO Pruebas cualitativas y semi-cuantitativa (DCA) HONGOS (VARIABLE INDEPENDIENTE) C 20 AL C 18 BL C 7 AL C 2 BL C 1 BA VARIABLE DEPENDIENTE ü Prueba actividad ligninolítica: Crecimiento del hongo y cambio de color del medio ü Prueba de presencia de enzima lacasa: cambio coloración del medio ü Prueba actividad celulolítica: diámetro del halo de hidrólisis de celulosa Pruebas cuantitativas (Arreglo factorial) ACTIVIDAD ENZIMÁTICA DE LACASAS ACTIVIDAD ENZIMÁTICA DE LIGNINA PEROXIDASAS 5 x 3 x 2=30 con 3 repeticiones 5 x 3 x 1=15 con 3 repeticiones 5 hongos 3 medios naturales para la producción de enzimas 2 sustratos 1 sustrato

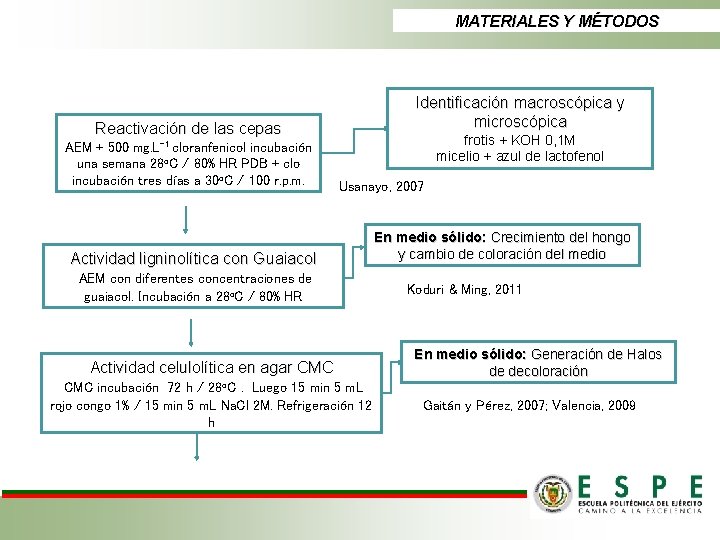
MATERIALES Y MÉTODOS Identificación macroscópica y microscópica Reactivación de las cepas AEM + 500 mg. L-1 cloranfenicol incubación una semana 28 o. C / 80% HR PDB + clo incubación tres días a 30 o. C / 100 r. p. m. frotis + KOH 0, 1 M micelio + azul de lactofenol Usanayo, 2007 Actividad ligninolítica con Guaiacol AEM con diferentes concentraciones de guaiacol. Incubación a 28 o. C / 80% HR Actividad celulolítica en agar CMC incubación 72 h / 28 o. C. Luego 15 min 5 m. L rojo congo 1% / 15 min 5 m. L Na. Cl 2 M. Refrigeración 12 h En medio sólido: Crecimiento del hongo y cambio de coloración del medio Koduri & Ming, 2011 En medio sólido: Generación de Halos de decoloración Gaitán y Pérez, 2007; Valencia, 2009

MATERIALES Y MÉTODOS Presencia de enzimas lacasas con ABTS siembra por disco en medio con ABTS / incubación 30 o. C / 80% HR Evaluar la efectividad de tres diferentes medios naturales para la producción de enzimas sal y concentración / incubación 30 o. C / 100 r. p. m / filtración Cuantificar la enzima lacasa utilizando dos sustratos ABTS y O-toluidina En medio sólido: Cambio de coloración del medio por oxidación del sustrato Córdoba, 2009 Kahraman & Gurdal, 2001 Castillo, 2004 Coronel et al. , 2001 Castillo, 2004 ABTS: 420 nm y O- toluidina: 627 nm Cuantificar la enzima lignina peroxidasa con ABTS: 420 nm Castillo, 2004 Téllez, 2010

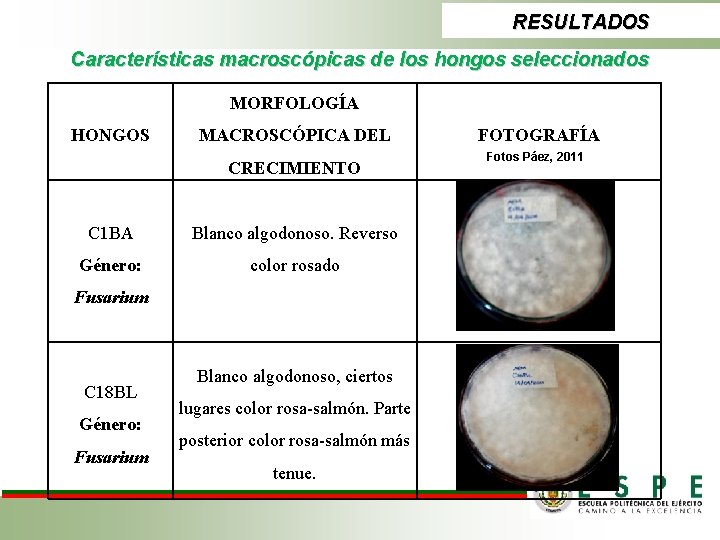
RESULTADOS Características macroscópicas de los hongos seleccionados MORFOLOGÍA HONGOS MACROSCÓPICA DEL CRECIMIENTO C 1 BA Blanco algodonoso. Reverso Género: color rosado Fusarium C 18 BL Género: Fusarium Blanco algodonoso, ciertos lugares color rosa-salmón. Parte posterior color rosa-salmón más tenue. FOTOGRAFÍA Fotos Páez, 2011

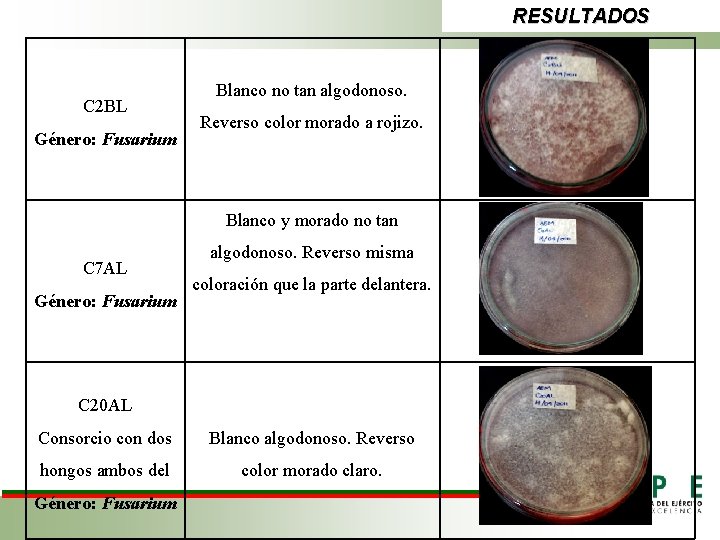
RESULTADOS C 2 BL Género: Fusarium Blanco no tan algodonoso. Reverso color morado a rojizo. Blanco y morado no tan C 7 AL Género: Fusarium algodonoso. Reverso misma coloración que la parte delantera. C 20 AL Consorcio con dos Blanco algodonoso. Reverso hongos ambos del color morado claro. Género: Fusarium

RESULTADOS Características microscópicas de los hongos seleccionados HONGOS C 1 BA Género: Fusarium MORFOLOGÍA MICROSCÓPICA Conidias pequeñas. Hifas tabicadas. Clamidospora. C 18 BL Población integralmente de microconidias, muy pocas Género: Fusarium macroconidias. Hifas tabicadas. Conidióforo simple. C 2 BL Población rica en microconidias. Hifas tabicadas. Ausencia Género: Fusarium de conidióforos. C 7 AL Género: Fusarium Macroconidias grandes y pequeñas unicelulares. Ausencia clamidospora. Conidióforos unicelulares. Hifas tabicadas. Ocasionalmente formación de rizomorfos. C 20 AL Consorcio con dos hongos del género Fusarium diferencia hongos ambos del en el tamaño de esporas. Microconidas. Hifas tabicadas. Género: Fusarium Observación de clamidosporas con azul de lactofenol Foto Páez, 2011

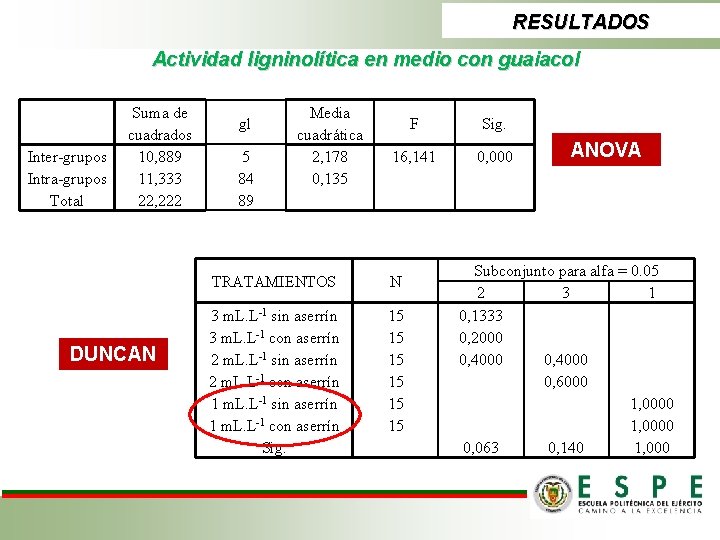
RESULTADOS Actividad ligninolítica en medio con guaiacol Crecimiento del hongo y cambio de coloración del medio Fotos Páez, 2011 Visualización microscópica a 40 x de los hongos

RESULTADOS Actividad ligninolítica en medio con guaiacol Inter-grupos Intra-grupos Total Suma de cuadrados 10, 889 11, 333 22, 222 DUNCAN gl 5 84 89 Media cuadrática 2, 178 0, 135 F Sig. 16, 141 0, 000 TRATAMIENTOS N 3 m. L. L-1 sin aserrín 3 m. L. L-1 con aserrín 2 m. L. L-1 sin aserrín 2 m. L. L-1 con aserrín 1 m. L. L-1 sin aserrín 1 m. L. L-1 con aserrín Sig. 15 15 15 ANOVA Subconjunto para alfa = 0. 05 2 3 1 0, 1333 0, 2000 0, 4000 0, 6000 1, 0000 0, 063 0, 140 1, 000

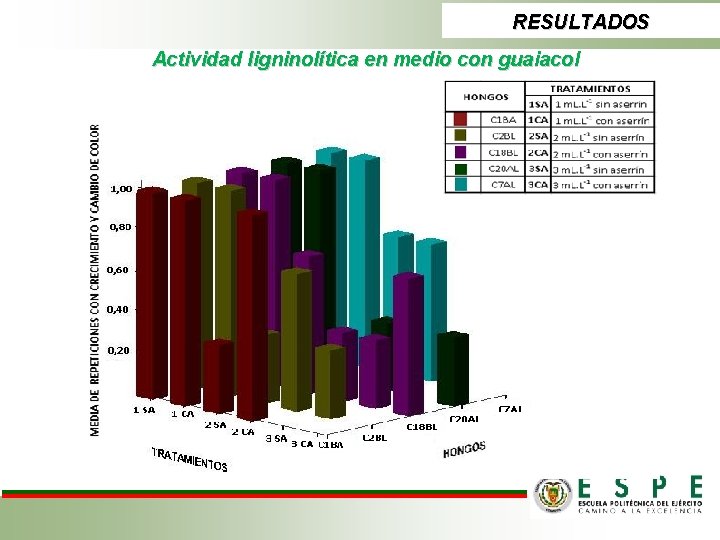
RESULTADOS Actividad ligninolítica en medio con guaiacol

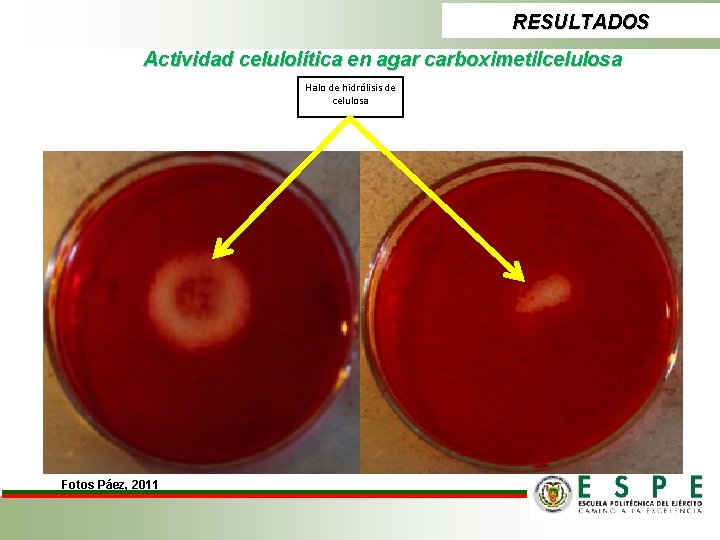
RESULTADOS Actividad celulolítica en agar carboximetilcelulosa Halo de hidrólisis de celulosa Fotos Páez, 2011

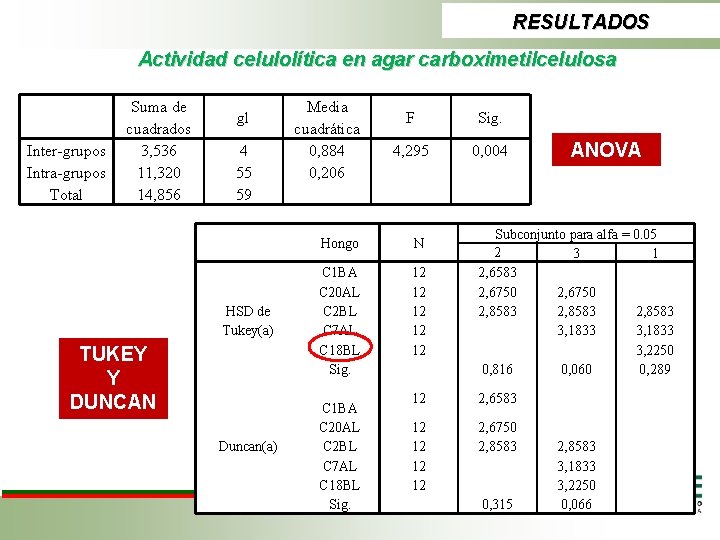
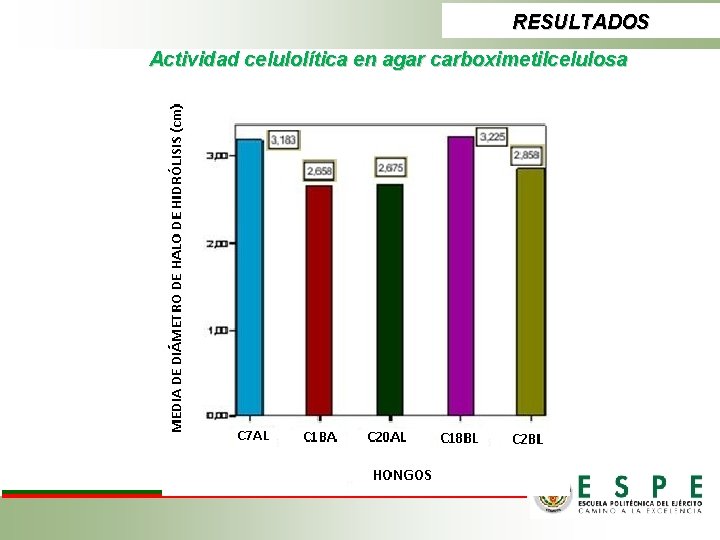
RESULTADOS Actividad celulolítica en agar carboximetilcelulosa Inter-grupos Intra-grupos Total Suma de cuadrados 3, 536 11, 320 14, 856 gl 4 55 59 HSD de Tukey(a) TUKEY Y DUNCAN Duncan(a) Media cuadrática 0, 884 0, 206 F Sig. 4, 295 0, 004 Hongo N C 1 BA C 20 AL C 2 BL C 7 AL C 18 BL Sig. 12 12 12 C 1 BA C 20 AL C 2 BL C 7 AL C 18 BL Sig. ANOVA Subconjunto para alfa = 0. 05 2 3 1 2, 6583 2, 6750 2, 8583 3, 1833 3, 2250 0, 816 0, 060 0, 289 12 2, 6583 12 12 2, 6750 2, 8583 0, 315 2, 8583 3, 1833 3, 2250 0, 066

RESULTADOS Actividad celulolítica en agar carboximetilcelulosa

RESULTADOS Presencia de la enzima lacasa en medio con ABTS Cambio de coloración del medio Fotos Páez, 2011

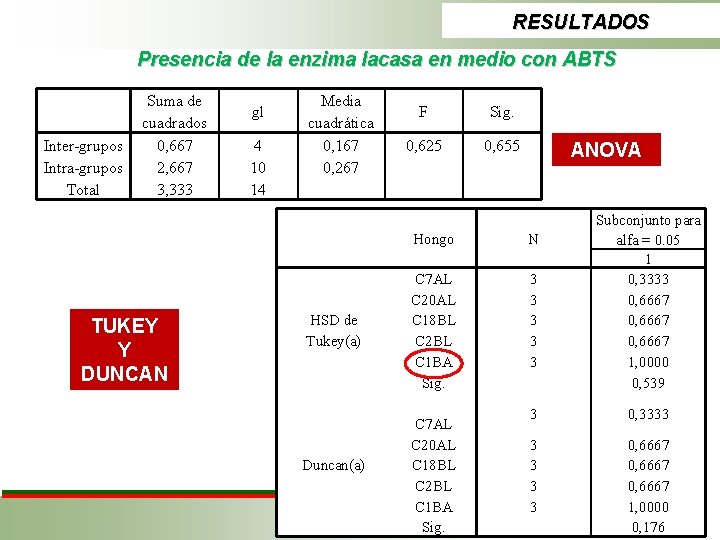
RESULTADOS Presencia de la enzima lacasa en medio con ABTS Inter-grupos Intra-grupos Total Suma de cuadrados 0, 667 2, 667 3, 333 TUKEY Y DUNCAN gl 4 10 14 Media cuadrática 0, 167 0, 267 HSD de Tukey(a) Duncan(a) F Sig. 0, 625 0, 655 ANOVA Hongo N C 7 AL C 20 AL C 18 BL C 2 BL C 1 BA Sig. 3 3 3 C 7 AL C 20 AL C 18 BL C 2 BL C 1 BA Sig. Subconjunto para alfa = 0. 05 1 0, 3333 0, 6667 1, 0000 0, 539 3 0, 3333 3 3 0, 6667 1, 0000 0, 176

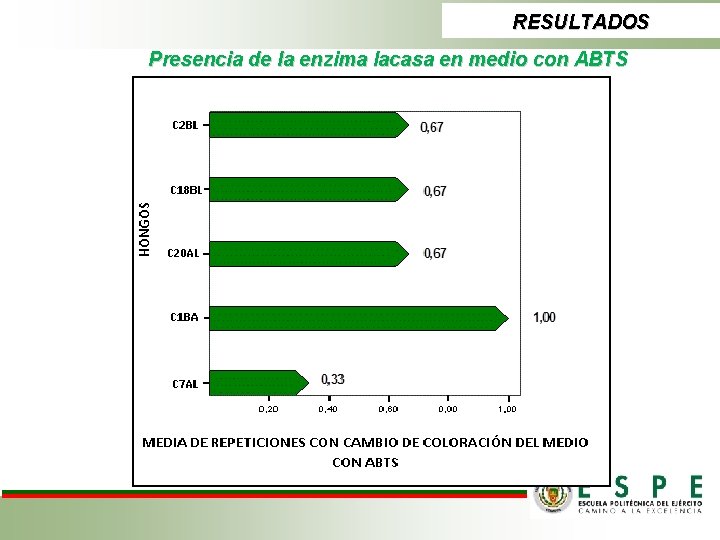
RESULTADOS Presencia de la enzima lacasa en medio con ABTS

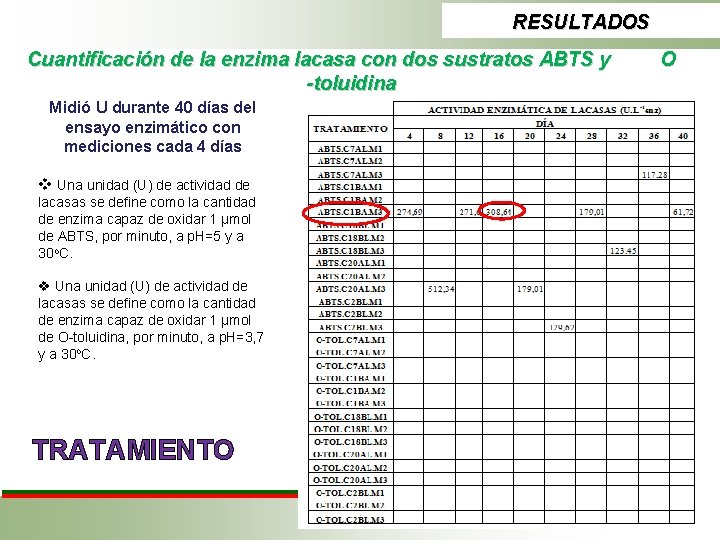
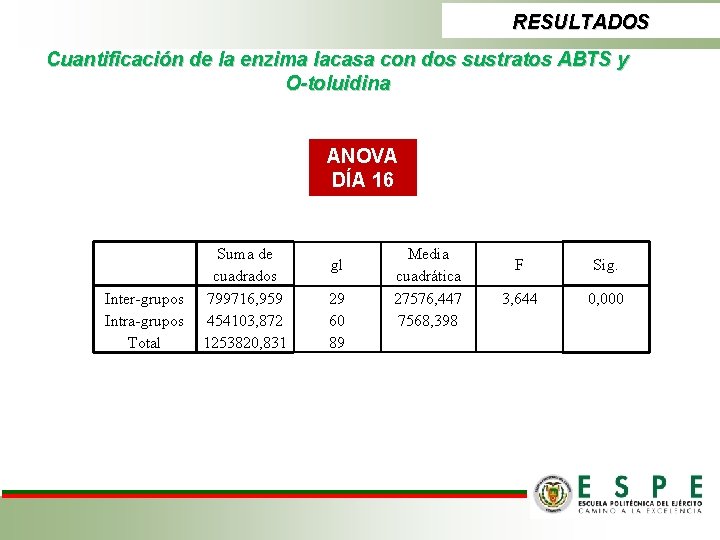
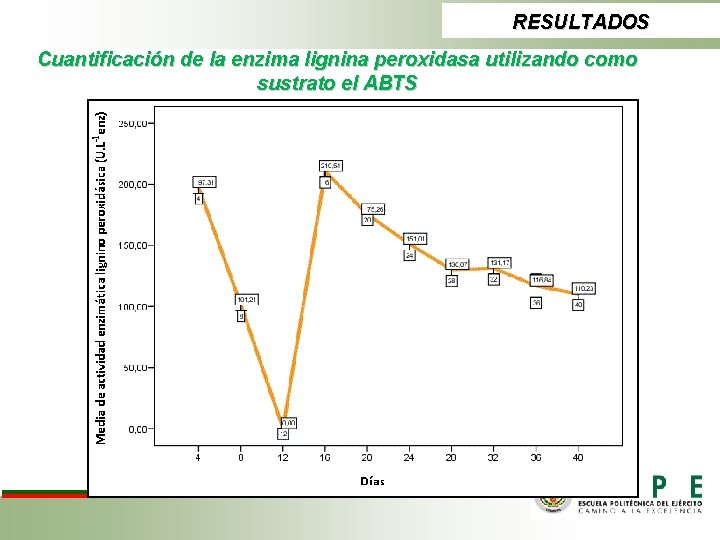
RESULTADOS Cuantificación de la enzima lacasa con dos sustratos ABTS y -toluidina Midió U durante 40 días del ensayo enzimático con mediciones cada 4 días v Una unidad (U) de actividad de lacasas se define como la cantidad de enzima capaz de oxidar 1 µmol de ABTS, por minuto, a p. H=5 y a 30 o. C. v Una unidad (U) de actividad de lacasas se define como la cantidad de enzima capaz de oxidar 1 µmol de O-toluidina, por minuto, a p. H=3, 7 y a 30 o. C. TRATAMIENTO O

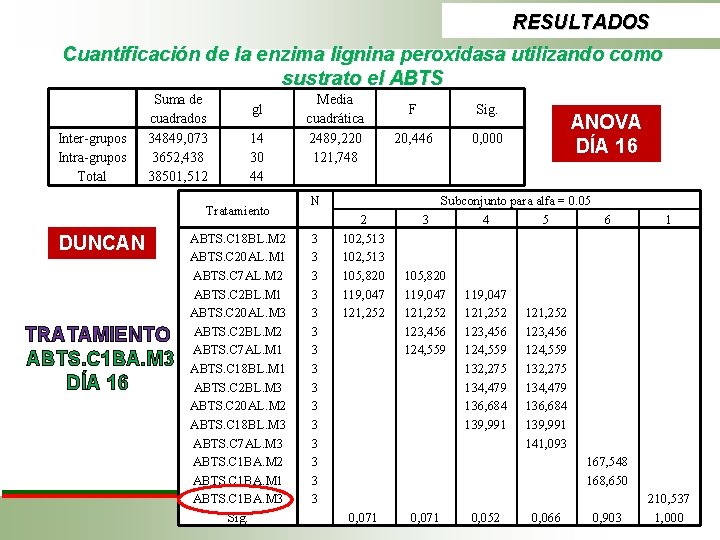
RESULTADOS Cuantificación de la enzima lacasa con dos sustratos ABTS y O-toluidina ANOVA DÍA 16 Inter-grupos Intra-grupos Total Suma de cuadrados 799716, 959 454103, 872 1253820, 831 gl 29 60 89 Media cuadrática 27576, 447 7568, 398 F Sig. 3, 644 0, 000

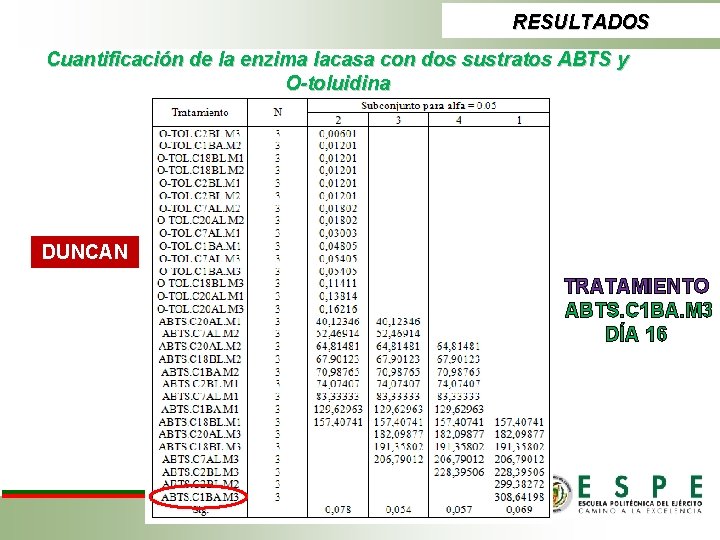
RESULTADOS Cuantificación de la enzima lacasa con dos sustratos ABTS y O-toluidina DUNCAN TRATAMIENTO ABTS. C 1 BA. M 3 DÍA 16

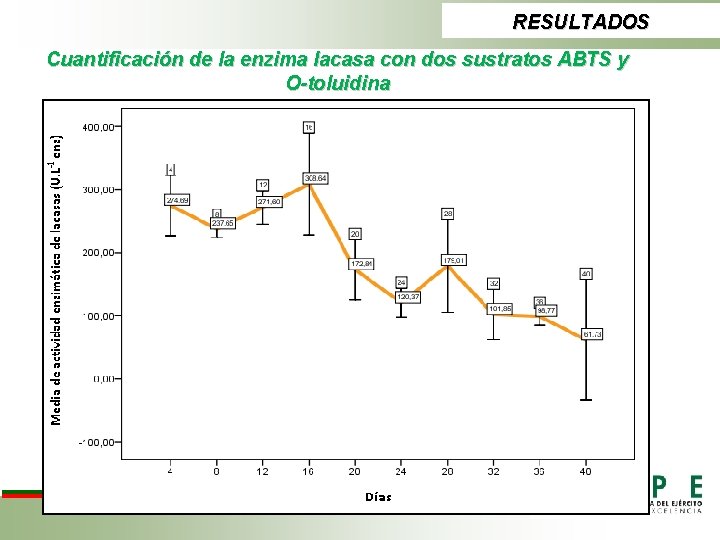
RESULTADOS Cuantificación de la enzima lacasa con dos sustratos ABTS y O-toluidina

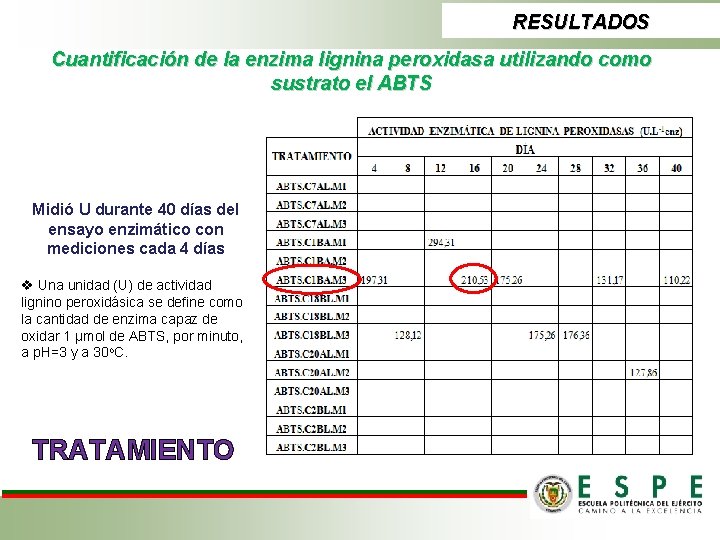
RESULTADOS Cuantificación de la enzima lignina peroxidasa utilizando como sustrato el ABTS Midió U durante 40 días del ensayo enzimático con mediciones cada 4 días v Una unidad (U) de actividad lignino peroxidásica se define como la cantidad de enzima capaz de oxidar 1 µmol de ABTS, por minuto, a p. H=3 y a 30 o. C. TRATAMIENTO

RESULTADOS Cuantificación de la enzima lignina peroxidasa utilizando como sustrato el ABTS Inter-grupos Intra-grupos Total Suma de cuadrados 34849, 073 3652, 438 38501, 512 gl 14 30 44 Tratamiento DUNCAN TRATAMIENTO ABTS. C 1 BA. M 3 DÍA 16 ABTS. C 18 BL. M 2 ABTS. C 20 AL. M 1 ABTS. C 7 AL. M 2 ABTS. C 2 BL. M 1 ABTS. C 20 AL. M 3 ABTS. C 2 BL. M 2 ABTS. C 7 AL. M 1 ABTS. C 18 BL. M 1 ABTS. C 2 BL. M 3 ABTS. C 20 AL. M 2 ABTS. C 18 BL. M 3 ABTS. C 7 AL. M 3 ABTS. C 1 BA. M 2 ABTS. C 1 BA. M 1 ABTS. C 1 BA. M 3 Sig. Media cuadrática 2489, 220 121, 748 N 3 3 3 3 2 102, 513 105, 820 119, 047 121, 252 F Sig. 20, 446 0, 000 ANOVA DÍA 16 Subconjunto para alfa = 0. 05 3 4 5 6 105, 820 119, 047 121, 252 123, 456 124, 559 132, 275 134, 479 136, 684 139, 991 141, 093 167, 548 168, 650 0, 071 0, 052 0, 066 0, 903 210, 537 1, 000

RESULTADOS Cuantificación de la enzima lignina peroxidasa utilizando como sustrato el ABTS

RESULTADOS Efectividad de tres diferentes medios naturales para la producción de enzimas Actividad enzimática en dependencia del medio LACASAS LIGNINA PEROXIDASAS Fotos Páez, 2011

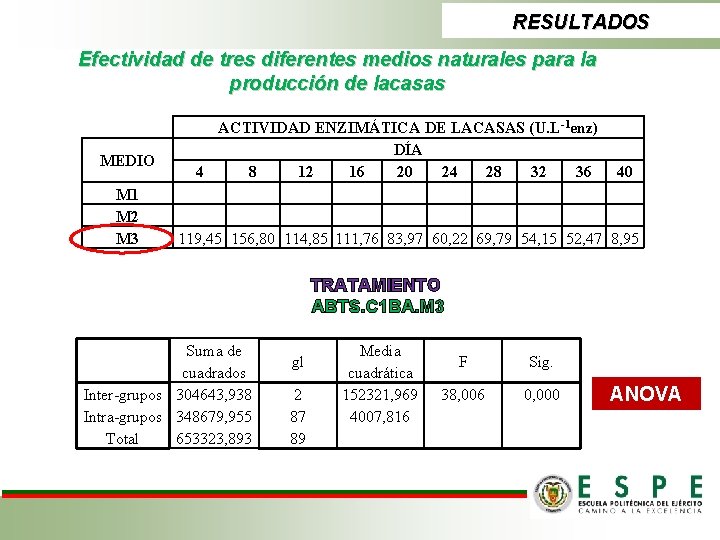
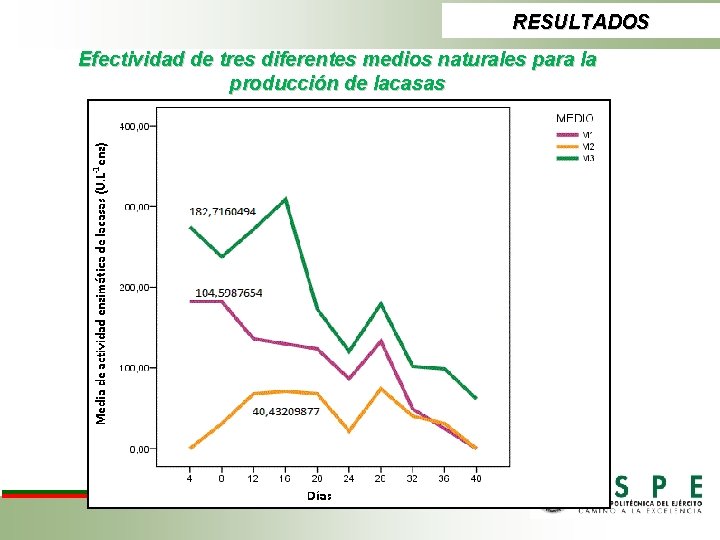
RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lacasas MEDIO M 1 M 2 M 3 ACTIVIDAD ENZIMÁTICA DE LACASAS (U. L-1 enz) DÍA 4 8 12 16 20 24 28 32 36 40 119, 45 156, 80 114, 85 111, 76 83, 97 60, 22 69, 79 54, 15 52, 47 8, 95 TRATAMIENTO ABTS. C 1 BA. M 3 Suma de cuadrados Inter-grupos 304643, 938 Intra-grupos 348679, 955 Total 653323, 893 gl 2 87 89 Media cuadrática 152321, 969 4007, 816 F Sig. 38, 006 0, 000 ANOVA

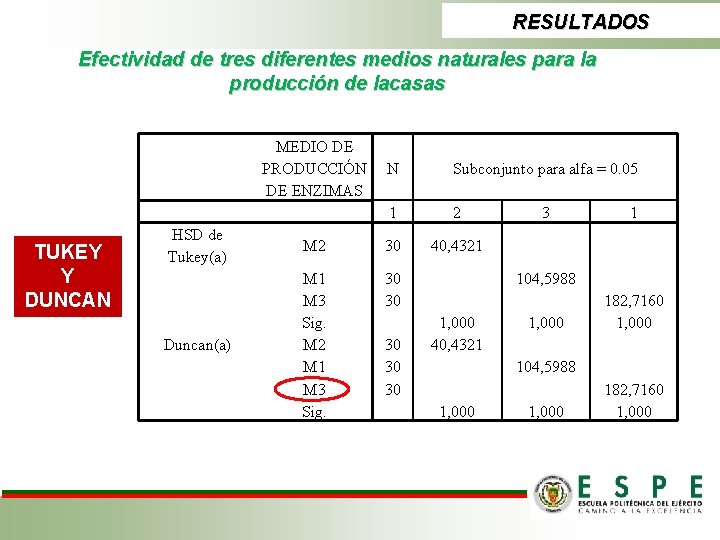
RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lacasas MEDIO DE PRODUCCIÓN DE ENZIMAS TUKEY Y DUNCAN N Subconjunto para alfa = 0. 05 1 2 40, 4321 HSD de Tukey(a) M 2 30 30 30 Duncan(a) M 1 M 3 Sig. M 2 M 1 M 3 Sig. 30 30 30 3 1 104, 5988 1, 000 40, 4321 1, 000 182, 7160 1, 000 104, 5988 1, 000 182, 7160 1, 000

RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lacasas

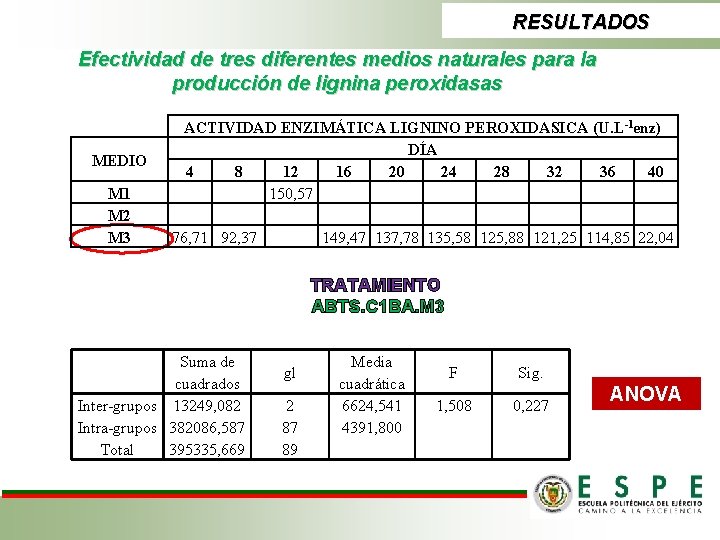
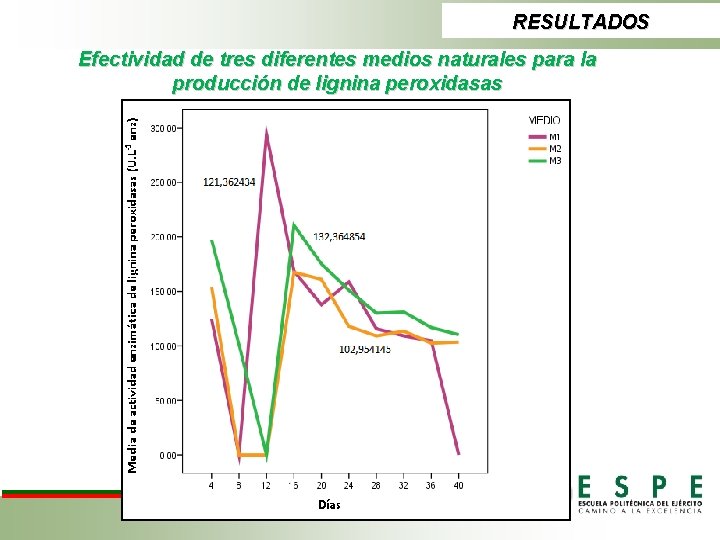
RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lignina peroxidasas MEDIO M 1 M 2 M 3 ACTIVIDAD ENZIMÁTICA LIGNINO PEROXIDASICA (U. L-1 enz) DÍA 4 8 12 16 20 24 28 32 36 40 150, 57 76, 71 92, 37 149, 47 137, 78 135, 58 125, 88 121, 25 114, 85 22, 04 TRATAMIENTO ABTS. C 1 BA. M 3 Suma de cuadrados Inter-grupos 13249, 082 Intra-grupos 382086, 587 Total 395335, 669 gl 2 87 89 Media cuadrática 6624, 541 4391, 800 F Sig. 1, 508 0, 227 ANOVA

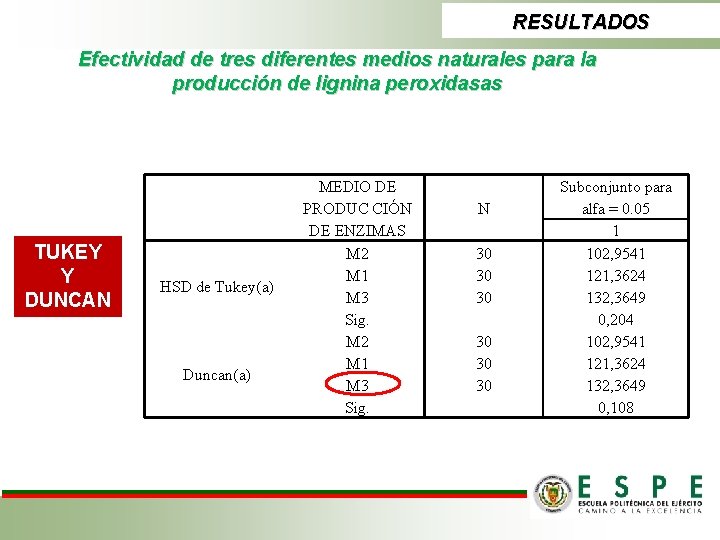
RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lignina peroxidasas TUKEY Y DUNCAN HSD de Tukey(a) Duncan(a) MEDIO DE PRODUC CIÓN DE ENZIMAS M 2 M 1 M 3 Sig. N 30 30 30 Subconjunto para alfa = 0. 05 1 102, 9541 121, 3624 132, 3649 0, 204 102, 9541 121, 3624 132, 3649 0, 108

RESULTADOS Efectividad de tres diferentes medios naturales para la producción de lignina peroxidasas

CONCLUSIONES v Los hongos estudiados pertenecen al género Fusarium. v Los cinco hongos seleccionados presentaron actividad ligninolítica, identificados por el crecimiento y cambio de coloración del medio por oxidación del guaiacol. v Los hongos estudiados presentaron actividad celulolítica (diámetro de halos de aclaramiento). C 18 BL presentó la mejor actividad, mientras que C 1 BA mostró la más baja. v Los hongos expusieron presencia de lacasas en ABTS. C 1 BA expuso el mejor resultado y C 7 AL , el menor. v El mejor tratamiento de actividad enzimática de lacasas fue ABTS. C 1 BA. M 3, con 308, 64 U. L-1 enz al día 16. v. El mejor tratamiento de cuantificación enzimática de lignina peroxidasas fue el ABTS. C 1 BA. M 3, con 210, 53 U. L-1 enz al día 16.

CONCLUSIONES v La expresión enzimática de lacasas y de lignina peroxidasas alcanzó su valor óptimo al día 16 de 40 días de ensayo. v. Los hongos que presentaron menor actividad celulolítica son aquellos que más actividad enzimática de lacasas y lignina peroxidasas expusieron. v El medio natural de producción de enzimas M 3 fue el más favorable para la producción de lacasas y lignina peroxidasas.

RECOMENDACIONES v Caracterizar los hongos por género y especie para optimizar condiciones de p. H y temperatura. v Optimizar p. H y temperatura de los dos sustratos utilizados, para incrementar la producción de enzimas. v Optimizar el medio de producción de enzimas con sales y producto ligninocelulósicos de afinidad para los hongos. v Determinar la actividad enzimática de manganeso peroxidasas y aplicar el complejo enzimático ligninolítico para procesos de biorremediación. v. Aplicar a nivel de laboratorio el uso de enzimas ligninolíticas en la degradación de colorantes provenientes de la industria textil. v. Diseñar un biorreactor, a escala semi-industrial o industrial, para aplicar las propiedades fúngicas encontradas para la degradación de colorantes de la industria textil.

AGRADECIMIENTOS Agradezco a las autoridades de la ESPE que permitieron el desarrollo de esta tesis con el financiamiento Proyecto de Investigación 2010 ESPE-CEINCI 014 ¨SELECCIÓN DE HONGOS EFICIENTES EN LA BIODEGRADACIÓN DE MATERIA ORGÁNICA Y COLORANTES REACTIVOS, TOLERANTES A METALES, PARA SU USO EN BIORREMEDIACIÓN DE AGUAS RESIDUALES DE LA INDUSTRIA TEXTIL¨. e instalaciones prestadas.

AGRADECIMIENTOS A mi directora y codirectora de tesis M. C. Alma Koch y a la Dra. Blanca Naranjo por su constante apoyo, al Ing. Abraham Oleas por impartirme un poco de su extenso conocimiento. A la Ing. Erica Castillo y al Ing. Mauricio Moreno. A mis compañeros del laboratorio y amigos. A todos muchas GRACIAS!!! Y María Auxiliadora por todas las bendiciones recibidas y a mi familia por acompañarme durante toda mi carrera. GRACIAS!!!