Der p H von Bden 270127 UE Umweltchemische
Der p. H von Böden 270127 UE Umweltchemische Übungen

Viele services des Bodens sind auf ein enges p. H Fenster begrenzt: Poröse Textur Belüftung Wasserspeicherung (Retentionsfähikeit) Retention und Bereitstellung von Nährstoffen Zu hoher p. H: zu rascher Abbau des organischen Bodenanteils • Zu niedriger p. H: Auswaschung von kationischen Nährstoffen • • •

Protonenquellen: 1. 2. 3. 4. 5. Humin- und Fulvosäuren aus dem Abbau des Lignins H⁺ Ionen von der Kohlensäure aus dem CO 2 der Luft saurer Regen (air pollution): HCl, NOx, SO₂ CO 2 aus dem Abbau (Veratmung) abgestorbenen pflz. Materials (Mineralisation), generell aus Oxidationsprozessen, wie Oxidation von NH₃: NH₃ + 2 O₂ NO₃⁻ + H₂O + H⁺ 6. 10% 30% des Boden CO 2 stammen aus der Wurzelatmung 7. Pflanzen sind lebende Kationenaustauscher: Bei der Kationenaufnahme durch die Pflanzenwurzel werden große Mengen Protonen an die Rhizosphäre abgegeben. Im allgemeinen nimmt die Pflanze über die Wurzeln nämlich bedeutend mehr Kationen, bes. Ca²⁺, Mg²⁺, K⁺, Na⁺ und NH₄⁺ aus dem Boden auf als Anionen wie H₂PO₄⁻, NO₃⁻ und SO₄²⁻. Zur Aufrechterhaltung des Ladungsgleichgewichtes werden H⁺ an den Boden abgegeben. Pflanzen besitzen daher einen Basenüberschuss (wichtig für ausgewogene Ernährung!) 8. Wurzelexsudate enthalten bedeutende Mengen organischer Säuren: Gemeinsam senken die 3 letztgenannten Prozesse den p. H bis etwa 2 cm Wurzelabstand um 2 Einheiten. 9. Durch leaching der bas. Bodenkomponenten Ca²⁺, Mg²⁺, K⁺, Na⁺ 10. Export (Abernten) der bas. Bodenkomponenten und Unterbrechen des Nährstoffkreislaufs, Fertilizer enthalten daher stets auch das bas. Ca. CO₃ 11. Kohlehaltige Böden
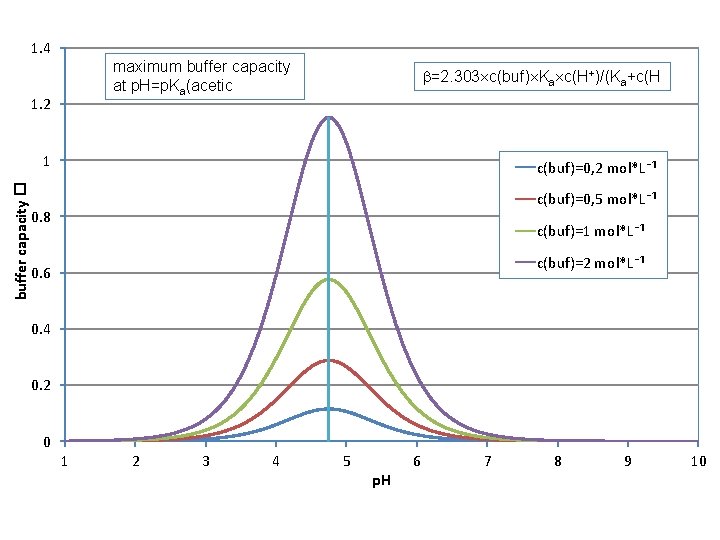
1. 4 maximum buffer capacity at p. H=p. Ka(acetic 1. 2 =2. 303 c(buf) Ka c(H+)/(Ka+c(H buffer capacity � 1 c(buf)=0, 2 mol*L⁻¹ c(buf)=0, 5 mol*L⁻¹ 0. 8 c(buf)=1 mol*L⁻¹ c(buf)=2 mol*L⁻¹ 0. 6 0. 4 0. 2 0 1 2 3 4 5 p. H 6 7 8 9 10

Heterogene Puffer Sonderform der homogenen Puffer: Eine der Pufferkomponeten steht als geringlöslicher Feststoff mit der Lösung im Gleichgewicht. Das heißt, eine der beiden Pufferkomponenten liegt unter der Voraussetzung, dass sich thermodynamisches Gleichgewicht genügend rasch einstellt, in einer stets konstanten Konzentration vor, welche • durch das Lp der festen Phase vorgegeben ist • generell klein ist (geringlösliche Gesteine wie etwa Ca. CO 3 ), sodass die Proportion c(ba. H⁺)/c(ba) ≠ 1 und daher p. H = p. Ks – log[c(ba. H⁺)/c(ba)] (Henderson-Hasselbalch-Gleichung) weit vom äquimolaren Verhältnis abweicht und sich damit generell der p. H heterogener Puffersysteme bedeutend vom p. KS entfernt, sodass die Pufferkapazität gering ist. Die Voraussetzungen für die Pufferung sind bei heterogenen Puffern also ungünstig, weil die Pufferkapazität geringer als bei ihrem Optimum bei [ba. H+]/[ba]=1 ist.

Die Wirksamkeit des heterogenen Puffers ist daher eine Frage der Geschwindigkeit, mit der die geringer lösliche Komponente (z. B. CO 32 ) aus der festen Phase (z. B. dem Ca. CO 3) in die Lösung nachgeliefert wird. Eine ganz wesentliche Rolle spielt hier wie stets für die Geschwindigkeit der Interaktion fester mit wässriger Phase die Korngröße. Aus den zuletzt genannten Gründen ist z. B. der Alumosilikatpuffer nur von geringer Wirksamkeit: Die Folge ist die bekannte Versauerung carbonatarmer Systeme (wie im Zentralalpenbereich Vorarlbergs oder in Skandinavien) durch den acid rain. Der Vorteil heterogener gegenüber homogener Puffersysteme liegt im nahezu unerschöpflichen Reservoir der festen Komponente. Vereinfachend lässt sich zusammenfassen, dass homogene Puffer die p. H Stabilisierung in Ober flächen gewässern besorgen (Ausnahme: Pufferung durch suspended matter), während heterogene Puffersysteme den p. H in Poren und Grund wässern kontrollieren und daher für die Stabilität des Boden-p. H zuständig sind. Heterogene Puffersysteme sind daher immer dann besonders wirksam, wenn die Geschwindigkeit des Säure /Basen eintrages gleich groß oder geringer ist wie/als die Geschwindigkeit des Löseprozesses der festen Pufferkomponente.

Heterogene Puffersysteme der Böden 1. Das heterogene Carbonat/Hydrogencarbonatsystem (Calciumcarbonat Kalkstein) sog. „basische Böden“ Die Pufferung liegt nicht bei p. H = p. Ks = 10. 33 sondern für das offene System in Abhängigkeit vom CO₂ Partialdruck zwischen p. H 8. 3 (CO₂ Konz. der Luft) und etwa p. H 7 (hundertfacher Partialdruck des CO₂ der Luft) 2. Humuspuffer sowohl Säure als auch Basenform sind fest. Pufferung bei p. H 6 bis p. H 4 3. Alumosilikatpuffer, bei Fehlen von Carbonaten sowohl Säure als auch Basenform sind fest. Verwitterung von primären Alumosilikaten: Saure Verwitterung der basischen Primärsilikate (z. B. Feldspäte) unter Aufnahme von Protonen zu deren Verwitterungsprodukten, den (sauren) Tonmineralen (Schichtsilikaten). Die Pufferreaktion ist mit einer Änderung der Struktur verknüpft: Primärsilikate + Protonen ⇌ x. Me²⁺ + Tonminerale Pufferung zw. p. H 6 und p. H 5
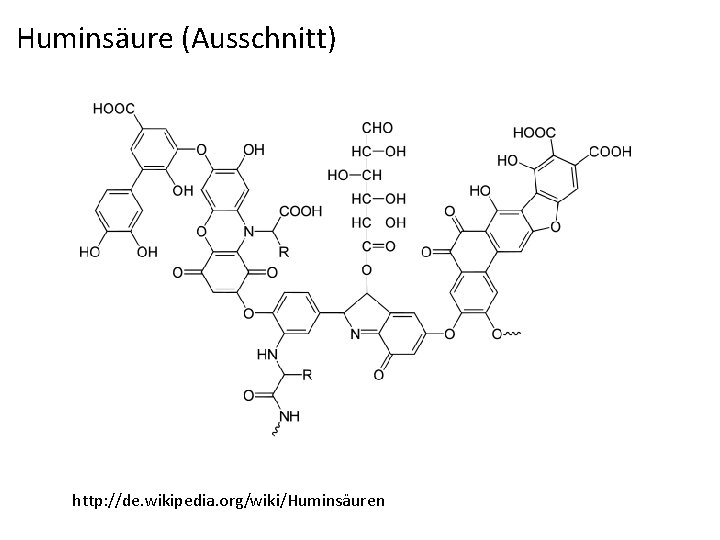
Huminsäure (Ausschnitt) http: //de. wikipedia. org/wiki/Huminsäuren

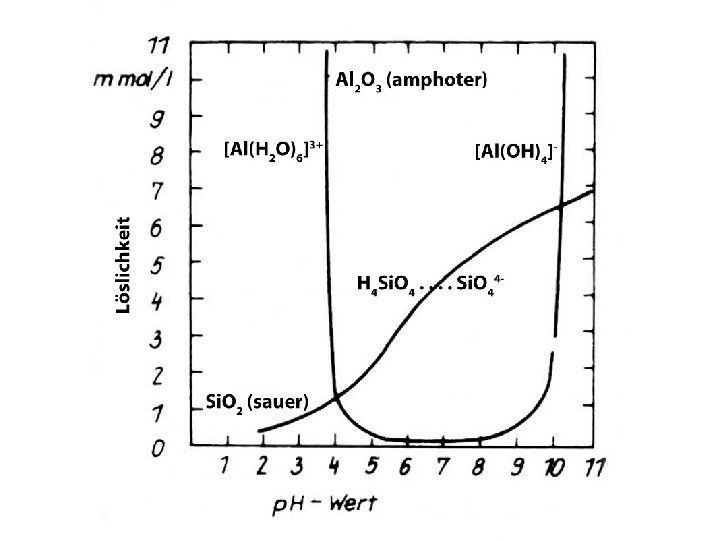
4. Austauschpuffer: (Tonminerale) sowohl Säure als auch Basenform sind fest. Pufferung bei p. H 5 bis p. H 4; Prinzip wie Humuspuffer bei Eintrag von Protonen kommt es zur Addition von H⁺ an Si O⁻ (bzw. Al O⁻) Gruppen, bei extremer Versauerung sogar zur Anlagerung von H⁺ an Si OH (bzw. Al OH) Gruppen unter Bildung von Si OH₂⁺ (bzw. Al OH₂⁺) Gruppen. Wir können daher die negativ geladene Form der Tonminerale als Base betrachten, die in Abhängigkeit vom p. H ein zusätzliches Protonenangebot abpuffert. 5. Heterogener Aluminiumpuffer Gibbsit Al(OH)₃ ist das letzte feste Endprodukt der Silikatverwitterung: Al₄(OH)₈[Si₄O₁₀] + 10 H₂O ⇌ 4 Al(OH)₃↓ + 4 H₄Si. O₄ Kaolinit Gibbsit gelöst Pufferreaktion: Al(OH)₃ + H⁺ + 3 H₂O ⇌ Al(OH)₂(H₂O)₄⁺ Die Wirksamkeit beginnt bei p. H <5

6. Heterogener Eisenpuffer: Bei p. H <3. 8 tritt zusätzlich Pufferung durch das System Eisen (als pedogenes Hydroxid oder Oxidhydrat) ein: Eisen geht damit in großem Maß stab in Lösung: Fe(OH)₃ + 3 H⁺ + 3 H₂O ⇌ Fe(H₂O)₆³⁺
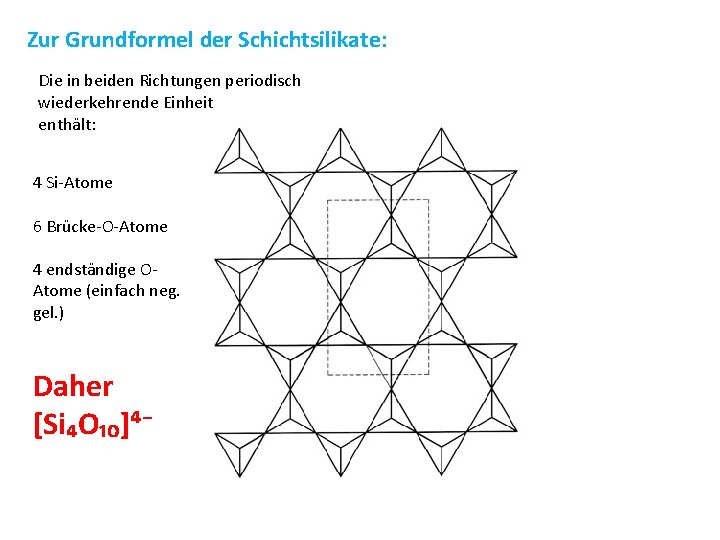
Zur Grundformel der Schichtsilikate: Die in beiden Richtungen periodisch wiederkehrende Einheit enthält: 4 Si Atome 6 Brücke O Atome 4 endständige O Atome (einfach neg. gel. ) Daher [Si₄O₁₀]⁴⁻
![Zweischichtsilikate: Kaolinit Al₄(OH)₈[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html Zweischichtsilikate: Kaolinit Al₄(OH)₈[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html](http://slidetodoc.com/presentation_image_h/15679b407aa847fbf10006fd42bce1e2/image-13.jpg)
Zweischichtsilikate: Kaolinit Al₄(OH)₈[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html
![Dreischichtsilikate: Talk Mg₃(OH)₂[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html Dreischichtsilikate: Talk Mg₃(OH)₂[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html](http://slidetodoc.com/presentation_image_h/15679b407aa847fbf10006fd42bce1e2/image-14.jpg)
Dreischichtsilikate: Talk Mg₃(OH)₂[Si₄O₁₀] http: //ruby. chemie. uni freiburg. de/Vorlesung/silicate_7_5. html

Vom Talk abgeleitet: Smektite („Tonminerale“) • Alumosilikate: Fähigkeit der strukturell bed. neg. Ladung (ζ Potential) daher Ionenaustauschereigenschaften • quellfähig, da aus übersättigten Porenlösungen auskristallisiert
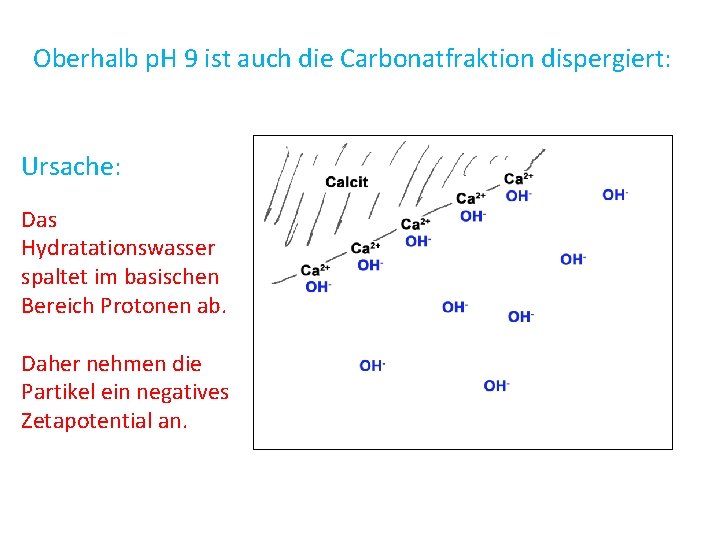
Oberhalb p. H 9 ist auch die Carbonatfraktion dispergiert: Ursache: Das Hydratationswasser spaltet im basischen Bereich Protonen ab. Daher nehmen die Partikel ein negatives Zetapotential an.
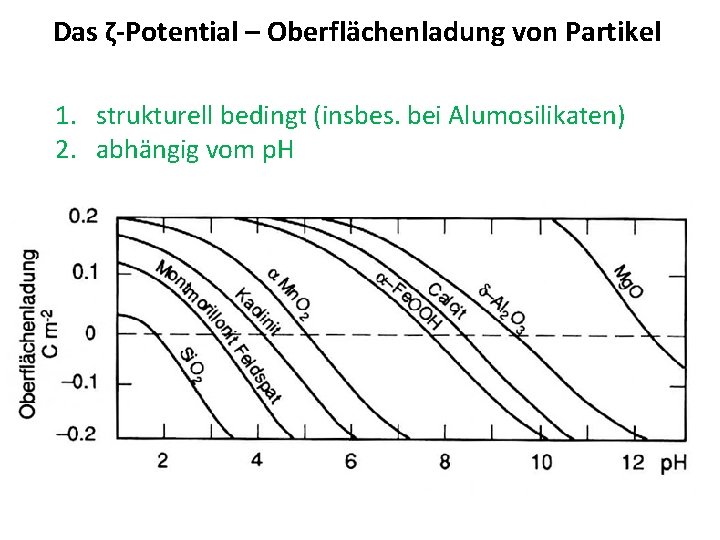
Das ζ-Potential – Oberflächenladung von Partikel 1. strukturell bedingt (insbes. bei Alumosilikaten) 2. abhängig vom p. H




Salzlebensräume sind Feuchtlebensräume 10. April 2013, Nationalparkbeirat Dr. Rudolf Krachler 21

Ohne Wasser kein Salzlebensraum 10. April 2013, Nationalparkbeirat Dr. Rudolf Krachler 22
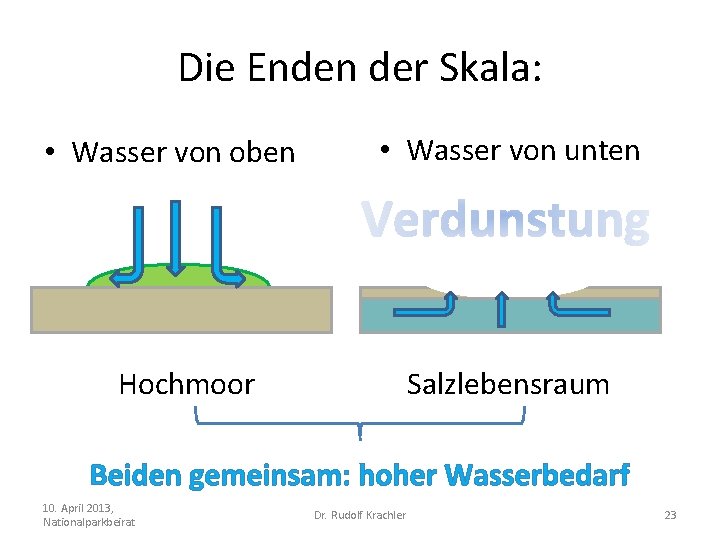
Die Enden der Skala: • Wasser von oben • Wasser von unten Hochmoor Salzlebensraum Beiden gemeinsam: hoher Wasserbedarf 10. April 2013, Nationalparkbeirat Dr. Rudolf Krachler 23

Lacken sind ASTATISCH (bis zu einem gewissen Grad) Auskleidung aus SALZTON Der Salzton ist wasserundurchlässig und erlaubt nur kapillaren Transport. („Lackenstauhorizont“ oder auch „salzführender Horizont“) Dr. Rudolf Krachler 24
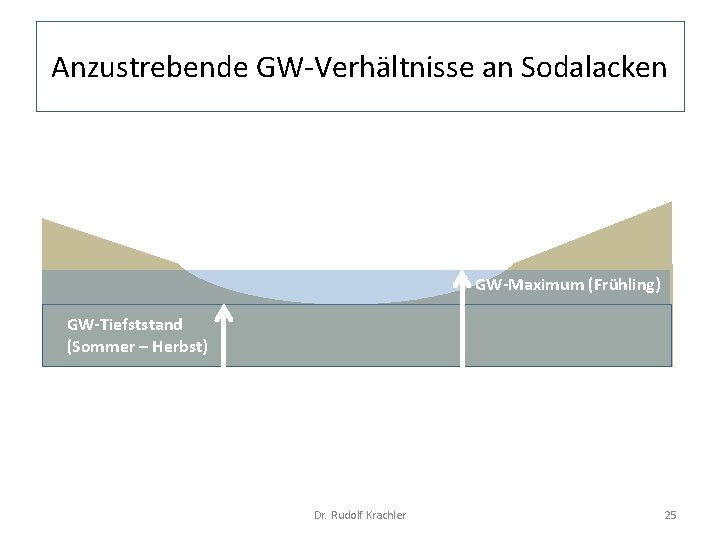
Anzustrebende GW Verhältnisse an Sodalacken GW-Maximum (Frühling) GW-Tiefststand (Sommer – Herbst) Dr. Rudolf Krachler 25
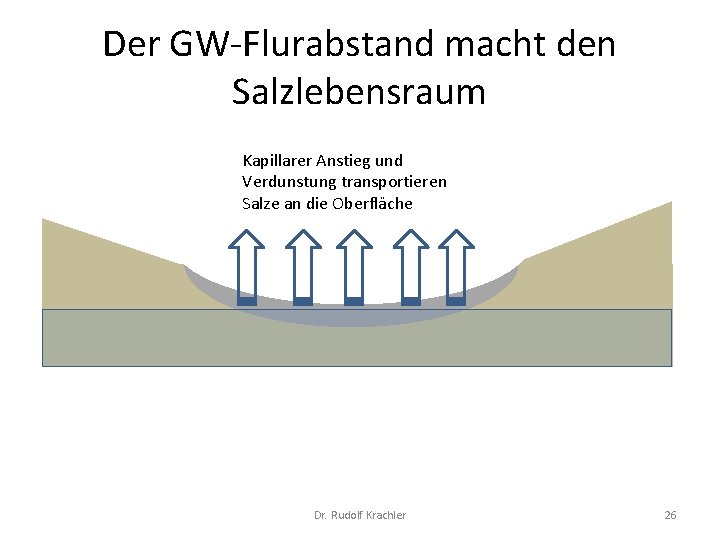
Der GW Flurabstand macht den Salzlebensraum Kapillarer Anstieg und Verdunstung transportieren Salze an die Oberfläche Dr. Rudolf Krachler 26
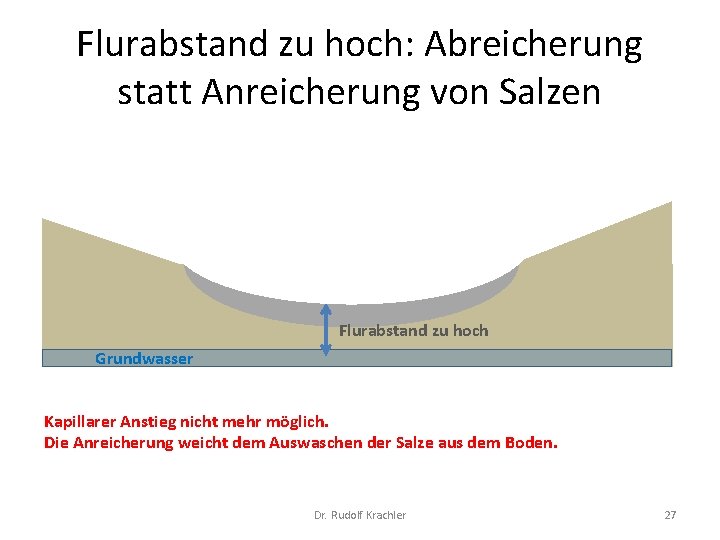
Flurabstand zu hoch: Abreicherung statt Anreicherung von Salzen Flurabstand zu hoch Grundwasser Kapillarer Anstieg nicht mehr möglich. Die Anreicherung weicht dem Auswaschen der Salze aus dem Boden. Dr. Rudolf Krachler 27
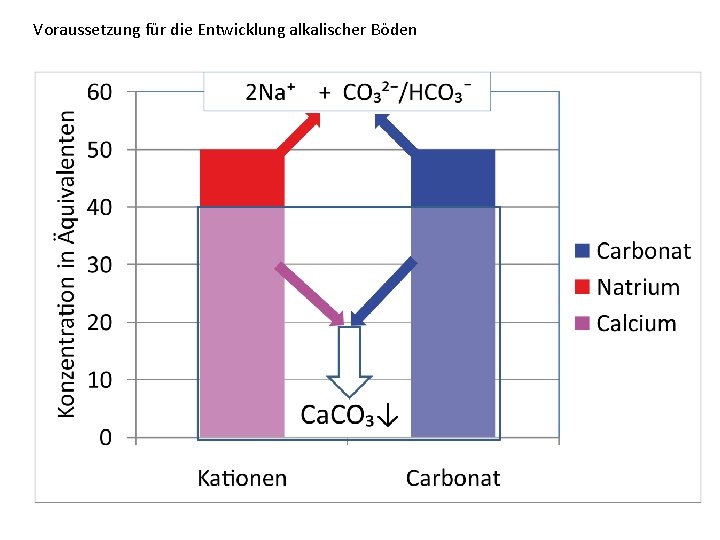
Voraussetzung für die Entwicklung alkalischer Böden
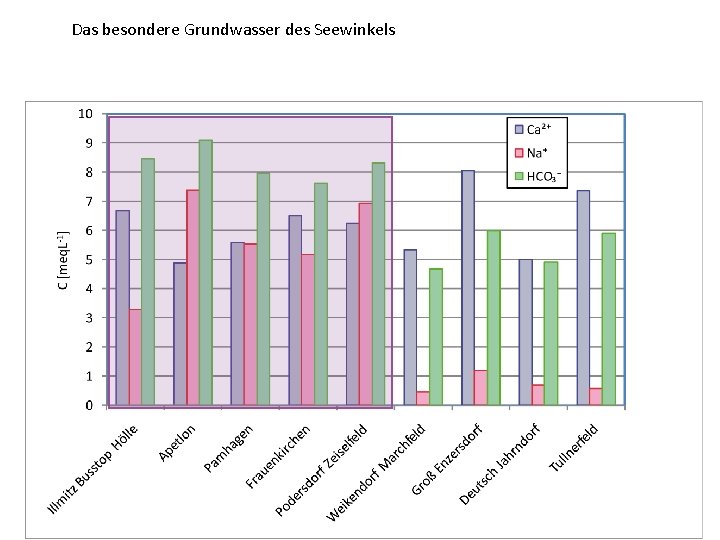
Das besondere Grundwasser des Seewinkels
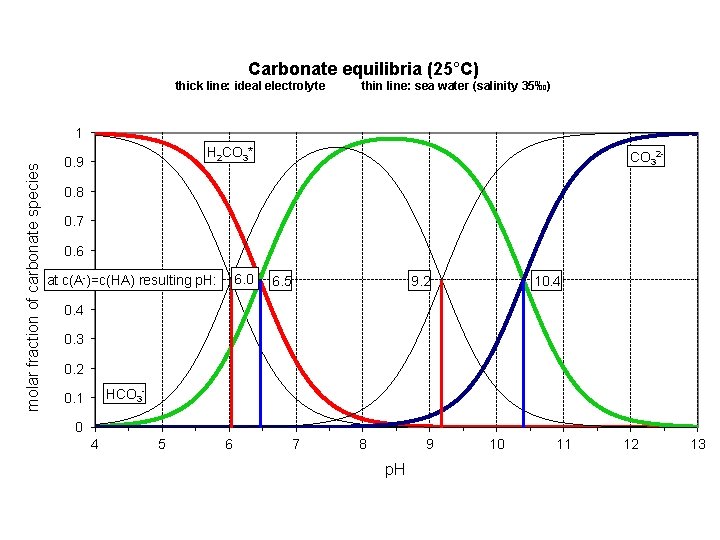
Carbonate equilibria (25°C) thick line: ideal electrolyte thin line: sea water (salinity 35‰) molar fraction of carbonate species 1 H 2 CO 3* 0. 9 CO 32 - 0. 8 0. 7 0. 6 6. 0 0. 5 -)=c(HA) resulting p. H: at c(A 6. 5 9. 2 10. 4 0. 3 0. 2 HCO 3 - 0. 1 0 4 5 6 7 8 9 p. H 10 11 12 13
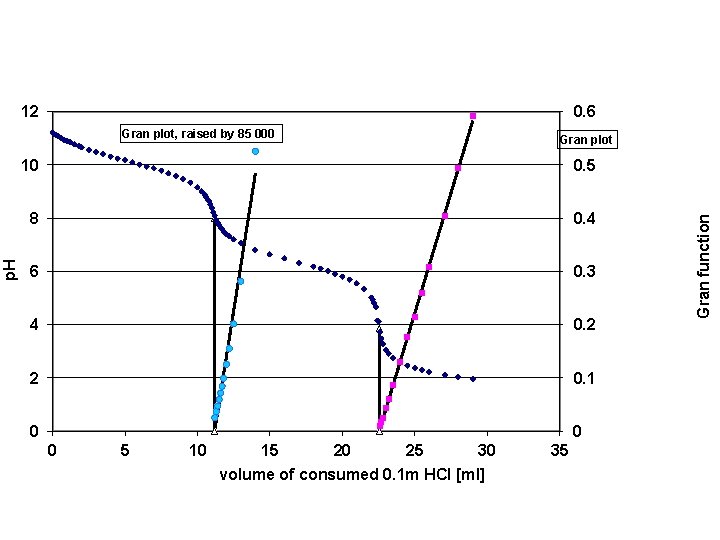
12 0. 6 Gran plot 10 0. 5 8 0. 4 6 0. 3 4 0. 2 2 0. 1 0 0 0 5 10 15 20 25 30 volume of consumed 0. 1 m HCl [ml] 35 Gran function p. H Gran plot, raised by 85 000
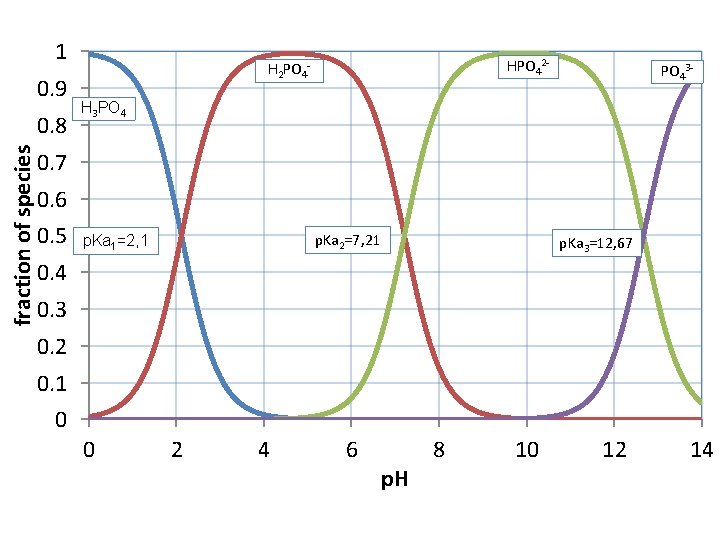
1 0. 9 fraction of species 0. 8 HPO 42 H 2 PO 4 PO 43 H 3 PO 4 0. 7 0. 6 0. 5 p. Ka 2=7, 21 p. Ka 1=2, 1 p. Ka 3=12, 67 0. 4 0. 3 0. 2 0. 1 0 0 2 4 6 p. H 8 10 12 14
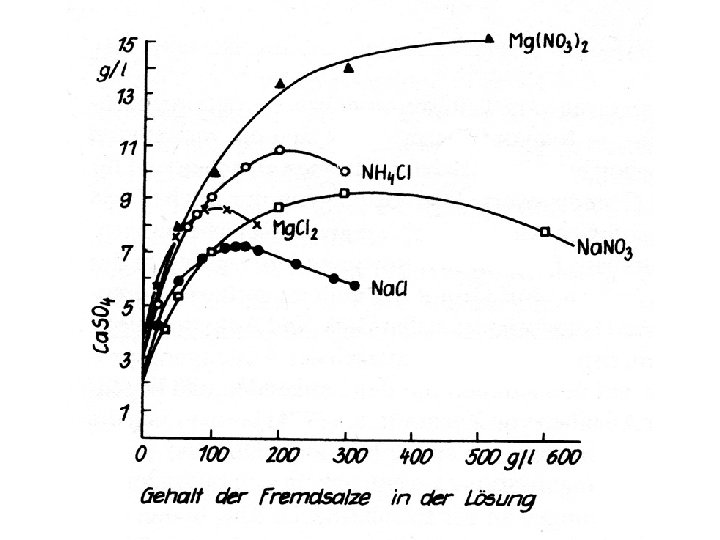

Warum Sodalacken trübe sind Stabile Trübe setzt ein negatives ζ Potential voraus, welches die Partikel in den Zustand der DISPERSION versetzt. • Natriumbeladung des Austauschkomplexes (Warum Na⁺? ) • geringe Salzkonzentration in der Lösung der Wassersäule • Weitgehende Abwesenheit von Ca²⁺ und Mg²⁺ • Hoher p. H, insbes. wichtig für das ζ Potential der Calcitpartikel Die Trübe ist daher saisonal nicht immer gleich stabil: Bei geringen Salzgehalten (im Spätsommer und Herbst) ist sie deutlicher ausgeprägt als im Frühsommer bei hohen Salzkonzentrationen.
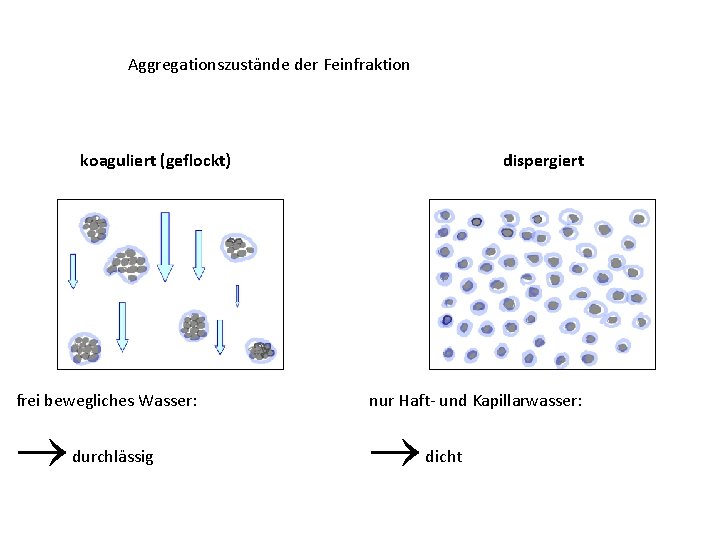
Aggregationszustände der Feinfraktion koaguliert (geflockt) dispergiert frei bewegliches Wasser: nur Haft und Kapillarwasser: durchlässig dicht
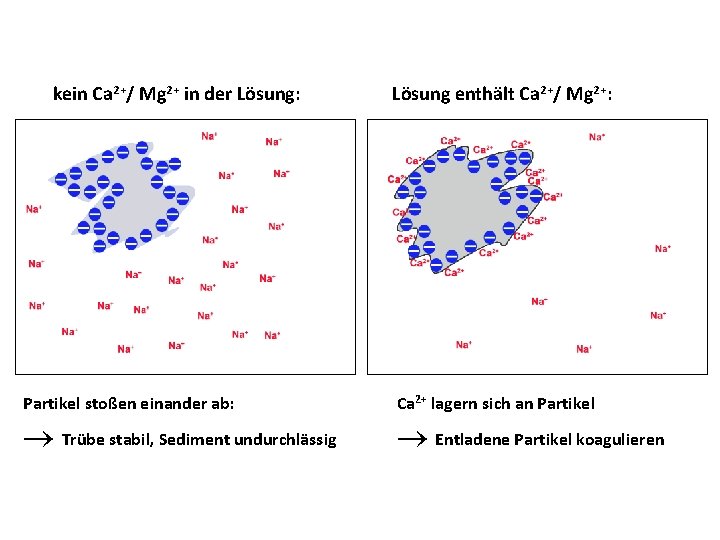
kein Ca 2+/ Mg 2+ in der Lösung: Lösung enthält Ca 2+/ Mg 2+: Partikel stoßen einander ab: Ca 2+ lagern sich an Partikel Trübe stabil, Sediment undurchlässig Entladene Partikel koagulieren

Weißalkaliböden oder Solonchake: • Aggregiert durch hohe Salzgehalte der Porenlösung: Als Folge der hohen Salzgehalte der Porenlösung ist der Austauschkomplex entladen und Solontchake sind im Allgemeinen gut aggregiert und durchlüftet. Gleichzeitig ist die Vegetation oft kaum entwickelt, woraus die geringen Humusgehalte und die helle Farbe zu verstehen sind. • Erkennungsmerkmal sind die häufig in Trockenperioden auftretenden Salzausblühungen. Diese sind bei entsprechender Niederschlagsarmut von März bis November möglich. • Die Grundvoraussetzung für das Bestehen von Solonchaken ist Wassersättigung bis an die Oberfläche, also geringe Grundwasserflurabstände. Solonchake setzen daher Muldenlagen voraus. • Solonchake sind wegen des sehr hohen Salzgehaltes im Oberboden nahezu vegetationsfrei. Ausschließlich wenige salztolerante Arten (Halopohyten) bilden für einige Wochen lockere Bestände. Dies erklärt den geringen Humushgehalt und die sehr helle, nahezu weiße Farbe. Für den Queller ist der Solonchak der typische und bevorzugte Standort, Queller ist daher ein Anzeiger für Solonchake.

Queller auf Solonchak, Legerilacke, Podersdorf

Schwarzalkaliböden oder Solonetze: • Dispergiert : Böden hoher Na+-Sättigung am Austausch komplex(Scheffer, S 156, 455), jedoch geringer Salzghalte in der Porenlösung. Deshalb sind Solonetze (im Gegensatz zu den Solontchaken) im feuchten Zustand stark dispergiert, schlecht durchlüftet und wenig wasserdurchlässig. Im trockenen Zustand bilden sie harte Schollen und werden von tiefen Schwundrissen durchzogen. Solonetze entstehen meist durch Entsalzung (der Porenlösung) aus Solontchaken infolge einer Grundwassersenkung oder Feuchterwerden des Klimas. In einem fortgeschrittenen Stadium der Entsalzung beschränkt sich der erhöhte Salzgehalt auf einen tieferliegenden B Horizont, während der darüber liegende bereits entsalzte A Horizont Vegetation zulässt und in Schwundrisse eindringender Humus die Dunkelfärbung bewirkt. Sie sind leicht an der für sie typischen Polygonstruktur (Schwundrisse) erkennbar, die sie im trockenen Zustand entwickeln. Das Maximum der Salzkonzentration befindet sich nicht in den Oberflächenschichten, sondern im darunterliegenden (B )Horizont, weil die Salze ebenso wie ein Teil der Tonfraktion durch Sickerprozesse in den Unterboden (B Horizont) verlagert wurden. Daraus geht schon hervor, dass die Entwicklung von Solonetzen einen wasserungesättigten Oberboden, somit im Vergleich zu Solonchaken größere Grundwasserflurabstände verlangt. Häufig gehen Solonetze daher auch aus Solonchaken bei sinkendem Grundwasserspiegel hervor.

Solonetz, Sechsmahdlacke, Apetlon
- Slides: 40